鲁教版九年级上册化学第三节 氧气氧气-氧气的实验室制法 课件(共24张PPT)
文档属性
| 名称 | 鲁教版九年级上册化学第三节 氧气氧气-氧气的实验室制法 课件(共24张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-06-27 00:00:00 | ||
图片预览






文档简介
(共24张PPT)
第三节
氧气
氧气有哪些用途?
如此重要的气体如何获得?
(一)、创设情境
在实验室如何
制取一瓶氧气呢?
选择反应物
选择反应装置
选择收集装置
实验操作
1、探究反应物的选择:
(1)小组讨论P—87页活动天地4—3
(2)实验探究实验室可以用过氧化氢在催化剂的作用下制取氧气。
(二)探究氧气的实验室制法
信息链接
1.水(H2O):加热至1000℃高温或通以直流电可分解为氧气和氢气,但耗电量较大。
2.二氧化碳(CO2):在植物光合作用下与水反应可产生氧气,反应缓慢。
3.高锰酸钾(KMnO4):紫黑色晶体,受热很快分解生成氧气,成本较高。
4.过氧化氢(H2O2):俗称双氧水,是一种无色液体每100ml
大约1.
80元,常温下会缓慢分解成水和氧气。
原料的来源、价格、反应条件难易(室温最好)、方法简单、绿色环保等因素。
制取物质应
考虑的因素
2、探究反应物的选择:
选择过氧化氢溶液分解制取氧气
(简捷、安全、环保、经济)
过氧化氢
水
+
氧气
实验一:取一支试管,加入5ml过氧化氢溶液,将带火星的木条伸入试管的管口,观察实验现象。
1、探究反应物的选择:
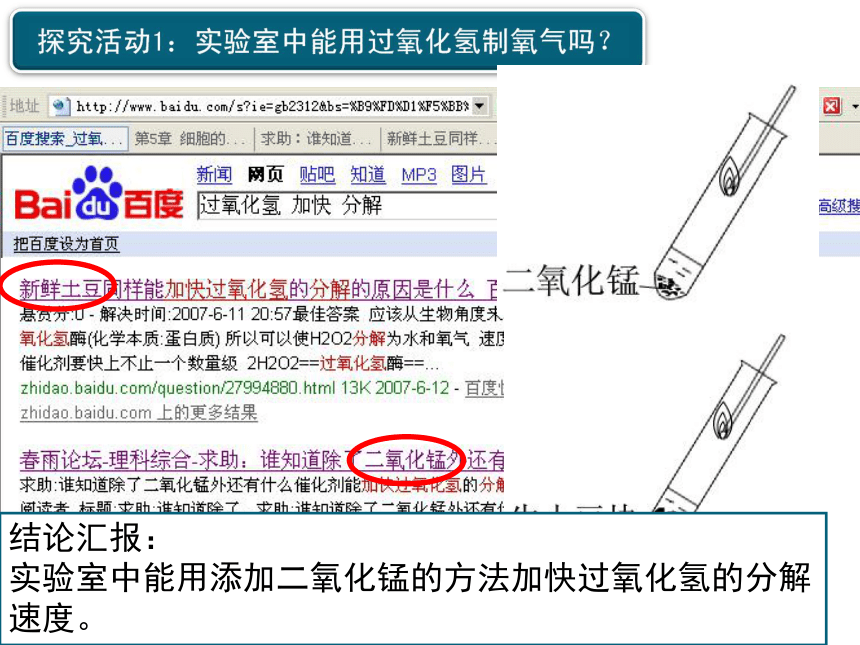
结论汇报:
实验室中能用添加二氧化锰的方法加快过氧化氢的分解速度。
实验二:另取一支试管,先加入少量二氧化锰,再加入5ml的过氧化氢溶液,将带火星的木条伸入试管口。观察发生的现象。
结论汇报:
实验室中能用过氧化氢添加二氧化锰的方法制备氧气。
2、探究反应物的选择:
过氧化氢
水
+ 氧气
MnO2
反应原理:
H2O2
H2O
O2
反应药品:
双氧水、二氧化锰
2、探究反应物的选择:
小资料:
1、将反应后的二氧化锰过滤、干燥、称量,发现二氧化锰的质量不发生改变。
2、将称量后的二氧化锰再次放入过氧化氢溶液中,发现有大量气泡冒出,该气泡能使带火星的木条复燃。
能够改变其他物质的化学反应速率,本身的质量和化学性质在反应前后不变的物质叫做催化剂。
加快或减慢
一变二不变
固固加热型
固液不加热型
√
根据反应物的状态和反应条件
3、另外一些常见过氧化氢制氧气的发生装置:
排水法
排空气法
向上排空气法
向下排空气法
3、探究收集装置:
小资料:
在通常状况下,氧气是一种没有颜色、没有气味的气体。在一个标准大气压下,氧气的密度是1.429g/L,比空气略大(空气的密度是1.293g/L)。它不易溶于水,1L升水中只能溶解约30mL氧气。
排水法
排空气法
向上排空气法
向下排空气法
3、探究收集装置:
√
√
实验室制取氧气的装置
或
4、实验操作
组装装置
检查气密性
装入药品
收集气体
检验
验满
放置
拆装置、清洗整理
注意事项:
1、装入药品前先检查装置气密性;
2、注意检验和验满的操作的不同;
3、用排水法收集时应等导气管末端均匀产生气泡时再收集。
动手实验:收集一瓶气体,操作步骤如下:
1、
下列关于催化剂的说法正确的是(
)
A.二氧化锰是催化剂。
B.催化剂能加快化学反应速率,增加生成物的质量。
C.没有催化剂,过氧化氢就不能产生氧气。
D.在过氧化氢制氧气的反应中,二氧化锰起催化作用
D
2、请从下列仪器中选用适当仪器用H2O2与MnO2制取并收集O2。
(1)写出仪器名称c
,e
;
(2)若用排空气法收集O2,产生并收集气体应该选用的仪器有(填代号)
,装入药品前必须进行的一步操作是
;
(3)文字表达式为
;
(4)检验O2是否已经集满的方法是:
。
h
锥形瓶
烧杯
cghb
检查气密性
将带火星的木条伸入集气瓶口,复燃则已集满。
你说我说
通过这节课的学习,你都收获了什么?
板书设计
二、氧气的实验室制法
1.反应原理:
2.选择装置
3.收集方法
4.检验方法
5.验满方法
过氧化氢
水
+氧气
H2O2
H2O
O2
催化剂
选择反应物
选择反应装置
选择收集装置
进行实验
一、实验室制备气体的过程
第三节
氧气
氧气有哪些用途?
如此重要的气体如何获得?
(一)、创设情境
在实验室如何
制取一瓶氧气呢?
选择反应物
选择反应装置
选择收集装置
实验操作
1、探究反应物的选择:
(1)小组讨论P—87页活动天地4—3
(2)实验探究实验室可以用过氧化氢在催化剂的作用下制取氧气。
(二)探究氧气的实验室制法
信息链接
1.水(H2O):加热至1000℃高温或通以直流电可分解为氧气和氢气,但耗电量较大。
2.二氧化碳(CO2):在植物光合作用下与水反应可产生氧气,反应缓慢。
3.高锰酸钾(KMnO4):紫黑色晶体,受热很快分解生成氧气,成本较高。
4.过氧化氢(H2O2):俗称双氧水,是一种无色液体每100ml
大约1.
80元,常温下会缓慢分解成水和氧气。
原料的来源、价格、反应条件难易(室温最好)、方法简单、绿色环保等因素。
制取物质应
考虑的因素
2、探究反应物的选择:
选择过氧化氢溶液分解制取氧气
(简捷、安全、环保、经济)
过氧化氢
水
+
氧气
实验一:取一支试管,加入5ml过氧化氢溶液,将带火星的木条伸入试管的管口,观察实验现象。
1、探究反应物的选择:
结论汇报:
实验室中能用添加二氧化锰的方法加快过氧化氢的分解速度。
实验二:另取一支试管,先加入少量二氧化锰,再加入5ml的过氧化氢溶液,将带火星的木条伸入试管口。观察发生的现象。
结论汇报:
实验室中能用过氧化氢添加二氧化锰的方法制备氧气。
2、探究反应物的选择:
过氧化氢
水
+ 氧气
MnO2
反应原理:
H2O2
H2O
O2
反应药品:
双氧水、二氧化锰
2、探究反应物的选择:
小资料:
1、将反应后的二氧化锰过滤、干燥、称量,发现二氧化锰的质量不发生改变。
2、将称量后的二氧化锰再次放入过氧化氢溶液中,发现有大量气泡冒出,该气泡能使带火星的木条复燃。
能够改变其他物质的化学反应速率,本身的质量和化学性质在反应前后不变的物质叫做催化剂。
加快或减慢
一变二不变
固固加热型
固液不加热型
√
根据反应物的状态和反应条件
3、另外一些常见过氧化氢制氧气的发生装置:
排水法
排空气法
向上排空气法
向下排空气法
3、探究收集装置:
小资料:
在通常状况下,氧气是一种没有颜色、没有气味的气体。在一个标准大气压下,氧气的密度是1.429g/L,比空气略大(空气的密度是1.293g/L)。它不易溶于水,1L升水中只能溶解约30mL氧气。
排水法
排空气法
向上排空气法
向下排空气法
3、探究收集装置:
√
√
实验室制取氧气的装置
或
4、实验操作
组装装置
检查气密性
装入药品
收集气体
检验
验满
放置
拆装置、清洗整理
注意事项:
1、装入药品前先检查装置气密性;
2、注意检验和验满的操作的不同;
3、用排水法收集时应等导气管末端均匀产生气泡时再收集。
动手实验:收集一瓶气体,操作步骤如下:
1、
下列关于催化剂的说法正确的是(
)
A.二氧化锰是催化剂。
B.催化剂能加快化学反应速率,增加生成物的质量。
C.没有催化剂,过氧化氢就不能产生氧气。
D.在过氧化氢制氧气的反应中,二氧化锰起催化作用
D
2、请从下列仪器中选用适当仪器用H2O2与MnO2制取并收集O2。
(1)写出仪器名称c
,e
;
(2)若用排空气法收集O2,产生并收集气体应该选用的仪器有(填代号)
,装入药品前必须进行的一步操作是
;
(3)文字表达式为
;
(4)检验O2是否已经集满的方法是:
。
h
锥形瓶
烧杯
cghb
检查气密性
将带火星的木条伸入集气瓶口,复燃则已集满。
你说我说
通过这节课的学习,你都收获了什么?
板书设计
二、氧气的实验室制法
1.反应原理:
2.选择装置
3.收集方法
4.检验方法
5.验满方法
过氧化氢
水
+氧气
H2O2
H2O
O2
催化剂
选择反应物
选择反应装置
选择收集装置
进行实验
一、实验室制备气体的过程
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
