第一单元 金属键 金属晶体 课件(22张PPT)
文档属性
| 名称 | 第一单元 金属键 金属晶体 课件(22张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-06-28 00:00:00 | ||
图片预览








文档简介
(共22张PPT)
第一单元
金属键
金属晶体
专题三
微粒间作用力与物质性质
第2课时
金属晶体
[学习目标]
(1)了解金属晶体内原子的几种常见排列方式;
(2)训练学生的动手能力和空间想象能力;
(3)培养学生的合作意识。
美丽的晶体
磷氯铅矿
玲珑剔透的石英
一、晶体与非晶体
晶体:具有规则几何外形的固体;
具有固定的熔沸点
非晶体:没有规则几何外形的固体
;没有固定的熔沸点
(阅读课本P34化学史话)
二、
晶体的分类(依据:构成晶体的粒子种类及粒子之间的作用)
分为:金属晶体、离子晶体、原子晶体、分子晶体、混合晶体。
三
晶胞:
金属晶体中能够反映晶体结构特征的基本重复单位
在金属晶体中,由于金属键没有方向性,金属原子如同半径相等的小球一样,彼此相切、紧密堆积成晶体。金属晶体中金属原子的紧密堆积是有一定规律的。
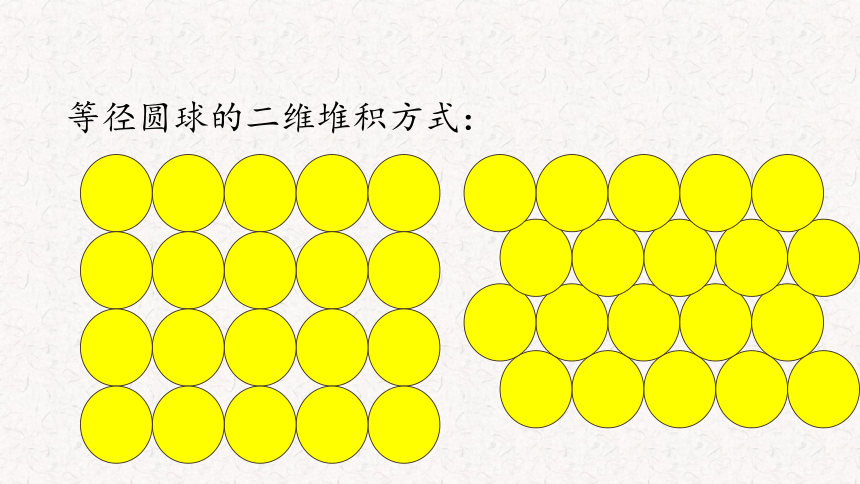
等径圆球的二维堆积方式:
三维空间堆积方式:
1.简单立方堆积
配位数概念:如果把一个金属原子视为一个球体,则一个圆球周围紧邻的球数为配位数。
金属钋(Po)属于简单立方堆积
配位数:6
2.
体心立方堆积:
属于体心立方堆积的金属有:
钠,钾,铬,钼,钨,铁。
配位数为:8
3.六方堆积:
1
2
3
4
5
6
1
2
3
4
5
6
A
B
A
B
属于六方堆积的金属有:
锌,钛,镁。
配位数为:12
4.面心立方最密堆积
1
2
3
4
5
6
1
2
3
4
5
6
1
2
3
4
5
6
B
C
A
属于面心立方堆积的金属有:
金,银,铜,铅。
配位数
12.
四
晶胞中金属原子数目的计算(平均值)
五
空间利用率的计算
空间利用率就是晶胞上占有的金属原子体积与
晶胞体积之比。
1.简单立方空间利用率的计算:
设原子半径为r,晶胞边长为a,则简单立方的空间利用率为:
一个原子的体积
空间利用率
=52.3%
2
体心立方空间利用率的计算:
设原子半径为r
、晶胞边长为a
,
根据勾股定理,
得:2a
2
+
a
2
=
(4r)
2
空间利用率
=
晶胞含有原子的体积
/
晶胞体积
100%
3.面心立方空间利用率的计算:
设金属原子半径为r,晶胞边长为a
(4r)2=2a2
a=
r
面心立方的空间利用率为
=74%
4.
六方堆积的空间利用率:
a
h
h=
a=2r
正六边形的面积s=
6
六方堆积的空间利用率:
=74%
堆积方式
晶胞类型
空间利用率
配位数
实例
面心立方最密堆积
堆积方式及性质小结
简单立方堆积
体心立方密堆积
六方最密堆积
面心立方
六方
体心立方
简单立方
74%
74%
68%
52%
12
12
8
6
Cu、Ag、Au
Mg、Ti、Zn
Na、K、Fe
Po
来日可期
第一单元
金属键
金属晶体
专题三
微粒间作用力与物质性质
第2课时
金属晶体
[学习目标]
(1)了解金属晶体内原子的几种常见排列方式;
(2)训练学生的动手能力和空间想象能力;
(3)培养学生的合作意识。
美丽的晶体
磷氯铅矿
玲珑剔透的石英
一、晶体与非晶体
晶体:具有规则几何外形的固体;
具有固定的熔沸点
非晶体:没有规则几何外形的固体
;没有固定的熔沸点
(阅读课本P34化学史话)
二、
晶体的分类(依据:构成晶体的粒子种类及粒子之间的作用)
分为:金属晶体、离子晶体、原子晶体、分子晶体、混合晶体。
三
晶胞:
金属晶体中能够反映晶体结构特征的基本重复单位
在金属晶体中,由于金属键没有方向性,金属原子如同半径相等的小球一样,彼此相切、紧密堆积成晶体。金属晶体中金属原子的紧密堆积是有一定规律的。
等径圆球的二维堆积方式:
三维空间堆积方式:
1.简单立方堆积
配位数概念:如果把一个金属原子视为一个球体,则一个圆球周围紧邻的球数为配位数。
金属钋(Po)属于简单立方堆积
配位数:6
2.
体心立方堆积:
属于体心立方堆积的金属有:
钠,钾,铬,钼,钨,铁。
配位数为:8
3.六方堆积:
1
2
3
4
5
6
1
2
3
4
5
6
A
B
A
B
属于六方堆积的金属有:
锌,钛,镁。
配位数为:12
4.面心立方最密堆积
1
2
3
4
5
6
1
2
3
4
5
6
1
2
3
4
5
6
B
C
A
属于面心立方堆积的金属有:
金,银,铜,铅。
配位数
12.
四
晶胞中金属原子数目的计算(平均值)
五
空间利用率的计算
空间利用率就是晶胞上占有的金属原子体积与
晶胞体积之比。
1.简单立方空间利用率的计算:
设原子半径为r,晶胞边长为a,则简单立方的空间利用率为:
一个原子的体积
空间利用率
=52.3%
2
体心立方空间利用率的计算:
设原子半径为r
、晶胞边长为a
,
根据勾股定理,
得:2a
2
+
a
2
=
(4r)
2
空间利用率
=
晶胞含有原子的体积
/
晶胞体积
100%
3.面心立方空间利用率的计算:
设金属原子半径为r,晶胞边长为a
(4r)2=2a2
a=
r
面心立方的空间利用率为
=74%
4.
六方堆积的空间利用率:
a
h
h=
a=2r
正六边形的面积s=
6
六方堆积的空间利用率:
=74%
堆积方式
晶胞类型
空间利用率
配位数
实例
面心立方最密堆积
堆积方式及性质小结
简单立方堆积
体心立方密堆积
六方最密堆积
面心立方
六方
体心立方
简单立方
74%
74%
68%
52%
12
12
8
6
Cu、Ag、Au
Mg、Ti、Zn
Na、K、Fe
Po
来日可期
