高中化学鲁科版 选修五 2.4 第1课时羧酸(共24张PPT)
文档属性
| 名称 | 高中化学鲁科版 选修五 2.4 第1课时羧酸(共24张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-06-29 00:00:00 | ||
图片预览




文档简介
(共24张PPT)
2018年6月27日星期三
§2.5
羧酸(第一课时)
=
1.睡前一杯冷开水,加一汤匙醋,喝后可助眠.
2.用醋涂抹蚊虫叮咬处,可减轻痒痛、消肿
3流鼻血时,用药棉蘸醋塞鼻,血即止
4.坐车前喝醋开水,防晕车
你知道吗?
美好生活
无醋不在
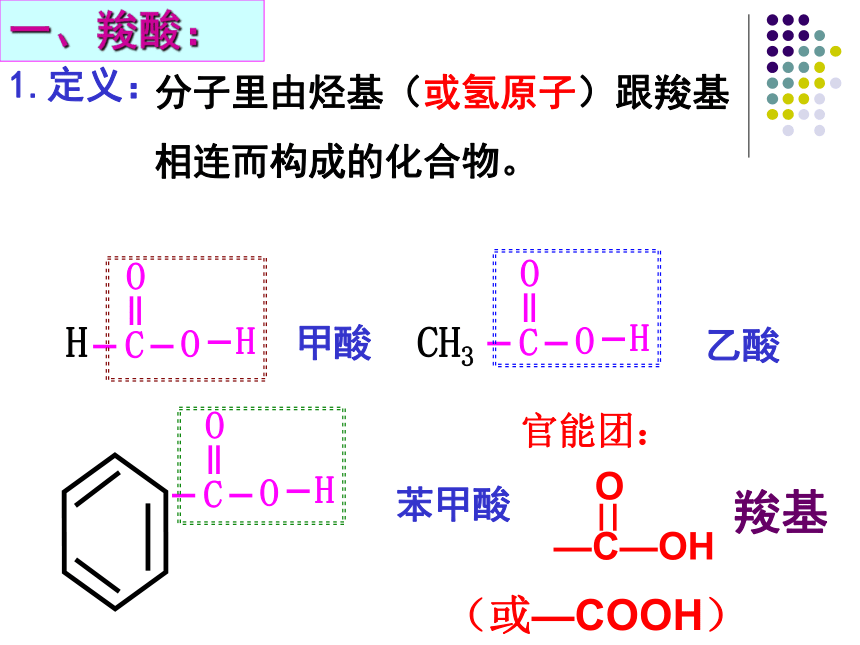
1.定义:
甲酸
乙酸
C
O
H
H
O
C
O
H
CH3
O
C
O
H
O
苯甲酸
一、羧酸:
羧基
官能团:
O
—C—OH
(或—COOH)
分子里由烃基(或氢原子)跟羧基
相连而构成的化合物。
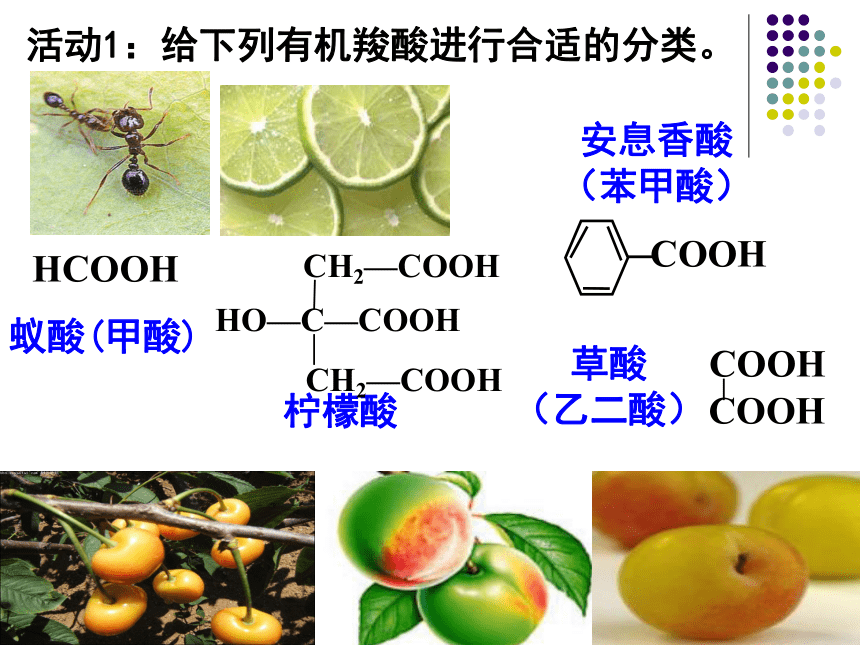
蚁酸(甲酸)
HCOOH
柠檬酸
HO—C—COOH
CH2—COOH
CH2—COOH
草酸
(乙二酸)
COOH
COOH
安息香酸
(苯甲酸)
COOH
活动1:给下列有机羧酸进行合适的分类。
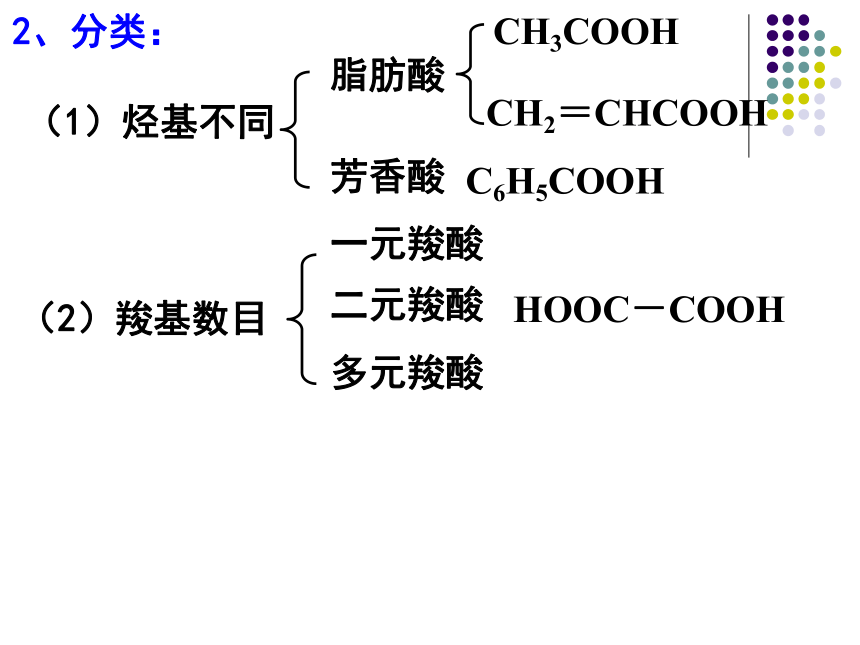
芳香酸
脂肪酸
CH3COOH
CH2=CHCOOH
C6H5COOH
2、分类:
(1)烃基不同
(2)羧基数目
一元羧酸
二元羧酸
多元羧酸
HOOC-COOH
一元羧酸和饱和一元羧酸的通式和分子式
一元羧酸的通式:R-COOH
饱和一元羧酸通式:CnH2n+1COOH(n
≥0)
或CnH2nO2(n≥1)
HCOOH(甲酸)、
CH3COOH(乙酸)、CH3CH2COOH(丙酸)是饱和一元羧酸。
活动2:你能写出C5H10O2属于羧酸的同分异构体吗?
无色、有刺激性气味的液体
与水、有机溶剂互溶
低于16.6℃就凝结成冰状晶体,
无水乙酸又称冰醋酸。
沸点117.9
℃,熔点16.6℃,
1、乙酸的物理性质
二、乙酸
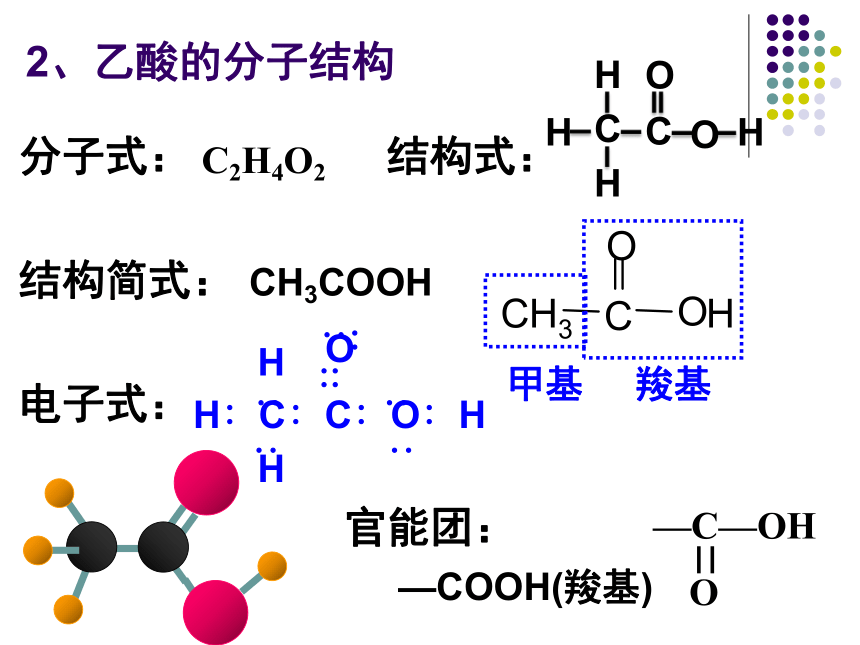
分子式:
结构式:
结构简式:
电子式:
官能团:
2、乙酸的分子结构
C2H4O2
C
H
O
O
C
H
H
H
CH3COOH
—COOH(羧基)
O
—C—OH
∶
O
H∶C∶C∶O∶H
H
H
∷
∶
∶
∶
∶
∶
甲基
羧基
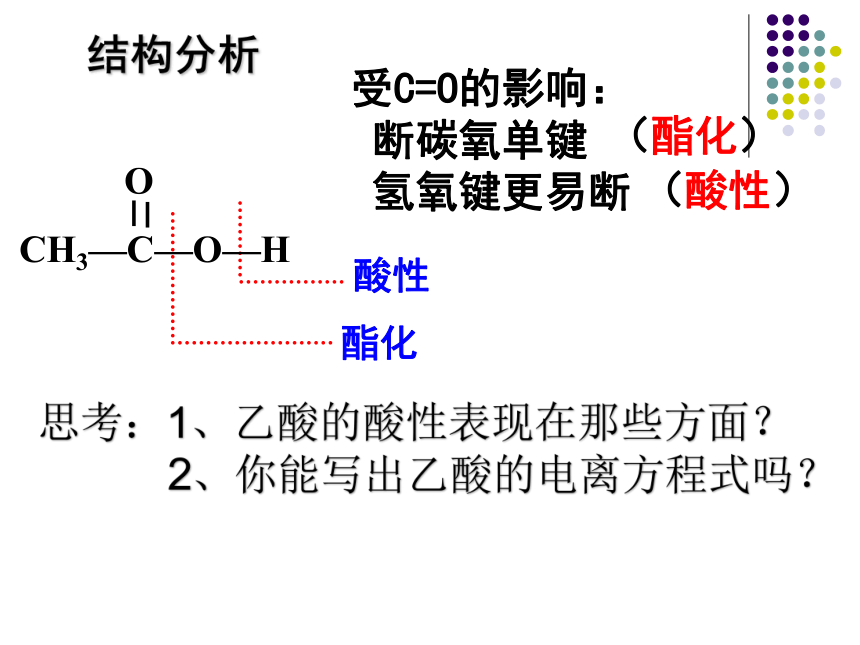
结构分析
受C=O的影响:
断碳氧单键
氢氧键更易断
(酯化)
(酸性)
O
CH3—C—O—H
酸性
酯化
思考:1、乙酸的酸性表现在那些方面?
2、你能写出乙酸的电离方程式吗?
请同学们根据现有的化学药品或自己寻找合适的试剂设计实验方案
①
证明乙酸有酸性;
②
比较乙酸、碳酸、苯酚的强弱。
科学探究一、
碳酸钠固体
乙酸溶液
苯酚钠溶液
酸性:
Na2CO3+2CH3COOH
2CH3COONa+CO2↑+H2O
乙酸>碳酸>苯酚
比较装置的优缺点、并写出反应的化学方程式
温故知新
代表物
结构简式
羟基氢的活性
酸性
与钠反应
与烧碱的反应
与纯碱的反应
乙醇
苯酚
乙酸
C2H5OH
C6H5OH
CH3COOH
增强
中性
比碳酸弱
比碳酸强
能
能,不产
生CO2
醇、酚、羧酸中羟基的比较
能
能
不能
能
能
不能
能,并产
生CO2
羟基的活泼性:羧酸>碳酸>苯酚>醇
与NaHCO3反应产生CO2是羧基存在的标志
(1)弱酸性
CH3COOH
CH3COO-
+
H+
酸性强弱
酸性:CH3COOH
H2CO3
C6H5OH
>
>
3、乙酸的化学性质
科学探究二、
可以用几种方法证明乙酸是弱酸?
证明乙酸是弱酸的方法:
1:配制一定浓度的乙酸测定PH值
2:配制一定浓度的乙酸钠溶液测定PH值
3:在相同条件下与同浓度的盐酸比较与金属反应的速率
CH3COOH
CH3COO-+H+
CH3-C-O-H
+
H-O-CH2-CH3
浓硫酸
=
O
(2)酯化反应
CH3-C-O-CH2-CH3
+
H2O
=
O
反应的基本规律:
酸脱-OH醇脱H
饱和碳酸钠溶液
乙醇、乙酸、浓硫酸
同位素示踪法
18
18
取代反应
温故知新
1.
试管倾斜加热的目的是什么?
2.浓硫酸的作用是什么?
3.得到的反应产物是否纯净?主要杂质有哪些?
4.饱和Na2CO3溶液有什么作用?
5.
为什么导管不插入饱和Na2CO3溶液中?有无其它防倒吸的方法?
催化剂,吸水剂
不纯净;乙酸、乙醇
①
中和乙酸
②
溶解乙醇③
降低酯在水中的溶解度,以便使酯分层析出。
防止受热不均匀发生倒吸
增大受热面积
安全瓶
思考与交流
根据化学平衡原理,提高乙酸乙酯产率的措施有:
(1)由于乙酸乙酯的沸点比乙酸、乙醇都低,因此从反应物中不断蒸出乙酸乙酯可提高其产率。
(2)使用过量的乙醇,可提高乙酸转化率。
(3)使用浓H2SO4作吸水剂,提高反应转化率。
P63
小结:
(1)弱酸性
CH3COOH
CH3COO-
+
H+
乙酸的化学性质
酸性:乙酸>碳酸>苯酚
(2)酯化反应
取代反应
甲酸
结构特点:既有羧基又有醛基
化学性质
醛基
羧基
氧化反应(如银镜反应)
酸性,酯化反应
O
H—C—O—H
拓展
(又名蚁酸)
HCOOH
活动:请用一种试剂鉴别下面四种有机物?乙醇、乙醛、乙酸、甲酸
新制Cu(OH)2悬浊液
谢谢指导!
作业与实践
⒈1mol有机物
⑴
Na
⑵
NaOH
⑶
NaHCO3
-CH_CH2_
HO_
-COOH
—
OH
CH2OH
—
最多能消耗下列各物质多少mol?
⒉化合物
COOH
OH
跟足量的下列哪种物质
的溶液反应可得到一钠盐C7H5O3Na(
)
NaOH
B.
Na2CO3
C.
NaHCO3
D.
NaCl
4
2
1
牛刀小试
【知识迁移】写出下列酸和醇的酯化反应
CH3COOCH3
+
H2O
CH3COOH
+
HOCH3
浓H2SO4
乙酸甲酯
浓H2SO4
+
2H2O
二乙酸乙二酯
环乙二酸乙二酯
浓H2SO4
2
2018年6月27日星期三
§2.5
羧酸(第一课时)
=
1.睡前一杯冷开水,加一汤匙醋,喝后可助眠.
2.用醋涂抹蚊虫叮咬处,可减轻痒痛、消肿
3流鼻血时,用药棉蘸醋塞鼻,血即止
4.坐车前喝醋开水,防晕车
你知道吗?
美好生活
无醋不在
1.定义:
甲酸
乙酸
C
O
H
H
O
C
O
H
CH3
O
C
O
H
O
苯甲酸
一、羧酸:
羧基
官能团:
O
—C—OH
(或—COOH)
分子里由烃基(或氢原子)跟羧基
相连而构成的化合物。
蚁酸(甲酸)
HCOOH
柠檬酸
HO—C—COOH
CH2—COOH
CH2—COOH
草酸
(乙二酸)
COOH
COOH
安息香酸
(苯甲酸)
COOH
活动1:给下列有机羧酸进行合适的分类。
芳香酸
脂肪酸
CH3COOH
CH2=CHCOOH
C6H5COOH
2、分类:
(1)烃基不同
(2)羧基数目
一元羧酸
二元羧酸
多元羧酸
HOOC-COOH
一元羧酸和饱和一元羧酸的通式和分子式
一元羧酸的通式:R-COOH
饱和一元羧酸通式:CnH2n+1COOH(n
≥0)
或CnH2nO2(n≥1)
HCOOH(甲酸)、
CH3COOH(乙酸)、CH3CH2COOH(丙酸)是饱和一元羧酸。
活动2:你能写出C5H10O2属于羧酸的同分异构体吗?
无色、有刺激性气味的液体
与水、有机溶剂互溶
低于16.6℃就凝结成冰状晶体,
无水乙酸又称冰醋酸。
沸点117.9
℃,熔点16.6℃,
1、乙酸的物理性质
二、乙酸
分子式:
结构式:
结构简式:
电子式:
官能团:
2、乙酸的分子结构
C2H4O2
C
H
O
O
C
H
H
H
CH3COOH
—COOH(羧基)
O
—C—OH
∶
O
H∶C∶C∶O∶H
H
H
∷
∶
∶
∶
∶
∶
甲基
羧基
结构分析
受C=O的影响:
断碳氧单键
氢氧键更易断
(酯化)
(酸性)
O
CH3—C—O—H
酸性
酯化
思考:1、乙酸的酸性表现在那些方面?
2、你能写出乙酸的电离方程式吗?
请同学们根据现有的化学药品或自己寻找合适的试剂设计实验方案
①
证明乙酸有酸性;
②
比较乙酸、碳酸、苯酚的强弱。
科学探究一、
碳酸钠固体
乙酸溶液
苯酚钠溶液
酸性:
Na2CO3+2CH3COOH
2CH3COONa+CO2↑+H2O
乙酸>碳酸>苯酚
比较装置的优缺点、并写出反应的化学方程式
温故知新
代表物
结构简式
羟基氢的活性
酸性
与钠反应
与烧碱的反应
与纯碱的反应
乙醇
苯酚
乙酸
C2H5OH
C6H5OH
CH3COOH
增强
中性
比碳酸弱
比碳酸强
能
能,不产
生CO2
醇、酚、羧酸中羟基的比较
能
能
不能
能
能
不能
能,并产
生CO2
羟基的活泼性:羧酸>碳酸>苯酚>醇
与NaHCO3反应产生CO2是羧基存在的标志
(1)弱酸性
CH3COOH
CH3COO-
+
H+
酸性强弱
酸性:CH3COOH
H2CO3
C6H5OH
>
>
3、乙酸的化学性质
科学探究二、
可以用几种方法证明乙酸是弱酸?
证明乙酸是弱酸的方法:
1:配制一定浓度的乙酸测定PH值
2:配制一定浓度的乙酸钠溶液测定PH值
3:在相同条件下与同浓度的盐酸比较与金属反应的速率
CH3COOH
CH3COO-+H+
CH3-C-O-H
+
H-O-CH2-CH3
浓硫酸
=
O
(2)酯化反应
CH3-C-O-CH2-CH3
+
H2O
=
O
反应的基本规律:
酸脱-OH醇脱H
饱和碳酸钠溶液
乙醇、乙酸、浓硫酸
同位素示踪法
18
18
取代反应
温故知新
1.
试管倾斜加热的目的是什么?
2.浓硫酸的作用是什么?
3.得到的反应产物是否纯净?主要杂质有哪些?
4.饱和Na2CO3溶液有什么作用?
5.
为什么导管不插入饱和Na2CO3溶液中?有无其它防倒吸的方法?
催化剂,吸水剂
不纯净;乙酸、乙醇
①
中和乙酸
②
溶解乙醇③
降低酯在水中的溶解度,以便使酯分层析出。
防止受热不均匀发生倒吸
增大受热面积
安全瓶
思考与交流
根据化学平衡原理,提高乙酸乙酯产率的措施有:
(1)由于乙酸乙酯的沸点比乙酸、乙醇都低,因此从反应物中不断蒸出乙酸乙酯可提高其产率。
(2)使用过量的乙醇,可提高乙酸转化率。
(3)使用浓H2SO4作吸水剂,提高反应转化率。
P63
小结:
(1)弱酸性
CH3COOH
CH3COO-
+
H+
乙酸的化学性质
酸性:乙酸>碳酸>苯酚
(2)酯化反应
取代反应
甲酸
结构特点:既有羧基又有醛基
化学性质
醛基
羧基
氧化反应(如银镜反应)
酸性,酯化反应
O
H—C—O—H
拓展
(又名蚁酸)
HCOOH
活动:请用一种试剂鉴别下面四种有机物?乙醇、乙醛、乙酸、甲酸
新制Cu(OH)2悬浊液
谢谢指导!
作业与实践
⒈1mol有机物
⑴
Na
⑵
NaOH
⑶
NaHCO3
-CH_CH2_
HO_
-COOH
—
OH
CH2OH
—
最多能消耗下列各物质多少mol?
⒉化合物
COOH
OH
跟足量的下列哪种物质
的溶液反应可得到一钠盐C7H5O3Na(
)
NaOH
B.
Na2CO3
C.
NaHCO3
D.
NaCl
4
2
1
牛刀小试
【知识迁移】写出下列酸和醇的酯化反应
CH3COOCH3
+
H2O
CH3COOH
+
HOCH3
浓H2SO4
乙酸甲酯
浓H2SO4
+
2H2O
二乙酸乙二酯
环乙二酸乙二酯
浓H2SO4
2
