人教版高中物理选修3-3 第八章气体 第3节理想气体的状态方程课件(共20张PPT)
文档属性
| 名称 | 人教版高中物理选修3-3 第八章气体 第3节理想气体的状态方程课件(共20张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 3.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 物理 | ||
| 更新时间 | 2020-06-29 00:00:00 | ||
图片预览







文档简介
(共20张PPT)
【问题1】三大气体实验定律内容是什么?
公式:
p1V1=p2V2
或pV
=C1
2、査理定律:
1、玻意耳定律:
3、盖-吕萨克定律:
【问题2】这些定律的适用范围是什么?
温度不太低,压强不太大。
【问题3】如果某种气体的三个状态参量(p、V、T)都发生了变化,它们之间又遵从什么规律呢?
第八章
气体
第3节
理想气体的状态方程
一.理想气体?
假设有这样一种气体,它在任何温度和任何压强下都能严格地遵从气体实验定律,我们把这样的气体叫做“理想气体”。
理想气体具有哪些特点呢?
1、理想气体是不存在的,是一种理想模型。
2、在温度不太低,压强不太大时实际气体都可看成是理想气体。
一定质量的理想气体的内能仅由温度决定
,与气体的体积无关.
4、从能量上说:理想气体分子除碰撞外,无相互作用的引力和斥力,故无分子势能,理想气体的内能只有分子动能。
3、从微观上说:理想气体分子本身的大小与分子间的距离相比可以忽略不计,视为质点。分子本身没有体积,即它所占据的空间认为都是可以被压缩的空间。
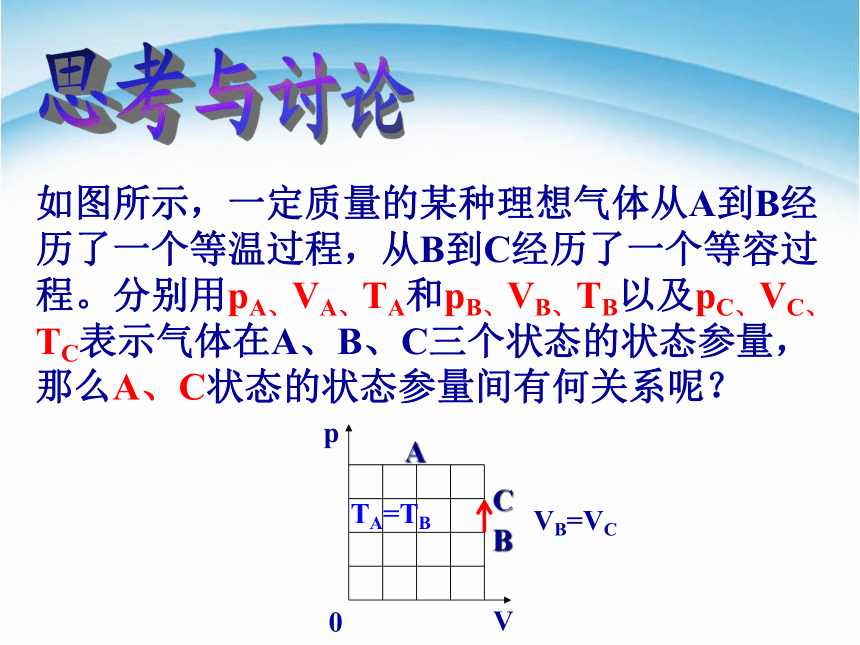
如图所示,一定质量的某种理想气体从A到B经历了一个等温过程,从B到C经历了一个等容过程。分别用pA、VA、TA和pB、VB、TB以及pC、VC、TC表示气体在A、B、C三个状态的状态参量,那么A、C状态的状态参量间有何关系呢?
从A→B为等温变化:由玻意耳定律
pAVA=pBVB
从B→C为等容变化:由查理定律
又TA=TB
VB=VC
解得:
二.推导理想气体状态方程(过程)
VB=VC
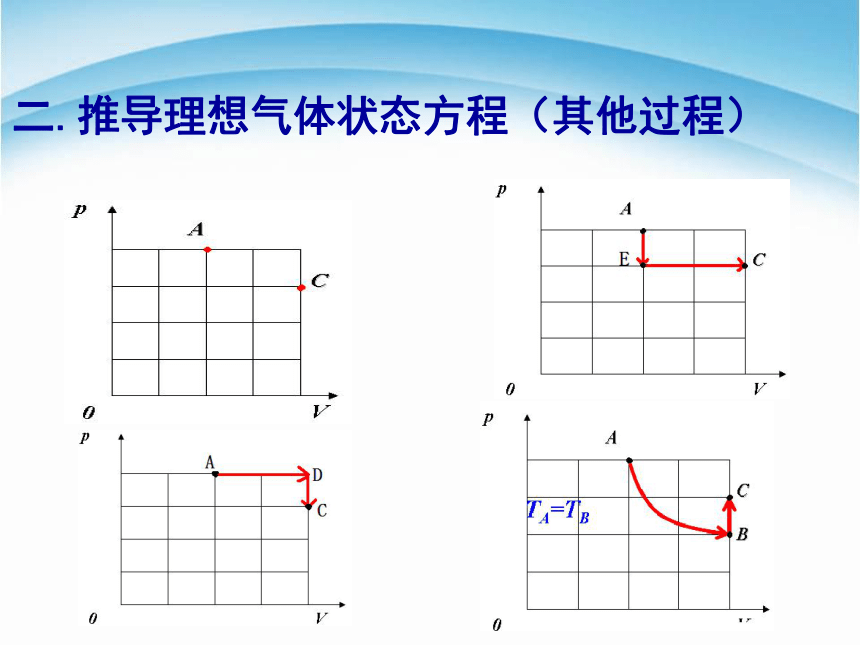
二.推导理想气体状态方程(其他过程)
二、理想气体的状态方程
1、内容:一定质量的某种理想气体在从一个状态变化到另一个状态时,尽管p、V、T都可能改变,但是压强跟体积的乘积与热力学温度的比值保持不变。
2、公式:
3、使用条件:
一定质量的某种理想气体.
注:恒量C由理想气体的质量和种类决定,即由理想气体的物质的量决定
三、克拉珀龙方程(仅做了解)
或
克拉珀龙方程是任意质量的理想气体的状态方程,它联系着某一确定状态下,各物理量的关系。
对实际气体只要温度不太低,压强不太大就可应用克拉珀龙方程解题.
例1:
一定质量的理想气体处于某一初始状态,现要使它的温度经过一系列状态变化后,回到初
始状态的温度,可能实现的过程是(
)
A
先保持压强不变而使体积膨胀
接着保持体积不变而增大压强
B
先保持压强不变而使体积减小
接着保持体积不变而减小压强
C
先保持体积不变而增大压强,
接着保持压强不变而使体积膨胀
D
先保持体积不变而减小压强,
接着保持压强不变而使体积膨胀
D
例2:
例3:?一水银气压计中混进了空气,因而在27℃,外界大气压为758mmHg时,这个水银气压计的读数为738mmHg,此时管中水银面距管顶80mm,当温度降至-3℃时,这个气压计的读数为743mmHg,求此时的实际大气压值为多少mmHg?
引导学生按以下步骤解答此题:
(1)该题研究对象是什么?
混入水银气压计中的空气
(2)画出该题两个状态的示意图:
p1=758-738=20mmHg?
V1=80Smm3
T1=273+27=300
K
T2=273+(-3)=270K
解得:?
p=762.2
mmHg
p2=p-743mmHg
V2=(738+80)S-743S=75Smm3
解:以混进水银气压计的空气为研究对象
初状态:
末状态:
由理想气体状态方程得:
二、理想气体状态方程与气体图象
1.一定质量的理想气体的各种图象
2.理想气体状态方程与一般状态变化图象
基本方法:化“一般”为“特殊”,下图是一定质量的某种理想气体的状态变化过程A→B→C→A.
过A、B、C三点作三条等压线
pA′A→B;压强增大,温度降低,体积缩小
B→C:温度升高,体积减小,压强增大
C→A温度降低,体积增大,压强减小
内径均匀的L形直角细玻璃管,一端封闭,一端开口竖直向上,用水银柱将一定质量空气封存在封闭端内,空气柱长4
cm,水银柱高58
cm,进入封闭端长2
cm,如图8-3-1所示,温度是87
℃,大气压强为75
cmHg,求:
图8-3-1
作业1
答案 (1)133
cmHg (2)-5
℃
小结:
一、理想气体:
在任何温度和任何压强下都能严格地遵从气体实验定律的气体
二、理想气体的状态方程
注:恒量C由理想气体的质量和种类决定,即由气体的物质的量决定
气体密度式
【问题1】三大气体实验定律内容是什么?
公式:
p1V1=p2V2
或pV
=C1
2、査理定律:
1、玻意耳定律:
3、盖-吕萨克定律:
【问题2】这些定律的适用范围是什么?
温度不太低,压强不太大。
【问题3】如果某种气体的三个状态参量(p、V、T)都发生了变化,它们之间又遵从什么规律呢?
第八章
气体
第3节
理想气体的状态方程
一.理想气体?
假设有这样一种气体,它在任何温度和任何压强下都能严格地遵从气体实验定律,我们把这样的气体叫做“理想气体”。
理想气体具有哪些特点呢?
1、理想气体是不存在的,是一种理想模型。
2、在温度不太低,压强不太大时实际气体都可看成是理想气体。
一定质量的理想气体的内能仅由温度决定
,与气体的体积无关.
4、从能量上说:理想气体分子除碰撞外,无相互作用的引力和斥力,故无分子势能,理想气体的内能只有分子动能。
3、从微观上说:理想气体分子本身的大小与分子间的距离相比可以忽略不计,视为质点。分子本身没有体积,即它所占据的空间认为都是可以被压缩的空间。
如图所示,一定质量的某种理想气体从A到B经历了一个等温过程,从B到C经历了一个等容过程。分别用pA、VA、TA和pB、VB、TB以及pC、VC、TC表示气体在A、B、C三个状态的状态参量,那么A、C状态的状态参量间有何关系呢?
从A→B为等温变化:由玻意耳定律
pAVA=pBVB
从B→C为等容变化:由查理定律
又TA=TB
VB=VC
解得:
二.推导理想气体状态方程(过程)
VB=VC
二.推导理想气体状态方程(其他过程)
二、理想气体的状态方程
1、内容:一定质量的某种理想气体在从一个状态变化到另一个状态时,尽管p、V、T都可能改变,但是压强跟体积的乘积与热力学温度的比值保持不变。
2、公式:
3、使用条件:
一定质量的某种理想气体.
注:恒量C由理想气体的质量和种类决定,即由理想气体的物质的量决定
三、克拉珀龙方程(仅做了解)
或
克拉珀龙方程是任意质量的理想气体的状态方程,它联系着某一确定状态下,各物理量的关系。
对实际气体只要温度不太低,压强不太大就可应用克拉珀龙方程解题.
例1:
一定质量的理想气体处于某一初始状态,现要使它的温度经过一系列状态变化后,回到初
始状态的温度,可能实现的过程是(
)
A
先保持压强不变而使体积膨胀
接着保持体积不变而增大压强
B
先保持压强不变而使体积减小
接着保持体积不变而减小压强
C
先保持体积不变而增大压强,
接着保持压强不变而使体积膨胀
D
先保持体积不变而减小压强,
接着保持压强不变而使体积膨胀
D
例2:
例3:?一水银气压计中混进了空气,因而在27℃,外界大气压为758mmHg时,这个水银气压计的读数为738mmHg,此时管中水银面距管顶80mm,当温度降至-3℃时,这个气压计的读数为743mmHg,求此时的实际大气压值为多少mmHg?
引导学生按以下步骤解答此题:
(1)该题研究对象是什么?
混入水银气压计中的空气
(2)画出该题两个状态的示意图:
p1=758-738=20mmHg?
V1=80Smm3
T1=273+27=300
K
T2=273+(-3)=270K
解得:?
p=762.2
mmHg
p2=p-743mmHg
V2=(738+80)S-743S=75Smm3
解:以混进水银气压计的空气为研究对象
初状态:
末状态:
由理想气体状态方程得:
二、理想气体状态方程与气体图象
1.一定质量的理想气体的各种图象
2.理想气体状态方程与一般状态变化图象
基本方法:化“一般”为“特殊”,下图是一定质量的某种理想气体的状态变化过程A→B→C→A.
过A、B、C三点作三条等压线
pA′
B→C:温度升高,体积减小,压强增大
C→A温度降低,体积增大,压强减小
内径均匀的L形直角细玻璃管,一端封闭,一端开口竖直向上,用水银柱将一定质量空气封存在封闭端内,空气柱长4
cm,水银柱高58
cm,进入封闭端长2
cm,如图8-3-1所示,温度是87
℃,大气压强为75
cmHg,求:
图8-3-1
作业1
答案 (1)133
cmHg (2)-5
℃
小结:
一、理想气体:
在任何温度和任何压强下都能严格地遵从气体实验定律的气体
二、理想气体的状态方程
注:恒量C由理想气体的质量和种类决定,即由气体的物质的量决定
气体密度式
