化学能与热能
图片预览





文档简介
(共30张PPT)
第二章 化学反应与能量
1 化学能与热能
回忆
一个化学反应过程中,除了生成了新物质外,还通常伴有:
能量变化
热能
电能
光能
声能
自主回顾
形成
化学键
吸收能量
放出能量
断裂
反应物的总能量与生成物总能量的
相对大小
吸热
放热
能量
1.
总能量
总质量
实验探究
升高
气泡
放热
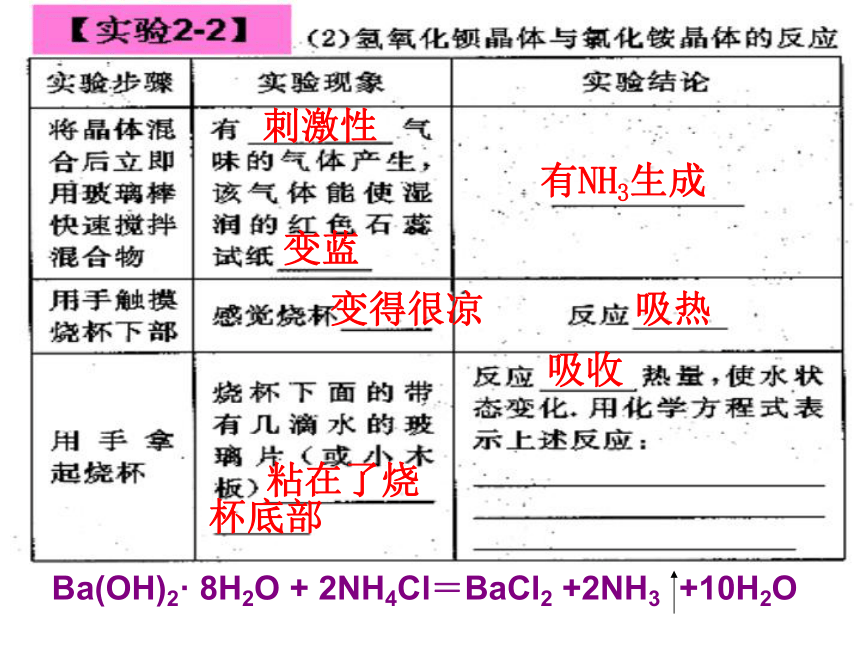
【实验2-1】
刺激性
变蓝
有NH3生成
变得很凉
吸热
粘在了烧
杯底部
吸收
Ba(OH)2· 8H2O + 2NH4Cl=BaCl2 +2NH3 +10H2O
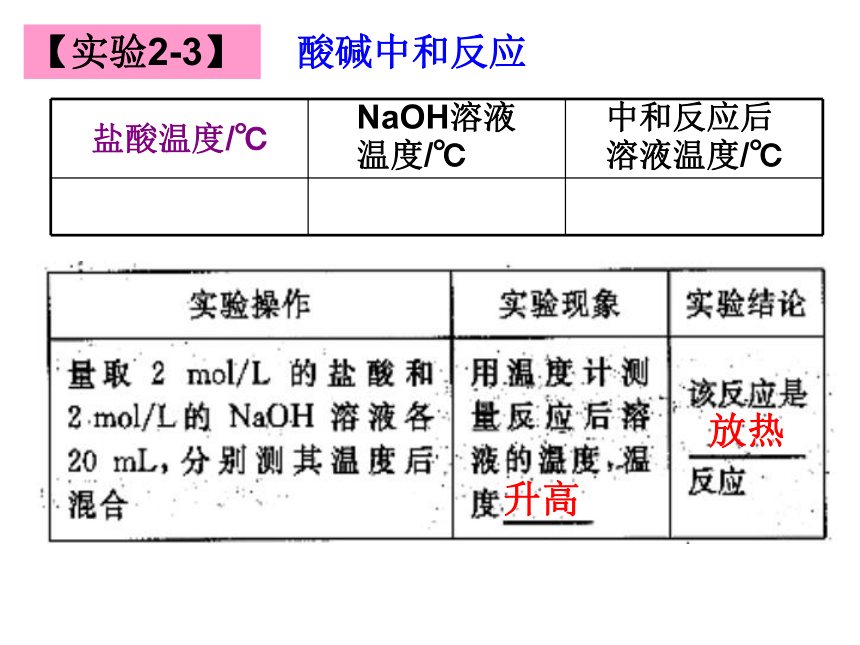
升高
放热
【实验2-3】
盐酸温度/℃ NaOH溶液
温度/℃ 中和反应后
溶液温度/℃
酸碱中和反应
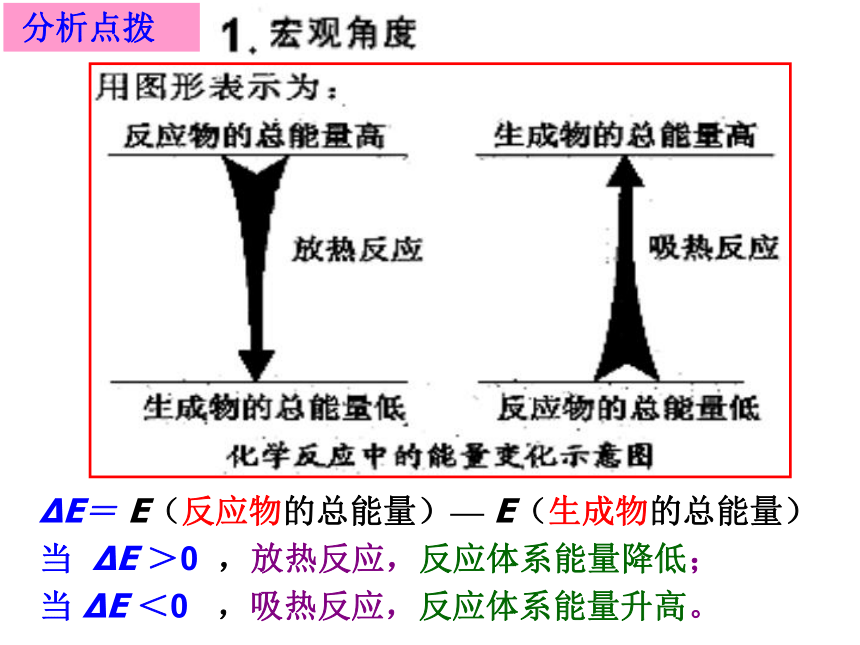
分析点拨
E= E(反应物的总能量)— E(生成物的总能量)
当 E >0 ,放热反应,反应体系能量降低;
当 E <0 ,吸热反应,反应体系能量升高。
反应过程的能量变化:
E(断键)= 679kJ ;
E(成键)= 862kJ
△E= E(成键) - E(断键) = 183kJ/mol
∴当△E>0,放热反应,反应体系能量降低;
当△E<0,吸热反应,反应体系能量升高;
A
即时练习
归纳总结:
思考练习
放热
降低
的部分能量通过化学反应转化为热能释放给环境
升高
吸热
反应物从环境中吸收能量.
反应物
思考与交流
1、保温隔热的效果一定要好。
2、酸碱浓度要准确。
3、温度计要读准,水银球要全浸在
4、实验操作时动作要快,以尽量
溶液中,且要稳定一段时间再读。
减少热量的散失。
太阳能 氢能 核能 生物质能
煤 石油 天然气
绿色
科学视野
1.社会发展与能源利用
新物质
能量
一试身手
物质之间发生化学反应时,一定发生变化的是
A.颜色 B.状态 C.化学键 D.原子核
一试身手
物质之间发生化学反应时,一定发生变化的是
A.颜色 B.状态 C.化学键 D.原子核
盐酸和NaOH溶液反应过程中无颜色变化
一试身手
物质之间发生化学反应时,一定发生变化的是
A.颜色 B.状态 C.化学键 D.原子核
盐酸和NaOH溶液反应过程中无颜色变化
H2和Cl2点燃后生成HCl过程中无状态变化
一试身手
物质之间发生化学反应时,一定发生变化的是
A.颜色 B.状态 C.化学键 D.原子核
化学变化的最小粒子是原子,原子核不变。
盐酸和NaOH溶液反应过程中无颜色变化
H2和Cl2点燃后生成HCl过程中无状态变化
一试身手
物质之间发生化学反应时,一定发生变化的是
A.颜色 B.状态 C.化学键 D.原子核
化学变化的最小粒子是原子,原子核不变。
盐酸和NaOH溶液反应过程中无颜色变化
H2和Cl2点燃后生成HCl过程中无状态变化
以下说法中不正确的是:
需要加热才能进行的反应一定是吸热反应
化学反应开始时都需要吸收能量
E(拆键) < E(成键),则反应放热
可逆反应若正向放热,则逆向一定吸热
以下说法中不正确的是:
需要加热才能进行的反应一定是吸热反应
化学反应开始时都需要吸收能量
E(拆键) < E(成键),则反应放热
可逆反应若正向放热,则逆向一定吸热
以下说法中不正确的是:
需要加热才能进行的反应一定是吸热反应
化学反应开始时都需要吸收能量
E(拆键) < E(成键),则反应放热
可逆反应若正向放热,则逆向一定吸热
以下说法中不正确的是:
需要加热才能进行的反应一定是吸热反应
化学反应开始时都需要吸收能量
E(拆键) < E(成键),则反应放热
可逆反应若正向放热,则逆向一定吸热
例:H2+I2 2HI,分析该反应的能量变化
以下说法中不正确的是:
需要加热才能进行的反应一定是吸热反应
化学反应开始时都需要吸收能量
E(拆键) < E(成键),则反应放热
可逆反应若正向放热,则逆向一定吸热
例:H2+I2 2HI,分析该反应的能量变化
正反应:拆开H2和I2的键,形成HI键; 逆反应:拆开HI键,形成H2和I2的键。
以下说法中不正确的是:
需要加热才能进行的反应一定是吸热反应
化学反应开始时都需要吸收能量
E(拆键) < E(成键),则反应放热
可逆反应若正向放热,则逆向一定吸热
例:H2+I2 2HI,分析该反应的能量变化
正反应:拆开H2和I2的键,形成HI键; 逆反应:拆开HI键,形成H2和I2的键。
以下说法中不正确的是:
需要加热才能进行的反应一定是吸热反应
化学反应开始时都需要吸收能量
E(拆键) < E(成键),则反应放热
可逆反应若正向放热,则逆向一定吸热
第二章 化学反应与能量
1 化学能与热能
回忆
一个化学反应过程中,除了生成了新物质外,还通常伴有:
能量变化
热能
电能
光能
声能
自主回顾
形成
化学键
吸收能量
放出能量
断裂
反应物的总能量与生成物总能量的
相对大小
吸热
放热
能量
1.
总能量
总质量
实验探究
升高
气泡
放热
【实验2-1】
刺激性
变蓝
有NH3生成
变得很凉
吸热
粘在了烧
杯底部
吸收
Ba(OH)2· 8H2O + 2NH4Cl=BaCl2 +2NH3 +10H2O
升高
放热
【实验2-3】
盐酸温度/℃ NaOH溶液
温度/℃ 中和反应后
溶液温度/℃
酸碱中和反应
分析点拨
E= E(反应物的总能量)— E(生成物的总能量)
当 E >0 ,放热反应,反应体系能量降低;
当 E <0 ,吸热反应,反应体系能量升高。
反应过程的能量变化:
E(断键)= 679kJ ;
E(成键)= 862kJ
△E= E(成键) - E(断键) = 183kJ/mol
∴当△E>0,放热反应,反应体系能量降低;
当△E<0,吸热反应,反应体系能量升高;
A
即时练习
归纳总结:
思考练习
放热
降低
的部分能量通过化学反应转化为热能释放给环境
升高
吸热
反应物从环境中吸收能量.
反应物
思考与交流
1、保温隔热的效果一定要好。
2、酸碱浓度要准确。
3、温度计要读准,水银球要全浸在
4、实验操作时动作要快,以尽量
溶液中,且要稳定一段时间再读。
减少热量的散失。
太阳能 氢能 核能 生物质能
煤 石油 天然气
绿色
科学视野
1.社会发展与能源利用
新物质
能量
一试身手
物质之间发生化学反应时,一定发生变化的是
A.颜色 B.状态 C.化学键 D.原子核
一试身手
物质之间发生化学反应时,一定发生变化的是
A.颜色 B.状态 C.化学键 D.原子核
盐酸和NaOH溶液反应过程中无颜色变化
一试身手
物质之间发生化学反应时,一定发生变化的是
A.颜色 B.状态 C.化学键 D.原子核
盐酸和NaOH溶液反应过程中无颜色变化
H2和Cl2点燃后生成HCl过程中无状态变化
一试身手
物质之间发生化学反应时,一定发生变化的是
A.颜色 B.状态 C.化学键 D.原子核
化学变化的最小粒子是原子,原子核不变。
盐酸和NaOH溶液反应过程中无颜色变化
H2和Cl2点燃后生成HCl过程中无状态变化
一试身手
物质之间发生化学反应时,一定发生变化的是
A.颜色 B.状态 C.化学键 D.原子核
化学变化的最小粒子是原子,原子核不变。
盐酸和NaOH溶液反应过程中无颜色变化
H2和Cl2点燃后生成HCl过程中无状态变化
以下说法中不正确的是:
需要加热才能进行的反应一定是吸热反应
化学反应开始时都需要吸收能量
E(拆键) < E(成键),则反应放热
可逆反应若正向放热,则逆向一定吸热
以下说法中不正确的是:
需要加热才能进行的反应一定是吸热反应
化学反应开始时都需要吸收能量
E(拆键) < E(成键),则反应放热
可逆反应若正向放热,则逆向一定吸热
以下说法中不正确的是:
需要加热才能进行的反应一定是吸热反应
化学反应开始时都需要吸收能量
E(拆键) < E(成键),则反应放热
可逆反应若正向放热,则逆向一定吸热
以下说法中不正确的是:
需要加热才能进行的反应一定是吸热反应
化学反应开始时都需要吸收能量
E(拆键) < E(成键),则反应放热
可逆反应若正向放热,则逆向一定吸热
例:H2+I2 2HI,分析该反应的能量变化
以下说法中不正确的是:
需要加热才能进行的反应一定是吸热反应
化学反应开始时都需要吸收能量
E(拆键) < E(成键),则反应放热
可逆反应若正向放热,则逆向一定吸热
例:H2+I2 2HI,分析该反应的能量变化
正反应:拆开H2和I2的键,形成HI键; 逆反应:拆开HI键,形成H2和I2的键。
以下说法中不正确的是:
需要加热才能进行的反应一定是吸热反应
化学反应开始时都需要吸收能量
E(拆键) < E(成键),则反应放热
可逆反应若正向放热,则逆向一定吸热
例:H2+I2 2HI,分析该反应的能量变化
正反应:拆开H2和I2的键,形成HI键; 逆反应:拆开HI键,形成H2和I2的键。
以下说法中不正确的是:
需要加热才能进行的反应一定是吸热反应
化学反应开始时都需要吸收能量
E(拆键) < E(成键),则反应放热
可逆反应若正向放热,则逆向一定吸热
