高中化学人教版(2019)必修 第一册第一章 物质及其变化 第二节 离子反应 课件(18张PPT)
文档属性
| 名称 | 高中化学人教版(2019)必修 第一册第一章 物质及其变化 第二节 离子反应 课件(18张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-06-30 00:00:00 | ||
图片预览





文档简介
(共18张PPT)
离
子
反
应
试剂
是否导电
NaCl
固体
水
氯化钠溶液
不
导
电
不
导
电
导
电
实
验
1
NaCl溶液中自由移动的离子是怎么产生的?
“氯化钠溶解在水中”的微观过程
主
题
一
电
离:化合物在水溶液中解离成自由移动离子的过程
主
题
一
电
离:化合物在水溶液中或熔融状态下解离成自由移动离子的过程
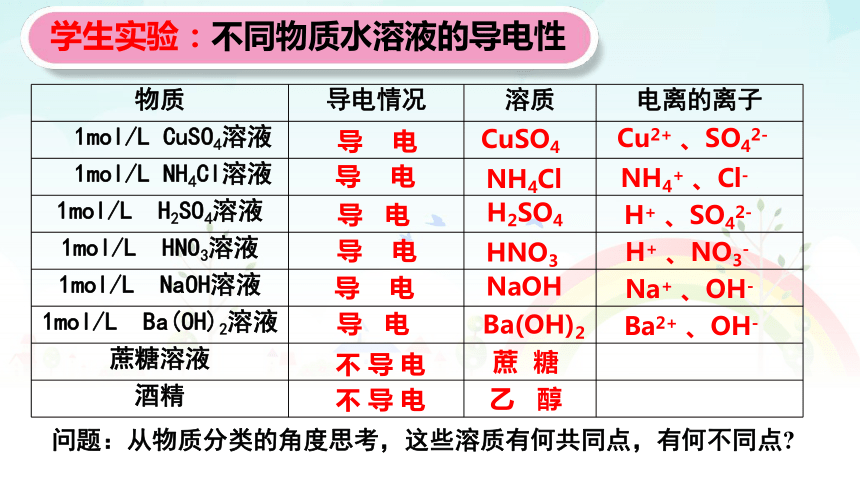
问题:从物质分类的角度思考,这些溶质有何共同点,有何不同点?
学生实验:不同物质水溶液的导电性
物质
导电情况
溶质
电离的离子
1mol/L
CuSO4溶液
1mol/L
NH4Cl溶液
1mol/L
H2SO4溶液
1mol/L
HNO3溶液
1mol/L
NaOH溶液
1mol/L
Ba(OH)2溶液
蔗糖溶液
酒精
不
导
电
不
导
电
导
电
导
电
导
电
导
电
导
电
导
电
蔗
糖
乙
醇
CuSO4
NH4Cl
H2SO4
HNO3
NaOH
Ba(OH)2
Cu2+
、SO42-
NH4+
、Cl-
H+
、SO42-
H+
、NO3-
Na+
、OH-
Ba2+
、OH-
主
题
二
非电解质
电解质
在水溶液中或熔融态下能导电的化合物
在水溶液中和熔融态下都不能导电的化合物
问题探究
1
CO2属于化合物,溶于水也导电,CO2属于电解质吗?
0.5
秒延迟符,无
意义,可删除.
想一想:
下列物质哪些是电解质?哪些是非电解质?哪些能导电?
①Cu
②固态NaCl
③O2
④纯H2SO4⑤BaSO4
⑥酒精水溶液
⑦KOH水溶液
⑧熔融状态KNO3 ⑨葡萄糖
⑩SO2
电解质:
非电解质:
能导电:
②④⑤⑧
⑨
⑩
①⑦⑧
启示:
1、能导电的物质不一定全是电解质。
3、电解质必须是化合物本身能电离出自由移动的离子而导电,不是发生化学反应生成的新物质导电
2、单质和混合物既不是电解质也不是非电解质
0.5
秒延迟符,无
意义,可删除.
电离方程式
等号左边写出化学式;
写
等号右边把化学式拆成阳、阴离子符号,离子所带电荷与相应元素的化合价相同;
拆
阴、阳离子前面配上系数。阴、阳离子所带电荷总数相等;
配
“等号”两边是否“守恒”(质量、电荷)
查
练习书写下列化合物的电离方程式
HCl、H2SO4、HNO3
NaOH、KOH、Ba(OH)2
FeCl3、Mg(NO3)2、(NH4)2SO4
主
题
三
酸
碱
盐
电离时产生的阳离子全部是H+的化合物
电离时产生的阴离子全部是OH-的化合物
酸根离子与金属离子或者铵根离子的化合物
【课后思考】某同学将一种叫硫酸氢钠的物质溶于水中,并分别做了一下实验:
(1)取少量溶液,向其中滴加紫色石蕊试液,溶液变为红色
(2)另取溶液少许,向其中加入BaCl2溶液,有白色沉淀生成
【思考】
(1)写出硫酸氢钠的电离方程式
(2)该同学根据以上分析认为硫酸氢钠应属于一种酸,对此你是否认可?
碱
盐
化合物
按导电性分
电解质
非电解质
活泼金属氧化物
H2O
大多数非金属氧化物
大部分有机物
NH3
(Na2O,Al2O3等)
(微弱导电)
(CO2,SO2等)
CH4
熔融状态下能导电
溶于水能导电
溶于水或熔融时能导电
酒精(C2H5OH)等
蔗糖
(导电)
(不导电)
酸
作业:
1、完成学案上的练习
2、预习下一课时内容
思考:
为什么湿手更易触电?
人手皮肤表面常因出汗而附着少量的氯化钠固体,手被水弄湿后,这些氯化钠溶于水生成自由移动的Na+和Cl-,增强了导电性。
……不用湿手扳开关、换灯泡,插、拔插头,不站在潮湿的桌椅上接触火线……
——初三物理“用电安全”
谢谢同学们的帮助!谢谢各位老师的指导!
离
子
反
应
试剂
是否导电
NaCl
固体
水
氯化钠溶液
不
导
电
不
导
电
导
电
实
验
1
NaCl溶液中自由移动的离子是怎么产生的?
“氯化钠溶解在水中”的微观过程
主
题
一
电
离:化合物在水溶液中解离成自由移动离子的过程
主
题
一
电
离:化合物在水溶液中或熔融状态下解离成自由移动离子的过程
问题:从物质分类的角度思考,这些溶质有何共同点,有何不同点?
学生实验:不同物质水溶液的导电性
物质
导电情况
溶质
电离的离子
1mol/L
CuSO4溶液
1mol/L
NH4Cl溶液
1mol/L
H2SO4溶液
1mol/L
HNO3溶液
1mol/L
NaOH溶液
1mol/L
Ba(OH)2溶液
蔗糖溶液
酒精
不
导
电
不
导
电
导
电
导
电
导
电
导
电
导
电
导
电
蔗
糖
乙
醇
CuSO4
NH4Cl
H2SO4
HNO3
NaOH
Ba(OH)2
Cu2+
、SO42-
NH4+
、Cl-
H+
、SO42-
H+
、NO3-
Na+
、OH-
Ba2+
、OH-
主
题
二
非电解质
电解质
在水溶液中或熔融态下能导电的化合物
在水溶液中和熔融态下都不能导电的化合物
问题探究
1
CO2属于化合物,溶于水也导电,CO2属于电解质吗?
0.5
秒延迟符,无
意义,可删除.
想一想:
下列物质哪些是电解质?哪些是非电解质?哪些能导电?
①Cu
②固态NaCl
③O2
④纯H2SO4⑤BaSO4
⑥酒精水溶液
⑦KOH水溶液
⑧熔融状态KNO3 ⑨葡萄糖
⑩SO2
电解质:
非电解质:
能导电:
②④⑤⑧
⑨
⑩
①⑦⑧
启示:
1、能导电的物质不一定全是电解质。
3、电解质必须是化合物本身能电离出自由移动的离子而导电,不是发生化学反应生成的新物质导电
2、单质和混合物既不是电解质也不是非电解质
0.5
秒延迟符,无
意义,可删除.
电离方程式
等号左边写出化学式;
写
等号右边把化学式拆成阳、阴离子符号,离子所带电荷与相应元素的化合价相同;
拆
阴、阳离子前面配上系数。阴、阳离子所带电荷总数相等;
配
“等号”两边是否“守恒”(质量、电荷)
查
练习书写下列化合物的电离方程式
HCl、H2SO4、HNO3
NaOH、KOH、Ba(OH)2
FeCl3、Mg(NO3)2、(NH4)2SO4
主
题
三
酸
碱
盐
电离时产生的阳离子全部是H+的化合物
电离时产生的阴离子全部是OH-的化合物
酸根离子与金属离子或者铵根离子的化合物
【课后思考】某同学将一种叫硫酸氢钠的物质溶于水中,并分别做了一下实验:
(1)取少量溶液,向其中滴加紫色石蕊试液,溶液变为红色
(2)另取溶液少许,向其中加入BaCl2溶液,有白色沉淀生成
【思考】
(1)写出硫酸氢钠的电离方程式
(2)该同学根据以上分析认为硫酸氢钠应属于一种酸,对此你是否认可?
碱
盐
化合物
按导电性分
电解质
非电解质
活泼金属氧化物
H2O
大多数非金属氧化物
大部分有机物
NH3
(Na2O,Al2O3等)
(微弱导电)
(CO2,SO2等)
CH4
熔融状态下能导电
溶于水能导电
溶于水或熔融时能导电
酒精(C2H5OH)等
蔗糖
(导电)
(不导电)
酸
作业:
1、完成学案上的练习
2、预习下一课时内容
思考:
为什么湿手更易触电?
人手皮肤表面常因出汗而附着少量的氯化钠固体,手被水弄湿后,这些氯化钠溶于水生成自由移动的Na+和Cl-,增强了导电性。
……不用湿手扳开关、换灯泡,插、拔插头,不站在潮湿的桌椅上接触火线……
——初三物理“用电安全”
谢谢同学们的帮助!谢谢各位老师的指导!
