专题《生活中的酸碱盐》复习
图片预览










文档简介
(共33张PPT)
小林个人资料介绍
小林去年也和你们一样,是一名九年级的学生,挺喜欢科学,对生活中的事情和现象老是喜欢问个为什么.而且在家经常摆弄一些瓶瓶罐罐,做些小实验,期间也遇到了很多的疑惑,现在大家不妨来看看他在生活中遇到的一些问题。你能帮助他解决?
Na
H
O
S
装饰花瓶
(妈妈的要求:选择花瓶内的两种或两种以上元素组成最多的化合物并进行分类,每一类物质代表一朵花插入花瓶内)
一天小林放学回到家看到妈妈在花瓶上插花,
连忙放下书包忙开。妈妈为了考考她,对装饰花瓶提了个 小小的 要求。你猜他会如何装饰这个特殊的花瓶?
碱
金属氧化物
盐
酸
非金属
氧化物
3月2日,318国道某路段发生翻车事故,车上装载的20吨浓盐酸从已翻倒的车顶上的出气阀中流了出来。沿着小溪缓慢地向下游流动,所经之处浓烟弥漫,草木毁坏。浓盐酸流经的鱼塘,水面浮起了许多鱼的尸体。过往车辆全都不敢通过浓烟区,318国道严重堵车 。事发后,省环保局派出监测专家和技术人员,赶赴现场调查处理。
浓雾
浓雾
小林看后纳闷:
1、为什么浓盐酸流经之处会浓雾弥漫?
2、池塘中鱼儿死亡的原因,有哪些可能?
可能1:浓盐酸有腐蚀性,使鱼被腐蚀而死亡
可能2:浓盐酸具有酸性,改变了河水的PH,使鱼无法生存
3、为什么过往车辆全都不敢通过雾区?
因为盐酸会与金属反应,腐蚀车上的金属制品,还会对车内人员产生伤害
4、小林想知道周围的河水是否受到盐酸的污染,请你告诉他该如何检测.
5 现场追踪报道:小林想消防官兵到场后
另一方面派人穿着防化服、佩带空气呼吸器等个人防护装备,深入污染区在翻车地点小溪下游筑起了4道石灰坝,并投放片碱(NaOH)、石灰[CaO和Ca(OH)2]进行处理。
消防官兵到场后一方面迅速出动2支水枪对酸雾进行稀释;
复分解反应为什么能够发生呢? 这是因为在这些反应物中含有一些“特殊”的阴、阳离子,它们能相互结合,形成水,沉淀或气体。如Na2SO4+BaCl2=2NaCl+BaSO4 中,实际参加反应的离子是Ba2+和SO42-而Cl-、Na+则是“旁观者”,并没有参加反应。
你能告诉小林,片碱和熟石灰与盐酸的反应中,实际参加反应的离子是哪些吗?
为了进一步了解片碱和熟石灰能消除盐酸带来污染的原因,小林查阅了课外资料:
+
Na+
OH-
H+
Cl-
Na+
H2O
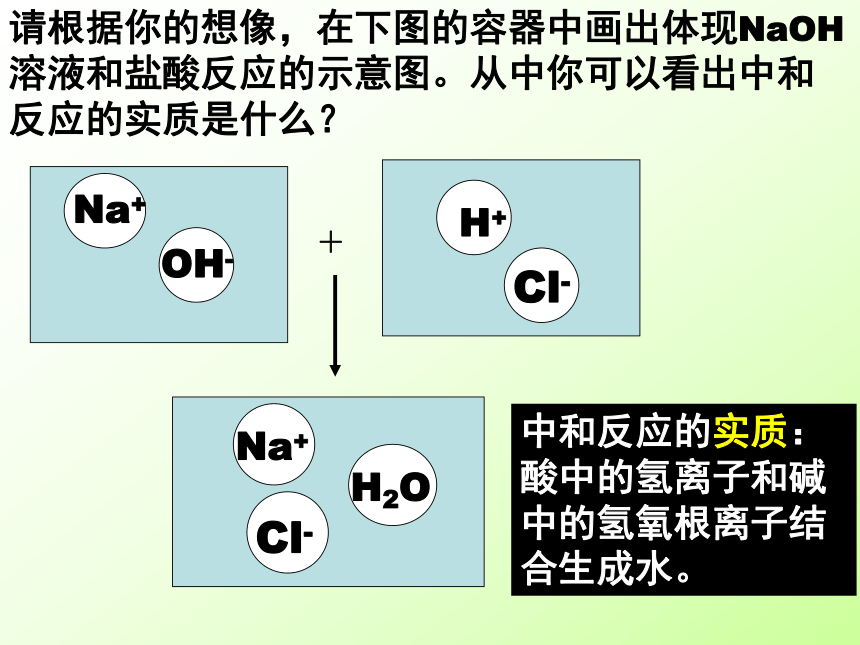
请根据你的想像,在下图的容器中画出体现NaOH溶液和盐酸反应的示意图。从中你可以看出中和反应的实质是什么?
中和反应的实质:酸中的氢离子和碱中的氢氧根离子结合生成水。
Cl-
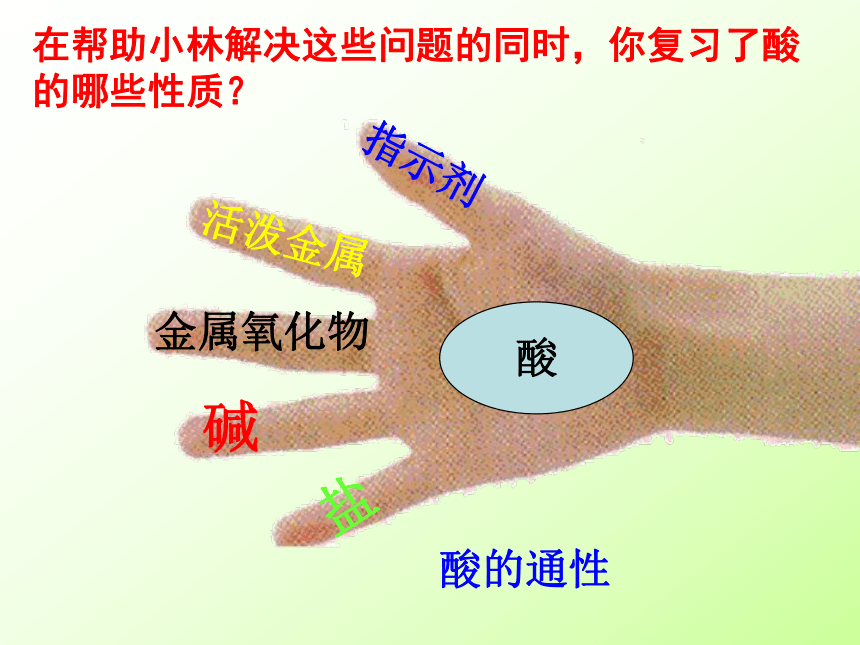
酸的通性
指示剂
活泼金属
金属氧化物
碱
盐
酸
在帮助小林解决这些问题的同时,你复习了酸的哪些性质?
一次,小林在家吃饼干时发现饼干变潮了,在包装袋中发现一包装有白色颗粒状固体的小纸袋,上面写着“干燥剂,主要成分生石灰”,小林认为可能是干燥剂失效导致饼干变潮的.为了证实自己的猜想,对其进行了探究,其过程如下,请你帮他完成剩余的疑难。
问题和猜想 实验步骤 实验现象 实验结论
问题1:小纸袋中的物质能否继续作干燥剂? 取足量小纸袋中的固体放入烧杯中,加水溶解,触摸杯壁 不能做干燥剂(CaO完全变质)
问题2:猜想变质后物质可能是什么
烧杯壁
不暖
碱
指 示 剂
酸
非金属
氧化物
盐
验证变质产物是Ca(OH)2 时你回顾了碱的哪些性质?
可溶性碱的通性
小林虽然很调皮,但在家会经常帮助妈妈做家务,还能烧出一桌的好菜。有一次炒菜时他发现炒的菜不咸反而有一种涩味.你猜他错用了哪种物质 你能帮助小林利用简单的方法鉴别食盐和这种物质吗
碳酸钠:Na2CO3
实验设计:
实验原理 实验步骤 实验现象和结论
方案一
方案二
方案三
鉴别的试剂:AgNO3和稀HNO3, CaCl2, Ca(OH)2, 稀盐酸, 酸碱指示剂, PH试纸等
区别:Na2CO3和NaCl
从中你知道了NaCl和Na2CO3有怎样的性质?
一次小林和同学们一起在实验室中做实验,实验时把废液全部倒在废液缸中,废液中含有ZnCl2、FeCl2、CuCl2。老师说小林你能想办法把废液中的金属铜全部回收吗?小林想了想,他先向其中加入稍过量的铁粉,充分反应后过滤,你认为滤液中含有的阳离子是_________,滤渣中含有_________,要得到纯净的金属铜,小林需要继续完成的实验是____________________________________ 。
Zn2+ Fe2+
Fe Cu
在滤渣中加入适量的稀盐酸,再过滤、洗涤、干燥
一天小林到摄影店去拍照片,得知废弃的定影液中含有一定量的AgNO3,他想银是贵重的金属,如何将银以单质的形式全部回收?他进行了如下活动:
(1)设计方案:①加入比银活泼的金属,②除去金属混合物中的杂质
(2)加入合适的金属:①过量的铜 ②过量的铁
你认为哪个更合适?原因是 : ,该方案的化学方程式: 。
(3)除去银粉中的混有的金属应加入 ,化学方程式是 ,
(4)实验过程: ①定影液加入过量活泼金属 操作a
金属混合物+溶液A
加适量试剂 操作b 金属银+溶液B
盐
酸
金属
碱
盐
盐的化学性质
小林的烦恼
暑假时,小林到他外婆家玩,发现附近出现了一个新的化工厂,而环境却变差了。工厂的废水未经处理就直接排放到附近的河道里,那条清澈见底的河水就变成了这样:
经调查,原来化工厂的ABCD四个车间排放出的废水中分别含有CuCl2、HCl、Na2CO3、NaOH中的一种,后来工厂对废水进行了如下处理:
1.将A废水与B的蓝色废水通入第一反应池,产生蓝色沉淀。
2.将C废水与D的酸性废水通入第二反应池,产生大量气泡。
3.将第一反应池上层的碱性废水与第二反应池流出的酸性废水通入第三反应池,最终废水显中性,再向外排放。
问:1.推断ABCD各车间废水分别是什么?
2.最终排出的废水中含有的溶质是什么?
3.写出各池中反应的化学方程式
2NaOH+CuCl2=Cu(OH)2 +2NaCl
Na2CO3+2HCl=2NaCl+CO2 +H2O
NaOH+HCl=NaCl+H2O
NaCl
3.写出各池中反应的化学方程式
2.最终排出的废水中含有的溶质是什么?
A:NaOH B: CuCl2
C: Na2CO3 D: HCl
问:1.推断ABCD各车间废水分别是什么?
使用这套方案一段时间后,外婆家附近的河水又变清澈了。
通过本节课的学习,你有什么收获、体会?
复分解反应发生的条件
1.酸 + 碱 → 盐 + 水
2.酸 + 盐 → 新酸 + 新盐
3.碱 + 盐 → 新碱+ 新盐
4.盐 + 盐 → 新盐+另一种新盐
生成物有沉淀、
气体或水
(可溶)
(可溶)
(可溶)
(可溶)
1、 Cu(OH) 2 +H 2 SO 4 =Na 2 SO 4 +2H 2 O
2、CaCO 3 +2HCl=CaCl 2 +H 2 O+CO 2
Na 2 SO 4 +2HCl=2NaCl+H 2 SO 4
3、K2 CO 3 +Ca(OH) 2 =CaCO 3 +2KOH
2Fe(OH) 3+3CuSO 4 =Fe 2 (SO 4) 3+3Cu(OH) 2
NaOH+KNO 3=NaNO 3+KOH
4、CuSO 4 +BaCO 3 =CuCO 3 +BaSO 4
BaCl 2 + 2AgNO 3 =Ba(NO 3 ) 2+2AgCl
判断下列化学方程式是否正确 并说明理由
想一想
部分置换反应发生的条件:
1. 金属 + 酸 → 盐 + 氢气
(H前)
2. 金属 + 盐 → 新金属 + 新盐
(前换后)
(稀HCl或稀H2SO4)
(可溶性盐)
按金属活动性顺序,一种活动性较强的金属能把另一中活动性较弱的金属从它的盐的水溶液中置换出来,排在氢前面的金属可以把酸中的氢置换出来。
有一些不法分子以铜锌合金(黄铜)假冒黄金进行诈骗。 请你至少设计2个实验方案,证明某黄色金属是真金还是黄铜。
自己动手腌制松花蛋
传统松花蛋的腌制会使松花蛋中含较多的铅元素,大量食用会危害人体健康。现在市面上出售的无铅松花蛋为我们解决了这个问题,其具体配料如下: NaOH 6克、NaCl 10克、Ca(OH)2 59克、茶叶 5克、H2O 210毫升,然后将蛋直接放入液体中泡制,你不妨动手试一试。
同时查阅资料了解该方法的化学原理。
谢谢你们的参与!
为你们的出色表现喝彩!
这天小林看见爸爸带着胶皮手套正在用一种白色粉末的水溶液清洗油烟机,一问才知道爸爸是在用附近化工厂买来的氢氧化钠在清洗,他很想知道买来的氢氧化钠是否纯净,于是他查阅了课外资料:
查阅资料:①在化工生产中,原料往往不能全部转化成产品;②工业上常用电解纯净的饱和食盐水的方法来得到烧碱溶液,再经过浓缩、蒸发等步骤制造固体烧碱; ③氯化银不溶于稀硝酸。
(1)猜测一下,该烧碱样品中可能含有哪些杂质?
(2)设计一个实验方案,来证实你的猜测是正确的。
(1)猜测____________________
猜测的依________________
样品溶液
向溶液中加入:
产生白色沉淀
过滤,向滤液中加入:
继续向溶液中加入:
结论
结论
结论
产生白色沉淀
无色酚酞变红
Ba(NO3)2溶液
过量
Na2CO3
无色酚酞
AgNO3和稀硝酸
NaOH
NaCl
样品中含有
小林个人资料介绍
小林去年也和你们一样,是一名九年级的学生,挺喜欢科学,对生活中的事情和现象老是喜欢问个为什么.而且在家经常摆弄一些瓶瓶罐罐,做些小实验,期间也遇到了很多的疑惑,现在大家不妨来看看他在生活中遇到的一些问题。你能帮助他解决?
Na
H
O
S
装饰花瓶
(妈妈的要求:选择花瓶内的两种或两种以上元素组成最多的化合物并进行分类,每一类物质代表一朵花插入花瓶内)
一天小林放学回到家看到妈妈在花瓶上插花,
连忙放下书包忙开。妈妈为了考考她,对装饰花瓶提了个 小小的 要求。你猜他会如何装饰这个特殊的花瓶?
碱
金属氧化物
盐
酸
非金属
氧化物
3月2日,318国道某路段发生翻车事故,车上装载的20吨浓盐酸从已翻倒的车顶上的出气阀中流了出来。沿着小溪缓慢地向下游流动,所经之处浓烟弥漫,草木毁坏。浓盐酸流经的鱼塘,水面浮起了许多鱼的尸体。过往车辆全都不敢通过浓烟区,318国道严重堵车 。事发后,省环保局派出监测专家和技术人员,赶赴现场调查处理。
浓雾
浓雾
小林看后纳闷:
1、为什么浓盐酸流经之处会浓雾弥漫?
2、池塘中鱼儿死亡的原因,有哪些可能?
可能1:浓盐酸有腐蚀性,使鱼被腐蚀而死亡
可能2:浓盐酸具有酸性,改变了河水的PH,使鱼无法生存
3、为什么过往车辆全都不敢通过雾区?
因为盐酸会与金属反应,腐蚀车上的金属制品,还会对车内人员产生伤害
4、小林想知道周围的河水是否受到盐酸的污染,请你告诉他该如何检测.
5 现场追踪报道:小林想消防官兵到场后
另一方面派人穿着防化服、佩带空气呼吸器等个人防护装备,深入污染区在翻车地点小溪下游筑起了4道石灰坝,并投放片碱(NaOH)、石灰[CaO和Ca(OH)2]进行处理。
消防官兵到场后一方面迅速出动2支水枪对酸雾进行稀释;
复分解反应为什么能够发生呢? 这是因为在这些反应物中含有一些“特殊”的阴、阳离子,它们能相互结合,形成水,沉淀或气体。如Na2SO4+BaCl2=2NaCl+BaSO4 中,实际参加反应的离子是Ba2+和SO42-而Cl-、Na+则是“旁观者”,并没有参加反应。
你能告诉小林,片碱和熟石灰与盐酸的反应中,实际参加反应的离子是哪些吗?
为了进一步了解片碱和熟石灰能消除盐酸带来污染的原因,小林查阅了课外资料:
+
Na+
OH-
H+
Cl-
Na+
H2O
请根据你的想像,在下图的容器中画出体现NaOH溶液和盐酸反应的示意图。从中你可以看出中和反应的实质是什么?
中和反应的实质:酸中的氢离子和碱中的氢氧根离子结合生成水。
Cl-
酸的通性
指示剂
活泼金属
金属氧化物
碱
盐
酸
在帮助小林解决这些问题的同时,你复习了酸的哪些性质?
一次,小林在家吃饼干时发现饼干变潮了,在包装袋中发现一包装有白色颗粒状固体的小纸袋,上面写着“干燥剂,主要成分生石灰”,小林认为可能是干燥剂失效导致饼干变潮的.为了证实自己的猜想,对其进行了探究,其过程如下,请你帮他完成剩余的疑难。
问题和猜想 实验步骤 实验现象 实验结论
问题1:小纸袋中的物质能否继续作干燥剂? 取足量小纸袋中的固体放入烧杯中,加水溶解,触摸杯壁 不能做干燥剂(CaO完全变质)
问题2:猜想变质后物质可能是什么
烧杯壁
不暖
碱
指 示 剂
酸
非金属
氧化物
盐
验证变质产物是Ca(OH)2 时你回顾了碱的哪些性质?
可溶性碱的通性
小林虽然很调皮,但在家会经常帮助妈妈做家务,还能烧出一桌的好菜。有一次炒菜时他发现炒的菜不咸反而有一种涩味.你猜他错用了哪种物质 你能帮助小林利用简单的方法鉴别食盐和这种物质吗
碳酸钠:Na2CO3
实验设计:
实验原理 实验步骤 实验现象和结论
方案一
方案二
方案三
鉴别的试剂:AgNO3和稀HNO3, CaCl2, Ca(OH)2, 稀盐酸, 酸碱指示剂, PH试纸等
区别:Na2CO3和NaCl
从中你知道了NaCl和Na2CO3有怎样的性质?
一次小林和同学们一起在实验室中做实验,实验时把废液全部倒在废液缸中,废液中含有ZnCl2、FeCl2、CuCl2。老师说小林你能想办法把废液中的金属铜全部回收吗?小林想了想,他先向其中加入稍过量的铁粉,充分反应后过滤,你认为滤液中含有的阳离子是_________,滤渣中含有_________,要得到纯净的金属铜,小林需要继续完成的实验是____________________________________ 。
Zn2+ Fe2+
Fe Cu
在滤渣中加入适量的稀盐酸,再过滤、洗涤、干燥
一天小林到摄影店去拍照片,得知废弃的定影液中含有一定量的AgNO3,他想银是贵重的金属,如何将银以单质的形式全部回收?他进行了如下活动:
(1)设计方案:①加入比银活泼的金属,②除去金属混合物中的杂质
(2)加入合适的金属:①过量的铜 ②过量的铁
你认为哪个更合适?原因是 : ,该方案的化学方程式: 。
(3)除去银粉中的混有的金属应加入 ,化学方程式是 ,
(4)实验过程: ①定影液加入过量活泼金属 操作a
金属混合物+溶液A
加适量试剂 操作b 金属银+溶液B
盐
酸
金属
碱
盐
盐的化学性质
小林的烦恼
暑假时,小林到他外婆家玩,发现附近出现了一个新的化工厂,而环境却变差了。工厂的废水未经处理就直接排放到附近的河道里,那条清澈见底的河水就变成了这样:
经调查,原来化工厂的ABCD四个车间排放出的废水中分别含有CuCl2、HCl、Na2CO3、NaOH中的一种,后来工厂对废水进行了如下处理:
1.将A废水与B的蓝色废水通入第一反应池,产生蓝色沉淀。
2.将C废水与D的酸性废水通入第二反应池,产生大量气泡。
3.将第一反应池上层的碱性废水与第二反应池流出的酸性废水通入第三反应池,最终废水显中性,再向外排放。
问:1.推断ABCD各车间废水分别是什么?
2.最终排出的废水中含有的溶质是什么?
3.写出各池中反应的化学方程式
2NaOH+CuCl2=Cu(OH)2 +2NaCl
Na2CO3+2HCl=2NaCl+CO2 +H2O
NaOH+HCl=NaCl+H2O
NaCl
3.写出各池中反应的化学方程式
2.最终排出的废水中含有的溶质是什么?
A:NaOH B: CuCl2
C: Na2CO3 D: HCl
问:1.推断ABCD各车间废水分别是什么?
使用这套方案一段时间后,外婆家附近的河水又变清澈了。
通过本节课的学习,你有什么收获、体会?
复分解反应发生的条件
1.酸 + 碱 → 盐 + 水
2.酸 + 盐 → 新酸 + 新盐
3.碱 + 盐 → 新碱+ 新盐
4.盐 + 盐 → 新盐+另一种新盐
生成物有沉淀、
气体或水
(可溶)
(可溶)
(可溶)
(可溶)
1、 Cu(OH) 2 +H 2 SO 4 =Na 2 SO 4 +2H 2 O
2、CaCO 3 +2HCl=CaCl 2 +H 2 O+CO 2
Na 2 SO 4 +2HCl=2NaCl+H 2 SO 4
3、K2 CO 3 +Ca(OH) 2 =CaCO 3 +2KOH
2Fe(OH) 3+3CuSO 4 =Fe 2 (SO 4) 3+3Cu(OH) 2
NaOH+KNO 3=NaNO 3+KOH
4、CuSO 4 +BaCO 3 =CuCO 3 +BaSO 4
BaCl 2 + 2AgNO 3 =Ba(NO 3 ) 2+2AgCl
判断下列化学方程式是否正确 并说明理由
想一想
部分置换反应发生的条件:
1. 金属 + 酸 → 盐 + 氢气
(H前)
2. 金属 + 盐 → 新金属 + 新盐
(前换后)
(稀HCl或稀H2SO4)
(可溶性盐)
按金属活动性顺序,一种活动性较强的金属能把另一中活动性较弱的金属从它的盐的水溶液中置换出来,排在氢前面的金属可以把酸中的氢置换出来。
有一些不法分子以铜锌合金(黄铜)假冒黄金进行诈骗。 请你至少设计2个实验方案,证明某黄色金属是真金还是黄铜。
自己动手腌制松花蛋
传统松花蛋的腌制会使松花蛋中含较多的铅元素,大量食用会危害人体健康。现在市面上出售的无铅松花蛋为我们解决了这个问题,其具体配料如下: NaOH 6克、NaCl 10克、Ca(OH)2 59克、茶叶 5克、H2O 210毫升,然后将蛋直接放入液体中泡制,你不妨动手试一试。
同时查阅资料了解该方法的化学原理。
谢谢你们的参与!
为你们的出色表现喝彩!
这天小林看见爸爸带着胶皮手套正在用一种白色粉末的水溶液清洗油烟机,一问才知道爸爸是在用附近化工厂买来的氢氧化钠在清洗,他很想知道买来的氢氧化钠是否纯净,于是他查阅了课外资料:
查阅资料:①在化工生产中,原料往往不能全部转化成产品;②工业上常用电解纯净的饱和食盐水的方法来得到烧碱溶液,再经过浓缩、蒸发等步骤制造固体烧碱; ③氯化银不溶于稀硝酸。
(1)猜测一下,该烧碱样品中可能含有哪些杂质?
(2)设计一个实验方案,来证实你的猜测是正确的。
(1)猜测____________________
猜测的依________________
样品溶液
向溶液中加入:
产生白色沉淀
过滤,向滤液中加入:
继续向溶液中加入:
结论
结论
结论
产生白色沉淀
无色酚酞变红
Ba(NO3)2溶液
过量
Na2CO3
无色酚酞
AgNO3和稀硝酸
NaOH
NaCl
样品中含有
