苏教版高二化学选修 化学反应原理专题1第一单元 化学反应中的热效应 课件 (共23张PPT)
文档属性
| 名称 | 苏教版高二化学选修 化学反应原理专题1第一单元 化学反应中的热效应 课件 (共23张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-07-04 00:00:00 | ||
图片预览






文档简介
(共23张PPT)
学起于思,思源于疑。
--------陈献章(明代学者)
化学反应中的热效应
分组实验
实验1:向一支试管中放入用砂纸打磨光亮的镁
条,加入1mL2mol/L的盐酸,用手触
摸试管外壁,有什么感觉?
实验2:在完好的塑料袋中依次加入2药匙氢氧
化钡晶体、1药匙氯化铵,排出空气,扎
紧袋口,揉搓使之充分混合,用手触摸塑
料袋,有什么感觉?
从热量变化角度看化学反应
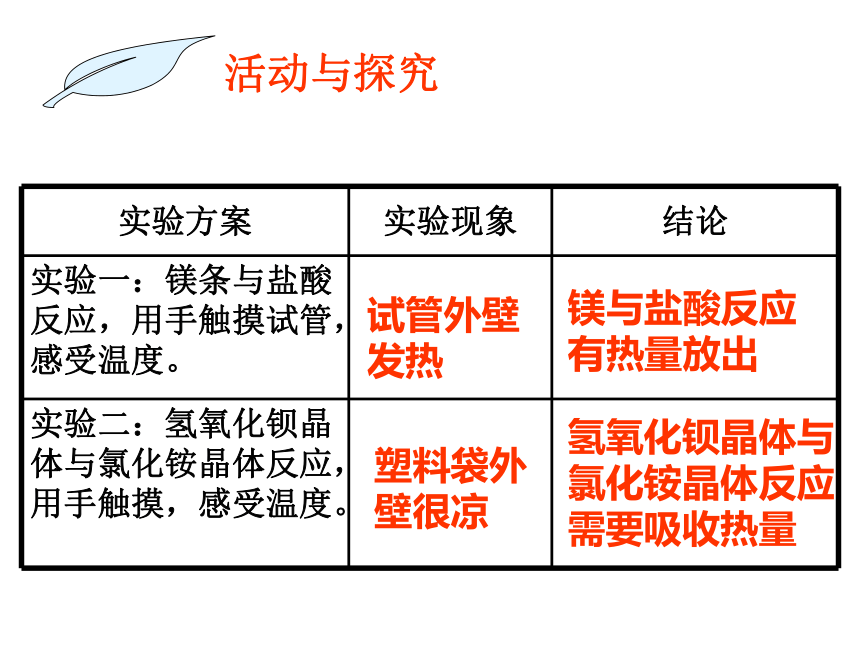
试管外壁
发热
镁与盐酸反应有热量放出
塑料袋外壁很凉
氢氧化钡晶体与氯化铵晶体反应需要吸收热量
实验方案
实验现象
结论
实验一:镁条与盐酸反应,用手触摸试管,感受温度。
实验二:氢氧化钡晶体与氯化铵晶体反应,用手触摸,感受温度。
吸热反应:吸收热量的化学反应。
一、放热反应与吸热反应
放热反应:放出热量的化学反应。
判断下列反应是放热反应还是吸热反应:
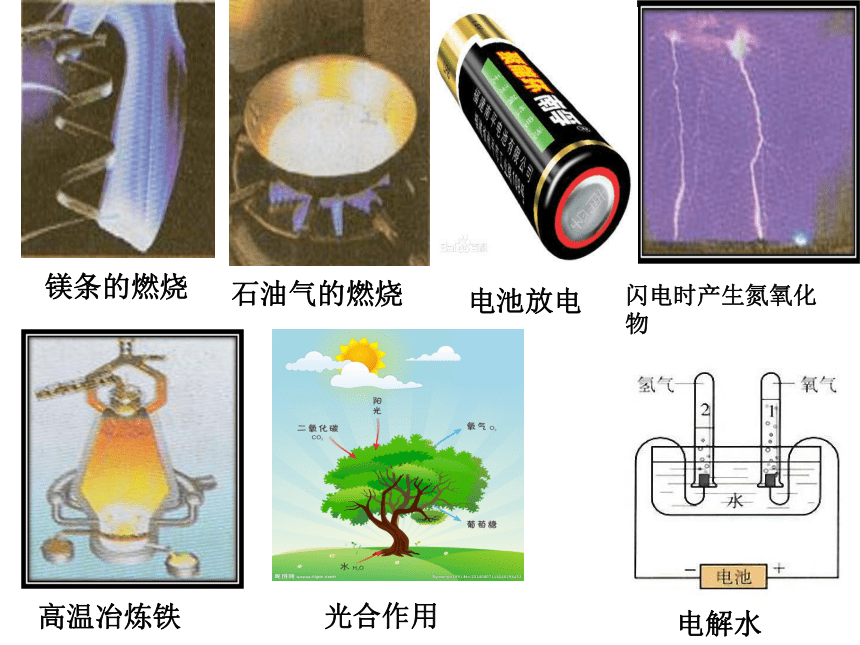
(1)镁条的燃烧;
(2)高温下木炭与二氧化碳分生成一氧化碳;
(3)氧化钙与水反应。
(4)盐酸和氢氧化钠溶液反应
放热反应
吸热反应
放热反应
放热反应
问题解决
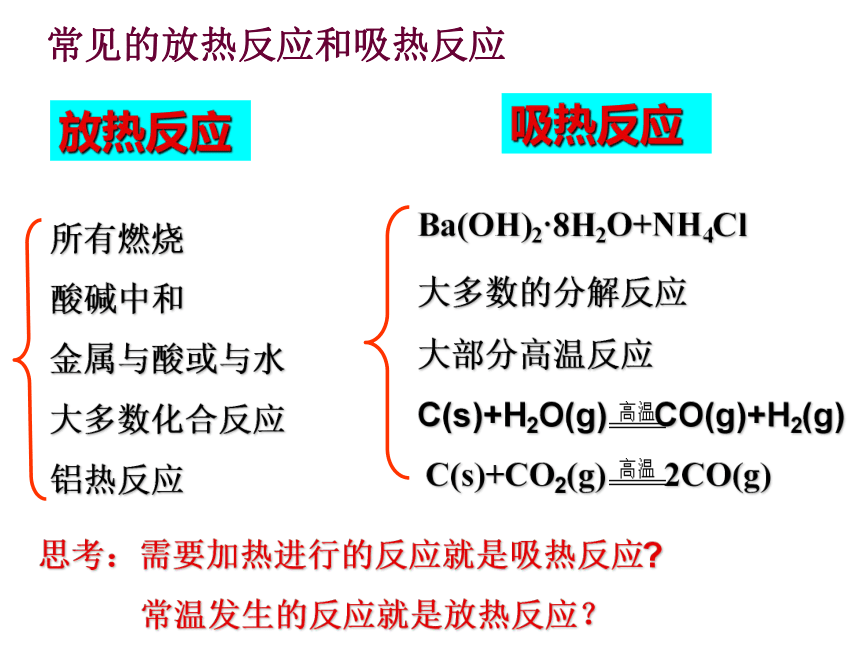
常见的放热反应和吸热反应
放热反应
吸热反应
思考:需要加热进行的反应就是吸热反应?
常温发生的反应就是放热反应?
交流与讨论
化学反应中为什么会有能量的变化?
宏观:
反应物和生成物所具有的能量不同.
从宏观角度分析
练习:
下列说法中错误的是(
)
A、化学反应过程中的能量变化,遵循能量守恒定律
B、化学反应中能量变化,除了热量外,还可以是光
能、电能等。
C、需要加热才能进行的化学反应一定是吸热反应
D、反应物的总能量高于生成物的总能量时,发生放
热反应。
C
微观
化学反应的实质:旧键的断裂、新键的形成
若断键吸收能量>成键放出能量
,
反应;
若断键吸收能量<成键放出能量,
反应。
吸热
放热
判断:
中热量变化?
化学键角度(微观)
反应热
(1)定义:在化学反应中放出或吸收的热量
(2)符号:
(3)单位:
△H
kJ
?mol-1
二、热化学方程式
1.定义:表明反应放出或吸收的热量的化学方程式
点燃
观察以下热化学反应方程式,你发现了什么?
2H2(g)
+
O2(g)==2H2O(g)
△H=-483.6
kJ/mol
2H2(g)
+
O2(g)==
2H2O(l)
△H=-571.6
kJ/mol
结论:同种物质聚集状态不同,能量不同
2H2(g)
+
O2(g)==
2H2O(l)
△H=-571.6
kJ/mol
H2(g)
+1/2O2(g)==
H2O(l)
△H=-285.8
kJ/mol
结论:
△H
的值与化学计量数成正比
化学计量数只表示物质的量,可用分数
2.热化学方程式的书写步骤
(1)写出正确的化学方程式
(2)标明各物质的聚集状态
(3)注明反应热
△H
“—”表示放热,“+”表示吸热,单位:kJ/mol。
①2SO2
+
O2
=
2SO3
△H
=
-196
.
6kJ
?
mol-1
课堂练习:
③
C(s)
+
O2(g)
=
CO2
(g)
△H
=
+
393
.6kJ
?
mol-1
判断下列热化学反应方程式书写是否正确?
×
×
×
例1.
已知每1
mol
碳完全燃烧生成二氧化碳时将放出393.6kJ热量,写出该反应的热化学方程式。
C(s)+O2(g)=CO2(g);△H=-393.6kJ/mol
例2.
已知每1
mol
甲烷完全燃烧生成二氧化碳和液态水时将放出889.6kJ热量,写出该反应的热化学方程式。
CH4(g)
+2O2(g)
=
CO2(g)
+
2H2O(l);△H
=-889.6kJ/mol
练一练:写出下列反应的热化学方程式
1.
1mol碳酸钙完全分解生成1mol
CaO和1mol
CO2气体,吸收178.5kJ热量。
2.
6g碳在氧气中完全燃烧,生成CO2气体,放出196.8kJ热量。
3.
已知2H2(g)
+O2(g)
=
2H2O(l)
△H
=-571.6
kJ/mol,
则反应H2(g)
+1/2
O2(g)
=
H2O(l)
△H
=?
2H2O(l)
=
2H2(g)
+O2(g)
△H
=?
B
5、
C金刚石(S)+O2(g)
=
CO2(g)
△H=-
395.5
KJ
?mol-1
(1)
C石墨(S)
+
O2(g)
=
CO2(g)
△H=-
393.4
KJ
?mol-1
(2)
写出石墨转化为金刚石方程式,并判断哪一种物质更稳
定。
石墨能量更低,更稳定。
C石墨(S)
=
C金刚石(S)
△H=+2.1
KJ
?mol-1
通过这节课你学到了什么?
1.能量转化的方式,特别是化学能与
热能的相互转化。
2.学会判定放热反应和吸热反应,学会热化学方程式的书写。
3.明确化学键的断裂和形成是化学反应中能量变化的主要原因。
学起于思,思源于疑。
--------陈献章(明代学者)
化学反应中的热效应
分组实验
实验1:向一支试管中放入用砂纸打磨光亮的镁
条,加入1mL2mol/L的盐酸,用手触
摸试管外壁,有什么感觉?
实验2:在完好的塑料袋中依次加入2药匙氢氧
化钡晶体、1药匙氯化铵,排出空气,扎
紧袋口,揉搓使之充分混合,用手触摸塑
料袋,有什么感觉?
从热量变化角度看化学反应
试管外壁
发热
镁与盐酸反应有热量放出
塑料袋外壁很凉
氢氧化钡晶体与氯化铵晶体反应需要吸收热量
实验方案
实验现象
结论
实验一:镁条与盐酸反应,用手触摸试管,感受温度。
实验二:氢氧化钡晶体与氯化铵晶体反应,用手触摸,感受温度。
吸热反应:吸收热量的化学反应。
一、放热反应与吸热反应
放热反应:放出热量的化学反应。
判断下列反应是放热反应还是吸热反应:
(1)镁条的燃烧;
(2)高温下木炭与二氧化碳分生成一氧化碳;
(3)氧化钙与水反应。
(4)盐酸和氢氧化钠溶液反应
放热反应
吸热反应
放热反应
放热反应
问题解决
常见的放热反应和吸热反应
放热反应
吸热反应
思考:需要加热进行的反应就是吸热反应?
常温发生的反应就是放热反应?
交流与讨论
化学反应中为什么会有能量的变化?
宏观:
反应物和生成物所具有的能量不同.
从宏观角度分析
练习:
下列说法中错误的是(
)
A、化学反应过程中的能量变化,遵循能量守恒定律
B、化学反应中能量变化,除了热量外,还可以是光
能、电能等。
C、需要加热才能进行的化学反应一定是吸热反应
D、反应物的总能量高于生成物的总能量时,发生放
热反应。
C
微观
化学反应的实质:旧键的断裂、新键的形成
若断键吸收能量>成键放出能量
,
反应;
若断键吸收能量<成键放出能量,
反应。
吸热
放热
判断:
中热量变化?
化学键角度(微观)
反应热
(1)定义:在化学反应中放出或吸收的热量
(2)符号:
(3)单位:
△H
kJ
?mol-1
二、热化学方程式
1.定义:表明反应放出或吸收的热量的化学方程式
点燃
观察以下热化学反应方程式,你发现了什么?
2H2(g)
+
O2(g)==2H2O(g)
△H=-483.6
kJ/mol
2H2(g)
+
O2(g)==
2H2O(l)
△H=-571.6
kJ/mol
结论:同种物质聚集状态不同,能量不同
2H2(g)
+
O2(g)==
2H2O(l)
△H=-571.6
kJ/mol
H2(g)
+1/2O2(g)==
H2O(l)
△H=-285.8
kJ/mol
结论:
△H
的值与化学计量数成正比
化学计量数只表示物质的量,可用分数
2.热化学方程式的书写步骤
(1)写出正确的化学方程式
(2)标明各物质的聚集状态
(3)注明反应热
△H
“—”表示放热,“+”表示吸热,单位:kJ/mol。
①2SO2
+
O2
=
2SO3
△H
=
-196
.
6kJ
?
mol-1
课堂练习:
③
C(s)
+
O2(g)
=
CO2
(g)
△H
=
+
393
.6kJ
?
mol-1
判断下列热化学反应方程式书写是否正确?
×
×
×
例1.
已知每1
mol
碳完全燃烧生成二氧化碳时将放出393.6kJ热量,写出该反应的热化学方程式。
C(s)+O2(g)=CO2(g);△H=-393.6kJ/mol
例2.
已知每1
mol
甲烷完全燃烧生成二氧化碳和液态水时将放出889.6kJ热量,写出该反应的热化学方程式。
CH4(g)
+2O2(g)
=
CO2(g)
+
2H2O(l);△H
=-889.6kJ/mol
练一练:写出下列反应的热化学方程式
1.
1mol碳酸钙完全分解生成1mol
CaO和1mol
CO2气体,吸收178.5kJ热量。
2.
6g碳在氧气中完全燃烧,生成CO2气体,放出196.8kJ热量。
3.
已知2H2(g)
+O2(g)
=
2H2O(l)
△H
=-571.6
kJ/mol,
则反应H2(g)
+1/2
O2(g)
=
H2O(l)
△H
=?
2H2O(l)
=
2H2(g)
+O2(g)
△H
=?
B
5、
C金刚石(S)+O2(g)
=
CO2(g)
△H=-
395.5
KJ
?mol-1
(1)
C石墨(S)
+
O2(g)
=
CO2(g)
△H=-
393.4
KJ
?mol-1
(2)
写出石墨转化为金刚石方程式,并判断哪一种物质更稳
定。
石墨能量更低,更稳定。
C石墨(S)
=
C金刚石(S)
△H=+2.1
KJ
?mol-1
通过这节课你学到了什么?
1.能量转化的方式,特别是化学能与
热能的相互转化。
2.学会判定放热反应和吸热反应,学会热化学方程式的书写。
3.明确化学键的断裂和形成是化学反应中能量变化的主要原因。
