科粤版九年级上册化学课件3.4 物质组成的表示式 (共16张PPT)
文档属性
| 名称 | 科粤版九年级上册化学课件3.4 物质组成的表示式 (共16张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 588.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-07-05 00:00:00 | ||
图片预览





文档简介
(共16张PPT)
3.4
物质组
成的表示式(三)
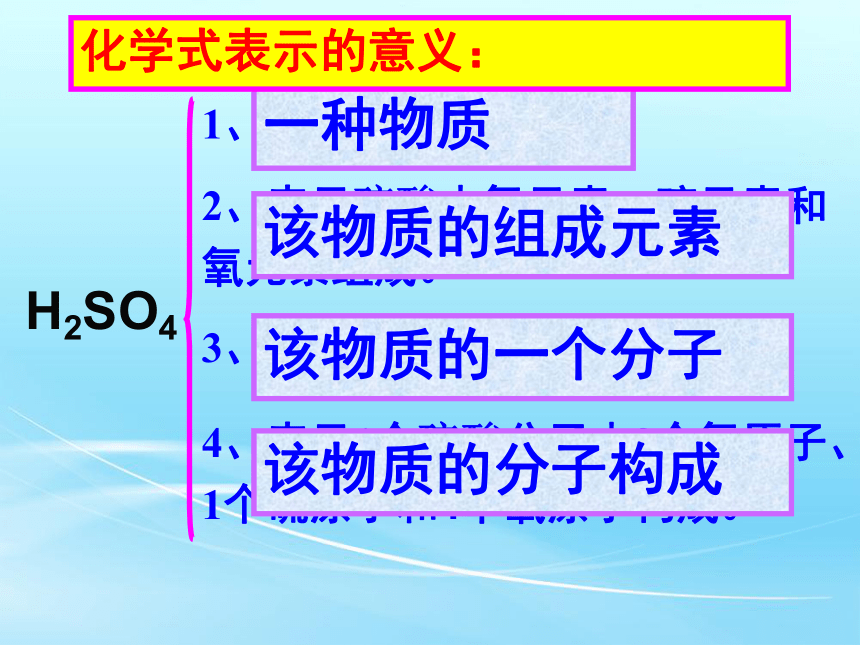
1、表示硫酸这种物质。
2、表示硫酸由氢元素、硫元素和氧元素组成。
3、表示1个硫酸分子。
4、表示1个硫酸分子由2个氢原子、1个硫原子和4个氧原子构成。
一种物质
该物质的组成元素
该物质的一个分子
该物质的分子构成
化学式表示的意义:
练习:H2O表示的意义有哪些?
三、有关化学式的计算
本节目标:
1、掌握相对分子质量的含义,名表相对分子质量与相对原子质量的关系;
2、了解根据已知的化学式,计算出物质的相对分子质量、各组成元素的质量比和某一元素的质量分数以及求某一种元素的质量和纯度的计算。
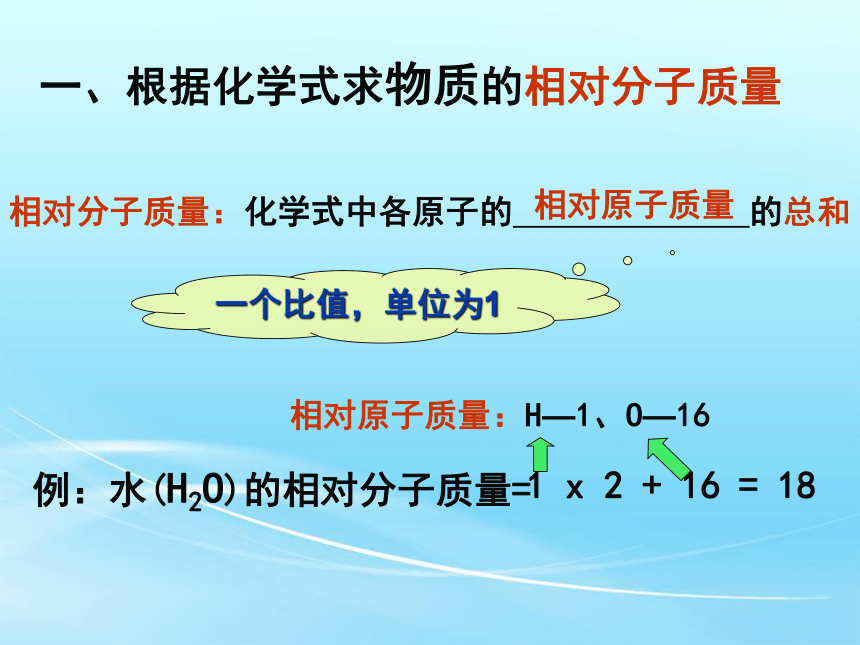
一、根据化学式求物质的相对分子质量
相对分子质量:化学式中各原子的
的总和
相对原子质量
例:水(H2O)的相对分子质量=
1
x
2
+
16
=
18
相对原子质量:H—1、O—16
一个比值,单位为1
练习:
CO2的相对分子质量=
CaCO3的相对分子质量=
CuSO4的相对分子质量=
Cu(OH)2
的相对分子质量=
5H2O的相对分子质量之和=
CuSO4
.5H2O的相对分子质量=
12
+
16
x
2
=
44
40+12+16x3=100
64+32+16x4=160
64+2x(16+1)=98
5x(1x2+16x1)=90
64+32+16x4+5x(1x2+16)=250
相对原子质量:H-1、O-16、C-12、Ca-40、
S-32、N-14、Cu-64
练习:一种新型的胃动力药——吗叮啉的化学式为C22H24ClN5O2
,该物质是由
种元素组成,每个分子中共含有
个原子,该物质的相对分子质量为
。
(C-12、H-1、Cl-35.5、N-14、O-16)
练习:计算化学式中的原子个数之比、原子个数之和。
计算水(H2O)中氢、氧原子的个数比及原子个数之和。
解:水中氢、氧原子的个数比=
2
:1
水分子中共含有3个原子
5
54
425.5
?二、计算组成化合物各元素的质量比
例:计算水(H2O)中氢、氧元素的质量比。
解:水中氢、氧原子的个数比=
2
:1,
故氢元素的质量:氧元素的质量=1×2
:16
=1
:8
练习:
1.硝酸铵(NH4NO3)中各元素的质量比
2.硫酸(H2SO4)中各元素的质量比
3.五水硫酸铜(CuSO4.5H2O)中硫元素与氧元素的质量比
相对原子质量:H-1、O-16、N-14
、S-32、
Cu-64
解:硝酸铵(NH4NO3)中氮元素、氢元素、氧元素的质量比=
14x2
:1x4
:16x3
=
7
:1
:12
解:硫酸(H2SO4)中氢元素、硫元素、氧元素的质量比=1x2:32:16x4
=
1:16:32
解:五水硫酸铜(CuSO4.5H2O)中硫元素与氧元素的质量比=32:16x9
=
2:9
5
例:海洛因是我国政府明令严禁的品,其化学式为C21H23NO5它是由
种元素组成,每个海洛因分子中共有
个原子,
其中碳元素与氮元素的质量比为
。
4
50
18:1
三、
计算化合物中某一元素的质量分数
例:求水(H2O)中氢元素的质量分数?
公式:
解:水(H2O)中氢
元素的质量分数=
X100%=11.1%
18
1
X
2
答:水中氢元素的质量分数为11.1%。
氢原子的个数×氢元素的相对原子质量
水的相对分子质量
×100%
=
1.求CaCO3中氧元素的质量分数?
?
?
2.
求NH4NO3中氮元素的质量分数?
?
?
3.求Fe2O3中氧元素的质量分数?
练习:
相对原子质量:H-1、O-16、N-14
、Ca-40、
Fe-56
48%?
35%
27.6%
练习:(兰州中考)
.某生产化肥碳酸氢铵(NH4HCO3)的企业,作了一个大型户外广告。如图所示:根据相关信息计算:
(1)碳酸氢铵(NH4HCO3
)中氮、氢、氧、碳四种元素的质量比_______________
(2)碳酸氢铵(NH4HCO3)中氮元素的质量分数为_______(结果精确到0.1%)
(3)通过计算判断该广告属于__________(填“虚假”或“真实”)广告?
(4)每袋该化肥中氮元素的质量小于____kg(结果精确到0.1)。
14:5:48:12
17.7%
虚假
8.9
宇宙牌化肥――国际首创
主要成分:
碳酸氢铵(NH4HCO3)
含氮量居全球化肥之首:24%
净含量:50kg/袋
“宇宙”化肥有限责任公司出品
四、求化合物中某元素的质量
例:
1.36克的水中含有氢元素多少克?
2.多少克水中含有2克的氢元素?
某元素的质量分数
五、
计算纯度
例:某不纯的硝酸铵[NH4NO3]化肥样品中氮元素的质量分数是17.5%,杂质不含氮元素,则化肥中硝酸铵的质量分数是多少?
公式:
解:化肥中硝酸铵
的质量分数=
X100%=50%
35%
17.5%
答:化肥中硝酸铵的质量分数是50%
。
练习、某地赤铁矿中主要有效成分是氧化铁[Fe2O3],杂质不含铁元素,铁元素的质量分数是28%,则赤铁矿中氧化铁质量分数是多少?
解:赤铁矿中
氧化铁质量分数=
28%
70%
X100%=40%
答:化肥中硝酸铵的质量分数是40%
。
3.4
物质组
成的表示式(三)
1、表示硫酸这种物质。
2、表示硫酸由氢元素、硫元素和氧元素组成。
3、表示1个硫酸分子。
4、表示1个硫酸分子由2个氢原子、1个硫原子和4个氧原子构成。
一种物质
该物质的组成元素
该物质的一个分子
该物质的分子构成
化学式表示的意义:
练习:H2O表示的意义有哪些?
三、有关化学式的计算
本节目标:
1、掌握相对分子质量的含义,名表相对分子质量与相对原子质量的关系;
2、了解根据已知的化学式,计算出物质的相对分子质量、各组成元素的质量比和某一元素的质量分数以及求某一种元素的质量和纯度的计算。
一、根据化学式求物质的相对分子质量
相对分子质量:化学式中各原子的
的总和
相对原子质量
例:水(H2O)的相对分子质量=
1
x
2
+
16
=
18
相对原子质量:H—1、O—16
一个比值,单位为1
练习:
CO2的相对分子质量=
CaCO3的相对分子质量=
CuSO4的相对分子质量=
Cu(OH)2
的相对分子质量=
5H2O的相对分子质量之和=
CuSO4
.5H2O的相对分子质量=
12
+
16
x
2
=
44
40+12+16x3=100
64+32+16x4=160
64+2x(16+1)=98
5x(1x2+16x1)=90
64+32+16x4+5x(1x2+16)=250
相对原子质量:H-1、O-16、C-12、Ca-40、
S-32、N-14、Cu-64
练习:一种新型的胃动力药——吗叮啉的化学式为C22H24ClN5O2
,该物质是由
种元素组成,每个分子中共含有
个原子,该物质的相对分子质量为
。
(C-12、H-1、Cl-35.5、N-14、O-16)
练习:计算化学式中的原子个数之比、原子个数之和。
计算水(H2O)中氢、氧原子的个数比及原子个数之和。
解:水中氢、氧原子的个数比=
2
:1
水分子中共含有3个原子
5
54
425.5
?二、计算组成化合物各元素的质量比
例:计算水(H2O)中氢、氧元素的质量比。
解:水中氢、氧原子的个数比=
2
:1,
故氢元素的质量:氧元素的质量=1×2
:16
=1
:8
练习:
1.硝酸铵(NH4NO3)中各元素的质量比
2.硫酸(H2SO4)中各元素的质量比
3.五水硫酸铜(CuSO4.5H2O)中硫元素与氧元素的质量比
相对原子质量:H-1、O-16、N-14
、S-32、
Cu-64
解:硝酸铵(NH4NO3)中氮元素、氢元素、氧元素的质量比=
14x2
:1x4
:16x3
=
7
:1
:12
解:硫酸(H2SO4)中氢元素、硫元素、氧元素的质量比=1x2:32:16x4
=
1:16:32
解:五水硫酸铜(CuSO4.5H2O)中硫元素与氧元素的质量比=32:16x9
=
2:9
5
例:海洛因是我国政府明令严禁的品,其化学式为C21H23NO5它是由
种元素组成,每个海洛因分子中共有
个原子,
其中碳元素与氮元素的质量比为
。
4
50
18:1
三、
计算化合物中某一元素的质量分数
例:求水(H2O)中氢元素的质量分数?
公式:
解:水(H2O)中氢
元素的质量分数=
X100%=11.1%
18
1
X
2
答:水中氢元素的质量分数为11.1%。
氢原子的个数×氢元素的相对原子质量
水的相对分子质量
×100%
=
1.求CaCO3中氧元素的质量分数?
?
?
2.
求NH4NO3中氮元素的质量分数?
?
?
3.求Fe2O3中氧元素的质量分数?
练习:
相对原子质量:H-1、O-16、N-14
、Ca-40、
Fe-56
48%?
35%
27.6%
练习:(兰州中考)
.某生产化肥碳酸氢铵(NH4HCO3)的企业,作了一个大型户外广告。如图所示:根据相关信息计算:
(1)碳酸氢铵(NH4HCO3
)中氮、氢、氧、碳四种元素的质量比_______________
(2)碳酸氢铵(NH4HCO3)中氮元素的质量分数为_______(结果精确到0.1%)
(3)通过计算判断该广告属于__________(填“虚假”或“真实”)广告?
(4)每袋该化肥中氮元素的质量小于____kg(结果精确到0.1)。
14:5:48:12
17.7%
虚假
8.9
宇宙牌化肥――国际首创
主要成分:
碳酸氢铵(NH4HCO3)
含氮量居全球化肥之首:24%
净含量:50kg/袋
“宇宙”化肥有限责任公司出品
四、求化合物中某元素的质量
例:
1.36克的水中含有氢元素多少克?
2.多少克水中含有2克的氢元素?
某元素的质量分数
五、
计算纯度
例:某不纯的硝酸铵[NH4NO3]化肥样品中氮元素的质量分数是17.5%,杂质不含氮元素,则化肥中硝酸铵的质量分数是多少?
公式:
解:化肥中硝酸铵
的质量分数=
X100%=50%
35%
17.5%
答:化肥中硝酸铵的质量分数是50%
。
练习、某地赤铁矿中主要有效成分是氧化铁[Fe2O3],杂质不含铁元素,铁元素的质量分数是28%,则赤铁矿中氧化铁质量分数是多少?
解:赤铁矿中
氧化铁质量分数=
28%
70%
X100%=40%
答:化肥中硝酸铵的质量分数是40%
。
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
