共价键2011.3(上课)
文档属性
| 名称 | 共价键2011.3(上课) |  | |
| 格式 | rar | ||
| 文件大小 | 641.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2011-05-30 15:04:52 | ||
图片预览


文档简介
(共9张PPT)
路桥中学 梁书
专题1 微观结构与物质的多样性
第二单元 微粒之间的相互作用力
§1. 2.1 共价键
e
e
e
e
e
e
e
e
e
e
e
e
e
e
1、非金属原子之间形成共价键后,分子中各原子最外层电子的数目达到多少?如何计算。
2、非金属原子之间形成共用电子对的数目是如何确定?
【交流与讨论】
共用电子对=8-最外层电子数(H除外)
3、当有多个原子时,如何确定中心原子?
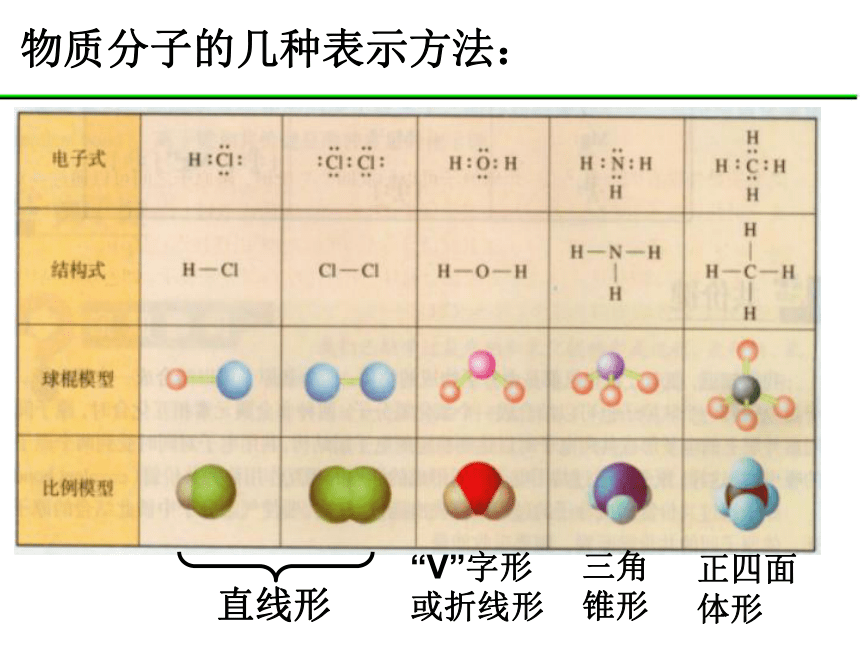
物质分子的几种表示方法:
直线形
“V”字形
或折线形
三角锥形
正四面体形
指出下列化合物所含化学键类型:
【试一试】
NaBr H2S NaOH SO2 MgCl2 H2SO4
【思考】NH4Cl中存在哪些键,属于什么化合物?
含有离子键的有: 。
含有共价键的有: 。
属于离子化合物的有: 。
属于共价化合物的有 : 。
NaBr NaOH MgCl2
H2S NaOH SO2 H2SO4
NaBr NaOH MgCl2
H2S SO2 H2SO4
【概念辨析】
判断下列说法是否正确
A、含有共价键的化合物一定是共价化合物。
B、在共价化合物中,可能存在着离子键。
C、离子化合物只含离子键。
D、全部由非金属组成的化合物一定是共价化合物
E、离子化合物中一定存在金属元素。
F、在气态单质分子中,一定存在共价键。
路桥中学 梁书
专题1 微观结构与物质的多样性
第二单元 微粒之间的相互作用力
§1. 2.1 共价键
e
e
e
e
e
e
e
e
e
e
e
e
e
e
1、非金属原子之间形成共价键后,分子中各原子最外层电子的数目达到多少?如何计算。
2、非金属原子之间形成共用电子对的数目是如何确定?
【交流与讨论】
共用电子对=8-最外层电子数(H除外)
3、当有多个原子时,如何确定中心原子?
物质分子的几种表示方法:
直线形
“V”字形
或折线形
三角锥形
正四面体形
指出下列化合物所含化学键类型:
【试一试】
NaBr H2S NaOH SO2 MgCl2 H2SO4
【思考】NH4Cl中存在哪些键,属于什么化合物?
含有离子键的有: 。
含有共价键的有: 。
属于离子化合物的有: 。
属于共价化合物的有 : 。
NaBr NaOH MgCl2
H2S NaOH SO2 H2SO4
NaBr NaOH MgCl2
H2S SO2 H2SO4
【概念辨析】
判断下列说法是否正确
A、含有共价键的化合物一定是共价化合物。
B、在共价化合物中,可能存在着离子键。
C、离子化合物只含离子键。
D、全部由非金属组成的化合物一定是共价化合物
E、离子化合物中一定存在金属元素。
F、在气态单质分子中,一定存在共价键。
