共价键公开课JJP
图片预览


文档简介
(共10张PPT)
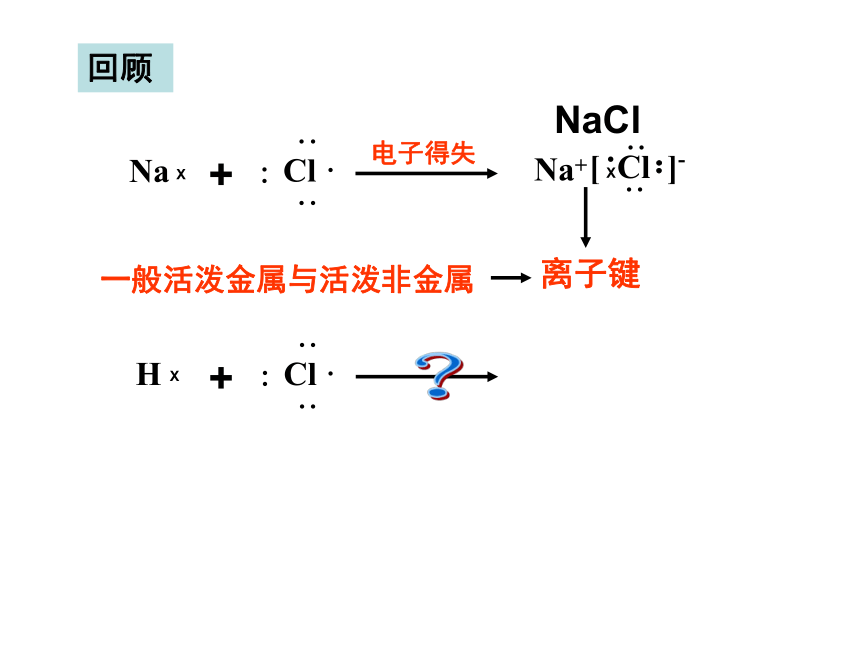
回顾
Cl ·
··
··
··
+
电子得失
离子键
Cl ·
··
··
··
+
H
X
Na
X
Na+
[ Cl ]-
··
··
:
.
X
一般活泼金属与活泼非金属
NaCl
··
· Cl
··
:
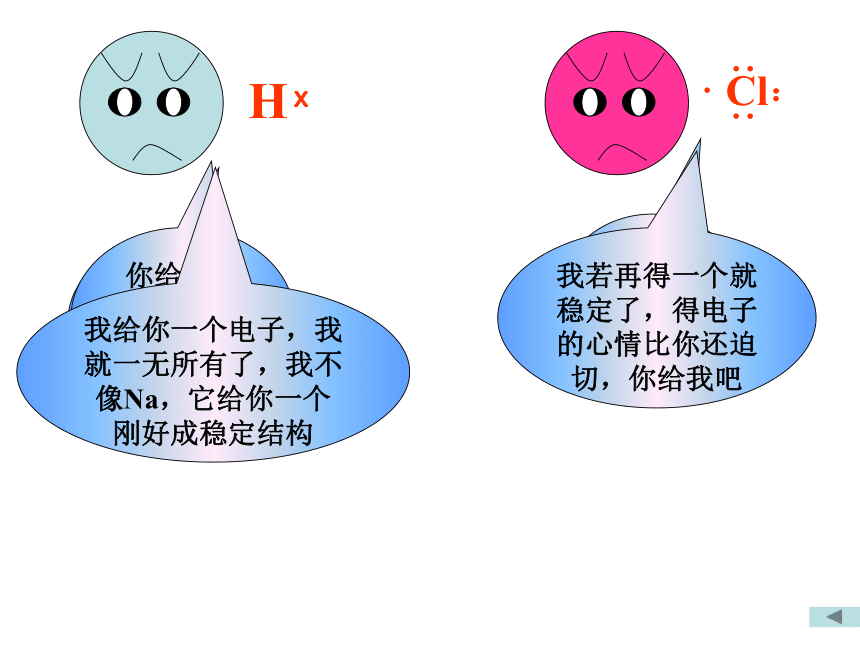
我最外层只有一个电子,不够稳定
我最外层有7个电子,也不够稳定
你给我一个电子吧,那我就成稳定结构了
我若再得一个就稳定了,得电子的心情比你还迫切,你给我吧
我给你一个电子,我就一无所有了,我不像Na,它给你一个刚好成稳定结构
H
x
··
· Cl
··
:
我要得1个电子,形成2e-稳定结构
我要得7个电子,形成8e-稳定结构
H
x
为达到稳定结构,都要得电子
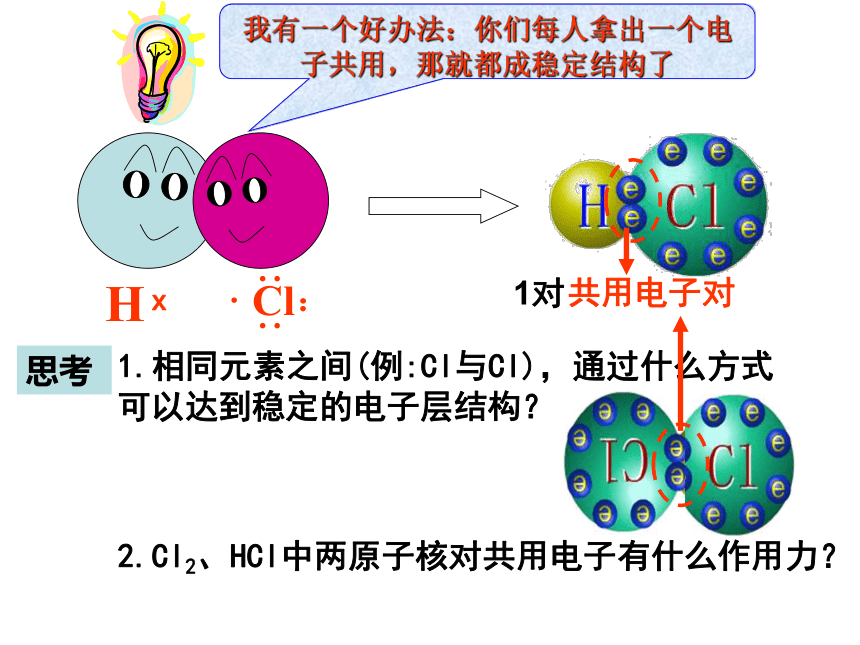
我有一个好办法:你们每人拿出一个电子共用,那就都成稳定结构了
H
x
··
· Cl
··
:
思考
1.相同元素之间(例:Cl与Cl),通过什么方式可以达到稳定的电子层结构?
2.Cl2、HCl中两原子核对共用电子有什么作用力?
共用电子对
1对
对共价键的理解
1.成键元素:
2.成键粒子:
3.成键本质:
一般是非金属元素和非金属元素
原子(相同或不同)
原子间通过共用电子对产生的强烈的相互作用力
请举例哪些常见物质中含有共价键?
共价键:原子之间通过共用电子对所形成的强烈
的相互作用
思考
1.请写出HCl、Cl2分子的电子式。
2.H2O分子中氢、氧原子的电子共用情况如何?
请写出H2O分子的电子式。
原子 H Cl O N C
共用电子对数
1
1
3.非金属元素原子间的共用电子对数与什么有关?
2
3
4
原子距稳定结构少几个电子,就拿出几个共用
判断原子的共用电子对数:
请写出N2、NH3、CH4、CO2的电子式。
练习
观察与思考
结构式:
用一条短线表示一对共用电子对,其它电子不标。
共价分子中各原子有一定的连接方式,分子有一定的空间结构
V字型 三角锥型 正四面体
知识巩固
1.请用电子式表示下列物质:CCl4、HClO
3.判断下列说法是否正确:
(1)共价键只存在于共价化合物中
(2)He分子内存在共价键
(3)离子化合物中只能含有离子键
(4)非金属元素原子间不能形成离子键
2.请用电子式表示NaOH
思考
PCl5中各原子均满足最外层为8e-的结构吗?
回顾
Cl ·
··
··
··
+
电子得失
离子键
Cl ·
··
··
··
+
H
X
Na
X
Na+
[ Cl ]-
··
··
:
.
X
一般活泼金属与活泼非金属
NaCl
··
· Cl
··
:
我最外层只有一个电子,不够稳定
我最外层有7个电子,也不够稳定
你给我一个电子吧,那我就成稳定结构了
我若再得一个就稳定了,得电子的心情比你还迫切,你给我吧
我给你一个电子,我就一无所有了,我不像Na,它给你一个刚好成稳定结构
H
x
··
· Cl
··
:
我要得1个电子,形成2e-稳定结构
我要得7个电子,形成8e-稳定结构
H
x
为达到稳定结构,都要得电子
我有一个好办法:你们每人拿出一个电子共用,那就都成稳定结构了
H
x
··
· Cl
··
:
思考
1.相同元素之间(例:Cl与Cl),通过什么方式可以达到稳定的电子层结构?
2.Cl2、HCl中两原子核对共用电子有什么作用力?
共用电子对
1对
对共价键的理解
1.成键元素:
2.成键粒子:
3.成键本质:
一般是非金属元素和非金属元素
原子(相同或不同)
原子间通过共用电子对产生的强烈的相互作用力
请举例哪些常见物质中含有共价键?
共价键:原子之间通过共用电子对所形成的强烈
的相互作用
思考
1.请写出HCl、Cl2分子的电子式。
2.H2O分子中氢、氧原子的电子共用情况如何?
请写出H2O分子的电子式。
原子 H Cl O N C
共用电子对数
1
1
3.非金属元素原子间的共用电子对数与什么有关?
2
3
4
原子距稳定结构少几个电子,就拿出几个共用
判断原子的共用电子对数:
请写出N2、NH3、CH4、CO2的电子式。
练习
观察与思考
结构式:
用一条短线表示一对共用电子对,其它电子不标。
共价分子中各原子有一定的连接方式,分子有一定的空间结构
V字型 三角锥型 正四面体
知识巩固
1.请用电子式表示下列物质:CCl4、HClO
3.判断下列说法是否正确:
(1)共价键只存在于共价化合物中
(2)He分子内存在共价键
(3)离子化合物中只能含有离子键
(4)非金属元素原子间不能形成离子键
2.请用电子式表示NaOH
思考
PCl5中各原子均满足最外层为8e-的结构吗?
