高中化学沪科版高一下学期6.1.1可逆反应中的化学平衡 (1)(共22张PPT)
文档属性
| 名称 | 高中化学沪科版高一下学期6.1.1可逆反应中的化学平衡 (1)(共22张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1008.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-07-10 00:00:00 | ||
图片预览






文档简介
(共22张PPT)
可逆反应中的化学平衡
高中化学高一下册(沪科课标版)
1868—1934
德国化学家
Fritz
Haber(弗里茨·哈伯
)
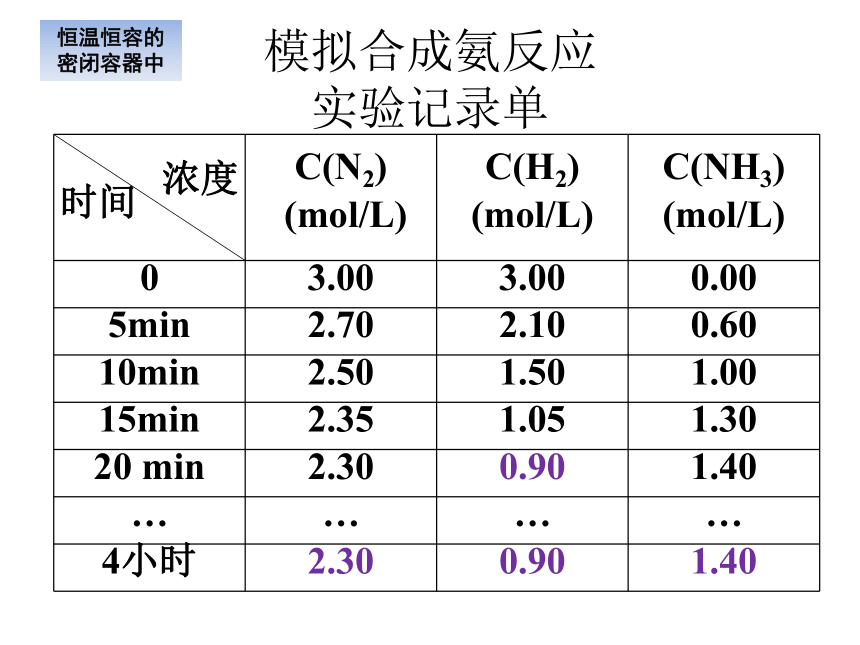
模拟合成氨反应
实验记录单
浓度
时间
C(N2)
(mol/L)
C(H2)
(mol/L)
C(NH3)
(mol/L)
0
3.00
3.00
0.00
5min
2.70
2.10
0.60
10min
2.50
1.50
1.00
15min
2.35
1.05
1.30
20
min
2.30
0.90
1.40
…
…
…
…
4小时
2.30
0.90
1.40
恒温恒容的
密闭容器中
大胆猜填,并计算前20min内用N2表示的化学反应速率。
模拟合成氨反应
实验记录单
浓度
时间
C(N2)
(mol/L)
C(H2)
(mol/L)
C(NH3)
(mol/L)
0
3.00
3.00
0.00
5min
2.70
2.10
0.60
10min
2.50
1.50
1.00
15min
2.35
1.05
1.30
20
min
2.30
0.90
1.40
…
…
…
…
4小时
2.30
0.90
1.40
恒温恒容的
密闭容器中
很多化学反应在进行时都具有可逆性,即它的生成物在同一条件下又能重新生成原来的反应物。
我们通常把在同一条件下正反应方向和逆反应方向均能进行的化学反应称为“可逆反应”。
可逆反应
模拟合成氨反应
浓度
时间
C(N2)
(mol/L)
C(H2)
(mol/L)
C(NH3)
(mol/L)
0
3.00
3.00
0.00
5min
2.70
2.10
0.60
10min
2.50
1.50
1.00
15min
2.35
1.05
1.30
20
min
2.30
0.90
1.40
…
…
…
…
4小时
2.30
0.90
1.40
恒温恒容的
密闭容器中
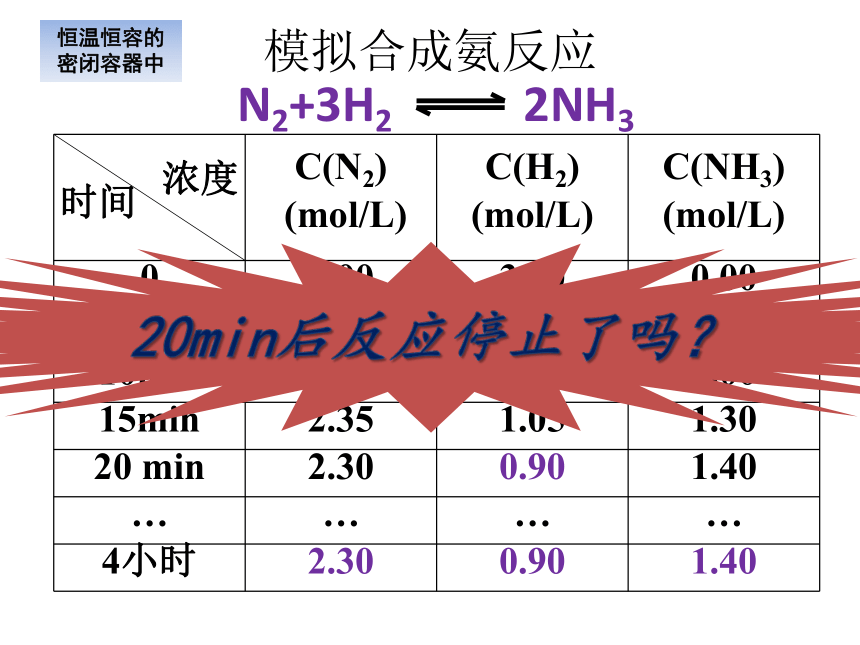
N2+3H2
2NH3
20min后反应停止了吗?
固体溶质
溶液中的溶质
溶解
结晶
模拟合成氨反应
浓度
时间
C(N2)
(mol/L)
C(H2)
(mol/L)
C(NH3)
(mol/L)
0
3.00
3.00
0.00
5min
2.70
2.10
0.60
10min
2.50
1.50
1.00
15min
2.35
1.05
1.30
20
min
2.30
0.90
1.40
…
…
…
…
4小时
2.30
0.90
1.40
恒温恒容的
密闭容器中
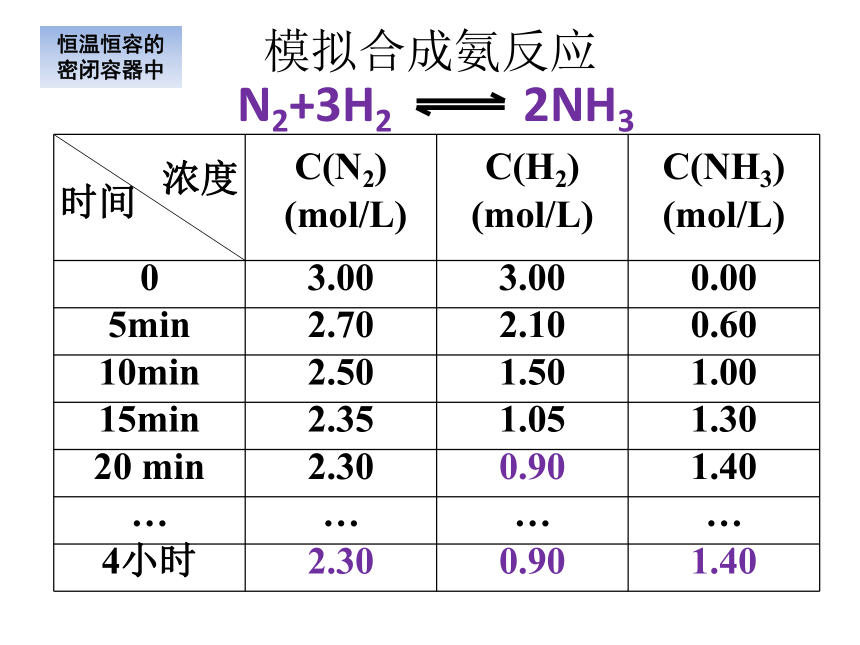
N2+3H2
2NH3
化学反应限度
在给定条件下化学反应所能达到或完成的最大程度,即该反应进行的限度。
化学反应的限度决定了反应物在该条件下的最大转化率。
化学平衡状态
1.谓衡器两端承受的重量相等。
2.谓权衡国政使得其平。
3.对立的各方面在数量上相等。
4.两个或两个以上的力作用于一个物体上,各个力互相抵消,使物体成相对的静止状态。亦泛指平稳,稳定。
5.哲学名词。事物处在量变阶段所显现的面貌,是绝对的、永恒的运动中所表现的暂时的、相对的静止。
……
1.谓衡器两端承受的重量相等。
2.谓权衡国政使得其平。
3.对立的各方面在数量上相等。
4.两个或两个以上的力作用于一个物体上,各个力互相抵消,使物体成相对的静止状态。亦泛指平稳,稳定。
5.哲学名词。事物处在量变阶段所显现的面貌,是绝对的、永恒的运动中所表现的暂时的、相对的静止。
……
动
态
平
衡
世界上没有绝对的、静止的平衡,平衡是一个动态的过程。动态平衡是物质系统在不断运动和变化情况下的宏观平衡。
在我们的生活中,许多状态都处于一种动态平衡中,例如大气平衡、水平衡、化学平衡、人口发展平衡、生态平衡、供求平衡等。
请根据实验记录单的数据,在同一幅图中画出正反应速率和逆反应速率随时间变化的曲线。
温馨提示:
1.随着反应的进行,N2和H2的浓度如何变化?NH3的浓度如何变化?
2.随着反应的进行,正反应的速率如何变化?逆反应的速率如何变化?
N2(g)+3H2(g)
2NH3(g)
模拟合成氨反应
浓度
时间
C(N2)
(mol/L)
C(H2)
(mol/L)
C(NH3)
(mol/L)
0
3.00
3.00
0.00
5min
2.70
2.10
0.60
10min
2.50
1.50
1.00
15min
2.35
1.05
1.30
20
min
2.30
0.90
1.40
…
…
…
…
4小时
2.30
0.90
1.40
恒温恒容的
密闭容器中
N2+3H2
2NH3
化学平衡状态
在一定条件下,当正、逆两个方向的反应速率相等时,反应体系中所有参加反应的物质的质量或浓度可以保持恒定,这时的状态也就是在给定条件下,反应达到了“限度”。对于可逆反应体系来说,我们称之为“化学平衡状态”。
化学平衡状态
【思考与交流】
在恒温恒容密闭容器中发生反应
N2(g)+3H2(g)
2NH3(g)
,下列能说明该反应已经达到化学平衡状态的是
。
①
V正(N2)=
3V逆(H2)
②单位时间内生成3mol
H2的同时生成
2mol
NH3
③单位时间内断开
nmol
H—H键的同时形成
2nmol
N—H键
④N2、H2、NH3的物质的量浓度之比为1:3:2的状态
⑤NH3的质量分数不再改变的状态
⑥NH3的体积分数不再改变的状态
②
⑤
⑥
【思考与交流】
在恒温恒容密闭容器中发生反应
N2(g)+3H2(g)
2NH3(g)
,下列能说明该反应已经达到化学平衡状态的是
。
⑦混合气体的颜色不再改变的状态
⑧容器内的温度不再改变的状态
⑨容器内的压强不再改变的状态
⑩混合气体的密度不再改变的状态
?混合气体的平均摩尔质量不再改变的状态
②
⑤
⑥
⑨
?
化学平衡状态
定义
特征
逆
等
动
定
变
建立
判定
直接
间接
v正=v逆
cA
mA
nA
VA%
mA%
颜色
P
ρ
T
M
V
【课后提升】
在恒温恒容密闭容器中发生反应
N2(g)+3H2(g)
2NH3(g)
,下列能说明该反应已经达到化学平衡状态的是
。
①
V正(N2)=
3V逆(H2)
②单位时间内生成3mol
H2的同时生成
2mol
NH3
③单位时间内断开
nmol
H—H键的同时形成
2nmol
N—H键
④N2、H2、NH3的物质的量浓度之比为1:3:2的状态
⑤NH3的质量分数不再改变的状态
⑥NH3的体积分数不再改变的状态
恒温恒压
【课后提升】
在恒温恒容密闭容器中发生反应
N2(g)+3H2(g)
2NH3(g)
,下列能说明该反应已经达到化学平衡状态的是
。
⑦混合气体的颜色不再改变的状态
⑧容器内的温度不再改变的状态
⑨容器内的压强不再改变的状态
⑩混合气体的密度不再改变的状态
?混合气体的平均摩尔质量不再改变的状态
恒温恒压
在恒温恒容密闭容器中充入3.00mol
N2和3.00mol
H2,发生反应N2(g)+3H2(g)
2NH3
(g)
,下列都能说明该反应已经达到化学平衡状态吗?
①N2的体积分数不再改变的状态
②H2的体积分数不再改变的状态
③NH3的体积分数不再改变的状态
【挑战升级】
观看影片《世纪天才·爱因斯坦(7)》
思考:
你是如何评价弗里茨·哈伯和因他而饮弹自尽的克拉克·哈伯夫人的?
结合第一次世界大战的历史背景,谈谈你
对科学、国家与战争的关系的理解。
【佳片有约】
可逆反应中的化学平衡
高中化学高一下册(沪科课标版)
1868—1934
德国化学家
Fritz
Haber(弗里茨·哈伯
)
模拟合成氨反应
实验记录单
浓度
时间
C(N2)
(mol/L)
C(H2)
(mol/L)
C(NH3)
(mol/L)
0
3.00
3.00
0.00
5min
2.70
2.10
0.60
10min
2.50
1.50
1.00
15min
2.35
1.05
1.30
20
min
2.30
0.90
1.40
…
…
…
…
4小时
2.30
0.90
1.40
恒温恒容的
密闭容器中
大胆猜填,并计算前20min内用N2表示的化学反应速率。
模拟合成氨反应
实验记录单
浓度
时间
C(N2)
(mol/L)
C(H2)
(mol/L)
C(NH3)
(mol/L)
0
3.00
3.00
0.00
5min
2.70
2.10
0.60
10min
2.50
1.50
1.00
15min
2.35
1.05
1.30
20
min
2.30
0.90
1.40
…
…
…
…
4小时
2.30
0.90
1.40
恒温恒容的
密闭容器中
很多化学反应在进行时都具有可逆性,即它的生成物在同一条件下又能重新生成原来的反应物。
我们通常把在同一条件下正反应方向和逆反应方向均能进行的化学反应称为“可逆反应”。
可逆反应
模拟合成氨反应
浓度
时间
C(N2)
(mol/L)
C(H2)
(mol/L)
C(NH3)
(mol/L)
0
3.00
3.00
0.00
5min
2.70
2.10
0.60
10min
2.50
1.50
1.00
15min
2.35
1.05
1.30
20
min
2.30
0.90
1.40
…
…
…
…
4小时
2.30
0.90
1.40
恒温恒容的
密闭容器中
N2+3H2
2NH3
20min后反应停止了吗?
固体溶质
溶液中的溶质
溶解
结晶
模拟合成氨反应
浓度
时间
C(N2)
(mol/L)
C(H2)
(mol/L)
C(NH3)
(mol/L)
0
3.00
3.00
0.00
5min
2.70
2.10
0.60
10min
2.50
1.50
1.00
15min
2.35
1.05
1.30
20
min
2.30
0.90
1.40
…
…
…
…
4小时
2.30
0.90
1.40
恒温恒容的
密闭容器中
N2+3H2
2NH3
化学反应限度
在给定条件下化学反应所能达到或完成的最大程度,即该反应进行的限度。
化学反应的限度决定了反应物在该条件下的最大转化率。
化学平衡状态
1.谓衡器两端承受的重量相等。
2.谓权衡国政使得其平。
3.对立的各方面在数量上相等。
4.两个或两个以上的力作用于一个物体上,各个力互相抵消,使物体成相对的静止状态。亦泛指平稳,稳定。
5.哲学名词。事物处在量变阶段所显现的面貌,是绝对的、永恒的运动中所表现的暂时的、相对的静止。
……
1.谓衡器两端承受的重量相等。
2.谓权衡国政使得其平。
3.对立的各方面在数量上相等。
4.两个或两个以上的力作用于一个物体上,各个力互相抵消,使物体成相对的静止状态。亦泛指平稳,稳定。
5.哲学名词。事物处在量变阶段所显现的面貌,是绝对的、永恒的运动中所表现的暂时的、相对的静止。
……
动
态
平
衡
世界上没有绝对的、静止的平衡,平衡是一个动态的过程。动态平衡是物质系统在不断运动和变化情况下的宏观平衡。
在我们的生活中,许多状态都处于一种动态平衡中,例如大气平衡、水平衡、化学平衡、人口发展平衡、生态平衡、供求平衡等。
请根据实验记录单的数据,在同一幅图中画出正反应速率和逆反应速率随时间变化的曲线。
温馨提示:
1.随着反应的进行,N2和H2的浓度如何变化?NH3的浓度如何变化?
2.随着反应的进行,正反应的速率如何变化?逆反应的速率如何变化?
N2(g)+3H2(g)
2NH3(g)
模拟合成氨反应
浓度
时间
C(N2)
(mol/L)
C(H2)
(mol/L)
C(NH3)
(mol/L)
0
3.00
3.00
0.00
5min
2.70
2.10
0.60
10min
2.50
1.50
1.00
15min
2.35
1.05
1.30
20
min
2.30
0.90
1.40
…
…
…
…
4小时
2.30
0.90
1.40
恒温恒容的
密闭容器中
N2+3H2
2NH3
化学平衡状态
在一定条件下,当正、逆两个方向的反应速率相等时,反应体系中所有参加反应的物质的质量或浓度可以保持恒定,这时的状态也就是在给定条件下,反应达到了“限度”。对于可逆反应体系来说,我们称之为“化学平衡状态”。
化学平衡状态
【思考与交流】
在恒温恒容密闭容器中发生反应
N2(g)+3H2(g)
2NH3(g)
,下列能说明该反应已经达到化学平衡状态的是
。
①
V正(N2)=
3V逆(H2)
②单位时间内生成3mol
H2的同时生成
2mol
NH3
③单位时间内断开
nmol
H—H键的同时形成
2nmol
N—H键
④N2、H2、NH3的物质的量浓度之比为1:3:2的状态
⑤NH3的质量分数不再改变的状态
⑥NH3的体积分数不再改变的状态
②
⑤
⑥
【思考与交流】
在恒温恒容密闭容器中发生反应
N2(g)+3H2(g)
2NH3(g)
,下列能说明该反应已经达到化学平衡状态的是
。
⑦混合气体的颜色不再改变的状态
⑧容器内的温度不再改变的状态
⑨容器内的压强不再改变的状态
⑩混合气体的密度不再改变的状态
?混合气体的平均摩尔质量不再改变的状态
②
⑤
⑥
⑨
?
化学平衡状态
定义
特征
逆
等
动
定
变
建立
判定
直接
间接
v正=v逆
cA
mA
nA
VA%
mA%
颜色
P
ρ
T
M
V
【课后提升】
在恒温恒容密闭容器中发生反应
N2(g)+3H2(g)
2NH3(g)
,下列能说明该反应已经达到化学平衡状态的是
。
①
V正(N2)=
3V逆(H2)
②单位时间内生成3mol
H2的同时生成
2mol
NH3
③单位时间内断开
nmol
H—H键的同时形成
2nmol
N—H键
④N2、H2、NH3的物质的量浓度之比为1:3:2的状态
⑤NH3的质量分数不再改变的状态
⑥NH3的体积分数不再改变的状态
恒温恒压
【课后提升】
在恒温恒容密闭容器中发生反应
N2(g)+3H2(g)
2NH3(g)
,下列能说明该反应已经达到化学平衡状态的是
。
⑦混合气体的颜色不再改变的状态
⑧容器内的温度不再改变的状态
⑨容器内的压强不再改变的状态
⑩混合气体的密度不再改变的状态
?混合气体的平均摩尔质量不再改变的状态
恒温恒压
在恒温恒容密闭容器中充入3.00mol
N2和3.00mol
H2,发生反应N2(g)+3H2(g)
2NH3
(g)
,下列都能说明该反应已经达到化学平衡状态吗?
①N2的体积分数不再改变的状态
②H2的体积分数不再改变的状态
③NH3的体积分数不再改变的状态
【挑战升级】
观看影片《世纪天才·爱因斯坦(7)》
思考:
你是如何评价弗里茨·哈伯和因他而饮弹自尽的克拉克·哈伯夫人的?
结合第一次世界大战的历史背景,谈谈你
对科学、国家与战争的关系的理解。
【佳片有约】
