鲁教版九年级下册化学 8.3海水“制碱” 第一课时纯碱的性质课件(16张PPT)
文档属性
| 名称 | 鲁教版九年级下册化学 8.3海水“制碱” 第一课时纯碱的性质课件(16张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-07-11 00:00:00 | ||
图片预览






文档简介
纯碱(苏打)在生活中的用途
Na2CO3
盐
第八单元 海水中的化学
第三节 海水“制碱”(1)纯碱的性质
白色粉末状固体,易溶于水
二、纯碱(Na2CO3)的性质
1、物理性质
2、化学性质
回忆一下,你已经知道Na2CO3都可以和哪些物质反应?
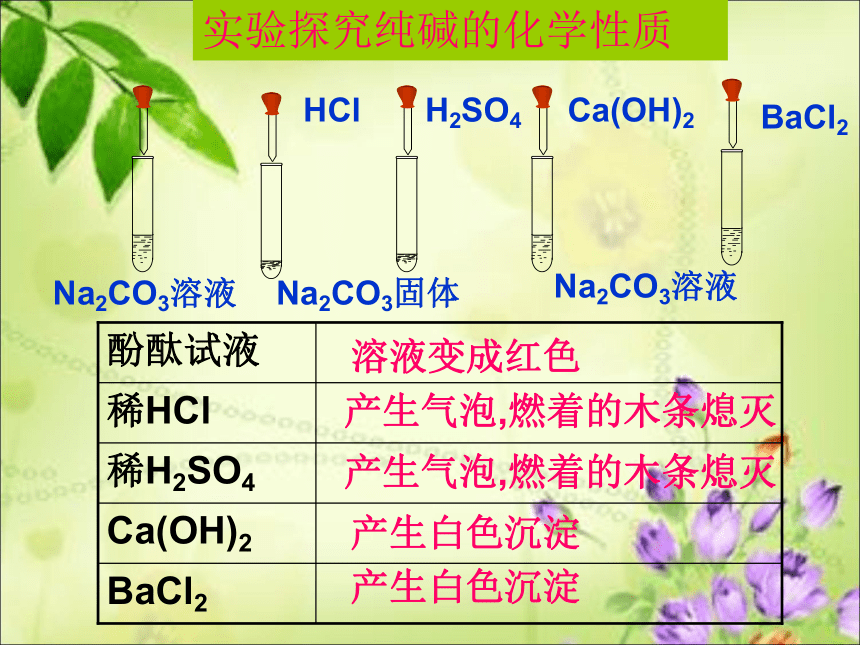
酚酞试液
稀HCl
稀H2SO4
Ca(OH)2
BaCl2
实验探究纯碱的化学性质
溶液变成红色
产生气泡,燃着的木条熄灭
产生气泡,燃着的木条熄灭
产生白色沉淀
产生白色沉淀
Na2CO3固体
Na2CO3溶液
HCl
H2SO4
Ca(OH)2
BaCl2
Na2CO3溶液
1. Na2CO3与指示剂作用(酚酞)
2. Na2CO3与稀HCl﹑稀H2SO4反应
3. Na2CO3与Ca(OH)2反应
4. Na2CO3与BaCl2反应
实验结论
Na2CO3+ 2HCl= 2NaCl+H2O +CO2↑
Na2CO3+H2SO4= Na2SO4+H2O+ CO2↑
Na2CO3+Ca(OH)2= 2NaOH+ Ca CO3↓
Na2CO3+BaCl2= 2NaCl+BaCO3↓
复分解反应
纯碱的化学性质
1.碳酸钠溶液呈碱性,能使指示剂变色。
2.碳酸钠能与酸发生复分解反应生成二氧化碳
Na2CO3 + 2HCl=2NaCl+H2O+CO2↑
Na2CO3 + H2SO4=Na2SO4+H2O+CO2↑
3.碳酸钠与碱溶液发生复分解反应
Na2CO3 + Ca(OH)2=CaCO3 ↓+2NaOH
4.碳酸钠与盐溶液发生复分解反应
Na2CO3 +BaCl2=BaCO3 ↓+2NaCl
小结
三、盐在水溶液中发生的反应
酸
碱
盐
盐
复分解反应
反应物可均溶
(↑ 或↓或H2O)
CaCO3+ Ba(OH)2
Na2CO3+ Ba(OH)2
只用一种试剂来鉴别NaOH、Ca(OH)2、稀H2SO4三种溶液,这种试剂是_______
A.氯化钡溶液 B.紫色石蕊试液
C.碳酸钠溶液 D.酚酞试液
C
思维训练
NaOH
Ca(OH)2
H2SO4
BaCl2
NaOH
Ca(OH)2
H2SO4
Na2CO3
小苏打在生产和生活中的用途
NaHCO3
盐
写出下列化学方程式
CaCO3 + HCl---
Na2CO3 + HCl---
NaHCO3 + HCl---
Na2CO3 + H2SO4---
思考
如何检验鸡蛋壳中含有碳酸根?
碳酸根的检验方法
加稀盐酸并将产生的气体通入澄清石灰水中
CaCO3+ 2HCl= CaCl2+H2O +CO2↑
CO2 + Ca(OH)2= CaCO3↓ + H2O
我的收获
纯碱的性质
物理性质:白色粉末状固体,易溶于水。
化学性质:
1.碳酸钠溶液呈碱性
2.碳酸钠与酸反应生成二氧化碳
Na2CO3 + 2HCl=2NaCl+H2O+CO2↑
3.碳酸钠与碱溶液反应
Na2CO3 + Ca(OH)2=CaCO3 ↓+2NaOH
4.碳酸钠与盐溶液反应
Na2CO3 +BaCl2=BaCO3 ↓+2NaCl
盐在水溶液中发生的反应
酸
碱
盐
盐
1、除去氯化钠中的杂质碳酸钠,下列方法不能实现的是________
A.加适量盐酸,蒸发结晶
B.加适量氯化钙,过滤后蒸发结晶
C.加适量氢氧化钡,过滤后蒸发结晶
D.加适量氢氧化钠,过滤后蒸发结晶
2、检验碳酸盐的正确方法是_____
A.滴加盐酸,产生使木条火焰熄灭的气体
B.滴加BaCl2溶液产生白色沉淀
C.加热,产生使澄清石灰水变浑浊的气体
D.滴加盐酸产生使澄清石灰水变浑浊的气体
挑战自我
C、D
D
3、学习碳酸钠知识时,老师做碳酸钠溶液和澄清石灰水反应演示实验,并对浑浊液过滤,得到澄清滤液.课堂上老师的提问和同学们的回答如图所示:
挑战自我
可能是NaOH和Ca(OH)2
(1)假设你是丁同学,请你也提出一个与甲、乙、丙同学不同的猜想,把猜想写在对话框中.并对你自己的猜想设计一个简单的实验加以证明.
挑战自我
实验步骤
实验现象
实验结论
取样于试管中,
____________
____________
自己的猜想正确
(2)你认为甲、乙、丙同学的猜想都合理吗?如有不合理的请说明理由:__________
_________________________________.
滴加Na2CO3溶液,
有白色沉淀生成
Na2CO3和Ca(OH)2能发生反应,不能共存。
乙不合理
(3)甲同学针对自己的猜想进行了如下实验:
(甲同学认为可能含有NaOH和Na2CO3)
挑战自我
实验步骤
实验现象
实验结论
取样于试管中,滴加几滴稀盐酸
没有气泡产生
甲的猜想不成立
你认为甲同学的实验设计是否正确?______请说明理由:___________________________________.
不正确
有NaOH存在,滴入少量盐酸先与NaOH反应就不会有CO2放出,但Na2CO3可能存在。
Na2CO3
盐
第八单元 海水中的化学
第三节 海水“制碱”(1)纯碱的性质
白色粉末状固体,易溶于水
二、纯碱(Na2CO3)的性质
1、物理性质
2、化学性质
回忆一下,你已经知道Na2CO3都可以和哪些物质反应?
酚酞试液
稀HCl
稀H2SO4
Ca(OH)2
BaCl2
实验探究纯碱的化学性质
溶液变成红色
产生气泡,燃着的木条熄灭
产生气泡,燃着的木条熄灭
产生白色沉淀
产生白色沉淀
Na2CO3固体
Na2CO3溶液
HCl
H2SO4
Ca(OH)2
BaCl2
Na2CO3溶液
1. Na2CO3与指示剂作用(酚酞)
2. Na2CO3与稀HCl﹑稀H2SO4反应
3. Na2CO3与Ca(OH)2反应
4. Na2CO3与BaCl2反应
实验结论
Na2CO3+ 2HCl= 2NaCl+H2O +CO2↑
Na2CO3+H2SO4= Na2SO4+H2O+ CO2↑
Na2CO3+Ca(OH)2= 2NaOH+ Ca CO3↓
Na2CO3+BaCl2= 2NaCl+BaCO3↓
复分解反应
纯碱的化学性质
1.碳酸钠溶液呈碱性,能使指示剂变色。
2.碳酸钠能与酸发生复分解反应生成二氧化碳
Na2CO3 + 2HCl=2NaCl+H2O+CO2↑
Na2CO3 + H2SO4=Na2SO4+H2O+CO2↑
3.碳酸钠与碱溶液发生复分解反应
Na2CO3 + Ca(OH)2=CaCO3 ↓+2NaOH
4.碳酸钠与盐溶液发生复分解反应
Na2CO3 +BaCl2=BaCO3 ↓+2NaCl
小结
三、盐在水溶液中发生的反应
酸
碱
盐
盐
复分解反应
反应物可均溶
(↑ 或↓或H2O)
CaCO3+ Ba(OH)2
Na2CO3+ Ba(OH)2
只用一种试剂来鉴别NaOH、Ca(OH)2、稀H2SO4三种溶液,这种试剂是_______
A.氯化钡溶液 B.紫色石蕊试液
C.碳酸钠溶液 D.酚酞试液
C
思维训练
NaOH
Ca(OH)2
H2SO4
BaCl2
NaOH
Ca(OH)2
H2SO4
Na2CO3
小苏打在生产和生活中的用途
NaHCO3
盐
写出下列化学方程式
CaCO3 + HCl---
Na2CO3 + HCl---
NaHCO3 + HCl---
Na2CO3 + H2SO4---
思考
如何检验鸡蛋壳中含有碳酸根?
碳酸根的检验方法
加稀盐酸并将产生的气体通入澄清石灰水中
CaCO3+ 2HCl= CaCl2+H2O +CO2↑
CO2 + Ca(OH)2= CaCO3↓ + H2O
我的收获
纯碱的性质
物理性质:白色粉末状固体,易溶于水。
化学性质:
1.碳酸钠溶液呈碱性
2.碳酸钠与酸反应生成二氧化碳
Na2CO3 + 2HCl=2NaCl+H2O+CO2↑
3.碳酸钠与碱溶液反应
Na2CO3 + Ca(OH)2=CaCO3 ↓+2NaOH
4.碳酸钠与盐溶液反应
Na2CO3 +BaCl2=BaCO3 ↓+2NaCl
盐在水溶液中发生的反应
酸
碱
盐
盐
1、除去氯化钠中的杂质碳酸钠,下列方法不能实现的是________
A.加适量盐酸,蒸发结晶
B.加适量氯化钙,过滤后蒸发结晶
C.加适量氢氧化钡,过滤后蒸发结晶
D.加适量氢氧化钠,过滤后蒸发结晶
2、检验碳酸盐的正确方法是_____
A.滴加盐酸,产生使木条火焰熄灭的气体
B.滴加BaCl2溶液产生白色沉淀
C.加热,产生使澄清石灰水变浑浊的气体
D.滴加盐酸产生使澄清石灰水变浑浊的气体
挑战自我
C、D
D
3、学习碳酸钠知识时,老师做碳酸钠溶液和澄清石灰水反应演示实验,并对浑浊液过滤,得到澄清滤液.课堂上老师的提问和同学们的回答如图所示:
挑战自我
可能是NaOH和Ca(OH)2
(1)假设你是丁同学,请你也提出一个与甲、乙、丙同学不同的猜想,把猜想写在对话框中.并对你自己的猜想设计一个简单的实验加以证明.
挑战自我
实验步骤
实验现象
实验结论
取样于试管中,
____________
____________
自己的猜想正确
(2)你认为甲、乙、丙同学的猜想都合理吗?如有不合理的请说明理由:__________
_________________________________.
滴加Na2CO3溶液,
有白色沉淀生成
Na2CO3和Ca(OH)2能发生反应,不能共存。
乙不合理
(3)甲同学针对自己的猜想进行了如下实验:
(甲同学认为可能含有NaOH和Na2CO3)
挑战自我
实验步骤
实验现象
实验结论
取样于试管中,滴加几滴稀盐酸
没有气泡产生
甲的猜想不成立
你认为甲同学的实验设计是否正确?______请说明理由:___________________________________.
不正确
有NaOH存在,滴入少量盐酸先与NaOH反应就不会有CO2放出,但Na2CO3可能存在。
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
