高中化学选修5人教版第二章第一节:脂肪烃(共34张PPT)
文档属性
| 名称 | 高中化学选修5人教版第二章第一节:脂肪烃(共34张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-07-13 00:00:00 | ||
图片预览









文档简介
(共34张PPT)
第二章
烃和卤代烃
第一节
脂
肪
烃
生活中常见的轮胎、PVC管材等都是以烃为主要原
料的产品,而脂肪烃是一类常见的烃。哪些有机物
属于脂肪烃?它们又有什么样的特性呢?
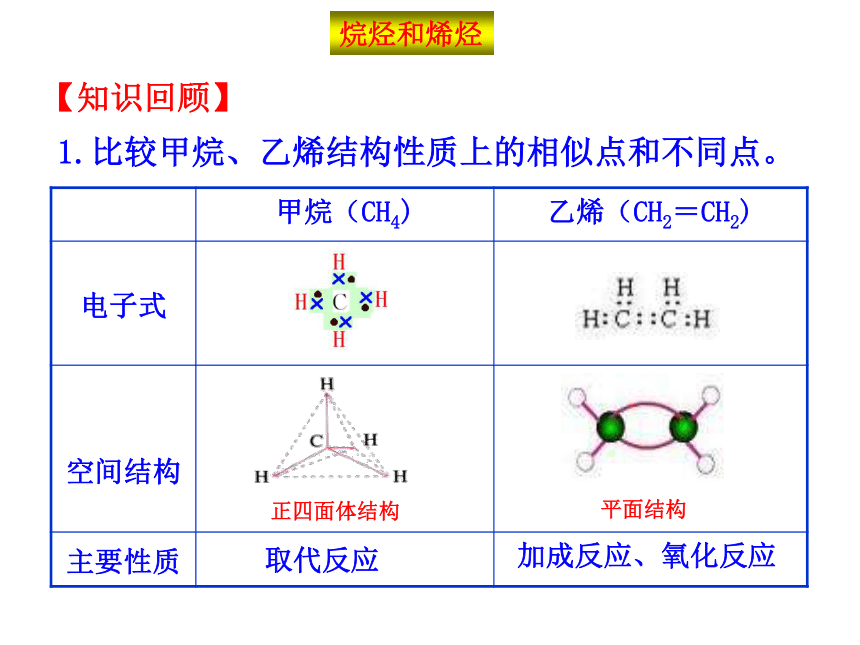
1.比较甲烷、乙烯结构性质上的相似点和不同点。
正四面体结构
平面结构
取代反应
加成反应、氧化反应
【知识回顾】
烷烃和烯烃
甲烷(CH4)
乙烯(CH2=CH2)
电子式
空间结构
主要性质
【活动探究】
根据教材P28表2-1和表2-2中给出的数据,以分子中碳原子数为横坐标,以沸点或相对密度为纵坐标,制作分子中碳原子数与沸点或相对密度变化的曲线图。
脂肪烃的物理性质递变规律
烷烃和烯烃
【归纳总结】
同系物物理性质的递变规律
烷烃和烯烃
分子中碳原子数
相对密度
2
4
6
8
10
12
14
16
0.6
0.4
0.2
0
烷烃
烯烃
递变原因:
分子间作用力随相对分子质量的增大而逐渐增大;导致物理性质上的递变
物理性质归纳
烷烃和烯烃的物理性质随着分
子中碳原子数的递增,呈现规
律性变化,沸点逐渐
,
相对密度逐渐
,常温下
的存在状态,____________
_________________。
升高
增大
气态逐渐过渡到液态、固态
烷烃和烯烃
烷烃的化学性质—与甲烷相似
通常情况下,甲烷性质稳定,与强酸、强碱和强氧化剂等一
般不发生化学反应。在特定条件下甲烷能与某些物质发生化
学反应,如可以燃烧和发生取代反应等。
CH4
CH3Cl
Cl2
Cl2
CH2Cl2
CHCl3
CCl4
Cl2
取代反应:
烷烃
【即时巩固】
下列有关烷烃的叙述中,正确的是( )
A.在烷烃分子中,所有的化学键都是单键
B.烷烃中除甲烷外,很多都能使酸性KMnO4溶液的紫
色褪去
C.分子通式为CnH2n+2的烃不一定是烷烃
D.有些烷烃在光照条件下不能与氯气发生取代反应
A
烷烃
烯烃化学性质——与乙烯相似
①加成反应(与H2、Br2、HX、H2O等):
使溴水褪色,可用于检测烯烃
②氧化反应
a.燃烧:火焰明亮,冒黑烟
b.催化氧化:
c.与酸性高锰酸钾溶液反应,使酸性高锰酸钾溶液褪色
烯烃
③加聚反应
由相对分子质量小的化合物分子互相结合成相
对分子质量大的高分子化合物的反应叫做聚合反应。
由不饱和的相对分子质量小的化合物分子结合
成相对分子质量大的化合物分子,这样的聚合反应
同时也是加成反应,所以这样的聚合反应又叫做加
聚反应。
烯烃
【即时巩固】
既可以用来鉴别乙烯和甲烷,又可用来除去甲烷中
混有的乙烯的方法是( )
A.通入足量溴水中
B.与足量的液溴反应
C.通入高锰酸钾酸性溶液中
D.一定条件下与H2反应
A
【提示】除去甲烷中混有的乙烯不能用高锰酸钾酸
性溶液,因为乙烯会被高锰酸钾酸性溶液氧化生成
二氧化碳气体,而引入新杂质。
烯烃
(1)通式:
1,3-丁二烯
CH2=CH-CH=CH2
(2)代表物:
CnH2n-2
【归纳总结】二烯烃
二烯烃
比较丁烷和1,3-丁二烯的结构
【问题探究】
【思考交流】
烷烃和二烯烃的结构和化学性质有什么区别?
①加成反应
②加聚反应
(3)化学性质:
二烯烃
由于碳碳双键不能旋转而导致分子中原子或原子团在空间的
排列方式不同所产生的异构现象,称为顺反异构。
(1)具有碳碳双键。
(2)组成双键的每个碳原子必须连接两个不同的原子或原子团。
即a′?b′,a?b,且a=a′、b=b′至少有一个存在。
1.顺反异构
2.顺反异构产生的条件
【归纳总结】
烯烃的顺反异构
【思考交流】
什么是顺反异构?顺反异构产生的原因是什么?
两个相同的原子或原子团在双键的同一侧时称为顺式异构。
两个相同的原子或原子团在双键的两侧时称为反式异构。
思考:互为顺反异构的物质在性质上有何关系?
【提示】化学性质几乎相同,物理性质略有差异。
3.顺式异构和反式异构
烯烃的顺反异构
下列物质中不存在顺反异构的是(
)
A.1,2-二氯乙烯
B.1,2-二氯丙烯
C.2-甲基-2-丁烯
D.2-氯-2-丁烯
C
【特别提醒】
能否形成顺反异构要看两个方面,一看是否有双键;二看双键两端的基团是否相同。
【即时巩固】
烯烃的顺反异构
分子里含有碳碳三键的一类脂肪烃称为炔烃。
1.概念:
2.炔烃的通式:CnH2n-2(n≥2)
3.炔烃的通性:
(1)物理性质:随着碳原子数的增多,沸点逐渐升高,液态时的密度逐渐增加;碳原子数小于等于4时为气态。
(2)化学性质:能发生氧化反应,加成反应。
炔烃
炔烃
乙炔
(1)乙炔的分子结构:
H—C≡C—H
结构简式:
CH≡CH或HC≡CH
结构式:
直线型,键角180°
空间结构:
1.碳碳三键的键能并不是碳碳单键的三倍,也不是碳碳双键和碳碳单键之和。说明三键中有两个键不稳定,容易断裂,有一个键较稳定。
2.含有三键结构的相邻四原子在同一直线上。
3.链烃分子里含有碳碳三键的不饱和烃称为炔烃。
4.乙炔是最简单的炔烃。
炔烃
①氧化反应:
a.可燃性:
火焰明亮,并伴有浓烟
b.乙炔能被酸性高锰酸钾溶液氧化,使酸性高锰酸钾溶液
褪色
(2)乙炔的化学性质:
炔烃
c.与HX等的反应
②加成反应
a.使溴水褪色
b.催化加氢
CH≡CH+2Br2
CHBr2CHBr2
CH≡CH+2H2
CH3CH3
催化剂
催化剂
炔烃
A.原料:CaC2与H2O
CaC2
+2H—OH
C2H2↑+Ca(OH)2
C.装置:
D.收集方法:
E.净化:
B.反应原理:
乙炔的实验室制取
【实验探究】
乙炔的实验室制取
实验中采用块状
CaC2和饱和食盐水,
为什么?
实验中为什么要采用分液漏斗?
制出的乙炔气体为什么先通入硫酸铜溶液?
乙炔的实验室制取
【特别提醒】
(1)反应装置不能用启普发生器,要改用圆底烧瓶
和分液漏斗。
(2)实验中常用饱和食盐水代替水,目的:为了减
缓反应速率,得到平稳的乙炔气流。
(3)纯净的乙炔气体是无色无味的气体。用电石和
水反应制取的乙炔,常闻到恶臭气味,是因为不纯净的电石与水作用时生成H2S、AsH3、PH3等有特殊气味的杂质气体,因此用硫酸铜溶液除去。
乙炔的实验室制取
下列叙述乙炔的结构和性质中,既不同于乙烯,也
不同于乙烷的是( )
A.存在不饱和键
B.不易发生取代反应,易发生加成反应
C.分子中的所有原子都处在同一条直线上
D.能使酸性KMnO4溶液褪色
C
【即时巩固】
炔烃
脂肪烃的来源及其应用
【思考交流】与同学交流分析原油的分馏及裂化的
产品和用途。
脂肪烃的来源有石油、天然气和煤等。
1.
石油通过常压分馏可以得到石油气、汽油、煤油、柴油等;而减压分馏可以得到润滑油、石蜡等分子质量较大的烷烃;通过石油的催化及裂解可以得到较多的轻质油和气态烯烃,气态烯烃是最基本的化工原料;而催化重整是获得芳香烃的主要途径。
脂肪烃的来源及其应用
脂肪烃的来源及其应用
2.天然气是高效清洁燃料,主要是烃类气体,以甲烷为主。
3.煤也是获得有机化合物的源泉。通过煤焦油的分馏可以获得各种芳香烃;通过煤的直接或间接液化,可以获得燃料油及多种化工原料。
脂肪烃的来源及其应用
烷烃
(碳碳单键)
烯烃
(碳碳双键)
炔烃
(碳碳三键)
取代反应
加成反应
加聚反应
加氢
加氢
加氢
1.下列关于乙烯和乙烷的说法中,不正确的是
A.乙烯属于不饱和链烃,乙烷属于饱和链烃
B.乙烯分子中所有原子处于同一平面上,乙烷分子
则为立体结构,所有原子不在同一平面上
C.乙烯分子中的
和乙烷分子中的C—C相比
较,双键的键能大,键长长
D.乙烯能使酸性KMnO4溶液褪色,乙烷不能
√
2.欲制取较纯净的1,2?二氯乙烷,可采用的方法
是
A.乙烯和HCl加成
B.乙烯和氯气加成
C.乙烷和Cl2按1:2的体积比在光照条件下反应
D.乙烯先与HCl加成,再与等物质的量的氯气在
光照条件下反应
【提示】取代反应不能得到纯净的取代产物,故C、D不正确;乙烯和HCl加成,产物为一氯乙烷,故A不正确。
√
3.由乙烯推测丙烯的结构或性质正确的是
A.分子中3个碳原子在同一直线上
B.分子中所有原子在同一平面上
C.与氯化氢加成只生成一种产物
D.能使酸性KMnO4溶液褪色
【提示】丙烯的结构简式为CH3CH=CH2,分子中3个碳原子在
同一平面上,但不在同一直线上,A错;丙烯分子中的—CH3
中C与H并不共面,B错;丙烯与HCl加成可生成CH3CH2CH2Cl或CH3CHClCH3,C错;丙烯分子中含有双键,可使酸性KMnO4溶液褪色,D正确。
√
4.下列关于乙炔的描述中,不正确的是
A.乙炔是无色有特殊臭味的气体
B.不能用启普发生器制取乙炔气体
C.乙炔易与溴水发生加成反应
D.乙炔分子中所有原子都在同一直线上
【提示】乙炔是一种无色、无味的气体,实验室制
得的乙炔因混有H2S和PH3而具有特殊的臭味;乙炔
为直线形分子,其分子中所有原子处于同一直线上。
√
5.下列叙述中,不正确的是
A.天然气是以甲烷为主要成分的高效清洁燃料
B.煤的干馏可得到煤焦油,通过煤焦油的分馏可
获得各种芳香烃
C.石油中含有烷烃和环烷烃,因此由石油不可能
获得芳香烃
D.通过石油的催化裂化及裂解可以得到轻质油和
气态烯烃
√
一种美好的心情,比十付良药更能解除生理上的疲惫和痛楚。
——马克思
第二章
烃和卤代烃
第一节
脂
肪
烃
生活中常见的轮胎、PVC管材等都是以烃为主要原
料的产品,而脂肪烃是一类常见的烃。哪些有机物
属于脂肪烃?它们又有什么样的特性呢?
1.比较甲烷、乙烯结构性质上的相似点和不同点。
正四面体结构
平面结构
取代反应
加成反应、氧化反应
【知识回顾】
烷烃和烯烃
甲烷(CH4)
乙烯(CH2=CH2)
电子式
空间结构
主要性质
【活动探究】
根据教材P28表2-1和表2-2中给出的数据,以分子中碳原子数为横坐标,以沸点或相对密度为纵坐标,制作分子中碳原子数与沸点或相对密度变化的曲线图。
脂肪烃的物理性质递变规律
烷烃和烯烃
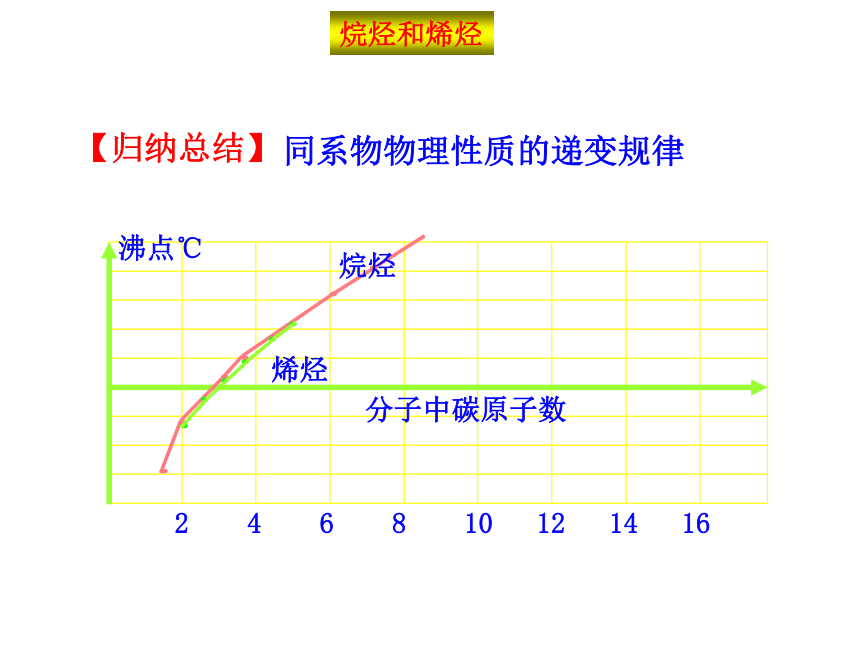
【归纳总结】
同系物物理性质的递变规律
烷烃和烯烃
分子中碳原子数
相对密度
2
4
6
8
10
12
14
16
0.6
0.4
0.2
0
烷烃
烯烃
递变原因:
分子间作用力随相对分子质量的增大而逐渐增大;导致物理性质上的递变
物理性质归纳
烷烃和烯烃的物理性质随着分
子中碳原子数的递增,呈现规
律性变化,沸点逐渐
,
相对密度逐渐
,常温下
的存在状态,____________
_________________。
升高
增大
气态逐渐过渡到液态、固态
烷烃和烯烃
烷烃的化学性质—与甲烷相似
通常情况下,甲烷性质稳定,与强酸、强碱和强氧化剂等一
般不发生化学反应。在特定条件下甲烷能与某些物质发生化
学反应,如可以燃烧和发生取代反应等。
CH4
CH3Cl
Cl2
Cl2
CH2Cl2
CHCl3
CCl4
Cl2
取代反应:
烷烃
【即时巩固】
下列有关烷烃的叙述中,正确的是( )
A.在烷烃分子中,所有的化学键都是单键
B.烷烃中除甲烷外,很多都能使酸性KMnO4溶液的紫
色褪去
C.分子通式为CnH2n+2的烃不一定是烷烃
D.有些烷烃在光照条件下不能与氯气发生取代反应
A
烷烃
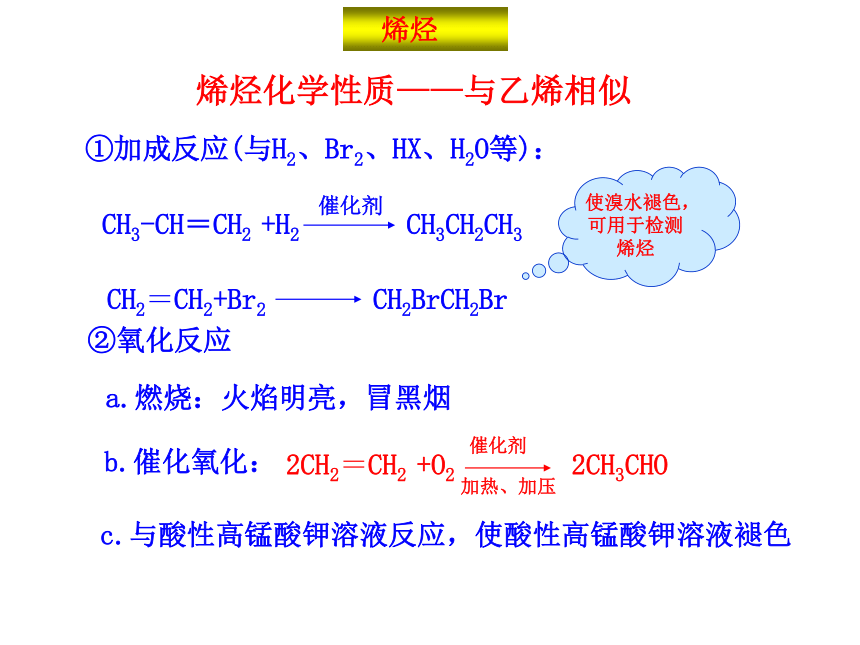
烯烃化学性质——与乙烯相似
①加成反应(与H2、Br2、HX、H2O等):
使溴水褪色,可用于检测烯烃
②氧化反应
a.燃烧:火焰明亮,冒黑烟
b.催化氧化:
c.与酸性高锰酸钾溶液反应,使酸性高锰酸钾溶液褪色
烯烃
③加聚反应
由相对分子质量小的化合物分子互相结合成相
对分子质量大的高分子化合物的反应叫做聚合反应。
由不饱和的相对分子质量小的化合物分子结合
成相对分子质量大的化合物分子,这样的聚合反应
同时也是加成反应,所以这样的聚合反应又叫做加
聚反应。
烯烃
【即时巩固】
既可以用来鉴别乙烯和甲烷,又可用来除去甲烷中
混有的乙烯的方法是( )
A.通入足量溴水中
B.与足量的液溴反应
C.通入高锰酸钾酸性溶液中
D.一定条件下与H2反应
A
【提示】除去甲烷中混有的乙烯不能用高锰酸钾酸
性溶液,因为乙烯会被高锰酸钾酸性溶液氧化生成
二氧化碳气体,而引入新杂质。
烯烃
(1)通式:
1,3-丁二烯
CH2=CH-CH=CH2
(2)代表物:
CnH2n-2
【归纳总结】二烯烃
二烯烃
比较丁烷和1,3-丁二烯的结构
【问题探究】
【思考交流】
烷烃和二烯烃的结构和化学性质有什么区别?
①加成反应
②加聚反应
(3)化学性质:
二烯烃
由于碳碳双键不能旋转而导致分子中原子或原子团在空间的
排列方式不同所产生的异构现象,称为顺反异构。
(1)具有碳碳双键。
(2)组成双键的每个碳原子必须连接两个不同的原子或原子团。
即a′?b′,a?b,且a=a′、b=b′至少有一个存在。
1.顺反异构
2.顺反异构产生的条件
【归纳总结】
烯烃的顺反异构
【思考交流】
什么是顺反异构?顺反异构产生的原因是什么?
两个相同的原子或原子团在双键的同一侧时称为顺式异构。
两个相同的原子或原子团在双键的两侧时称为反式异构。
思考:互为顺反异构的物质在性质上有何关系?
【提示】化学性质几乎相同,物理性质略有差异。
3.顺式异构和反式异构
烯烃的顺反异构
下列物质中不存在顺反异构的是(
)
A.1,2-二氯乙烯
B.1,2-二氯丙烯
C.2-甲基-2-丁烯
D.2-氯-2-丁烯
C
【特别提醒】
能否形成顺反异构要看两个方面,一看是否有双键;二看双键两端的基团是否相同。
【即时巩固】
烯烃的顺反异构
分子里含有碳碳三键的一类脂肪烃称为炔烃。
1.概念:
2.炔烃的通式:CnH2n-2(n≥2)
3.炔烃的通性:
(1)物理性质:随着碳原子数的增多,沸点逐渐升高,液态时的密度逐渐增加;碳原子数小于等于4时为气态。
(2)化学性质:能发生氧化反应,加成反应。
炔烃
炔烃
乙炔
(1)乙炔的分子结构:
H—C≡C—H
结构简式:
CH≡CH或HC≡CH
结构式:
直线型,键角180°
空间结构:
1.碳碳三键的键能并不是碳碳单键的三倍,也不是碳碳双键和碳碳单键之和。说明三键中有两个键不稳定,容易断裂,有一个键较稳定。
2.含有三键结构的相邻四原子在同一直线上。
3.链烃分子里含有碳碳三键的不饱和烃称为炔烃。
4.乙炔是最简单的炔烃。
炔烃
①氧化反应:
a.可燃性:
火焰明亮,并伴有浓烟
b.乙炔能被酸性高锰酸钾溶液氧化,使酸性高锰酸钾溶液
褪色
(2)乙炔的化学性质:
炔烃
c.与HX等的反应
②加成反应
a.使溴水褪色
b.催化加氢
CH≡CH+2Br2
CHBr2CHBr2
CH≡CH+2H2
CH3CH3
催化剂
催化剂
炔烃
A.原料:CaC2与H2O
CaC2
+2H—OH
C2H2↑+Ca(OH)2
C.装置:
D.收集方法:
E.净化:
B.反应原理:
乙炔的实验室制取
【实验探究】
乙炔的实验室制取
实验中采用块状
CaC2和饱和食盐水,
为什么?
实验中为什么要采用分液漏斗?
制出的乙炔气体为什么先通入硫酸铜溶液?
乙炔的实验室制取
【特别提醒】
(1)反应装置不能用启普发生器,要改用圆底烧瓶
和分液漏斗。
(2)实验中常用饱和食盐水代替水,目的:为了减
缓反应速率,得到平稳的乙炔气流。
(3)纯净的乙炔气体是无色无味的气体。用电石和
水反应制取的乙炔,常闻到恶臭气味,是因为不纯净的电石与水作用时生成H2S、AsH3、PH3等有特殊气味的杂质气体,因此用硫酸铜溶液除去。
乙炔的实验室制取
下列叙述乙炔的结构和性质中,既不同于乙烯,也
不同于乙烷的是( )
A.存在不饱和键
B.不易发生取代反应,易发生加成反应
C.分子中的所有原子都处在同一条直线上
D.能使酸性KMnO4溶液褪色
C
【即时巩固】
炔烃
脂肪烃的来源及其应用
【思考交流】与同学交流分析原油的分馏及裂化的
产品和用途。
脂肪烃的来源有石油、天然气和煤等。
1.
石油通过常压分馏可以得到石油气、汽油、煤油、柴油等;而减压分馏可以得到润滑油、石蜡等分子质量较大的烷烃;通过石油的催化及裂解可以得到较多的轻质油和气态烯烃,气态烯烃是最基本的化工原料;而催化重整是获得芳香烃的主要途径。
脂肪烃的来源及其应用
脂肪烃的来源及其应用
2.天然气是高效清洁燃料,主要是烃类气体,以甲烷为主。
3.煤也是获得有机化合物的源泉。通过煤焦油的分馏可以获得各种芳香烃;通过煤的直接或间接液化,可以获得燃料油及多种化工原料。
脂肪烃的来源及其应用
烷烃
(碳碳单键)
烯烃
(碳碳双键)
炔烃
(碳碳三键)
取代反应
加成反应
加聚反应
加氢
加氢
加氢
1.下列关于乙烯和乙烷的说法中,不正确的是
A.乙烯属于不饱和链烃,乙烷属于饱和链烃
B.乙烯分子中所有原子处于同一平面上,乙烷分子
则为立体结构,所有原子不在同一平面上
C.乙烯分子中的
和乙烷分子中的C—C相比
较,双键的键能大,键长长
D.乙烯能使酸性KMnO4溶液褪色,乙烷不能
√
2.欲制取较纯净的1,2?二氯乙烷,可采用的方法
是
A.乙烯和HCl加成
B.乙烯和氯气加成
C.乙烷和Cl2按1:2的体积比在光照条件下反应
D.乙烯先与HCl加成,再与等物质的量的氯气在
光照条件下反应
【提示】取代反应不能得到纯净的取代产物,故C、D不正确;乙烯和HCl加成,产物为一氯乙烷,故A不正确。
√
3.由乙烯推测丙烯的结构或性质正确的是
A.分子中3个碳原子在同一直线上
B.分子中所有原子在同一平面上
C.与氯化氢加成只生成一种产物
D.能使酸性KMnO4溶液褪色
【提示】丙烯的结构简式为CH3CH=CH2,分子中3个碳原子在
同一平面上,但不在同一直线上,A错;丙烯分子中的—CH3
中C与H并不共面,B错;丙烯与HCl加成可生成CH3CH2CH2Cl或CH3CHClCH3,C错;丙烯分子中含有双键,可使酸性KMnO4溶液褪色,D正确。
√
4.下列关于乙炔的描述中,不正确的是
A.乙炔是无色有特殊臭味的气体
B.不能用启普发生器制取乙炔气体
C.乙炔易与溴水发生加成反应
D.乙炔分子中所有原子都在同一直线上
【提示】乙炔是一种无色、无味的气体,实验室制
得的乙炔因混有H2S和PH3而具有特殊的臭味;乙炔
为直线形分子,其分子中所有原子处于同一直线上。
√
5.下列叙述中,不正确的是
A.天然气是以甲烷为主要成分的高效清洁燃料
B.煤的干馏可得到煤焦油,通过煤焦油的分馏可
获得各种芳香烃
C.石油中含有烷烃和环烷烃,因此由石油不可能
获得芳香烃
D.通过石油的催化裂化及裂解可以得到轻质油和
气态烯烃
√
一种美好的心情,比十付良药更能解除生理上的疲惫和痛楚。
——马克思
