人教版高二化学选修5第四章第二节 糖类(共31张PPT)
文档属性
| 名称 | 人教版高二化学选修5第四章第二节 糖类(共31张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 5.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-07-17 00:00:00 | ||
图片预览










文档简介
(共31张PPT)
第四章
生命中的有机化学物质
第二节
糖
类
学习目标
1.
了解糖类的组成和分类方法;
2.
掌握葡萄糖的结构特点和化学性质。
3.
初步了解单糖的应用
学习重点:葡萄糖的化学性质
含
糖
类
物
质
含
糖
类
物
质
(一)、来源
绿色植物光合反应的产物。
(二)、组成
人们对糖类物质的最初认识认为糖类物质的组成元素是C、H、O;而且很多糖类物质中H、O个数之比为2∶1,故把它们称为碳水化合物,通式为Cm(H2O)n
。
由C、H、O元素组成。
糖类概况:
但是:
通式并不能反映糖类的结构特点。
实验证明,糖类物质中:
①糖类物质中不存在水分子;
②有些糖类物质中的H、O原子个数之比不符合2∶1。如:脱氧核糖(C5H10O4)、鼠李糖(C6H12O5);
③有些物质分子中的H、O原子个数之比符合2∶1的又不是糖类。乙酸C2H4O2
,甲醛CH2O
糖类的认识?
鼠李糖
C6H12O5
甲醛
CH2O
,
乙酸
C2H4O2
(三)、定义
如何定义糖类?
(四)、糖类如何分类?
-葡萄糖、果糖及核糖
-麦芽糖、蔗糖
-淀粉、纤维素
糖类定义为多羟基醛﹑多羟基酮和它们的脱水缩合物。
1mol糖水解后能产生2~10mol单糖,
以二糖最为重要;
根据水解及水解后的产物分为:
单糖:
不能水解的糖
多糖:1mol水解产生很多摩尔单糖
低聚糖:
1
mol糖水解生成n
mol单糖
判断下列说法是否正确
(1)糖类也叫碳水化合物,所以糖类中存在水分子。(
)
(2)所有符合通式Cn(H2O)m的有机化合物都是糖类.(
)
(3)所有的糖类都符合通式Cn(H2O)m
。(
)
(4)含有C、H、O三种元素的有机物叫糖(
)
(5)糖类物质都有甜味(
)
×
×
×
×
×
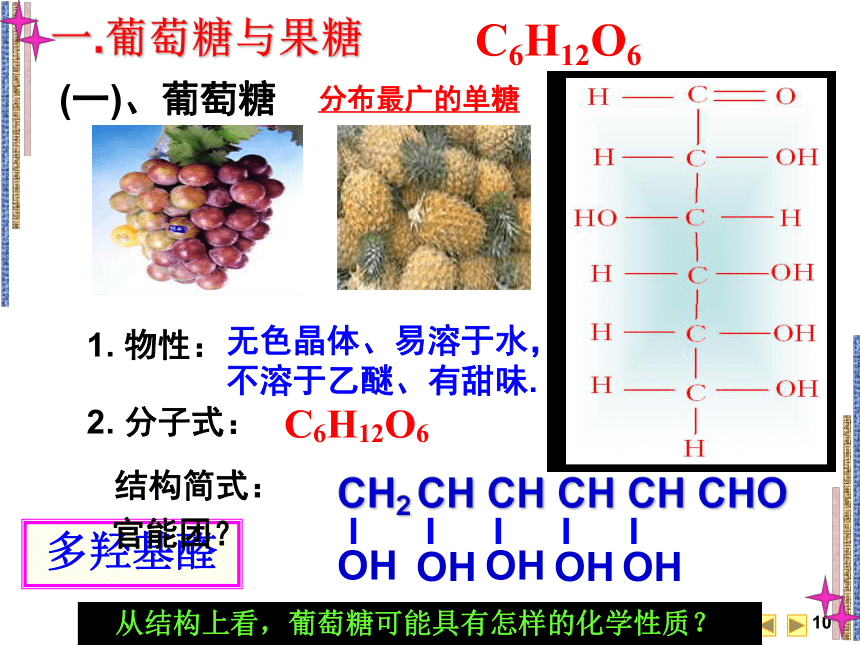
一.葡萄糖与果糖
(一)、葡萄糖
C6H12O6
无色晶体、易溶于水,稍溶于乙醇,不溶于乙醚、有甜味.
1.
物性:
2.
分子式:
C6H12O6
结构简式:
多羟基醛
从结构上看,葡萄糖可能具有怎样的化学性质?
分布最广的单糖
官能团?
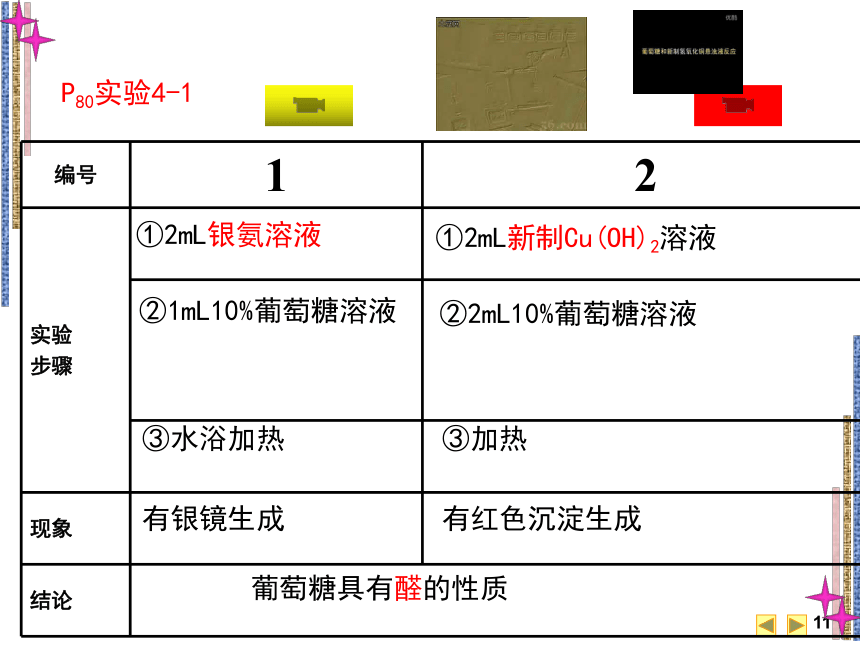
P80实验4-1
①2mL银氨溶液
②1mL10%葡萄糖溶液
③水浴加热
①2mL新制Cu(OH)2溶液
③加热
②2mL10%葡萄糖溶液
有银镜生成
有红色沉淀生成
葡萄糖具有醛的性质
编号
1
2
实验
步骤
现象
结论
实验4-1
葡萄糖的银镜反应
葡萄糖与新制Cu(OH)2的反应
CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O
实验注意事项:……
CH2OH(CHOH)4COONa+Cu2O↓+3H2O
与新制氢氧化铜的反应,在医疗上检测尿糖。
阅读:糖尿病的检测
健康人:胰腺中的胰岛素控制血糖的水平,食物消化后血糖上升,胰腺释放胰岛素消耗和储存葡萄糖(肝和肌肉),导致葡萄糖水平下降,使得胰腺减少胰岛素的释放。
糖尿病:糖尿病人不能生产足够的胰岛素,血液和尿液中葡萄糖含量高,身体靠分解脂肪产生能量并产生酮酸,严重时导致中毒。
检测
血糖的检测:医院用专门仪器检测
方法
糖尿的检测:在家中用尿糖试纸浸入尿液中,约1秒钟取出,在1分钟内观察试纸的颜色,并与标准比色板对比,即得出测定结果。
化学原理:与新制Cu(OH)2的反应
注意:治疗糖尿病的最终目的是要控制血糖,而尿糖检测只是粗略地了解血糖水平。
(一)、葡萄糖
4.
化学性质:
银镜反应;与新制Cu(OH)2反应;
(2)具多元醇的性质:
(1)具醛的性质:
酯化反应
与H2加成(还原)
(己六醇)
酸
+
醇
→
酯
+
水
葡萄糖能使溴水褪色
CH2OH(CHOH
)4CHO
+
Br2+
H2O
CH2OH(CHOH
)4COOH
+
2HBr
(葡萄糖酸)
5
5
五乙酸葡萄糖酯
多元醇的性质
(与乙酸发生酯化反应)
(3)
生理氧化
——
人体能量主要来源:
C6H12O6(s)
+
6O2(g)
6CO2(g)
+
6H2O(l)
(4)
发酵转化为乙醇:
酿酒
1、银镜反应
2、与新制Cu(OH)2悬浊液反应
5、氧化反应
小结:葡萄糖的化学性质
3、加氢还原
4、酯化反应
5.
用途
营养物质,
制糖果,
制镜、热水瓶胆镀银,
酿酒,
制药。
(一)、葡萄糖
【反馈练习】
1、葡萄糖是一种单糖的主要原因是(
)
A.结构简单
B.不能水解的糖
C.分子中含羟基和醛基的个数少
D.分子中含碳原子个数少
2、把NaOH溶液和CuSO4溶液加入某病人的尿液中,微热时,如果观察到红色沉淀,说明该尿液中含有(
)
A.食醋
B.白酒
C.食盐
D.葡萄糖
B
D
3.下列关于葡萄糖的化学性质不正确
的是(
)
A.能和金属钠反应放出氢气
B.能和H2发生加成反应
C.能发生银镜反应
D.水解反应
E.能发生酯化反应
D
【反馈练习】
(二)、果糖
1.
物性:
2.分子式:
3.
结构简式:
无色晶体、易溶于水、乙醇和乙醚、有甜味.最甜
C6H12O6
多羟基酮
4.
化性:
①
多元醇
的性质;
②体内氧化,程度缓慢;
存在于蜂蜜、水果中。天然存在的糖中最甜的一种。代谢不需胰岛素的调节,对糖尿病患者无害。
=O
[科学探究(P.80)]果糖是否也像葡萄糖一样具有还原性,能发生银镜反应呢?
与Na反应放出氢气,酯化反应
分子式:C6H12O6
结构简式:
CH2OHCHOHCHOHCHOHCOCH2OH
多羟基酮,是葡萄糖的同分异构体。
在碱性条件下,果糖分子中羰基受多个羟基的影响:
多羟基酮在碱性条件下转化成醛:果糖部分转变为葡萄糖.
③还原性:
银镜反应;与新制Cu(OH)2反应
葡萄糖与果糖
葡萄糖:
果糖:
分子式:C6H12O6
互为同分异构体
如何区分葡萄糖和果糖?
葡萄糖能使溴水褪色
在酸性条件下,果糖不被溴水氧化,可用溴水区分葡萄糖和果糖。
CH2OH(CHOH
)4CHO
+
Br2+
H2O
CH2OH(CHOH
)4COOH
+
2HBr
分子式:
结构简式:
官能团:
C6H12O6
CH2OH(CHOH
)4CHO
醛基、醇羟基
葡萄糖
化学性质
果糖:CH2OH(CHOH
)3COCH2OH
同分异构体
—OH的性质
①与Na反应放出氢气;
②Cu/Ag催化下与O2催化氧化成醛/酮
③与羧酸发生酯化反应。1:5
④与浓HX,△,生成卤代烃和水
⑤浓H2SO4,△,生成烯烃和水。
●核糖简介:
CH2OH-CHOH-CHOH-CHOH-CHO
(核糖)
脱氧核糖是核糖的一个2位羟基被氢取代的衍生物??。它在细胞中作为脱氧核糖核酸DNA的组分,十分重要。
CH2OH-CHOH-CHOH-CH2CHO
(脱氧核糖)
核糖是核糖核酸(RNA)的重要组成部分,具有醛糖的特性
(C5H10O5)
(C5H10O4)
4、
葡萄糖的结构简式CH2OH(CHOH)4CHO,
由此判断下列关于葡萄糖性质的叙述中不正确的是:(
)
A.葡萄糖具有醇类物质能发生酯化反应的
化学性质
B.葡萄糖具有醛类物质的还原性
C.葡萄糖完全燃烧的产物为CO2和H2O
D.充分燃烧等质量的葡萄糖和甲醛,所需氧气物质的量不相同。
D
5、下列关于糖类的叙述正确的是(
)
A.含有C、H、O三种元素的有机物是糖类
B.糖类物质均能发生银镜反应
C.糖类物质都有甜味
D.糖是多羟基醛或多羟基铜以及能水解
生成它的物质
D
6、以葡萄糖为原料经一步反应不能得到的是(
)
A、乙醛
B、二氧化碳
C、已六醇
D、葡萄糖酸
,
A
7.
在一定的条件下,既可以发生氧化反应,又可以发生还原反应,又可以和酸发生酯化反应的是(
)
A、乙醇
B、乙醛
C、乙酸
D、葡萄糖
D
练一练:
8、下列物质具有相同的最简式的组是(
)
A、乙醛
葡萄糖
B、乙酸
乙醛
C、乙醇
葡萄糖
D、甲酸甲酯
葡萄糖
9、葡萄糖所不具有的性质是(
)
A、和H2发生加成反应
B、和银氨溶液发生氧化反应
C、和酸发生酯化反应
D、和NaOH溶液反应
D
D
第四章
生命中的有机化学物质
第二节
糖
类
学习目标
1.
了解糖类的组成和分类方法;
2.
掌握葡萄糖的结构特点和化学性质。
3.
初步了解单糖的应用
学习重点:葡萄糖的化学性质
含
糖
类
物
质
含
糖
类
物
质
(一)、来源
绿色植物光合反应的产物。
(二)、组成
人们对糖类物质的最初认识认为糖类物质的组成元素是C、H、O;而且很多糖类物质中H、O个数之比为2∶1,故把它们称为碳水化合物,通式为Cm(H2O)n
。
由C、H、O元素组成。
糖类概况:
但是:
通式并不能反映糖类的结构特点。
实验证明,糖类物质中:
①糖类物质中不存在水分子;
②有些糖类物质中的H、O原子个数之比不符合2∶1。如:脱氧核糖(C5H10O4)、鼠李糖(C6H12O5);
③有些物质分子中的H、O原子个数之比符合2∶1的又不是糖类。乙酸C2H4O2
,甲醛CH2O
糖类的认识?
鼠李糖
C6H12O5
甲醛
CH2O
,
乙酸
C2H4O2
(三)、定义
如何定义糖类?
(四)、糖类如何分类?
-葡萄糖、果糖及核糖
-麦芽糖、蔗糖
-淀粉、纤维素
糖类定义为多羟基醛﹑多羟基酮和它们的脱水缩合物。
1mol糖水解后能产生2~10mol单糖,
以二糖最为重要;
根据水解及水解后的产物分为:
单糖:
不能水解的糖
多糖:1mol水解产生很多摩尔单糖
低聚糖:
1
mol糖水解生成n
mol单糖
判断下列说法是否正确
(1)糖类也叫碳水化合物,所以糖类中存在水分子。(
)
(2)所有符合通式Cn(H2O)m的有机化合物都是糖类.(
)
(3)所有的糖类都符合通式Cn(H2O)m
。(
)
(4)含有C、H、O三种元素的有机物叫糖(
)
(5)糖类物质都有甜味(
)
×
×
×
×
×
一.葡萄糖与果糖
(一)、葡萄糖
C6H12O6
无色晶体、易溶于水,稍溶于乙醇,不溶于乙醚、有甜味.
1.
物性:
2.
分子式:
C6H12O6
结构简式:
多羟基醛
从结构上看,葡萄糖可能具有怎样的化学性质?
分布最广的单糖
官能团?
P80实验4-1
①2mL银氨溶液
②1mL10%葡萄糖溶液
③水浴加热
①2mL新制Cu(OH)2溶液
③加热
②2mL10%葡萄糖溶液
有银镜生成
有红色沉淀生成
葡萄糖具有醛的性质
编号
1
2
实验
步骤
现象
结论
实验4-1
葡萄糖的银镜反应
葡萄糖与新制Cu(OH)2的反应
CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O
实验注意事项:……
CH2OH(CHOH)4COONa+Cu2O↓+3H2O
与新制氢氧化铜的反应,在医疗上检测尿糖。
阅读:糖尿病的检测
健康人:胰腺中的胰岛素控制血糖的水平,食物消化后血糖上升,胰腺释放胰岛素消耗和储存葡萄糖(肝和肌肉),导致葡萄糖水平下降,使得胰腺减少胰岛素的释放。
糖尿病:糖尿病人不能生产足够的胰岛素,血液和尿液中葡萄糖含量高,身体靠分解脂肪产生能量并产生酮酸,严重时导致中毒。
检测
血糖的检测:医院用专门仪器检测
方法
糖尿的检测:在家中用尿糖试纸浸入尿液中,约1秒钟取出,在1分钟内观察试纸的颜色,并与标准比色板对比,即得出测定结果。
化学原理:与新制Cu(OH)2的反应
注意:治疗糖尿病的最终目的是要控制血糖,而尿糖检测只是粗略地了解血糖水平。
(一)、葡萄糖
4.
化学性质:
银镜反应;与新制Cu(OH)2反应;
(2)具多元醇的性质:
(1)具醛的性质:
酯化反应
与H2加成(还原)
(己六醇)
酸
+
醇
→
酯
+
水
葡萄糖能使溴水褪色
CH2OH(CHOH
)4CHO
+
Br2+
H2O
CH2OH(CHOH
)4COOH
+
2HBr
(葡萄糖酸)
5
5
五乙酸葡萄糖酯
多元醇的性质
(与乙酸发生酯化反应)
(3)
生理氧化
——
人体能量主要来源:
C6H12O6(s)
+
6O2(g)
6CO2(g)
+
6H2O(l)
(4)
发酵转化为乙醇:
酿酒
1、银镜反应
2、与新制Cu(OH)2悬浊液反应
5、氧化反应
小结:葡萄糖的化学性质
3、加氢还原
4、酯化反应
5.
用途
营养物质,
制糖果,
制镜、热水瓶胆镀银,
酿酒,
制药。
(一)、葡萄糖
【反馈练习】
1、葡萄糖是一种单糖的主要原因是(
)
A.结构简单
B.不能水解的糖
C.分子中含羟基和醛基的个数少
D.分子中含碳原子个数少
2、把NaOH溶液和CuSO4溶液加入某病人的尿液中,微热时,如果观察到红色沉淀,说明该尿液中含有(
)
A.食醋
B.白酒
C.食盐
D.葡萄糖
B
D
3.下列关于葡萄糖的化学性质不正确
的是(
)
A.能和金属钠反应放出氢气
B.能和H2发生加成反应
C.能发生银镜反应
D.水解反应
E.能发生酯化反应
D
【反馈练习】
(二)、果糖
1.
物性:
2.分子式:
3.
结构简式:
无色晶体、易溶于水、乙醇和乙醚、有甜味.最甜
C6H12O6
多羟基酮
4.
化性:
①
多元醇
的性质;
②体内氧化,程度缓慢;
存在于蜂蜜、水果中。天然存在的糖中最甜的一种。代谢不需胰岛素的调节,对糖尿病患者无害。
=O
[科学探究(P.80)]果糖是否也像葡萄糖一样具有还原性,能发生银镜反应呢?
与Na反应放出氢气,酯化反应
分子式:C6H12O6
结构简式:
CH2OHCHOHCHOHCHOHCOCH2OH
多羟基酮,是葡萄糖的同分异构体。
在碱性条件下,果糖分子中羰基受多个羟基的影响:
多羟基酮在碱性条件下转化成醛:果糖部分转变为葡萄糖.
③还原性:
银镜反应;与新制Cu(OH)2反应
葡萄糖与果糖
葡萄糖:
果糖:
分子式:C6H12O6
互为同分异构体
如何区分葡萄糖和果糖?
葡萄糖能使溴水褪色
在酸性条件下,果糖不被溴水氧化,可用溴水区分葡萄糖和果糖。
CH2OH(CHOH
)4CHO
+
Br2+
H2O
CH2OH(CHOH
)4COOH
+
2HBr
分子式:
结构简式:
官能团:
C6H12O6
CH2OH(CHOH
)4CHO
醛基、醇羟基
葡萄糖
化学性质
果糖:CH2OH(CHOH
)3COCH2OH
同分异构体
—OH的性质
①与Na反应放出氢气;
②Cu/Ag催化下与O2催化氧化成醛/酮
③与羧酸发生酯化反应。1:5
④与浓HX,△,生成卤代烃和水
⑤浓H2SO4,△,生成烯烃和水。
●核糖简介:
CH2OH-CHOH-CHOH-CHOH-CHO
(核糖)
脱氧核糖是核糖的一个2位羟基被氢取代的衍生物??。它在细胞中作为脱氧核糖核酸DNA的组分,十分重要。
CH2OH-CHOH-CHOH-CH2CHO
(脱氧核糖)
核糖是核糖核酸(RNA)的重要组成部分,具有醛糖的特性
(C5H10O5)
(C5H10O4)
4、
葡萄糖的结构简式CH2OH(CHOH)4CHO,
由此判断下列关于葡萄糖性质的叙述中不正确的是:(
)
A.葡萄糖具有醇类物质能发生酯化反应的
化学性质
B.葡萄糖具有醛类物质的还原性
C.葡萄糖完全燃烧的产物为CO2和H2O
D.充分燃烧等质量的葡萄糖和甲醛,所需氧气物质的量不相同。
D
5、下列关于糖类的叙述正确的是(
)
A.含有C、H、O三种元素的有机物是糖类
B.糖类物质均能发生银镜反应
C.糖类物质都有甜味
D.糖是多羟基醛或多羟基铜以及能水解
生成它的物质
D
6、以葡萄糖为原料经一步反应不能得到的是(
)
A、乙醛
B、二氧化碳
C、已六醇
D、葡萄糖酸
,
A
7.
在一定的条件下,既可以发生氧化反应,又可以发生还原反应,又可以和酸发生酯化反应的是(
)
A、乙醇
B、乙醛
C、乙酸
D、葡萄糖
D
练一练:
8、下列物质具有相同的最简式的组是(
)
A、乙醛
葡萄糖
B、乙酸
乙醛
C、乙醇
葡萄糖
D、甲酸甲酯
葡萄糖
9、葡萄糖所不具有的性质是(
)
A、和H2发生加成反应
B、和银氨溶液发生氧化反应
C、和酸发生酯化反应
D、和NaOH溶液反应
D
D
