新人教版高中选修5化学4.3:蛋白质和核酸(46张PPT)
文档属性
| 名称 | 新人教版高中选修5化学4.3:蛋白质和核酸(46张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-07-18 00:00:00 | ||
图片预览








文档简介
(共46张PPT)
新课标人教版高中化学选修5
第四章
生命中的基础有机化学物质
第三节蛋白质和核酸
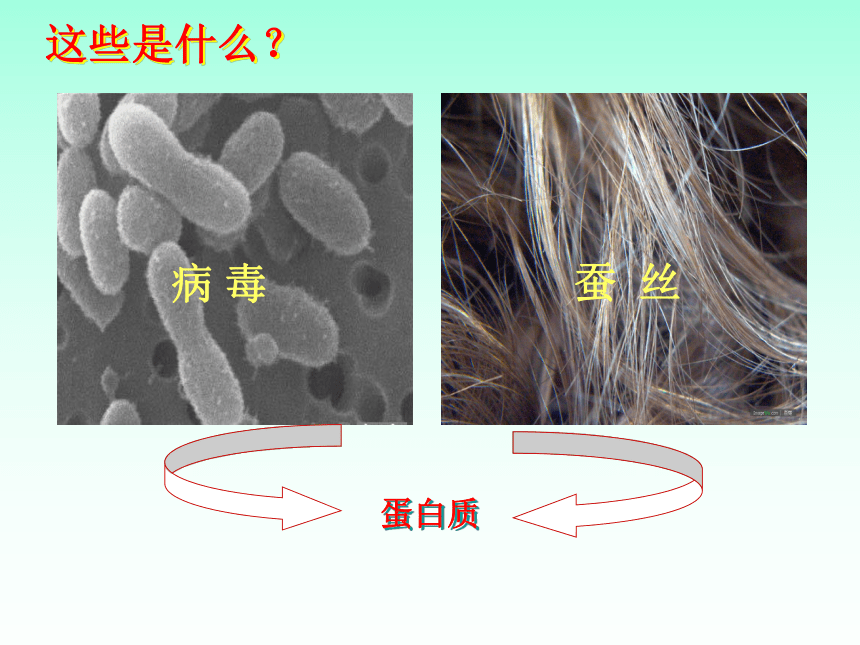
蛋白质
病
毒
蚕
丝
这些是什么?
没有蛋白质就没有生命
鲜
活
的
生
命
蛋
白
质
保
持
2、蛋白质的生物学重要性
(1).
蛋白质是生物体重要组成成分
蛋白质是细胞内最丰富的有机分子,占人体干重的45%,某些组织含量更高,例如脾、肺及横纹肌等高达80%。
分布广:
含量高:
所有器官、组织都含有蛋白质;细胞的各个部分都含有蛋白质。
1、什么是蛋白质?
蛋白质是由许多氨基酸通过肽键相连形成的高分子含氮有机化合物。
蛋白质占干重
人体中(中年人)
人体
45%
水55%
细菌
50%~80%
蛋白质19%
真菌
14%~52%
脂肪19%
酵母菌
14%~50%
糖类<1%
白地菌50%
无机盐7%
1)作为生物催化剂
2)代谢调节作用
3)免疫保护作用
4)物质的转运和存储
5)运动与支持作用
6)参与细胞间信息传递
(2)蛋白质具有重要的生物学功能
(3)氧化供能
第一课时
1.充分利用的图片,模型,多媒体等教学手段,增强知识的直观性。
2.通过讨论与交流,启发思维,逐步养成良好的学习习惯和学习方法。
1.掌握氨基酸的结构和性质,了解蛋白质的结构,了解核酸和酶的基本知识。
2.
进一步理解结构决定性质的理念。
知识与技能
教学目标
过程与方法
1.激发学习化学、探究化学原理的兴趣
。
2.强化理论与实际的联系,学以致用。
3.
增强民族自豪感。
情感态度与价值观
重点
难点
1.氨基酸的性质。
2.蛋白质的性质。
蛋白质的组成
教学重难点
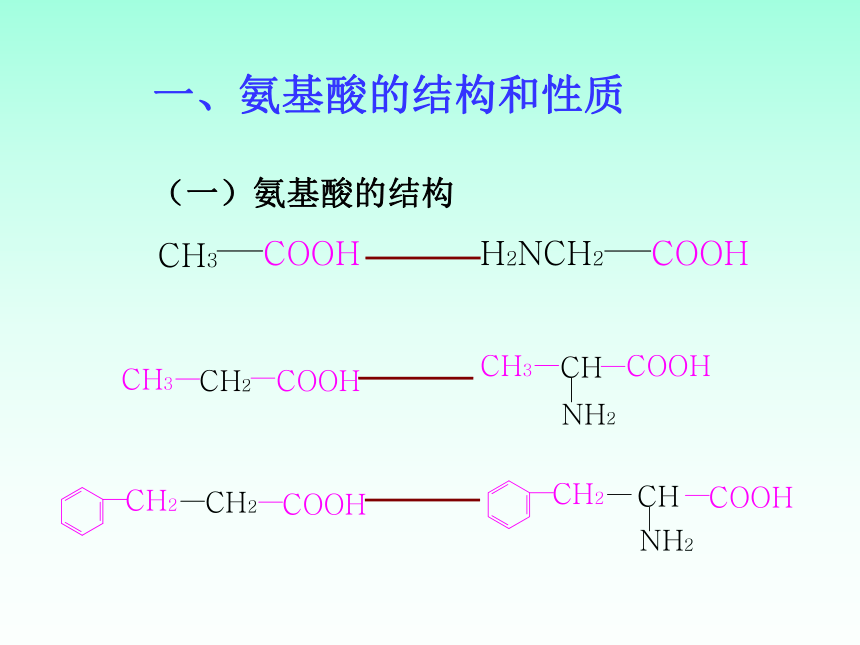
一、氨基酸的结构和性质
(一)氨基酸的结构
N
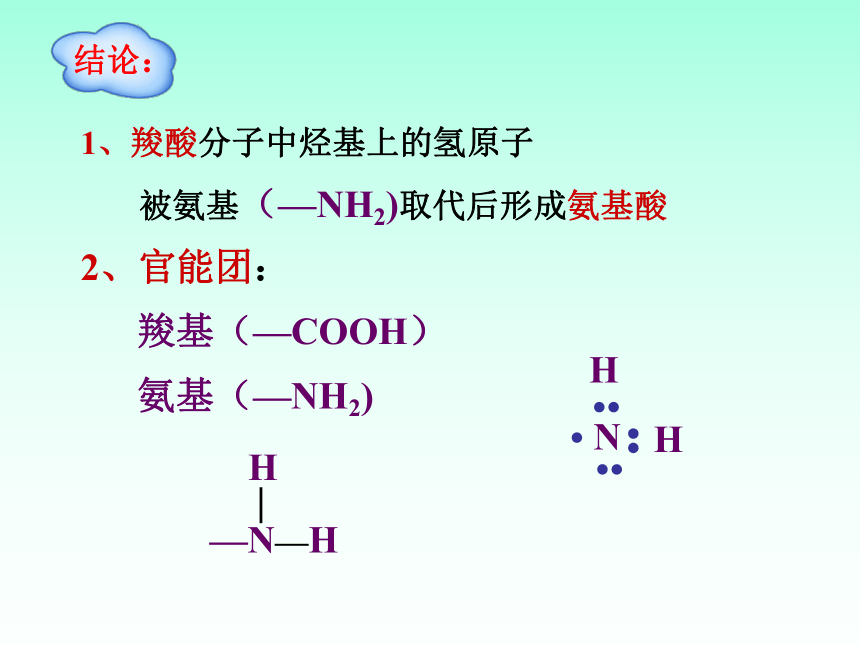
1、羧酸分子中烃基上的氢原子
被氨基(—NH2)取代后形成氨基酸
2、官能团:
羧基(—COOH)
氨基(—NH2)
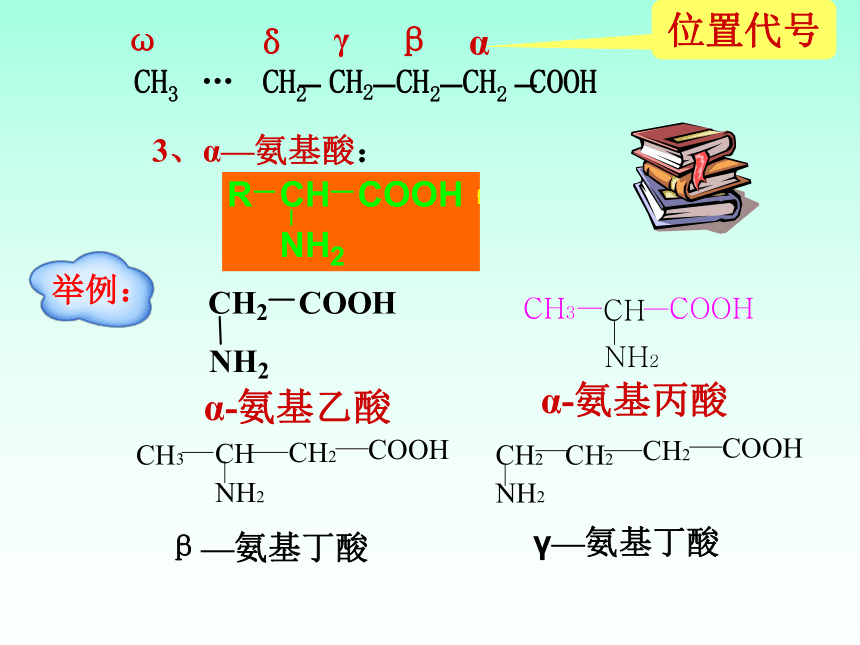
3、α—氨基酸:
α-氨基乙酸
α-氨基丙酸
α
β
γ
δ
ω
β—氨基丁酸
γ—氨基丁酸
位置代号
(二)氨基酸的性质
1、物理性质:
无色晶体,
熔点较高,约在230℃以上,
在水中溶解度不一,一般难溶于乙醇、乙醚,而溶于强酸或强碱溶液中。
2、化学性质:
结构决定性质,由氨基酸的结构推测氨基酸可能具有哪些化学性质?
羧基(—COOH)
氨基(—NH2)
具有羧酸的性质如:酸性
具有胺的性质如:碱性
由于这两种官能团的相互影响,又显示出一些特殊性质。如:两性。
(1)氨基酸的两性
+
H2O
与酸反应,体现碱性
与碱反应,体现酸性
+
甘氨酰甘氨酸
肽键
(2)成肽反应(缩合反应)
肽键:由一个氨基酸的?-羧基与另一个氨基酸的?-氨基脱水缩合而形成的化学键。
肽:由氨基酸通过肽键缩合而形成的化合物。
两分子氨基酸缩合形成二肽,三分子氨基酸缩合则形成三肽……
由十个以内氨基酸相连而成的肽称为寡肽,
由更多的氨基酸相连形成的肽称多肽。
五
肽
肽键
多
肽
当多肽链(相对分子质量大于10000)具有了完整的空间结构后,就形成了蛋白质。
肽键
蛋白质——牛核糖核酸酶的结构
二、蛋白质的结构与性质
碳
50%
氢
7%
氧
23%
氮
16%
硫
0~3%
其他
微
量
(一)蛋白质的元素组成
主要有C、H、O、N和S。
少量蛋白质含有少量磷或金属元素铁、铜、锌、锰、钴、钼,个别蛋白质还含有碘
。
属天然高分子化合物
各种蛋白质的含氮量很接近,平均为16%。
100克样品中蛋白质的含量
(
g
%
)
=
每克样品含氮克数×
6.25×100
1/16%
由于体内的含氮物质以蛋白质为主,因此,只要测定生物样品中的含氮量,就可以根据以下公式推算出蛋白质的大致含量:
附:蛋白质元素组成的特点
三聚氰胺(H2NCN)3
67%
(二)蛋白质的分子结构
一级结构(primary
structure)
二级结构(secondary
structure)
三级结构(tertiary
structure)
四级结构(quaternary
structure)
1、蛋白质的一级结构(多肽链)
定义
蛋白质的一级结构指蛋白质多肽链中氨基酸的排列顺序。
主要的化学键
肽键,有些蛋白质还包括二硫键。
附:牛胰岛素的一级结构
蛋白质分子中各段肽链主链骨架原子的空间分布状态(主链的空间构象),并不涉及氨基酸残基侧链的构象
。
(1)定义:
(2)主要的化学键:
氢键
2、蛋白质的二级结构(螺旋结构)
(3)二级结构的几种类型:
?-螺旋
(
?
-helix
)
?-折叠
(
?-pleated
sheet
)
?-转角
(
?-turn
)
无规卷曲
(
random
coil
)
?-螺旋
?-折叠(
?-片层)
?-转角
3、
三级结构(空间排布)
只含一个肽链的蛋白质,只具三级结构。如:肌红蛋白
(Mb)
多肽链上所有原子在三维空间的排布。
定义:
4、蛋白质的四级结构(立体组合)
蛋白质分子中各亚基的空间排布及相互联系,称为蛋白质的四级结构。
有些蛋白质分子含有二条或多条多肽链,每一条多肽链都有完整的三级结构,称为蛋白质的亚基
。
血红蛋白的四级结构
(三)蛋白质的性质
1.
蛋白质的两性
2.
蛋白质的水解反应
蛋白质
α—氨基酸
酶
3.
蛋白质的盐析
盐析:加入大量的电解质,去掉蛋白质的电荷和水化膜,使其沉淀析出的现象称盐析。
特点:可逆过程
4、蛋白质的变性
定义:在某些物理或化学因素的作用下,蛋白质的理化性质、生物功能部分或全部改变。
物理因素:加热、加压、剧烈搅拌、振荡、紫外线、超声波等。
化学因素:强酸、强碱、重金属盐、有机溶剂、表面活性剂等。
变性因素:
实际应用:
杀菌消毒、临床化验、试剂存贮等。
特
点:
不可逆过程
5、蛋白质的颜色反应
蛋白质+HNO3
黄色
有些含有苯丙氨酸、色氨酸或酪氨酸的蛋白质,遇浓硝酸会显白色,加热之后变黄色,放冷之后,加浓氨水,变橙色。称为黄蛋白反应。这是残基中的苯环被硝化的缘故。
三、酶
1、酶:
由活细胞合成的,对其特异底物起高效催化作用的蛋白质,使机体内催化各种代谢反应最主要的催化剂。
2、酶与一般催化剂的共同点:
在反应前后没有质和量的变化;只能催化热力学允许的化学反应;只能加速可逆反应的进程,而不改变反应的平衡点。
酶
3、酶促反应的特点
酶促反应具有极高的效率
酶促反应具有高度的特异性
酶促反应的可调节性
四、核酸
以核苷酸为基本组成单位,通过3’
5’磷酸二酯键连接形成的一类生物大分子。
1、定义:
携带和传递遗传信息
2、生理意义:
3、分类:
(RNA)
mRNA
tRNA
rRNA
(DNA)
以基因的形式荷载遗传信息,并作为基因复制和转录的模板。
作为蛋白质合成的直接模板,指导蛋白质的生物合成。
在蛋白质的生物合成过程中负责搬运氨基酸。
与蛋白质共同构成核糖体,作为蛋白质生物合成的场所。
课堂小结
1、氨基酸的结构,氨基酸的两性和成肽反应
2、蛋白质的结构特点,蛋白质的两性,盐析及变性。
3、酶的概念,酶促反应的特点
4、核酸的组成,分类及功能。
1.根据氨基酸中氨基和羧基的相对数目,可将氨基酸分为______、_______和_______氨基酸。
2.核酸可分为__________和____________两类。
课堂练习
中性
酸性
碱性
脱氧核糖核酸
核糖核酸
3.蛋白质分子的主要化学键是(
)
A.
氢键
B.
二硫键
C.酯键
D.
肽键
4.重金属盐能使人畜中毒,这是由于它在
体内(
)
A.
发生了盐析作用
B.
氧化反应
C.使蛋白质变性
D.
生成配合物
D
C
5.遗传信息的载体是(
)
A
rRNA
B
mRNA
C
DNA
D
rRNA
C
6.鉴别:
葡萄糖
蛋白质
淀粉
再
见
祝
同
学
们
学
习
愉
快
课后作业
P94
1~5题
新课标人教版高中化学选修5
第四章
生命中的基础有机化学物质
第三节蛋白质和核酸
蛋白质
病
毒
蚕
丝
这些是什么?
没有蛋白质就没有生命
鲜
活
的
生
命
蛋
白
质
保
持
2、蛋白质的生物学重要性
(1).
蛋白质是生物体重要组成成分
蛋白质是细胞内最丰富的有机分子,占人体干重的45%,某些组织含量更高,例如脾、肺及横纹肌等高达80%。
分布广:
含量高:
所有器官、组织都含有蛋白质;细胞的各个部分都含有蛋白质。
1、什么是蛋白质?
蛋白质是由许多氨基酸通过肽键相连形成的高分子含氮有机化合物。
蛋白质占干重
人体中(中年人)
人体
45%
水55%
细菌
50%~80%
蛋白质19%
真菌
14%~52%
脂肪19%
酵母菌
14%~50%
糖类<1%
白地菌50%
无机盐7%
1)作为生物催化剂
2)代谢调节作用
3)免疫保护作用
4)物质的转运和存储
5)运动与支持作用
6)参与细胞间信息传递
(2)蛋白质具有重要的生物学功能
(3)氧化供能
第一课时
1.充分利用的图片,模型,多媒体等教学手段,增强知识的直观性。
2.通过讨论与交流,启发思维,逐步养成良好的学习习惯和学习方法。
1.掌握氨基酸的结构和性质,了解蛋白质的结构,了解核酸和酶的基本知识。
2.
进一步理解结构决定性质的理念。
知识与技能
教学目标
过程与方法
1.激发学习化学、探究化学原理的兴趣
。
2.强化理论与实际的联系,学以致用。
3.
增强民族自豪感。
情感态度与价值观
重点
难点
1.氨基酸的性质。
2.蛋白质的性质。
蛋白质的组成
教学重难点
一、氨基酸的结构和性质
(一)氨基酸的结构
N
1、羧酸分子中烃基上的氢原子
被氨基(—NH2)取代后形成氨基酸
2、官能团:
羧基(—COOH)
氨基(—NH2)
3、α—氨基酸:
α-氨基乙酸
α-氨基丙酸
α
β
γ
δ
ω
β—氨基丁酸
γ—氨基丁酸
位置代号
(二)氨基酸的性质
1、物理性质:
无色晶体,
熔点较高,约在230℃以上,
在水中溶解度不一,一般难溶于乙醇、乙醚,而溶于强酸或强碱溶液中。
2、化学性质:
结构决定性质,由氨基酸的结构推测氨基酸可能具有哪些化学性质?
羧基(—COOH)
氨基(—NH2)
具有羧酸的性质如:酸性
具有胺的性质如:碱性
由于这两种官能团的相互影响,又显示出一些特殊性质。如:两性。
(1)氨基酸的两性
+
H2O
与酸反应,体现碱性
与碱反应,体现酸性
+
甘氨酰甘氨酸
肽键
(2)成肽反应(缩合反应)
肽键:由一个氨基酸的?-羧基与另一个氨基酸的?-氨基脱水缩合而形成的化学键。
肽:由氨基酸通过肽键缩合而形成的化合物。
两分子氨基酸缩合形成二肽,三分子氨基酸缩合则形成三肽……
由十个以内氨基酸相连而成的肽称为寡肽,
由更多的氨基酸相连形成的肽称多肽。
五
肽
肽键
多
肽
当多肽链(相对分子质量大于10000)具有了完整的空间结构后,就形成了蛋白质。
肽键
蛋白质——牛核糖核酸酶的结构
二、蛋白质的结构与性质
碳
50%
氢
7%
氧
23%
氮
16%
硫
0~3%
其他
微
量
(一)蛋白质的元素组成
主要有C、H、O、N和S。
少量蛋白质含有少量磷或金属元素铁、铜、锌、锰、钴、钼,个别蛋白质还含有碘
。
属天然高分子化合物
各种蛋白质的含氮量很接近,平均为16%。
100克样品中蛋白质的含量
(
g
%
)
=
每克样品含氮克数×
6.25×100
1/16%
由于体内的含氮物质以蛋白质为主,因此,只要测定生物样品中的含氮量,就可以根据以下公式推算出蛋白质的大致含量:
附:蛋白质元素组成的特点
三聚氰胺(H2NCN)3
67%
(二)蛋白质的分子结构
一级结构(primary
structure)
二级结构(secondary
structure)
三级结构(tertiary
structure)
四级结构(quaternary
structure)
1、蛋白质的一级结构(多肽链)
定义
蛋白质的一级结构指蛋白质多肽链中氨基酸的排列顺序。
主要的化学键
肽键,有些蛋白质还包括二硫键。
附:牛胰岛素的一级结构
蛋白质分子中各段肽链主链骨架原子的空间分布状态(主链的空间构象),并不涉及氨基酸残基侧链的构象
。
(1)定义:
(2)主要的化学键:
氢键
2、蛋白质的二级结构(螺旋结构)
(3)二级结构的几种类型:
?-螺旋
(
?
-helix
)
?-折叠
(
?-pleated
sheet
)
?-转角
(
?-turn
)
无规卷曲
(
random
coil
)
?-螺旋
?-折叠(
?-片层)
?-转角
3、
三级结构(空间排布)
只含一个肽链的蛋白质,只具三级结构。如:肌红蛋白
(Mb)
多肽链上所有原子在三维空间的排布。
定义:
4、蛋白质的四级结构(立体组合)
蛋白质分子中各亚基的空间排布及相互联系,称为蛋白质的四级结构。
有些蛋白质分子含有二条或多条多肽链,每一条多肽链都有完整的三级结构,称为蛋白质的亚基
。
血红蛋白的四级结构
(三)蛋白质的性质
1.
蛋白质的两性
2.
蛋白质的水解反应
蛋白质
α—氨基酸
酶
3.
蛋白质的盐析
盐析:加入大量的电解质,去掉蛋白质的电荷和水化膜,使其沉淀析出的现象称盐析。
特点:可逆过程
4、蛋白质的变性
定义:在某些物理或化学因素的作用下,蛋白质的理化性质、生物功能部分或全部改变。
物理因素:加热、加压、剧烈搅拌、振荡、紫外线、超声波等。
化学因素:强酸、强碱、重金属盐、有机溶剂、表面活性剂等。
变性因素:
实际应用:
杀菌消毒、临床化验、试剂存贮等。
特
点:
不可逆过程
5、蛋白质的颜色反应
蛋白质+HNO3
黄色
有些含有苯丙氨酸、色氨酸或酪氨酸的蛋白质,遇浓硝酸会显白色,加热之后变黄色,放冷之后,加浓氨水,变橙色。称为黄蛋白反应。这是残基中的苯环被硝化的缘故。
三、酶
1、酶:
由活细胞合成的,对其特异底物起高效催化作用的蛋白质,使机体内催化各种代谢反应最主要的催化剂。
2、酶与一般催化剂的共同点:
在反应前后没有质和量的变化;只能催化热力学允许的化学反应;只能加速可逆反应的进程,而不改变反应的平衡点。
酶
3、酶促反应的特点
酶促反应具有极高的效率
酶促反应具有高度的特异性
酶促反应的可调节性
四、核酸
以核苷酸为基本组成单位,通过3’
5’磷酸二酯键连接形成的一类生物大分子。
1、定义:
携带和传递遗传信息
2、生理意义:
3、分类:
(RNA)
mRNA
tRNA
rRNA
(DNA)
以基因的形式荷载遗传信息,并作为基因复制和转录的模板。
作为蛋白质合成的直接模板,指导蛋白质的生物合成。
在蛋白质的生物合成过程中负责搬运氨基酸。
与蛋白质共同构成核糖体,作为蛋白质生物合成的场所。
课堂小结
1、氨基酸的结构,氨基酸的两性和成肽反应
2、蛋白质的结构特点,蛋白质的两性,盐析及变性。
3、酶的概念,酶促反应的特点
4、核酸的组成,分类及功能。
1.根据氨基酸中氨基和羧基的相对数目,可将氨基酸分为______、_______和_______氨基酸。
2.核酸可分为__________和____________两类。
课堂练习
中性
酸性
碱性
脱氧核糖核酸
核糖核酸
3.蛋白质分子的主要化学键是(
)
A.
氢键
B.
二硫键
C.酯键
D.
肽键
4.重金属盐能使人畜中毒,这是由于它在
体内(
)
A.
发生了盐析作用
B.
氧化反应
C.使蛋白质变性
D.
生成配合物
D
C
5.遗传信息的载体是(
)
A
rRNA
B
mRNA
C
DNA
D
rRNA
C
6.鉴别:
葡萄糖
蛋白质
淀粉
再
见
祝
同
学
们
学
习
愉
快
课后作业
P94
1~5题
