鲁科版(2019)高中化学 必修二 学案 2.1化学键与物质构成
文档属性
| 名称 | 鲁科版(2019)高中化学 必修二 学案 2.1化学键与物质构成 |
|
|
| 格式 | docx | ||
| 文件大小 | 90.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-07-22 00:00:00 | ||
图片预览


文档简介
化学键与物质构成
【学习目标】
1.认识化学键的涵义,知道离子键和共价键的形成与区别。
2.理解离子键、共价键的成因和本质。
3.能用电子式和结构表示常见物质的结构。
【学习重难点】
重点:化学键、离子键、共价键的的含义,化学键与化学反应的实质。
难点:对离子键、共价键的成因和本质理解。
【学习过程】
【要点精析】
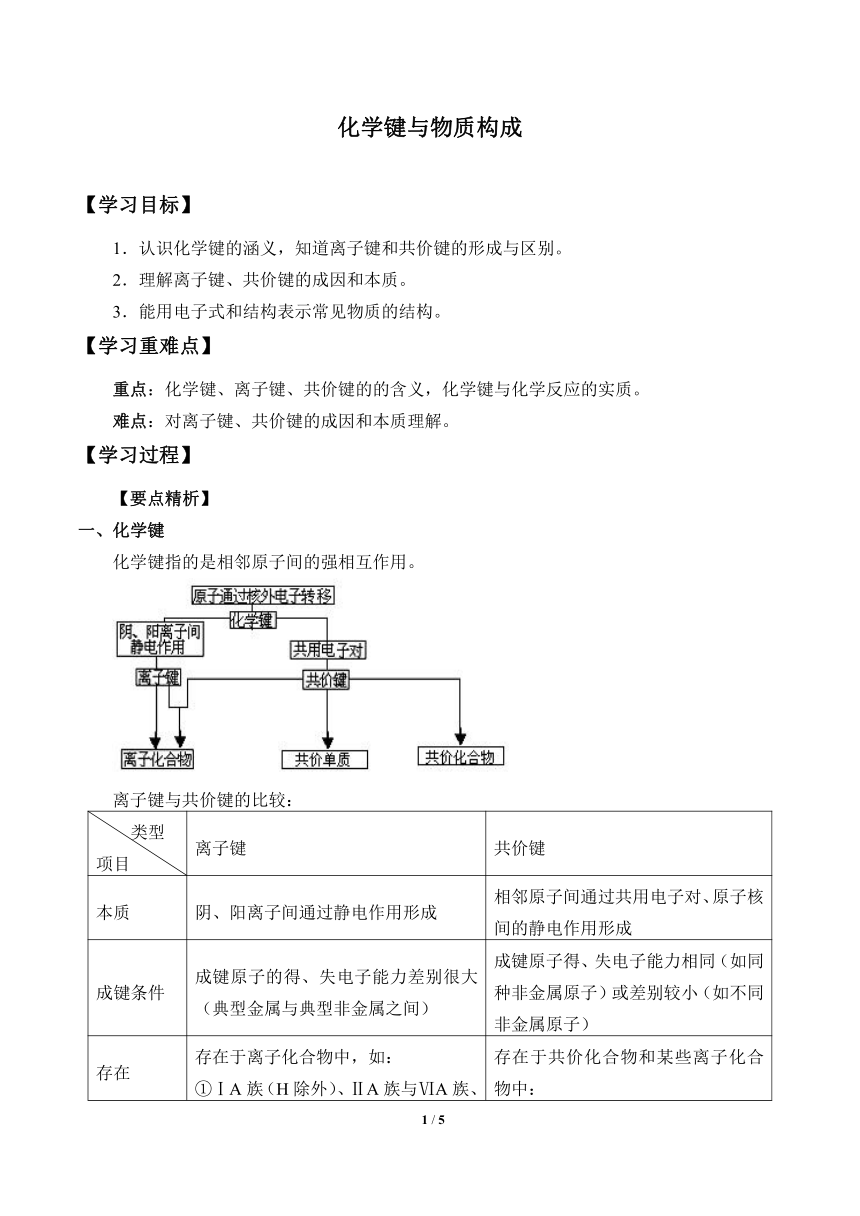
一、化学键
化学键指的是相邻原子间的强相互作用。
离子键与共价键的比较:
类型
项目
离子键
共价键
本质
阴、阳离子间通过静电作用形成
相邻原子间通过共用电子对、原子核间的静电作用形成
成键条件
成键原子的得、失电子能力差别很大(典型金属与典型非金属之间)
成键原子得、失电子能力相同(如同种非金属原子)或差别较小(如不同非金属原子)
存在
存在于离子化合物中,如:
①ⅠA族(H除外)、ⅡA族与ⅥA族、ⅦA族间形成化合物
②强碱
③大部分盐
存在于共价化合物和某些离子化合物中:
①共价单质如H2、O2、N2、X2
②共价化合物如HX、H2O2
③某些离子化合物如NaOH、Na2O2
二、化学键与物质分类
根据化合物中所含化学键的类型,可将化合物分为离子化合物和共价化合物:
类型
项目
离子化合物
共价化合物
定义
阴、阳离子通过离子键形成的化合物
原子间通过共价键形成的化合物
比较
含有阴阳离子和离子键,可能含有共价键。
含有共价键,一定不含阴阳离子和离子键
与常见物质类别的关系
①典型金属氧化物
②强碱
③大部分盐
①非金属氢化物
②非金属氧化物
③酸
例1:关于化学键的下列叙述中,正确的是( )
A.构成物质的分子中一定含有化学键 B.离子化合物可能含共价健
C.共价化合物可能含离子键 D.离子化合物中一定含有金属元素
解析:稀有气体为单原子分子,该分子中无共价键;离子化合物中可以含有共价键,如;共价化合物中不可能有离子键;氯化铵、硝酸铵等铵盐是离子化合物,其组成元素全部是非金属元素。
答案:选B。
例2:不属于离子化合物的是( )
A.Na2O2 B.CaF2 C.SO2 D.Ba(OH)2
解析:离子化合物主要包括;①由活泼金属和活泼非金属形成的化合物,如CaF2、Na2O2;②绝大多数盐,如铵盐、硫酸盐,硝酸盐等;③强碱如NaOH、Ca(OH)2、Ba(OH)2。
答案:选C
例3:下列化合物中所有化学键都是共价键的是( )
A.Na2O2 B.NaOH C.BaCl2 D.CH4
解析:活泼金属与活泼非金属之间形成离子键,绝大多数盐和强碱是离子化合物;非金属元素之间形成共价键。在A、C中只有离子键,B中既有离子键又有共价键。
答案:选D。
例4:M元素的一个原子失去两个电子转移到R元素的两个原子中去形成化合物,下列说法中正确的是( )
A.M与R形成化合物的化学式为M2R B.M与R形成的化合物是离子化合物
C.M与R形成的化合物是共价化合物 D.M与R的化合物的固体能导电
解析:一个M原子失去2个电子转移到2个R原子上,M为+2价,R为-1价,M与R形成化合物的化学式为MR2,由于电子发生得失而不是形成共用电子对,所以MR2一定为离子化合物,离子化合物只有在熔化或溶于水时才能导电,固态时虽然有离子存在,但不能自由移动,所以不导电。
答案:选B。
【强化训练】
一、选择题(以下各题有1个正确答案)
1.有下列电子层结构的各原子中最难形成离子的是( )
A. B. C. D.
2.易与形成离子化合物的是( )
A. B. C. D.
3.下列物质中属于共价化合物的是( )
A.Na2O2 B.NaHSO4 C.HNO3 D.I2
4.下列物质中属于离子化合物的是( )
A.Na2O B.HNO3 C.HCl D.NH3
5.下列化合物中所有化学键都是共价键的是( )
A.NH4Cl B.NaOH C.CaF2 D.CH4
6.与Ne的核外电子排布相同的阴离子跟与Ar的核外电子排布相同的阳离子所形成的化合物是( )
A.MgBr2 B.Na2S C.CaF2 D.KCl
7.下列物质中,既有离子键,又有共价键的是( )
A.H2O B.CaCl2 C.KOH D.Cl2
8.下列过程中要破坏离子键的是( )
A.氯化钠固体溶于水 B.氯气溶于水
C.碘晶体升华 D.钠与氯反应
9.下列说法正确的是( )
A.离子化合物中,一个阴离子可同时与多个阳离子间有静电作用
B.离子化合物中的阳离子,只能是金属离子
C.凡金属跟非金属元素化合时都形成离子键
D.溶于水可以导电的化合物一定是离子化合物
10.下列各数值表示有关元素的原子序数,各组中能以离子键相互结合成稳定化合物的是( )
A.10与19 B.6与16 C.11与17 D.14与8
11.下列物质中,只有离子键的是( )
A.NaOH B.NaCl C.H2 D.HCl
12.物质间发生化学反应时,一定发生变化的是( )
A.颜色 B.状态 C.化学键 D.原子核
13.下列物质中,由离子构成的是( )
A.干冰 B.NH4Cl固体 C.H3PO4固体 D.HCl
二、填空题
14.在下列空白处填写“可能与不可能”和“一定或不一定”
(1)非金属之间______形成离子键
(2)复杂的阴离子或者阳离子中_________含有共价键
(3)稀有气体分子中_________含化学键
(4)离子化合中__________含有共价键
(5)共价化合物中________含有离子键
15.用电子式表示:
(1)钾原子______(2)氯原子______(3)过氧化钠______(4)氢氧化钾____(5)氢氧根离子______
(6)硫离子______(7)氯化钙____(8)氯化铵________(9)硫化钾的形成过程____________________
答案:
1.A
2.D
3.C
4.A
5.D
6.C
7.C
8.A
9.A
10.C
11.B
12.C
13.B
14(1)可能
(2)一定
(3)不可能
(4)可能
(5)不可能
15.略
【学习目标】
1.认识化学键的涵义,知道离子键和共价键的形成与区别。
2.理解离子键、共价键的成因和本质。
3.能用电子式和结构表示常见物质的结构。
【学习重难点】
重点:化学键、离子键、共价键的的含义,化学键与化学反应的实质。
难点:对离子键、共价键的成因和本质理解。
【学习过程】
【要点精析】
一、化学键
化学键指的是相邻原子间的强相互作用。
离子键与共价键的比较:
类型
项目
离子键
共价键
本质
阴、阳离子间通过静电作用形成
相邻原子间通过共用电子对、原子核间的静电作用形成
成键条件
成键原子的得、失电子能力差别很大(典型金属与典型非金属之间)
成键原子得、失电子能力相同(如同种非金属原子)或差别较小(如不同非金属原子)
存在
存在于离子化合物中,如:
①ⅠA族(H除外)、ⅡA族与ⅥA族、ⅦA族间形成化合物
②强碱
③大部分盐
存在于共价化合物和某些离子化合物中:
①共价单质如H2、O2、N2、X2
②共价化合物如HX、H2O2
③某些离子化合物如NaOH、Na2O2
二、化学键与物质分类
根据化合物中所含化学键的类型,可将化合物分为离子化合物和共价化合物:
类型
项目
离子化合物
共价化合物
定义
阴、阳离子通过离子键形成的化合物
原子间通过共价键形成的化合物
比较
含有阴阳离子和离子键,可能含有共价键。
含有共价键,一定不含阴阳离子和离子键
与常见物质类别的关系
①典型金属氧化物
②强碱
③大部分盐
①非金属氢化物
②非金属氧化物
③酸
例1:关于化学键的下列叙述中,正确的是( )
A.构成物质的分子中一定含有化学键 B.离子化合物可能含共价健
C.共价化合物可能含离子键 D.离子化合物中一定含有金属元素
解析:稀有气体为单原子分子,该分子中无共价键;离子化合物中可以含有共价键,如;共价化合物中不可能有离子键;氯化铵、硝酸铵等铵盐是离子化合物,其组成元素全部是非金属元素。
答案:选B。
例2:不属于离子化合物的是( )
A.Na2O2 B.CaF2 C.SO2 D.Ba(OH)2
解析:离子化合物主要包括;①由活泼金属和活泼非金属形成的化合物,如CaF2、Na2O2;②绝大多数盐,如铵盐、硫酸盐,硝酸盐等;③强碱如NaOH、Ca(OH)2、Ba(OH)2。
答案:选C
例3:下列化合物中所有化学键都是共价键的是( )
A.Na2O2 B.NaOH C.BaCl2 D.CH4
解析:活泼金属与活泼非金属之间形成离子键,绝大多数盐和强碱是离子化合物;非金属元素之间形成共价键。在A、C中只有离子键,B中既有离子键又有共价键。
答案:选D。
例4:M元素的一个原子失去两个电子转移到R元素的两个原子中去形成化合物,下列说法中正确的是( )
A.M与R形成化合物的化学式为M2R B.M与R形成的化合物是离子化合物
C.M与R形成的化合物是共价化合物 D.M与R的化合物的固体能导电
解析:一个M原子失去2个电子转移到2个R原子上,M为+2价,R为-1价,M与R形成化合物的化学式为MR2,由于电子发生得失而不是形成共用电子对,所以MR2一定为离子化合物,离子化合物只有在熔化或溶于水时才能导电,固态时虽然有离子存在,但不能自由移动,所以不导电。
答案:选B。
【强化训练】
一、选择题(以下各题有1个正确答案)
1.有下列电子层结构的各原子中最难形成离子的是( )
A. B. C. D.
2.易与形成离子化合物的是( )
A. B. C. D.
3.下列物质中属于共价化合物的是( )
A.Na2O2 B.NaHSO4 C.HNO3 D.I2
4.下列物质中属于离子化合物的是( )
A.Na2O B.HNO3 C.HCl D.NH3
5.下列化合物中所有化学键都是共价键的是( )
A.NH4Cl B.NaOH C.CaF2 D.CH4
6.与Ne的核外电子排布相同的阴离子跟与Ar的核外电子排布相同的阳离子所形成的化合物是( )
A.MgBr2 B.Na2S C.CaF2 D.KCl
7.下列物质中,既有离子键,又有共价键的是( )
A.H2O B.CaCl2 C.KOH D.Cl2
8.下列过程中要破坏离子键的是( )
A.氯化钠固体溶于水 B.氯气溶于水
C.碘晶体升华 D.钠与氯反应
9.下列说法正确的是( )
A.离子化合物中,一个阴离子可同时与多个阳离子间有静电作用
B.离子化合物中的阳离子,只能是金属离子
C.凡金属跟非金属元素化合时都形成离子键
D.溶于水可以导电的化合物一定是离子化合物
10.下列各数值表示有关元素的原子序数,各组中能以离子键相互结合成稳定化合物的是( )
A.10与19 B.6与16 C.11与17 D.14与8
11.下列物质中,只有离子键的是( )
A.NaOH B.NaCl C.H2 D.HCl
12.物质间发生化学反应时,一定发生变化的是( )
A.颜色 B.状态 C.化学键 D.原子核
13.下列物质中,由离子构成的是( )
A.干冰 B.NH4Cl固体 C.H3PO4固体 D.HCl
二、填空题
14.在下列空白处填写“可能与不可能”和“一定或不一定”
(1)非金属之间______形成离子键
(2)复杂的阴离子或者阳离子中_________含有共价键
(3)稀有气体分子中_________含化学键
(4)离子化合中__________含有共价键
(5)共价化合物中________含有离子键
15.用电子式表示:
(1)钾原子______(2)氯原子______(3)过氧化钠______(4)氢氧化钾____(5)氢氧根离子______
(6)硫离子______(7)氯化钙____(8)氯化铵________(9)硫化钾的形成过程____________________
答案:
1.A
2.D
3.C
4.A
5.D
6.C
7.C
8.A
9.A
10.C
11.B
12.C
13.B
14(1)可能
(2)一定
(3)不可能
(4)可能
(5)不可能
15.略
