人教版高二物理选修3-5第十八章 三节氢原子光谱、四节玻尔的原子模型(共26张PPT)
文档属性
| 名称 | 人教版高二物理选修3-5第十八章 三节氢原子光谱、四节玻尔的原子模型(共26张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 3.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 物理 | ||
| 更新时间 | 2020-07-22 00:00:00 | ||
图片预览





文档简介
(共26张PPT)
第十八章:原子结构
第
3
节:氢原子光谱
第
4
节:玻尔的原子模型
早在17世纪,牛顿就发现了日光通过三棱镜后的色散现象,并把实验中得到的彩色光带叫做光谱。
1.光谱?
定义:光按波长展开,获得波长和强度分布的记录。
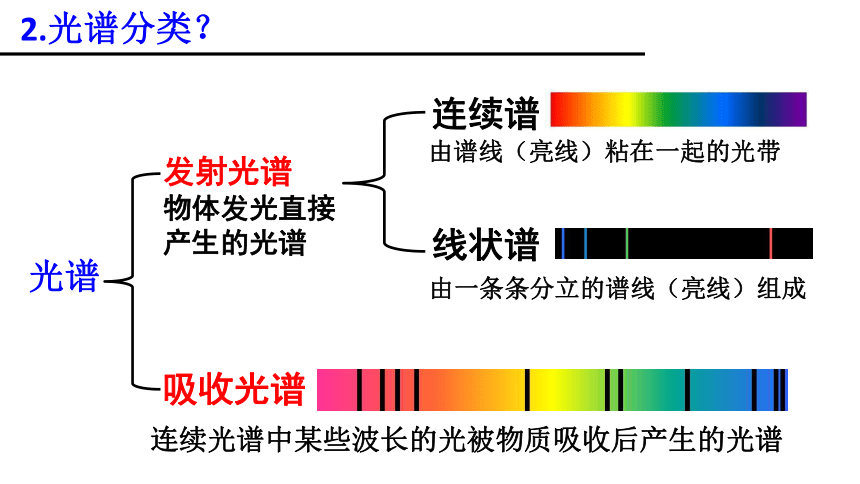
2.光谱分类?
发射光谱
物体发光直接产生的光谱
吸收光谱
光谱
线状谱
由谱线(亮线)粘在一起的光带
由一条条分立的谱线(亮线)组成
连续光谱中某些波长的光被物质吸收后产生的光谱
炽热的固体、液体和高压气体的发射光谱是连续光谱
(如白炽灯丝发出的光、烛焰、炽热的钢水发出的光)
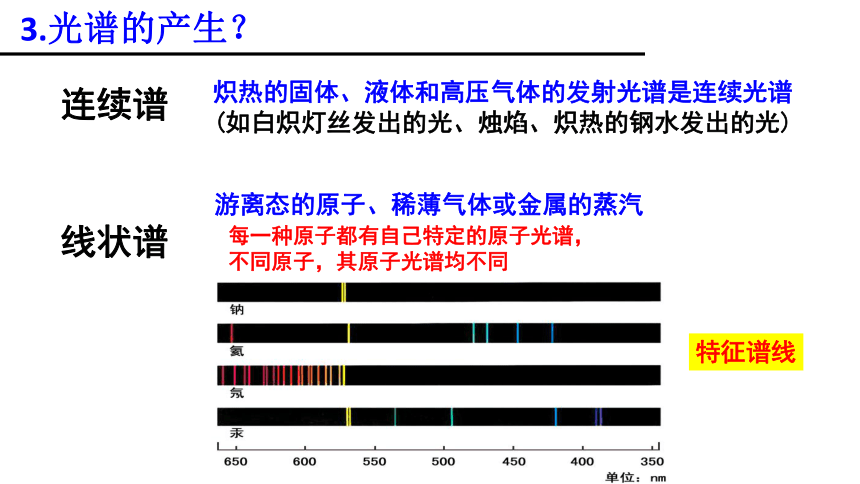
3.光谱的产生?
连续谱
线状谱
游离态的原子、稀薄气体或金属的蒸汽
每一种原子都有自己特定的原子光谱,不同原子,其原子光谱均不同
特征谱线
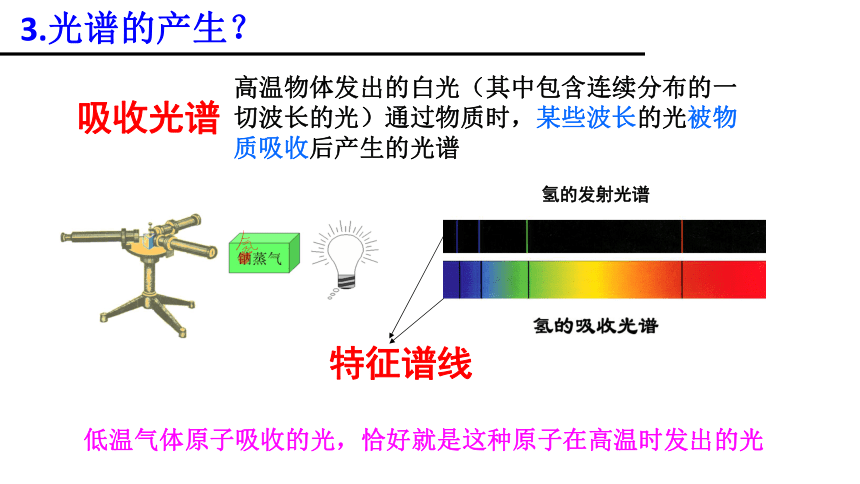
3.光谱的产生?
高温物体发出的白光(其中包含连续分布的一切波长的光)通过物质时,某些波长的光被物质吸收后产生的光谱
低温气体原子吸收的光,恰好就是这种原子在高温时发出的光
吸收光谱
特征谱线
4.太阳光谱是发射光谱还是吸收光谱?
太阳光谱上的暗线,
是太阳表面气体的吸收光谱。
从这些谱线,
可确定太阳表面的气体组成。
例如,
氦是1870年先在太阳光谱中发现,
后在地球找到它的踪迹。
5.光谱分析
光谱分析:由于每种原子都有自己的特征谱线,因此可以根据光谱来鉴别物质和确定的化学组成。这种方法叫做光谱分析。
各种光谱
连续光谱
H的发射光谱
钠的发射光谱
钠的吸收光谱
太阳的吸收光谱
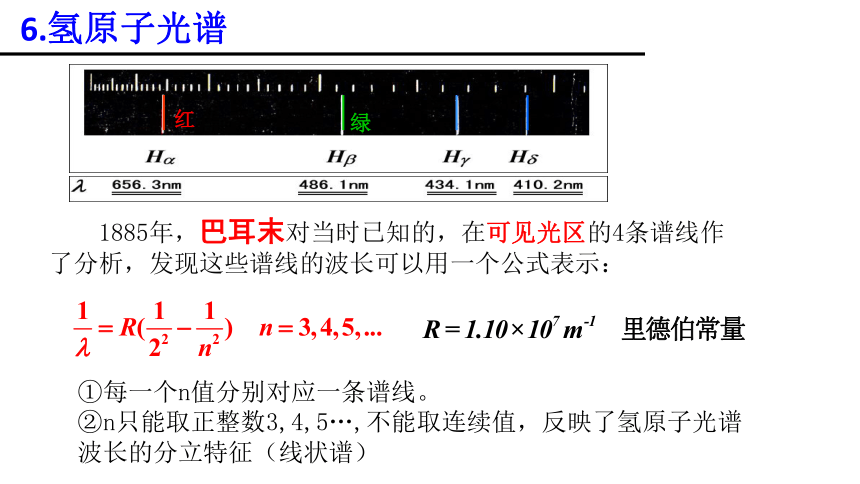
6.氢原子光谱
1885年,巴耳末对当时已知的,在可见光区的4条谱线作了分析,发现这些谱线的波长可以用一个公式表示:
①每一个n值分别对应一条谱线。
②n只能取正整数3,4,5…,不能取连续值,反映了氢原子光谱波长的分立特征(线状谱)
第
4
节:玻尔的原子模型
卢瑟福模型的困难
核外电子绕核运动
事实上:原子是稳定的、原子光谱是线状谱。
一.波尔原子理论假说
(三个重要假设)
针对原子核式结构模型提出
围绕原子核运动的电子轨道半径只能是某些分立的数值。且电子在这些轨道上绕核的转动是稳定的,不产生电磁辐射,也就是说,电子的轨道是量子化的。
假说1:轨道量子化
一.波尔原子理论假说
(三个重要假设)
针对原子的稳定性提出
假说2:能级(定态)假说
电子在不同的轨道上运动时,原子处于不同的状态.原子在不同的状态中具有不同的能量,所以原子的能量也量子化的.
一.波尔原子理论假说
(三个重要假设)
原子从Em能级跃迁到En能级(
Em>En
)时,会放出能量为hv的光子,其能量由前后能级差决定:
二.氢原子的能量
电子和原子核系统势能
电子动能
?
?
?
?
?
?
?
?
1.这里的电势能
Ep<0,原因是规定了无限远处的电势能为零。
这样越是里面轨道电势能越少,负得越多。
2.跃迁时电子动能、原子电势能与原子能量的变化:当轨道
半径减小时,库仑引力做正功,原子的电势能
Ep
减小,电子动能增大,原子能量减小。反之,轨道半径增大时,原子电势能增大,电子动能减小,原子能量增大。
对能级的理解:
激发态
基态
1.能级:氢原子的各个定态的能量值
2.基态和激发态
?比基态能量高的定态叫激发态(n>1)
?能量最低的定态叫基态
?从激发态跃迁到基态时,放出光子;从基态跃迁到激发态时,
吸收能量
三.氢原子能级(量子化)
1.向下跃迁
发射光子
⑴一个原子跃迁可能的光子频率有
(n-1)
种
⑵大量原子跃迁可能的光子频率有
种
四.核外电子的跃迁
2.向上跃迁
吸收能量
⑴光子照射
电子剩余动能
跃迁:
电离:
⑵实物粒子激发
电子剩余动能
四.核外电子的跃迁
赖曼系(紫外线)
巴耳末系(可见光)
帕邢系(红外线)
布喇开系
逢德系
轨道与能级相对应
成功解释了氢光谱的所有谱线
在解决核外电子的运动时成功引入了量子化的观念
同时又应用了“粒子、轨道”等经典概念和有关牛顿力学规律
除了氢原子光谱外,在解决其他问题上遇到了很大的困难.
氦原子光谱
量子化条件的引进没有适当的理论解释。
玻尔理论成功的解释并预言了氢原子辐射的电磁波的问题,但是也有它的局限性.
五.波尔模型的局限性
讨论1:
根据玻尔理论,氢原子的电子从外层轨道跃迁到内层轨道后
A.原子的能量增加,电子的动能减少
B.原子的能量增加,电子的动能增加
C.原子的能量减少,电子的动能减少
D.原子的能量减少,电子的动能增加
讨论2:欲将处于基态的氢原子激发,下列可行的措施是
A.用10.2
eV的光子照射
B.用11
eV的光子照射
C.用14
eV的光子照射
D.用11
eV的电子碰撞
练习3:用能量为1.87
eV的光子照射n=3
激发态氢原子时,氢原子
A.不会吸收这个光子
B.吸收该光子后被电离,电离后的电子动能
为0.36
eV
C.吸收该光子后被电离,电离后电子的动能
为零
D.吸收该光子后不会被电离
第十八章:原子结构
第
3
节:氢原子光谱
第
4
节:玻尔的原子模型
早在17世纪,牛顿就发现了日光通过三棱镜后的色散现象,并把实验中得到的彩色光带叫做光谱。
1.光谱?
定义:光按波长展开,获得波长和强度分布的记录。
2.光谱分类?
发射光谱
物体发光直接产生的光谱
吸收光谱
光谱
线状谱
由谱线(亮线)粘在一起的光带
由一条条分立的谱线(亮线)组成
连续光谱中某些波长的光被物质吸收后产生的光谱
炽热的固体、液体和高压气体的发射光谱是连续光谱
(如白炽灯丝发出的光、烛焰、炽热的钢水发出的光)
3.光谱的产生?
连续谱
线状谱
游离态的原子、稀薄气体或金属的蒸汽
每一种原子都有自己特定的原子光谱,不同原子,其原子光谱均不同
特征谱线
3.光谱的产生?
高温物体发出的白光(其中包含连续分布的一切波长的光)通过物质时,某些波长的光被物质吸收后产生的光谱
低温气体原子吸收的光,恰好就是这种原子在高温时发出的光
吸收光谱
特征谱线
4.太阳光谱是发射光谱还是吸收光谱?
太阳光谱上的暗线,
是太阳表面气体的吸收光谱。
从这些谱线,
可确定太阳表面的气体组成。
例如,
氦是1870年先在太阳光谱中发现,
后在地球找到它的踪迹。
5.光谱分析
光谱分析:由于每种原子都有自己的特征谱线,因此可以根据光谱来鉴别物质和确定的化学组成。这种方法叫做光谱分析。
各种光谱
连续光谱
H的发射光谱
钠的发射光谱
钠的吸收光谱
太阳的吸收光谱
6.氢原子光谱
1885年,巴耳末对当时已知的,在可见光区的4条谱线作了分析,发现这些谱线的波长可以用一个公式表示:
①每一个n值分别对应一条谱线。
②n只能取正整数3,4,5…,不能取连续值,反映了氢原子光谱波长的分立特征(线状谱)
第
4
节:玻尔的原子模型
卢瑟福模型的困难
核外电子绕核运动
事实上:原子是稳定的、原子光谱是线状谱。
一.波尔原子理论假说
(三个重要假设)
针对原子核式结构模型提出
围绕原子核运动的电子轨道半径只能是某些分立的数值。且电子在这些轨道上绕核的转动是稳定的,不产生电磁辐射,也就是说,电子的轨道是量子化的。
假说1:轨道量子化
一.波尔原子理论假说
(三个重要假设)
针对原子的稳定性提出
假说2:能级(定态)假说
电子在不同的轨道上运动时,原子处于不同的状态.原子在不同的状态中具有不同的能量,所以原子的能量也量子化的.
一.波尔原子理论假说
(三个重要假设)
原子从Em能级跃迁到En能级(
Em>En
)时,会放出能量为hv的光子,其能量由前后能级差决定:
二.氢原子的能量
电子和原子核系统势能
电子动能
?
?
?
?
?
?
?
?
1.这里的电势能
Ep<0,原因是规定了无限远处的电势能为零。
这样越是里面轨道电势能越少,负得越多。
2.跃迁时电子动能、原子电势能与原子能量的变化:当轨道
半径减小时,库仑引力做正功,原子的电势能
Ep
减小,电子动能增大,原子能量减小。反之,轨道半径增大时,原子电势能增大,电子动能减小,原子能量增大。
对能级的理解:
激发态
基态
1.能级:氢原子的各个定态的能量值
2.基态和激发态
?比基态能量高的定态叫激发态(n>1)
?能量最低的定态叫基态
?从激发态跃迁到基态时,放出光子;从基态跃迁到激发态时,
吸收能量
三.氢原子能级(量子化)
1.向下跃迁
发射光子
⑴一个原子跃迁可能的光子频率有
(n-1)
种
⑵大量原子跃迁可能的光子频率有
种
四.核外电子的跃迁
2.向上跃迁
吸收能量
⑴光子照射
电子剩余动能
跃迁:
电离:
⑵实物粒子激发
电子剩余动能
四.核外电子的跃迁
赖曼系(紫外线)
巴耳末系(可见光)
帕邢系(红外线)
布喇开系
逢德系
轨道与能级相对应
成功解释了氢光谱的所有谱线
在解决核外电子的运动时成功引入了量子化的观念
同时又应用了“粒子、轨道”等经典概念和有关牛顿力学规律
除了氢原子光谱外,在解决其他问题上遇到了很大的困难.
氦原子光谱
量子化条件的引进没有适当的理论解释。
玻尔理论成功的解释并预言了氢原子辐射的电磁波的问题,但是也有它的局限性.
五.波尔模型的局限性
讨论1:
根据玻尔理论,氢原子的电子从外层轨道跃迁到内层轨道后
A.原子的能量增加,电子的动能减少
B.原子的能量增加,电子的动能增加
C.原子的能量减少,电子的动能减少
D.原子的能量减少,电子的动能增加
讨论2:欲将处于基态的氢原子激发,下列可行的措施是
A.用10.2
eV的光子照射
B.用11
eV的光子照射
C.用14
eV的光子照射
D.用11
eV的电子碰撞
练习3:用能量为1.87
eV的光子照射n=3
激发态氢原子时,氢原子
A.不会吸收这个光子
B.吸收该光子后被电离,电离后的电子动能
为0.36
eV
C.吸收该光子后被电离,电离后电子的动能
为零
D.吸收该光子后不会被电离
