人教版高中选修四化学3.4-难溶电解质的溶解平衡-两课时 (共34张PPT)
文档属性
| 名称 | 人教版高中选修四化学3.4-难溶电解质的溶解平衡-两课时 (共34张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-07-26 00:00:00 | ||
图片预览









文档简介
(共34张PPT)
人教版选修4
·
化学反应原理
第三章
水溶液中的离子平衡
第四节
难溶电解质的溶解平衡
1.什么是饱和溶液?
在一定温度下,在一定量的溶剂里,不能再溶解某种溶质的溶液,叫做这种溶质的饱和溶液。
复
习
2.如何判断某NaCl溶液是否已经达到饱和?
讨论1:
在NaCl的饱和溶液中,再加入固体溶质,固体会不会继续溶解?是否发生着溶解过程?
饱和NaCl溶液
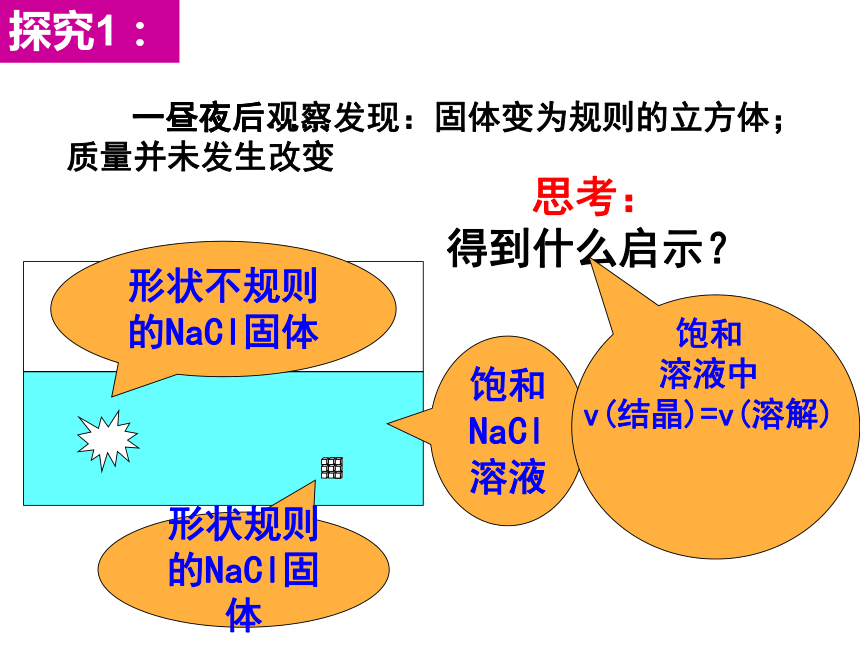
一昼夜后观察发现:固体变为规则的立方体;质量并未发生改变
思考:
得到什么启示?
一昼夜后……
探究1:
结论:NaCl的饱和溶液中存在溶解平衡
我们知道,溶液中有难溶于水的沉淀生成是离子反应发生的条件之一。例如,AgNO3溶液与NaCl溶液混合,生成白色沉淀AgCl:Ag++Cl-=AgCl↓,如果上述两种溶液是等物质的量浓度、等体积的,一般认为反应可以进行到底。
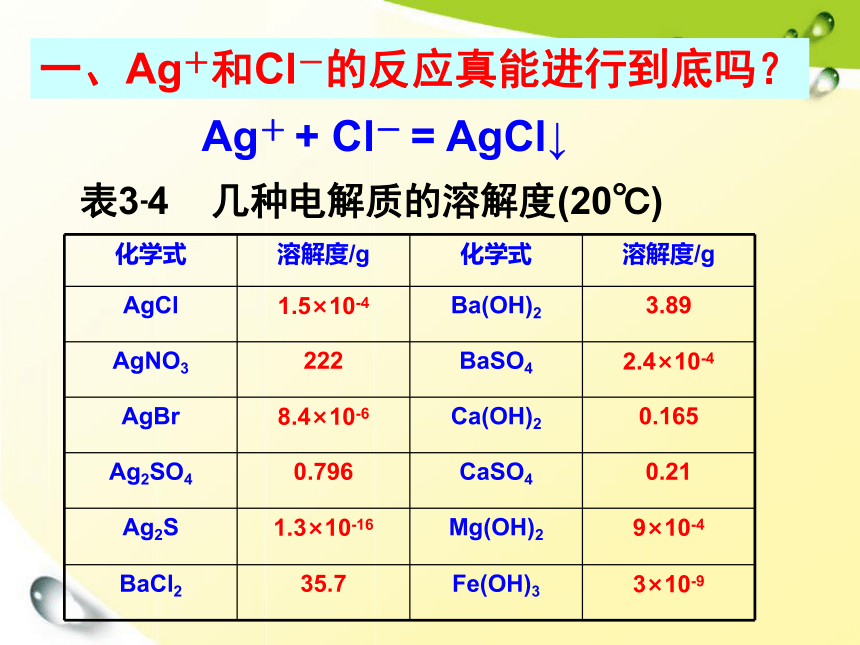
一、Ag+和Cl-的反应真能进行到底吗?
一、Ag+和Cl-的反应真能进行到底吗?
Ag+
+
Cl-
=
AgCl↓
表3-4
几种电解质的溶解度(20℃)
化学式
溶解度/g
化学式
溶解度/g
AgCl
1.5×10-4
Ba(OH)2
3.89
AgNO3
222
BaSO4
2.4×10-4
AgBr
8.4×10-6
Ca(OH)2
0.165
Ag2SO4
0.796
CaSO4
0.21
Ag2S
1.3×10-16
Mg(OH)2
9×10-4
BaCl2
35.7
Fe(OH)3
3×10-9
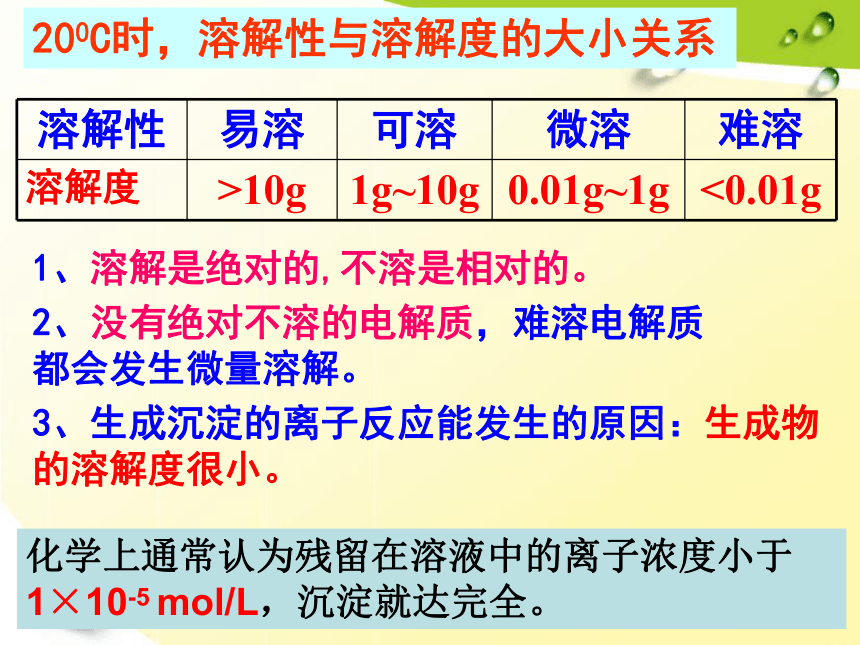
200C时,溶解性与溶解度的大小关系
1、溶解是绝对的,不溶是相对的。
2、没有绝对不溶的电解质,难溶电解质
都会发生微量溶解。
3、生成沉淀的离子反应能发生的原因:生成物的溶解度很小。
化学上通常认为残留在溶液中的离子浓度小于1×10-5
mol/L,沉淀就达完全。
溶解性
易溶
可溶
微溶
难溶
溶解度
>10g
1g~10g
0.01g~1g
<0.01g
【实验】向盛有2
mL
0.1mol/LAgNO3溶液的试管中加入2
mL
0.1
mol/L
NaCl溶液。
讨论3:
现象:有白色沉淀生成,说明溶液中依然有Ag+
Cl-存在,即Ag+和Cl-的反应不能进行到底。
(1)是否恰好反应?
(2)溶液中是否还含有Ag+和Cl-?
【继续试验】取上层清液,滴加NaCl溶液,
有何现象?说明了什么?
沉淀是难溶物,但不是绝对不溶,只不过溶解
度很小,难溶物在水中存在溶解平衡。
初始状态:V(溶解)
>
V(沉淀)
溶解平衡:V(溶解)
=
V(沉淀)
得到饱和AgCl溶液,建立溶解平衡
思考:把AgCl固体加到水中都发生着怎样的过程?
二、难溶电解质的溶解平衡
1、概念:
在一定条件下,难溶电解质___________的速率等于离子重新_____________的速率,溶液中各离子的浓度__________的状态。(也叫沉淀溶解平衡)
溶解成离子
结合成沉淀
保持不变
2、溶解平衡的建立
以AgCl(s)的溶解平衡为例
3、表达方法
4、溶解平衡的特征
标明物质状态和可逆符号
逆、等、动、定、变
5、生成难溶电解质的离子反应的限度
离子浓度小于1×10-5mol/L时,认为反应完全。
6、沉淀溶解平衡的影响因素
①内因:电解质本身的性质。
只要是饱和溶液都存在溶解平衡。
绝对不溶的物质是没有的
不同难溶物其溶解度差别也很大
0.01g
10g
难溶
微溶
易溶
可溶
1g
②外因
加相同离子,平衡向沉淀方向移动。
温度:
浓度:
加水,平衡向溶解方向移动;
(Ca(OH)2除外)
升温,多数平衡向溶解方向移动。
1、下列说法中正确的是(
)
A.物质的溶解性为难溶,则该物质不溶于水
B.不溶于水的物质溶解度为0
C.绝对不溶解的物质是不存在的
D.某粒子被沉淀完全是指该粒子在溶液中的浓度为零
2、下列对沉淀溶解平衡的描述正确的是
(
)
A.开始时,溶液中各离子浓度相等
B.平衡时,沉淀的速率和溶解的速率相等
C.平衡时,溶液中溶质的离子浓度相等,且保持不变
D.平衡时,如果再加入难溶性的该沉淀物,将促进溶解
练习
C
B
3.(1)AgCl(s)
Ag+(aq)+Cl-(aq)
(2)AgCl===Ag++Cl-
问(1)式和(2)式所表示的意义?
4.常温条件下,CaCO3在水中的溶解度大还是在Na2CO3溶液中的溶解度大?
三.溶度积常数
1.定义
2.表达式
Ksp=[c(Mn+)]m·[c(Am—)]n
在难溶电解质的饱和溶液中,当溶解与结晶速率相等时,溶液达到溶解平衡状态,则该反应的平衡常数表示为:Ksp,AgCl
=[Ag+][Cl-]。该常数称为难溶电解质的溶度积常数,简称溶度积。
3、溶度积规则
AnBm(s)
nAm+(aq)
+
mBn-(aq)
Qc>Ksp时,溶液过饱和,有沉淀析出,直至达到平衡.
Qc=Ksp时,沉淀与饱和溶液的平衡.
QcQc称为离子积,其表达式中离子浓度是任意的,为此瞬间溶液中的实际浓度.
②溶度积规则
①离子积
Qc=
c(Am+)n
·
c(Bn-)m
讨论:溶度积和溶解度都可以表示难溶电解质在水中的溶解能力,分析下表,你将如何看待溶度积和溶解度的关系?
结论:相同类型的难溶电解质的Ksp越小溶解度越小
一定条件下:
注意:只有在同种类型的电解质之间才能通过Ksp的
大小来直接比较溶解度的大小。
类型
化学式
溶度积Ksp
溶解度/g
AB
AgBr
5.0×10-13
8.4×10-6
AB
AgCl
1.8×10-10
1.5×10-4
A2B
Ag2CrO4
1.1×10-12
2.2×10-3
A2B
Ag2S
6.3×10-50
1.3×10-16
练一练
1、下列叙述正确的是(
)
A.由于AgCl水溶液导电性很弱,所以它是弱电解质
B.难溶电解质离子浓度的乘积就是该物质的溶度积常数
C.溶度积常数大者,溶解度也大
D.用水稀释含有AgCl固体的溶液时,
AgCl的溶度积常数不变。
D
练习1:25℃时,Ksp?(AgBr)=?5.0×10-10,求AgBr的饱和溶液中的c(Ag+)和c(Br-)。
4、利用溶度积计算某种离子的浓度:
练习2:25℃时,Ksp?[Mg(OH)2]=?1.8×10-11,求Mg(OH)2的饱和溶液中的C(Mg2+)和c(OH-)
C(Mg2+)=1.65×10-4,c(OH-)=3.3×10-4
c(Ag+)=c(Br-
)=2.2×10-5
6.判断能否生成沉淀
例:25℃时,在1.00?L?0.03?mol/L?AgNO3溶液中加入0.50?L?0.06?mol/L的CaCl2溶液,能否生成AgCl沉淀?
已知:AgCl的Ksp=1.8×10-10
c(Ag+)=(0.03?mol/L×1.00?L)÷(1.00?L+0.50?L)
=0.020?mol/L?
c(Cl-)=(0.06?mol/L×2×0.50?L)÷(1.00?L+0.50?L)
=0.040?mol/L?
Qc=c(Ag+)·c(Cl-)=0.020?mol/L×0.040?mol/L
=8.0×10-4
由于Qc>Ksp,所以有AgCl沉淀生成。
例:实验测得某水样中的铁离子的浓度为6×10-6mol·l-1
若要使水中的铁离子转化为沉淀,则溶液的PH值至少要控制在多少以上?[已知Fe(OH)3的Ksp为2.6×10-39]
解:设溶液中的OH-离子的浓度最少为X才能使水中的铁离子转化为沉淀。
KSP=c(Fe3+)
·c3(OH-)
=2.6×10-39
=6×10-6×X3
求得X=7.57×10-12mol·L-1=c(OH-)
C(H+)=1.32×10-3mol·L-1
PH=2.88
答:PH至少要控制在2.88以上。
7.计算某离子开始沉淀的pH值
第四节
难溶电解质的溶解平衡
Dissolution
electrolyte
equlibrium
?
第二课时
二、沉淀反应的应用
1、沉淀的生成
(1)应用:生成难溶电解质的沉淀,是工业生产、环保工程和科学研究中除杂或提纯物质的重要方法之一。
工业废水的处理
工业废水
硫化物等
重金属离子(如Cu2+、Hg2+等)转化成沉淀
(2)方法
a
、调pH
如:工业原料氯化铵中混有氯化铁,加氨水调pH值至7-8
b
、加沉淀剂:
如沉淀Cu2+、Hg2+等,以Na2S、H2S做沉淀剂
Cu2++S2-=CuS↓
Hg2++S2-=HgS↓
加氨水,OH-
浓度上升,平衡右移,有利于生成沉淀
c、同离子效应法:
例如,硫酸钡在硫酸中的溶解度比在纯水中小。
硫酸中硫酸根浓度大,使平衡左移有利于沉淀生成。
2、沉淀的溶解
(1)原理
设法不断移去溶解平衡体系中的相应离子,使平衡向沉淀溶解的方向移动
1、石灰乳中存在下列平衡:
Ca(OH)2(s)
Ca2+(aq)+2OH-(aq),加入下列溶液,可使Ca(OH)2减少的是(
)
A.Na2CO3溶液
B.KCl溶液
C.NaOH溶液
D.CaCl2溶液
A
练习:
【实验3-4】
有白色沉淀析出
白色沉淀转化为黄色
黄色沉淀转化为黑色
AgCl
AgI
Ag2S
3、沉淀的转化
步骤
1mLNaCl和10滴AgNO3溶混合(均为0.1mol/L)
向所得固液混合物中滴加10滴0.1mol/LKI溶液
向新得固液混合物中滴加10滴0.1mol/L
Na2S溶液
现象
[讨论]:从实验中可以得到什么结论?
实验说明:沉淀可以从溶解度小的向溶解度更小的方向转化,两者差别越大,转化越容易。
物质
溶解度/g
AgCl
1.5×10-4
AgI
9.6×10-9
Ag2S
1.3×10-16
练习:
1、在NaCl溶液中含有少量的Na2S,欲将S2-除去,可加入
( )
A.CuCl2 B.AgCl
C.NaOH
D.Ag2S
B
2、已知25℃时,AgCl的溶度积Ksp=1.8×10-10,则下列说法正确的是
( )
A.向饱和AgCl水溶液中加入盐酸,Ksp值变大B.AgNO3溶液与NaCl溶液混合后的溶液中,一定有c(Ag+)=c(Cl-)
C.温度一定时,当溶液中c(Ag+)·c(Cl-)=Ksp时,此溶液中必有AgCl的沉淀析出
D.将AgCl加入到较浓的KI溶液中,部分AgCl转化为AgI,因为AgCl溶解度大于AgI
D
人教版选修4
·
化学反应原理
第三章
水溶液中的离子平衡
第四节
难溶电解质的溶解平衡
1.什么是饱和溶液?
在一定温度下,在一定量的溶剂里,不能再溶解某种溶质的溶液,叫做这种溶质的饱和溶液。
复
习
2.如何判断某NaCl溶液是否已经达到饱和?
讨论1:
在NaCl的饱和溶液中,再加入固体溶质,固体会不会继续溶解?是否发生着溶解过程?
饱和NaCl溶液
一昼夜后观察发现:固体变为规则的立方体;质量并未发生改变
思考:
得到什么启示?
一昼夜后……
探究1:
结论:NaCl的饱和溶液中存在溶解平衡
我们知道,溶液中有难溶于水的沉淀生成是离子反应发生的条件之一。例如,AgNO3溶液与NaCl溶液混合,生成白色沉淀AgCl:Ag++Cl-=AgCl↓,如果上述两种溶液是等物质的量浓度、等体积的,一般认为反应可以进行到底。
一、Ag+和Cl-的反应真能进行到底吗?
一、Ag+和Cl-的反应真能进行到底吗?
Ag+
+
Cl-
=
AgCl↓
表3-4
几种电解质的溶解度(20℃)
化学式
溶解度/g
化学式
溶解度/g
AgCl
1.5×10-4
Ba(OH)2
3.89
AgNO3
222
BaSO4
2.4×10-4
AgBr
8.4×10-6
Ca(OH)2
0.165
Ag2SO4
0.796
CaSO4
0.21
Ag2S
1.3×10-16
Mg(OH)2
9×10-4
BaCl2
35.7
Fe(OH)3
3×10-9
200C时,溶解性与溶解度的大小关系
1、溶解是绝对的,不溶是相对的。
2、没有绝对不溶的电解质,难溶电解质
都会发生微量溶解。
3、生成沉淀的离子反应能发生的原因:生成物的溶解度很小。
化学上通常认为残留在溶液中的离子浓度小于1×10-5
mol/L,沉淀就达完全。
溶解性
易溶
可溶
微溶
难溶
溶解度
>10g
1g~10g
0.01g~1g
<0.01g
【实验】向盛有2
mL
0.1mol/LAgNO3溶液的试管中加入2
mL
0.1
mol/L
NaCl溶液。
讨论3:
现象:有白色沉淀生成,说明溶液中依然有Ag+
Cl-存在,即Ag+和Cl-的反应不能进行到底。
(1)是否恰好反应?
(2)溶液中是否还含有Ag+和Cl-?
【继续试验】取上层清液,滴加NaCl溶液,
有何现象?说明了什么?
沉淀是难溶物,但不是绝对不溶,只不过溶解
度很小,难溶物在水中存在溶解平衡。
初始状态:V(溶解)
>
V(沉淀)
溶解平衡:V(溶解)
=
V(沉淀)
得到饱和AgCl溶液,建立溶解平衡
思考:把AgCl固体加到水中都发生着怎样的过程?
二、难溶电解质的溶解平衡
1、概念:
在一定条件下,难溶电解质___________的速率等于离子重新_____________的速率,溶液中各离子的浓度__________的状态。(也叫沉淀溶解平衡)
溶解成离子
结合成沉淀
保持不变
2、溶解平衡的建立
以AgCl(s)的溶解平衡为例
3、表达方法
4、溶解平衡的特征
标明物质状态和可逆符号
逆、等、动、定、变
5、生成难溶电解质的离子反应的限度
离子浓度小于1×10-5mol/L时,认为反应完全。
6、沉淀溶解平衡的影响因素
①内因:电解质本身的性质。
只要是饱和溶液都存在溶解平衡。
绝对不溶的物质是没有的
不同难溶物其溶解度差别也很大
0.01g
10g
难溶
微溶
易溶
可溶
1g
②外因
加相同离子,平衡向沉淀方向移动。
温度:
浓度:
加水,平衡向溶解方向移动;
(Ca(OH)2除外)
升温,多数平衡向溶解方向移动。
1、下列说法中正确的是(
)
A.物质的溶解性为难溶,则该物质不溶于水
B.不溶于水的物质溶解度为0
C.绝对不溶解的物质是不存在的
D.某粒子被沉淀完全是指该粒子在溶液中的浓度为零
2、下列对沉淀溶解平衡的描述正确的是
(
)
A.开始时,溶液中各离子浓度相等
B.平衡时,沉淀的速率和溶解的速率相等
C.平衡时,溶液中溶质的离子浓度相等,且保持不变
D.平衡时,如果再加入难溶性的该沉淀物,将促进溶解
练习
C
B
3.(1)AgCl(s)
Ag+(aq)+Cl-(aq)
(2)AgCl===Ag++Cl-
问(1)式和(2)式所表示的意义?
4.常温条件下,CaCO3在水中的溶解度大还是在Na2CO3溶液中的溶解度大?
三.溶度积常数
1.定义
2.表达式
Ksp=[c(Mn+)]m·[c(Am—)]n
在难溶电解质的饱和溶液中,当溶解与结晶速率相等时,溶液达到溶解平衡状态,则该反应的平衡常数表示为:Ksp,AgCl
=[Ag+][Cl-]。该常数称为难溶电解质的溶度积常数,简称溶度积。
3、溶度积规则
AnBm(s)
nAm+(aq)
+
mBn-(aq)
Qc>Ksp时,溶液过饱和,有沉淀析出,直至达到平衡.
Qc=Ksp时,沉淀与饱和溶液的平衡.
Qc
②溶度积规则
①离子积
Qc=
c(Am+)n
·
c(Bn-)m
讨论:溶度积和溶解度都可以表示难溶电解质在水中的溶解能力,分析下表,你将如何看待溶度积和溶解度的关系?
结论:相同类型的难溶电解质的Ksp越小溶解度越小
一定条件下:
注意:只有在同种类型的电解质之间才能通过Ksp的
大小来直接比较溶解度的大小。
类型
化学式
溶度积Ksp
溶解度/g
AB
AgBr
5.0×10-13
8.4×10-6
AB
AgCl
1.8×10-10
1.5×10-4
A2B
Ag2CrO4
1.1×10-12
2.2×10-3
A2B
Ag2S
6.3×10-50
1.3×10-16
练一练
1、下列叙述正确的是(
)
A.由于AgCl水溶液导电性很弱,所以它是弱电解质
B.难溶电解质离子浓度的乘积就是该物质的溶度积常数
C.溶度积常数大者,溶解度也大
D.用水稀释含有AgCl固体的溶液时,
AgCl的溶度积常数不变。
D
练习1:25℃时,Ksp?(AgBr)=?5.0×10-10,求AgBr的饱和溶液中的c(Ag+)和c(Br-)。
4、利用溶度积计算某种离子的浓度:
练习2:25℃时,Ksp?[Mg(OH)2]=?1.8×10-11,求Mg(OH)2的饱和溶液中的C(Mg2+)和c(OH-)
C(Mg2+)=1.65×10-4,c(OH-)=3.3×10-4
c(Ag+)=c(Br-
)=2.2×10-5
6.判断能否生成沉淀
例:25℃时,在1.00?L?0.03?mol/L?AgNO3溶液中加入0.50?L?0.06?mol/L的CaCl2溶液,能否生成AgCl沉淀?
已知:AgCl的Ksp=1.8×10-10
c(Ag+)=(0.03?mol/L×1.00?L)÷(1.00?L+0.50?L)
=0.020?mol/L?
c(Cl-)=(0.06?mol/L×2×0.50?L)÷(1.00?L+0.50?L)
=0.040?mol/L?
Qc=c(Ag+)·c(Cl-)=0.020?mol/L×0.040?mol/L
=8.0×10-4
由于Qc>Ksp,所以有AgCl沉淀生成。
例:实验测得某水样中的铁离子的浓度为6×10-6mol·l-1
若要使水中的铁离子转化为沉淀,则溶液的PH值至少要控制在多少以上?[已知Fe(OH)3的Ksp为2.6×10-39]
解:设溶液中的OH-离子的浓度最少为X才能使水中的铁离子转化为沉淀。
KSP=c(Fe3+)
·c3(OH-)
=2.6×10-39
=6×10-6×X3
求得X=7.57×10-12mol·L-1=c(OH-)
C(H+)=1.32×10-3mol·L-1
PH=2.88
答:PH至少要控制在2.88以上。
7.计算某离子开始沉淀的pH值
第四节
难溶电解质的溶解平衡
Dissolution
electrolyte
equlibrium
?
第二课时
二、沉淀反应的应用
1、沉淀的生成
(1)应用:生成难溶电解质的沉淀,是工业生产、环保工程和科学研究中除杂或提纯物质的重要方法之一。
工业废水的处理
工业废水
硫化物等
重金属离子(如Cu2+、Hg2+等)转化成沉淀
(2)方法
a
、调pH
如:工业原料氯化铵中混有氯化铁,加氨水调pH值至7-8
b
、加沉淀剂:
如沉淀Cu2+、Hg2+等,以Na2S、H2S做沉淀剂
Cu2++S2-=CuS↓
Hg2++S2-=HgS↓
加氨水,OH-
浓度上升,平衡右移,有利于生成沉淀
c、同离子效应法:
例如,硫酸钡在硫酸中的溶解度比在纯水中小。
硫酸中硫酸根浓度大,使平衡左移有利于沉淀生成。
2、沉淀的溶解
(1)原理
设法不断移去溶解平衡体系中的相应离子,使平衡向沉淀溶解的方向移动
1、石灰乳中存在下列平衡:
Ca(OH)2(s)
Ca2+(aq)+2OH-(aq),加入下列溶液,可使Ca(OH)2减少的是(
)
A.Na2CO3溶液
B.KCl溶液
C.NaOH溶液
D.CaCl2溶液
A
练习:
【实验3-4】
有白色沉淀析出
白色沉淀转化为黄色
黄色沉淀转化为黑色
AgCl
AgI
Ag2S
3、沉淀的转化
步骤
1mLNaCl和10滴AgNO3溶混合(均为0.1mol/L)
向所得固液混合物中滴加10滴0.1mol/LKI溶液
向新得固液混合物中滴加10滴0.1mol/L
Na2S溶液
现象
[讨论]:从实验中可以得到什么结论?
实验说明:沉淀可以从溶解度小的向溶解度更小的方向转化,两者差别越大,转化越容易。
物质
溶解度/g
AgCl
1.5×10-4
AgI
9.6×10-9
Ag2S
1.3×10-16
练习:
1、在NaCl溶液中含有少量的Na2S,欲将S2-除去,可加入
( )
A.CuCl2 B.AgCl
C.NaOH
D.Ag2S
B
2、已知25℃时,AgCl的溶度积Ksp=1.8×10-10,则下列说法正确的是
( )
A.向饱和AgCl水溶液中加入盐酸,Ksp值变大B.AgNO3溶液与NaCl溶液混合后的溶液中,一定有c(Ag+)=c(Cl-)
C.温度一定时,当溶液中c(Ag+)·c(Cl-)=Ksp时,此溶液中必有AgCl的沉淀析出
D.将AgCl加入到较浓的KI溶液中,部分AgCl转化为AgI,因为AgCl溶解度大于AgI
D
