硫酸的制备和性质
图片预览







文档简介
(共25张PPT)
专题4 硫、氮和可持续发展
第一单元 含硫化合物的性质和应用
硫酸的制备和性质
亲爱的水: 我在这里把我的内心毫无保留地展现给你,我承认我很粘人;每当我遇上你,我就有种沸腾的感觉,我全身会发出大量的热;当我见不到你时,我会在空气中寻找你的气息,寻找每一丝你的痕迹,最终和你在一起。
水,为了找到你, 就算变成稀硫酸,也不会后悔。相信我,我是不挥发的, 最终定能等到你;水,就算你改头换面隐藏在有机物中,我也会把氢氧重新合成你。
水,没有了你,虽然我也和铁,铝接触过,但我选择了拒绝,因为我放不下你。
水,我可以对门捷列夫发誓,我会爱你一辈子。
98%的浓硫酸
一、物理性质
无色粘稠状液体,98.3%浓硫酸密度1.84g / cm3,高沸点(难挥发)酸338℃,易溶与水(任意比混溶)
1.浓硫酸
亲爱的水: 我在这里把我的内心毫无保留地展现给你,我承认我很粘人;每当我遇上你,我就有种沸腾的感觉,我全身会发出大量的热;当我见不到你时,我会在空气中寻找你的气息,寻找每一丝你的痕迹,最终和你在一起。
水,为了找到你, 就算变成稀硫酸,也不会后悔。相信我,我是不挥发的, 最终定能等到你;水,就算你改头换面隐藏在有机物中,我也会把氢氧重新合成你。
水,没有了你,虽然我也和铁,铝接触过,但我选择了拒绝,因为我放不下你。
水,我可以对门捷列夫发誓,我会爱你一辈子。
98%的浓硫酸
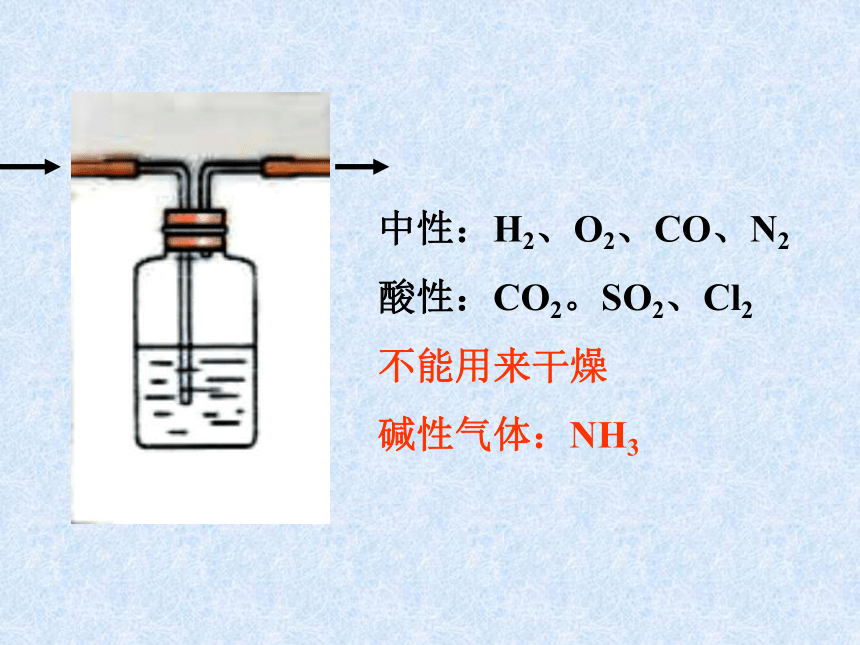
浓硫酸可以吸收:
吸水性
混在气体中的水蒸气
结晶水合物中的部分结晶水
浓硫酸的特性1
CuSO4 · 5H2O CuSO4(白色粉末)
实验1 向装有胆矾的试管中加入约2滴管的浓硫酸,振荡,静置片刻,观察现象。
中性:H2、O2、CO、N2
酸性:CO2。SO2、Cl2
不能用来干燥
碱性气体:NH3
亲爱的水: 我在这里把我的内心毫无保留地展现给你,我承认我很粘人;每当我遇上你,我就有种沸腾的感觉,我全身会发出大量的热;当我见不到你时,我会在空气中寻找你的气息,寻找每一丝你的痕迹,最终和你在一起。
水,为了找到你, 就算变成稀硫酸,也不会后悔。相信我,我是不挥发的, 最终定能等到你;水,就算你改头换面隐藏在有机物中,我也会把氢氧重新合成你。
水,没有了你,虽然我也和铁,铝接触过,但我选择了拒绝,因为我放不下你。
水,我可以对门捷列夫发誓,我会爱你一辈子。
98%的浓硫酸
浓硫酸可以把有机物中的H 、O两种元素按原子个数比为2:1(即按水的组成)生成水脱去
脱水性(炭化)
浓硫酸的特性2
实验2:向装有一小块猪肉的试管中加入约2滴管的浓硫酸,稍稍加热,观察现象。
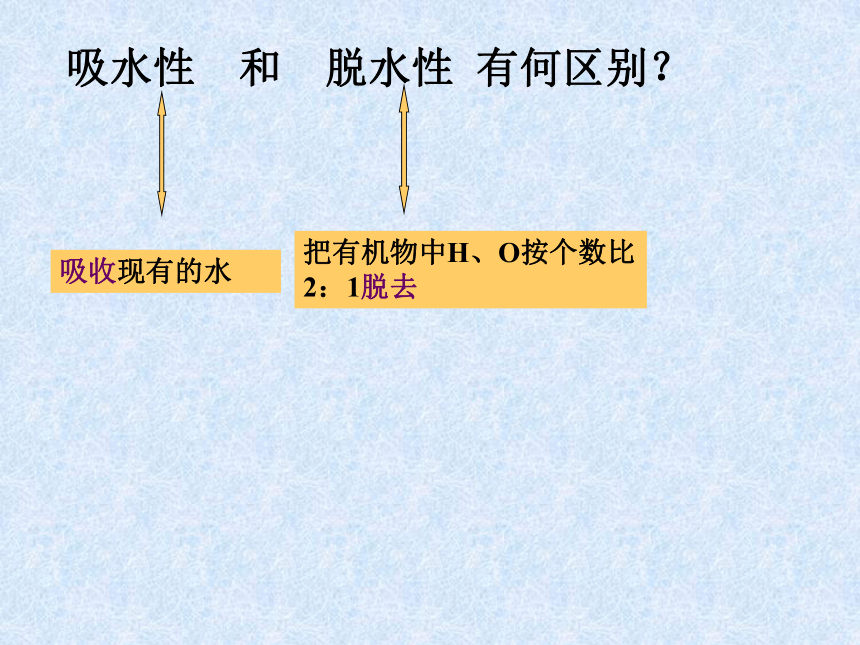
吸水性 和 脱水性 有何区别?
吸收现有的水
把有机物中H、O按个数比2:1脱去
如果你在做实验时,不慎将浓H2SO4沾到皮肤上,你应如何正确处理 (当然了,首先不要惊慌了)
先用一块干布迅速拭去浓H2SO4然后用大量水冲洗,再用稀NaHCO3溶液擦洗.切不可马上用水冲洗,否则可能会灼伤皮肤
浓硫酸的特性3
实验3 往试管中加入约2克蔗糖,加入几滴水,搅拌均匀,然后加入5ml溶质的质量分数为98%的浓硫酸,迅速搅拌,观察实验现象
现象
蔗糖由白变黑
蔗糖体积显著膨胀,呈疏松海绵状
有能使品红褪色的气体生成
放出大量的热
亲爱的水: 我在这里把我的内心毫无保留地展现给你,我承认我很粘人;每当我遇上你,我就有种沸腾的感觉,我全身会发出大量的热;当我见不到你时,我会在空气中寻找你的气息,寻找每一丝你的痕迹,最终和你在一起。
水,为了找到你, 就算变成稀硫酸,也不会后悔。相信我,我是不挥发的, 最终定能等到你;水,就算你改头换面隐藏在有机物中,我也会把氢氧重新合成你。
水,没有了你,虽然我也和铁,铝接触过,但我选择了拒绝,因为我放不下你。
水,我可以对门捷列夫发誓,我会爱你一辈子。
98%的浓硫酸
常温与铁和铝的反应
水,没有了你,虽然我也和铁,铝接触过,但我选择了拒绝
浓硫酸的特性4
实验4 将一小撮铜丝放入装有沸腾的浓硫酸的试管中,观察实验现象.
(1)常温与铁和铝的反应
(2)与金属反应总结:
浓硫酸的氧化性是由+6价的S原子表现出来的,
还原产物一般为SO2 ,不生成H2,体现强氧化性和酸性
金属 + 浓H2SO4 硫酸盐 + SO2 + H2O
(除Au、Pt外)
△
在浓硫酸溶液和稀硫酸溶液中硫酸的存在形式有何不同?
稀H2SO4
H+、 SO42﹣
浓H2SO4
H+、 SO42﹣
H2SO4 分子
在今后学习、解题中涉及到硫酸的内容一定要注意硫酸的浓度.
H2SO4 分子
1、请你为浓硫酸设计一张简历,形式如下
姓名 种类
出生地
外貌特征
与水的关系
特长
荣获的称号
浓硫酸
酸
忆往昔
硫酸的制取
在公元650~683年 “炼石胆取精华法”
——《黄帝九鼎神丹经诀》
18世纪40年代前,欧洲很多地方用绿矾(FeSO4·7H2O)为原料,放在蒸馏釜中煅烧而制得硫酸。
CuSO4·5H2O == CuO + SO3 ↑+ 5H2O
2FeSO4·7H2O == Fe2O3 + SO2 ↑+ SO3↑ +14 H2O
SO3 + H2O == H2SO4
SO3 + H2O == H2SO4
硫酸工业生产流程动画
硫酸的工业生产
沸 腾 炉
接 触 室
吸 收 塔
净化
冷 却
看今朝
1、请你为浓硫酸设计一张简历,形式如下
姓名 种类
出生地
外貌特征
与水的关系
特长
荣获的称号
浓硫酸
酸
沸腾炉
接触室
吸收塔
1、吸水性 2、脱水性
3、与金属——强氧化性和酸性
4、与非金属——强氧化性
与水以任意比互溶,密度比水大,遇水放热,只能进入水中不能允许水进入。
无色油状液体
硫酸的美誉——化学工业之母
工业上常用硫酸的年产量来衡量一个国家的化工生产能力
1、请你为浓硫酸设计一张简历,形式如下
姓名 种类
出生地
外貌特征
与水的关系
特长
荣获的称号
浓硫酸
酸
沸腾炉
接触室
吸收塔
1、吸水性 2、脱水性
3、与金属——强氧化性和酸性
4、与非金属——强氧化性
与水以任意比互溶,密度比水大,遇水放热,只能进入水中不能允许水进入。
无色油状液体
化学工业之母
[课堂练习]
2、问题解决:一铁罐车运载浓硫酸发生事故。思考:
(1)铁可与硫酸反应,为何可将浓硫酸密闭在铁罐中?在此铁罐出口处腐蚀严重,这说明了浓硫酸具有什么性质?
(2)清洗此铁罐时一定要远离火源,为什么呢?
(3)道路被破坏,树木被烧死的原因是什么呢?
(4)如何处理被泄露的硫酸呢?
1.(1)冷的浓硫酸能使铁钝化,所以可将浓硫酸密闭在铁罐中。铁罐出口处腐蚀严重,说明浓硫酸具有吸水性。
(2)稀硫酸与铁反应生成氢气,有火源可能引起爆炸。
(3)浓硫酸的强腐蚀性。
(4)洒石灰。
参考答案:
课堂练习
3、下列现象反应了硫酸的哪些主要性质
(1)浓硫酸滴在木条上,过了一会儿,木条变黑( )
(2)敞口放置浓硫酸时,质量有所增加( )
(3)锌粒投入稀硫酸中,有气泡产生( )
(4)把铜片放入浓硫酸里加热,有气体产生( )
(6)使蓝色石蕊试纸先变红后变黑( )
(7)利用NaCl固体跟浓硫酸反应可制HCl气体( )
脱水性
吸水性
酸性、强氧化性
酸性
高沸点性
酸性、脱水性
再 见 !
专题4 硫、氮和可持续发展
第一单元 含硫化合物的性质和应用
硫酸的制备和性质
亲爱的水: 我在这里把我的内心毫无保留地展现给你,我承认我很粘人;每当我遇上你,我就有种沸腾的感觉,我全身会发出大量的热;当我见不到你时,我会在空气中寻找你的气息,寻找每一丝你的痕迹,最终和你在一起。
水,为了找到你, 就算变成稀硫酸,也不会后悔。相信我,我是不挥发的, 最终定能等到你;水,就算你改头换面隐藏在有机物中,我也会把氢氧重新合成你。
水,没有了你,虽然我也和铁,铝接触过,但我选择了拒绝,因为我放不下你。
水,我可以对门捷列夫发誓,我会爱你一辈子。
98%的浓硫酸
一、物理性质
无色粘稠状液体,98.3%浓硫酸密度1.84g / cm3,高沸点(难挥发)酸338℃,易溶与水(任意比混溶)
1.浓硫酸
亲爱的水: 我在这里把我的内心毫无保留地展现给你,我承认我很粘人;每当我遇上你,我就有种沸腾的感觉,我全身会发出大量的热;当我见不到你时,我会在空气中寻找你的气息,寻找每一丝你的痕迹,最终和你在一起。
水,为了找到你, 就算变成稀硫酸,也不会后悔。相信我,我是不挥发的, 最终定能等到你;水,就算你改头换面隐藏在有机物中,我也会把氢氧重新合成你。
水,没有了你,虽然我也和铁,铝接触过,但我选择了拒绝,因为我放不下你。
水,我可以对门捷列夫发誓,我会爱你一辈子。
98%的浓硫酸
浓硫酸可以吸收:
吸水性
混在气体中的水蒸气
结晶水合物中的部分结晶水
浓硫酸的特性1
CuSO4 · 5H2O CuSO4(白色粉末)
实验1 向装有胆矾的试管中加入约2滴管的浓硫酸,振荡,静置片刻,观察现象。
中性:H2、O2、CO、N2
酸性:CO2。SO2、Cl2
不能用来干燥
碱性气体:NH3
亲爱的水: 我在这里把我的内心毫无保留地展现给你,我承认我很粘人;每当我遇上你,我就有种沸腾的感觉,我全身会发出大量的热;当我见不到你时,我会在空气中寻找你的气息,寻找每一丝你的痕迹,最终和你在一起。
水,为了找到你, 就算变成稀硫酸,也不会后悔。相信我,我是不挥发的, 最终定能等到你;水,就算你改头换面隐藏在有机物中,我也会把氢氧重新合成你。
水,没有了你,虽然我也和铁,铝接触过,但我选择了拒绝,因为我放不下你。
水,我可以对门捷列夫发誓,我会爱你一辈子。
98%的浓硫酸
浓硫酸可以把有机物中的H 、O两种元素按原子个数比为2:1(即按水的组成)生成水脱去
脱水性(炭化)
浓硫酸的特性2
实验2:向装有一小块猪肉的试管中加入约2滴管的浓硫酸,稍稍加热,观察现象。
吸水性 和 脱水性 有何区别?
吸收现有的水
把有机物中H、O按个数比2:1脱去
如果你在做实验时,不慎将浓H2SO4沾到皮肤上,你应如何正确处理 (当然了,首先不要惊慌了)
先用一块干布迅速拭去浓H2SO4然后用大量水冲洗,再用稀NaHCO3溶液擦洗.切不可马上用水冲洗,否则可能会灼伤皮肤
浓硫酸的特性3
实验3 往试管中加入约2克蔗糖,加入几滴水,搅拌均匀,然后加入5ml溶质的质量分数为98%的浓硫酸,迅速搅拌,观察实验现象
现象
蔗糖由白变黑
蔗糖体积显著膨胀,呈疏松海绵状
有能使品红褪色的气体生成
放出大量的热
亲爱的水: 我在这里把我的内心毫无保留地展现给你,我承认我很粘人;每当我遇上你,我就有种沸腾的感觉,我全身会发出大量的热;当我见不到你时,我会在空气中寻找你的气息,寻找每一丝你的痕迹,最终和你在一起。
水,为了找到你, 就算变成稀硫酸,也不会后悔。相信我,我是不挥发的, 最终定能等到你;水,就算你改头换面隐藏在有机物中,我也会把氢氧重新合成你。
水,没有了你,虽然我也和铁,铝接触过,但我选择了拒绝,因为我放不下你。
水,我可以对门捷列夫发誓,我会爱你一辈子。
98%的浓硫酸
常温与铁和铝的反应
水,没有了你,虽然我也和铁,铝接触过,但我选择了拒绝
浓硫酸的特性4
实验4 将一小撮铜丝放入装有沸腾的浓硫酸的试管中,观察实验现象.
(1)常温与铁和铝的反应
(2)与金属反应总结:
浓硫酸的氧化性是由+6价的S原子表现出来的,
还原产物一般为SO2 ,不生成H2,体现强氧化性和酸性
金属 + 浓H2SO4 硫酸盐 + SO2 + H2O
(除Au、Pt外)
△
在浓硫酸溶液和稀硫酸溶液中硫酸的存在形式有何不同?
稀H2SO4
H+、 SO42﹣
浓H2SO4
H+、 SO42﹣
H2SO4 分子
在今后学习、解题中涉及到硫酸的内容一定要注意硫酸的浓度.
H2SO4 分子
1、请你为浓硫酸设计一张简历,形式如下
姓名 种类
出生地
外貌特征
与水的关系
特长
荣获的称号
浓硫酸
酸
忆往昔
硫酸的制取
在公元650~683年 “炼石胆取精华法”
——《黄帝九鼎神丹经诀》
18世纪40年代前,欧洲很多地方用绿矾(FeSO4·7H2O)为原料,放在蒸馏釜中煅烧而制得硫酸。
CuSO4·5H2O == CuO + SO3 ↑+ 5H2O
2FeSO4·7H2O == Fe2O3 + SO2 ↑+ SO3↑ +14 H2O
SO3 + H2O == H2SO4
SO3 + H2O == H2SO4
硫酸工业生产流程动画
硫酸的工业生产
沸 腾 炉
接 触 室
吸 收 塔
净化
冷 却
看今朝
1、请你为浓硫酸设计一张简历,形式如下
姓名 种类
出生地
外貌特征
与水的关系
特长
荣获的称号
浓硫酸
酸
沸腾炉
接触室
吸收塔
1、吸水性 2、脱水性
3、与金属——强氧化性和酸性
4、与非金属——强氧化性
与水以任意比互溶,密度比水大,遇水放热,只能进入水中不能允许水进入。
无色油状液体
硫酸的美誉——化学工业之母
工业上常用硫酸的年产量来衡量一个国家的化工生产能力
1、请你为浓硫酸设计一张简历,形式如下
姓名 种类
出生地
外貌特征
与水的关系
特长
荣获的称号
浓硫酸
酸
沸腾炉
接触室
吸收塔
1、吸水性 2、脱水性
3、与金属——强氧化性和酸性
4、与非金属——强氧化性
与水以任意比互溶,密度比水大,遇水放热,只能进入水中不能允许水进入。
无色油状液体
化学工业之母
[课堂练习]
2、问题解决:一铁罐车运载浓硫酸发生事故。思考:
(1)铁可与硫酸反应,为何可将浓硫酸密闭在铁罐中?在此铁罐出口处腐蚀严重,这说明了浓硫酸具有什么性质?
(2)清洗此铁罐时一定要远离火源,为什么呢?
(3)道路被破坏,树木被烧死的原因是什么呢?
(4)如何处理被泄露的硫酸呢?
1.(1)冷的浓硫酸能使铁钝化,所以可将浓硫酸密闭在铁罐中。铁罐出口处腐蚀严重,说明浓硫酸具有吸水性。
(2)稀硫酸与铁反应生成氢气,有火源可能引起爆炸。
(3)浓硫酸的强腐蚀性。
(4)洒石灰。
参考答案:
课堂练习
3、下列现象反应了硫酸的哪些主要性质
(1)浓硫酸滴在木条上,过了一会儿,木条变黑( )
(2)敞口放置浓硫酸时,质量有所增加( )
(3)锌粒投入稀硫酸中,有气泡产生( )
(4)把铜片放入浓硫酸里加热,有气体产生( )
(6)使蓝色石蕊试纸先变红后变黑( )
(7)利用NaCl固体跟浓硫酸反应可制HCl气体( )
脱水性
吸水性
酸性、强氧化性
酸性
高沸点性
酸性、脱水性
再 见 !
