硫酸的制备和性质
图片预览





文档简介
(共24张PPT)
§2 硫酸的制备和性质
第一单元 含硫化合物的性质和应用
看图说成语
望梅止渴
打一个化学物质!
硫(流)酸
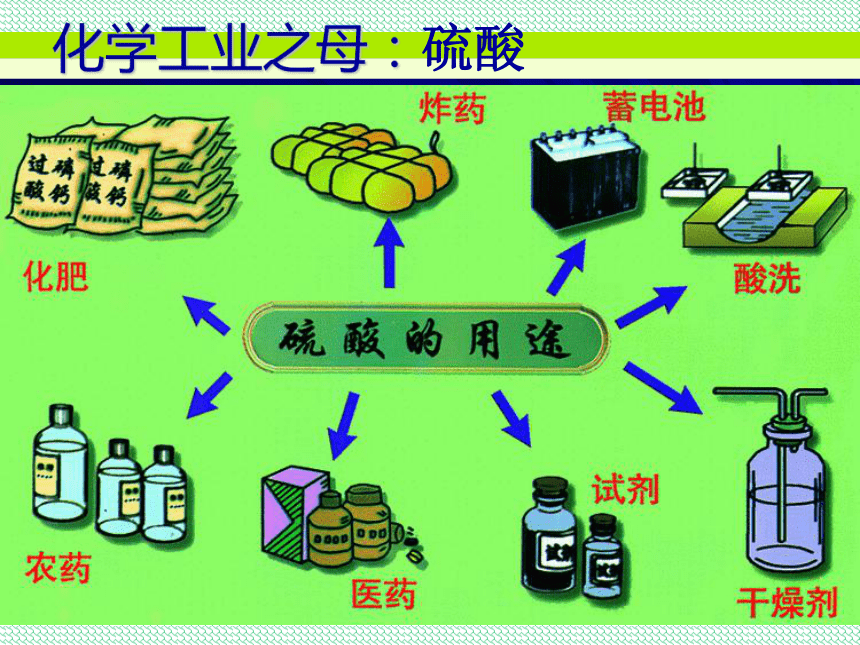
化学工业之母:硫酸
含硫矿石
硫磺
S
黄铁矿
FeS2
含硫矿石
重晶石(硫酸钡)
BaSO4
绿矾
FeSO4·7H2O
胆矾
CuSO4·5H2O
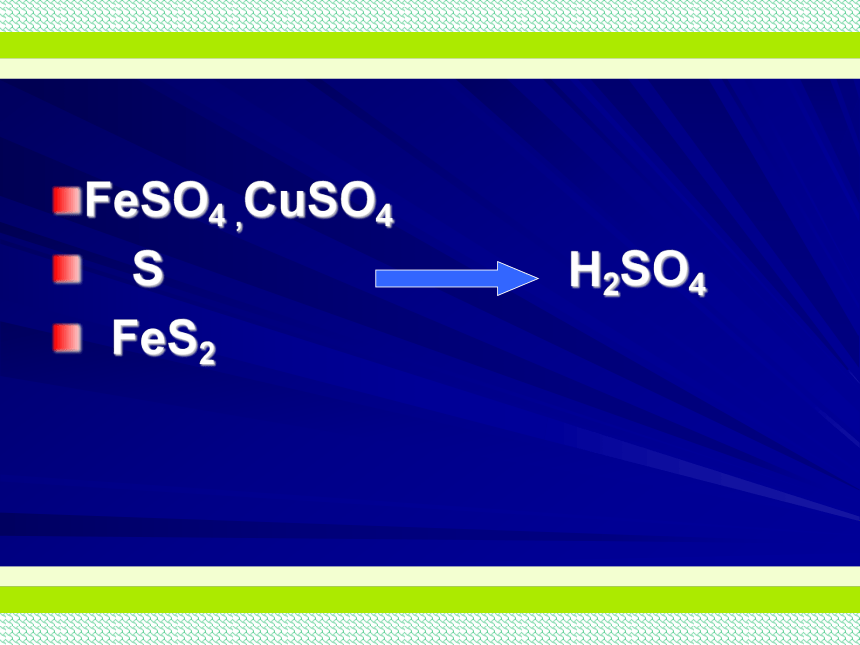
FeSO4 ,CuSO4
S H2SO4
FeS2
硫酸的制备
在公元650~683年,炼丹家孤刚子在其所著《黄帝九鼎神丹经诀》记载着“炼石胆取精华法”,即干馏胆矾而获得硫酸。
CuSO4 CuO+SO3↑ ;SO3+H2O=H2SO4。
公元8世纪阿拉伯炼金家贾比尔发现,将硝石和绿矾一起蒸馏,所得气体溶于水得硫酸(绿矾油)。
2FeSO4 Fe2O3+SO2+SO3,
SO3+H2O=H2SO4。
早在1000多年前,人类就已采用加热胆矾或绿矾的方法来制取硫酸。
硫酸的制备
19世纪后期,接触法制硫酸获得工业应用,目前已成为生产硫酸的主要方法。它以硫磺或黄铁矿为原料,通过空气氧化生成SO2、SO3,再用水吸收SO3得到硫酸。
接触法制硫酸
【学生实验】
【学生实验1】在二只表面皿中分别加入1药匙硫酸铜晶体,分别滴加2滴管酸液,观察实验现象。
【学生实验2】取白纸于表面皿上,分别用玻璃棒蘸取两种酸液在纸上写字,然后用酒精灯火焰上方烘烤,观察实验现象。
实验时间:2-3min
温馨提示:取用浓硫酸时避免滴在桌面、手和衣服上。如果不慎滴到皮肤上,先用布轻轻擦去,再用水冲洗。
比较
浓硫酸的吸水性和脱水性
如:空气中的水分、物质中的湿存水、结晶水合物中的结晶水等,形成硫酸的水合物。
原来就有水
原来没有水
是指浓硫酸吸收现成游离的水分子。
是指浓硫酸将有机物中的H、O按原子个数比2:1(即水的组成比例)脱去。
脱水性
吸水性
新闻报道
新 闻 回 放
2008年7月14日14:45分,上三高速上虞境内,一辆橘红色的大货车与一辆满载浓硫酸的红色槽车发生追尾相撞。铝制槽车尾部阀门被撞掉,粘稠的浓硫酸喷涌而出,在路面上四处流淌,地面焦黑一片,当硫酸流入路旁沟渠,沟渠中的水顿时泛起水泡,产生大量白雾。一股呛鼻的怪味在空气中渐渐弥散开去。路过司机见此状况,束手无策,不知如何应对才好。
如果你是消防队员,到现场后准备怎么处理?
新闻报道
后续报道
接到报警后,上虞市110指挥中心立即派遣出上虞市消防大队赶赴现场。消防大队官兵穿着防护服赶到现场后,立即展开工作。他们首先阻止了浓硫酸流向附近水域,接着向路面以及水渠喷洒石灰和液碱,中和了泄露的硫酸,同时消防大队三支高压水枪组成一面水幕,有效防止了呛鼻的SO2气体的扩散。到15时许,上三高速交通已恢复正常。
小结
浓硫酸的性质
物理性质
特 性
吸水性
脱水性
强氧化性
金属
非金属
化合物
高沸点
高密度
难挥发
易溶水
2010.12.11
小结:硫酸的工业制备---接触法
SO2的制取
SO2氧化成SO3
SO3转化为 H2SO4
3个主要设备
3个生产阶段
3个反应方程式
SO3+H2O=H2SO4
2SO2+O2 2SO3
△
催化剂
沸腾炉
接触室
吸收塔
点燃
S+O2=SO2
4FeS2+11O2=2Fe2O3+8SO2
高温
3种主要原料:硫或含硫矿石;空气;98.3%的H2SO4
§2 硫酸的制备和性质
第一单元 含硫化合物的性质和应用
看图说成语
望梅止渴
打一个化学物质!
硫(流)酸
化学工业之母:硫酸
含硫矿石
硫磺
S
黄铁矿
FeS2
含硫矿石
重晶石(硫酸钡)
BaSO4
绿矾
FeSO4·7H2O
胆矾
CuSO4·5H2O
FeSO4 ,CuSO4
S H2SO4
FeS2
硫酸的制备
在公元650~683年,炼丹家孤刚子在其所著《黄帝九鼎神丹经诀》记载着“炼石胆取精华法”,即干馏胆矾而获得硫酸。
CuSO4 CuO+SO3↑ ;SO3+H2O=H2SO4。
公元8世纪阿拉伯炼金家贾比尔发现,将硝石和绿矾一起蒸馏,所得气体溶于水得硫酸(绿矾油)。
2FeSO4 Fe2O3+SO2+SO3,
SO3+H2O=H2SO4。
早在1000多年前,人类就已采用加热胆矾或绿矾的方法来制取硫酸。
硫酸的制备
19世纪后期,接触法制硫酸获得工业应用,目前已成为生产硫酸的主要方法。它以硫磺或黄铁矿为原料,通过空气氧化生成SO2、SO3,再用水吸收SO3得到硫酸。
接触法制硫酸
【学生实验】
【学生实验1】在二只表面皿中分别加入1药匙硫酸铜晶体,分别滴加2滴管酸液,观察实验现象。
【学生实验2】取白纸于表面皿上,分别用玻璃棒蘸取两种酸液在纸上写字,然后用酒精灯火焰上方烘烤,观察实验现象。
实验时间:2-3min
温馨提示:取用浓硫酸时避免滴在桌面、手和衣服上。如果不慎滴到皮肤上,先用布轻轻擦去,再用水冲洗。
比较
浓硫酸的吸水性和脱水性
如:空气中的水分、物质中的湿存水、结晶水合物中的结晶水等,形成硫酸的水合物。
原来就有水
原来没有水
是指浓硫酸吸收现成游离的水分子。
是指浓硫酸将有机物中的H、O按原子个数比2:1(即水的组成比例)脱去。
脱水性
吸水性
新闻报道
新 闻 回 放
2008年7月14日14:45分,上三高速上虞境内,一辆橘红色的大货车与一辆满载浓硫酸的红色槽车发生追尾相撞。铝制槽车尾部阀门被撞掉,粘稠的浓硫酸喷涌而出,在路面上四处流淌,地面焦黑一片,当硫酸流入路旁沟渠,沟渠中的水顿时泛起水泡,产生大量白雾。一股呛鼻的怪味在空气中渐渐弥散开去。路过司机见此状况,束手无策,不知如何应对才好。
如果你是消防队员,到现场后准备怎么处理?
新闻报道
后续报道
接到报警后,上虞市110指挥中心立即派遣出上虞市消防大队赶赴现场。消防大队官兵穿着防护服赶到现场后,立即展开工作。他们首先阻止了浓硫酸流向附近水域,接着向路面以及水渠喷洒石灰和液碱,中和了泄露的硫酸,同时消防大队三支高压水枪组成一面水幕,有效防止了呛鼻的SO2气体的扩散。到15时许,上三高速交通已恢复正常。
小结
浓硫酸的性质
物理性质
特 性
吸水性
脱水性
强氧化性
金属
非金属
化合物
高沸点
高密度
难挥发
易溶水
2010.12.11
小结:硫酸的工业制备---接触法
SO2的制取
SO2氧化成SO3
SO3转化为 H2SO4
3个主要设备
3个生产阶段
3个反应方程式
SO3+H2O=H2SO4
2SO2+O2 2SO3
△
催化剂
沸腾炉
接触室
吸收塔
点燃
S+O2=SO2
4FeS2+11O2=2Fe2O3+8SO2
高温
3种主要原料:硫或含硫矿石;空气;98.3%的H2SO4
