人教版高中化学选4-4第四节 金属的电化学腐蚀与防护(共20张PPT)
文档属性
| 名称 | 人教版高中化学选4-4第四节 金属的电化学腐蚀与防护(共20张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-07-29 00:00:00 | ||
图片预览







文档简介
(共20张PPT)
第四章
电化学基础
第四节
金属的电化学腐蚀与防护
铁锈斑斑,让人心酸;
据有关专家介绍,全球每一分钟就有1吨钢腐蚀成铁锈,目前我国由于金属材料的腐蚀损失每年大约5000亿元人民币,约占我国国民生产总值的4%左右。
铁锈斑斑,让人心酸;
钢铁生锈,大桥断裂!
一、金属的电化学腐蚀
3、金属腐蚀的类型
化学腐蚀
电化学腐蚀
2、金属腐蚀的本质:
1、金属腐蚀:
是指金属或合金与周围的气体或液体物质发生氧化还原反应而引起损耗的现象。
钢铁及其制品通常为含碳的铁合金,在潮湿的环境里或湿度较大的环境里长期放置,比在干燥的环境下放置,哪个更易生锈变红,原因是什么?
化学腐蚀:
金属跟接触到的干燥气体(如O2、Cl2、SO2等)
或非电解质液体(如石油)等直接发生化学反应而引起的腐蚀。
化学腐蚀的速度随着温度升高而加快。
电化学腐蚀:
不纯的金属跟电解质溶液接触,会发生原电池反应,比较活泼的金属失去电子而被氧化的腐蚀。
3、金属腐蚀的类型
一、金属的电化学腐蚀
腐蚀速率与什么有关系?
(常见普遍
,
腐蚀速率较快)
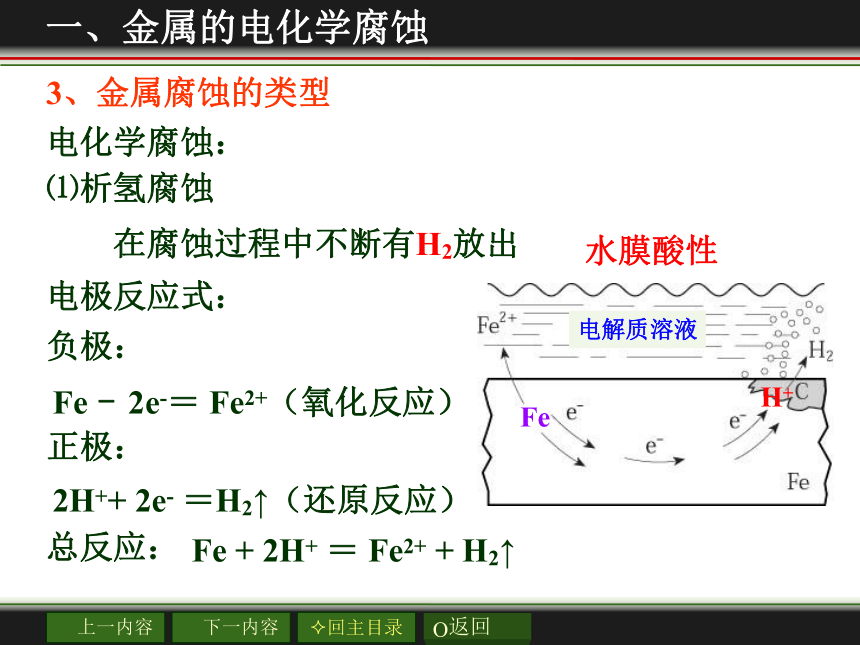
电化学腐蚀:
⑴析氢腐蚀
电极反应式:
负极:
正极:
总反应:
Fe
-
2e-=
Fe2+(氧化反应)
2H++
2e-
=H2↑(还原反应)
Fe
+
2H+
=
Fe2+
+
H2↑
在腐蚀过程中不断有H2放出
一、金属的电化学腐蚀
3、金属腐蚀的类型
电化学腐蚀:
⑵吸氧腐蚀
电极反应式:
负极:
正极:
总反应:
2Fe
-
4e-=
2Fe2+(氧化反应)
2H2O
+
O2
+
4e-
=
4OH-(还原反应)
2Fe
+
O2
+
2H2O
=
2Fe(OH)2
在腐蚀过程中吸收O2
4Fe(OH)2
+
O2
+
2H2O
=
4Fe(OH)3
Fe2O3·xH2O
铁锈
脱水
一、金属的电化学腐蚀
3、金属腐蚀的类型
一、金属的电化学腐蚀
3、金属腐蚀的类型
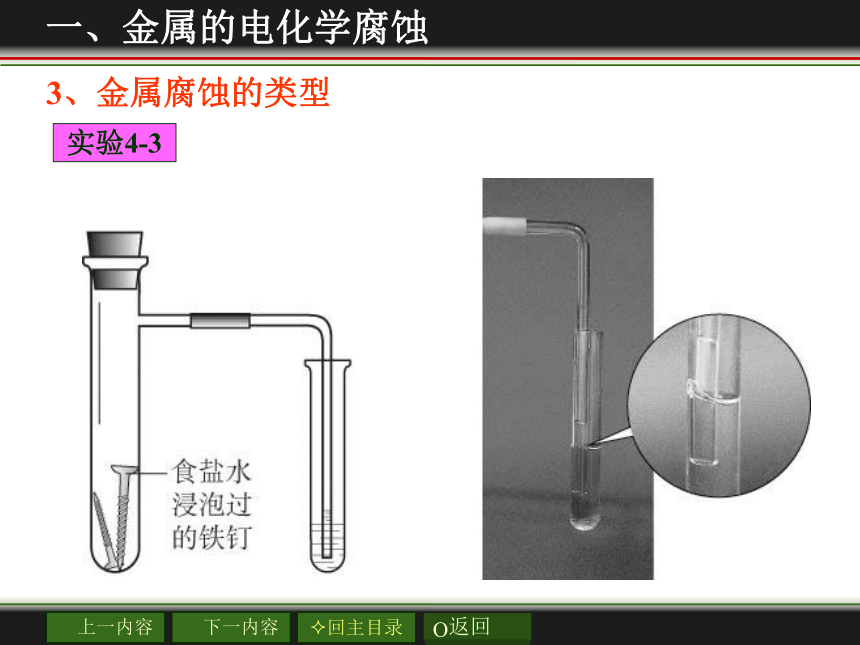
实验4-3
钢铁的析氢腐蚀和吸氧腐蚀的比较
水膜呈弱酸性或中性
水膜酸性较强
2Fe
-
4e-=
2Fe2+
2H2O
+
O2
+
4e-
=
4OH-
2H++
2e-
=H2↑
通常两种腐蚀同时存在,但以后者更普遍。
析氢腐蚀
吸氧腐蚀
条件
正极反应
负极反应
联系
化学腐蚀与电化腐蚀的比较
金属跟氧化性物质
直接接触
不纯金属或合金跟电解质溶液及氧化剂接触
无电流产生
有微弱的电流产生
金属被氧化的过程
较活泼金属被氧化的过程
两者往往同时发生,电化腐蚀更普遍
化学腐蚀
电化腐蚀
条件
有无
电流
本质
联系
1.相对于在内河行驶的轮船来说,海轮更容易被腐蚀。
因为海水中含有较多的氯化钠等盐类,导电能力比内河的水更强,而在电解质溶液中,电化学腐蚀更容易进行。
2.用于连接铜板的铁螺丝容易生锈。
是由于铁与铜及空气中的水蒸汽构成了原电池,铁作原电池的负极,因此铁易被腐蚀而生锈。
3.炒过菜的铁锅未及时洗净(残液中含有NaCl),不久便会出现红褐色锈斑。
(
-
)
(
+
)
原电池的负极也可称为阳极,
正极也可称为阴极
铁
Fe
原理
:
形成原电池反应时,让被保护金属做正极,不反应,起到保护作用;而活泼金属做负极受到腐蚀。
1.牺牲阳极的阴极保护法
二、金属的电化学保护
牺牲阳极的阴极保护法
原理
:
将被保护金属与另一附加电极作为电解池的两个极,使被保护的金属作为阴极,在外加直流电的作用下使阴极得到保护。此法主要用于防止土壤、海水及水中金属设备的腐蚀。
2.外加电流的阴极保护法
外加电流的阴极保护法
二、金属的电化学保护
2.外加电流的阴极保护法
1.牺牲阳极的阴极保护法
1.在金属表面覆盖保护层
2.改变金属内部的组织结构,制成合金
三、金属防腐蚀的其它方法
二、金属的电化学保护
讨论:
1.电压表指针有何变化?为什么?
2.Zn、Fe两极上发生了什么反应?
3.Fe2+与[Fe(CN)6]3-反应生成带有
特征蓝色的铁氰化亚铁沉淀:
3
Fe2+
+2[Fe(CN)6]3-
=Fe3[Fe(CN)6]2
↓
在这个装置中有没有产生?说明什么?
科学探究
用实验验证牺牲阳极的阴极保护法
往Fe电极附近滴入K3[Fe(CN)
6]溶液,溶液不变蓝色。即
溶液中不存在Fe2+,证明Fe未被腐蚀。
电压计指针有偏移,Zn片与Fe片构成
了原电池,产生电流。
阳极:Zn-2e-
=
Zn2+
阴极:2H+
+
2e-
=
H2↑
1、下列各情况,在其中Fe片腐蚀由快到慢的顺序是
(5)
(2)
(1)
(3)
(4)
课堂练习
金属腐蚀的快慢程度:电解池的阳极>原电池的负极>化学腐蚀>原电池的正极>电解池的阴极
金属腐蚀
我国作为世界上钢铁产量最多的国家(
2005
年全国生产钢材37117.02万吨)
,每年被腐蚀的铁占到我国钢铁年产量的十分之一,因为金属腐蚀而造成的损失占到国内生产总值的
2%~4%;约合人民币:3000亿元(2005年我国国内生产总值将达15万亿元)。
根据各国调查结果,一般说来,金属腐蚀所造成的经济损失大致为该国国民生产总值的4%左右。
另据国外统计,金属腐蚀的年损失远远超过水灾、火灾、风灾和地震(平均值)损失的总和,在这里还不包括由于腐蚀导致的停工、减产和爆炸等造成的间接损失。
看后:你有何感想?
金属腐蚀
金属腐蚀的主要害处,不仅在于金属本身的损失,更严重的是金属制品结构损坏所造成的损失比金属本身要大到无法估量。
腐蚀不仅造成经济损失,也经常对安全构成威胁。
国内外都曾发生过许多灾难性腐蚀事故,如飞机因某一零部件破裂而坠毁;桥梁因钢梁产生裂缝而塌陷;油管因穿孔或裂缝而漏油,引起着火爆炸;化工厂中储酸槽穿孔泄漏,造成重大环境污染;管道和设备跑、冒、滴、漏,破坏生产环境,有毒气体如Cl2、H2S、HCN等的泄漏,更会危及工作人员和附近居民的生命安全。
面对这样惊人的数据
和金属腐蚀危害事实,
大家有没有想过,
铁怎么会被腐蚀?
怎样防腐?
看后:你有何感想?
第四章
电化学基础
第四节
金属的电化学腐蚀与防护
铁锈斑斑,让人心酸;
据有关专家介绍,全球每一分钟就有1吨钢腐蚀成铁锈,目前我国由于金属材料的腐蚀损失每年大约5000亿元人民币,约占我国国民生产总值的4%左右。
铁锈斑斑,让人心酸;
钢铁生锈,大桥断裂!
一、金属的电化学腐蚀
3、金属腐蚀的类型
化学腐蚀
电化学腐蚀
2、金属腐蚀的本质:
1、金属腐蚀:
是指金属或合金与周围的气体或液体物质发生氧化还原反应而引起损耗的现象。
钢铁及其制品通常为含碳的铁合金,在潮湿的环境里或湿度较大的环境里长期放置,比在干燥的环境下放置,哪个更易生锈变红,原因是什么?
化学腐蚀:
金属跟接触到的干燥气体(如O2、Cl2、SO2等)
或非电解质液体(如石油)等直接发生化学反应而引起的腐蚀。
化学腐蚀的速度随着温度升高而加快。
电化学腐蚀:
不纯的金属跟电解质溶液接触,会发生原电池反应,比较活泼的金属失去电子而被氧化的腐蚀。
3、金属腐蚀的类型
一、金属的电化学腐蚀
腐蚀速率与什么有关系?
(常见普遍
,
腐蚀速率较快)
电化学腐蚀:
⑴析氢腐蚀
电极反应式:
负极:
正极:
总反应:
Fe
-
2e-=
Fe2+(氧化反应)
2H++
2e-
=H2↑(还原反应)
Fe
+
2H+
=
Fe2+
+
H2↑
在腐蚀过程中不断有H2放出
一、金属的电化学腐蚀
3、金属腐蚀的类型
电化学腐蚀:
⑵吸氧腐蚀
电极反应式:
负极:
正极:
总反应:
2Fe
-
4e-=
2Fe2+(氧化反应)
2H2O
+
O2
+
4e-
=
4OH-(还原反应)
2Fe
+
O2
+
2H2O
=
2Fe(OH)2
在腐蚀过程中吸收O2
4Fe(OH)2
+
O2
+
2H2O
=
4Fe(OH)3
Fe2O3·xH2O
铁锈
脱水
一、金属的电化学腐蚀
3、金属腐蚀的类型
一、金属的电化学腐蚀
3、金属腐蚀的类型
实验4-3
钢铁的析氢腐蚀和吸氧腐蚀的比较
水膜呈弱酸性或中性
水膜酸性较强
2Fe
-
4e-=
2Fe2+
2H2O
+
O2
+
4e-
=
4OH-
2H++
2e-
=H2↑
通常两种腐蚀同时存在,但以后者更普遍。
析氢腐蚀
吸氧腐蚀
条件
正极反应
负极反应
联系
化学腐蚀与电化腐蚀的比较
金属跟氧化性物质
直接接触
不纯金属或合金跟电解质溶液及氧化剂接触
无电流产生
有微弱的电流产生
金属被氧化的过程
较活泼金属被氧化的过程
两者往往同时发生,电化腐蚀更普遍
化学腐蚀
电化腐蚀
条件
有无
电流
本质
联系
1.相对于在内河行驶的轮船来说,海轮更容易被腐蚀。
因为海水中含有较多的氯化钠等盐类,导电能力比内河的水更强,而在电解质溶液中,电化学腐蚀更容易进行。
2.用于连接铜板的铁螺丝容易生锈。
是由于铁与铜及空气中的水蒸汽构成了原电池,铁作原电池的负极,因此铁易被腐蚀而生锈。
3.炒过菜的铁锅未及时洗净(残液中含有NaCl),不久便会出现红褐色锈斑。
(
-
)
(
+
)
原电池的负极也可称为阳极,
正极也可称为阴极
铁
Fe
原理
:
形成原电池反应时,让被保护金属做正极,不反应,起到保护作用;而活泼金属做负极受到腐蚀。
1.牺牲阳极的阴极保护法
二、金属的电化学保护
牺牲阳极的阴极保护法
原理
:
将被保护金属与另一附加电极作为电解池的两个极,使被保护的金属作为阴极,在外加直流电的作用下使阴极得到保护。此法主要用于防止土壤、海水及水中金属设备的腐蚀。
2.外加电流的阴极保护法
外加电流的阴极保护法
二、金属的电化学保护
2.外加电流的阴极保护法
1.牺牲阳极的阴极保护法
1.在金属表面覆盖保护层
2.改变金属内部的组织结构,制成合金
三、金属防腐蚀的其它方法
二、金属的电化学保护
讨论:
1.电压表指针有何变化?为什么?
2.Zn、Fe两极上发生了什么反应?
3.Fe2+与[Fe(CN)6]3-反应生成带有
特征蓝色的铁氰化亚铁沉淀:
3
Fe2+
+2[Fe(CN)6]3-
=Fe3[Fe(CN)6]2
↓
在这个装置中有没有产生?说明什么?
科学探究
用实验验证牺牲阳极的阴极保护法
往Fe电极附近滴入K3[Fe(CN)
6]溶液,溶液不变蓝色。即
溶液中不存在Fe2+,证明Fe未被腐蚀。
电压计指针有偏移,Zn片与Fe片构成
了原电池,产生电流。
阳极:Zn-2e-
=
Zn2+
阴极:2H+
+
2e-
=
H2↑
1、下列各情况,在其中Fe片腐蚀由快到慢的顺序是
(5)
(2)
(1)
(3)
(4)
课堂练习
金属腐蚀的快慢程度:电解池的阳极>原电池的负极>化学腐蚀>原电池的正极>电解池的阴极
金属腐蚀
我国作为世界上钢铁产量最多的国家(
2005
年全国生产钢材37117.02万吨)
,每年被腐蚀的铁占到我国钢铁年产量的十分之一,因为金属腐蚀而造成的损失占到国内生产总值的
2%~4%;约合人民币:3000亿元(2005年我国国内生产总值将达15万亿元)。
根据各国调查结果,一般说来,金属腐蚀所造成的经济损失大致为该国国民生产总值的4%左右。
另据国外统计,金属腐蚀的年损失远远超过水灾、火灾、风灾和地震(平均值)损失的总和,在这里还不包括由于腐蚀导致的停工、减产和爆炸等造成的间接损失。
看后:你有何感想?
金属腐蚀
金属腐蚀的主要害处,不仅在于金属本身的损失,更严重的是金属制品结构损坏所造成的损失比金属本身要大到无法估量。
腐蚀不仅造成经济损失,也经常对安全构成威胁。
国内外都曾发生过许多灾难性腐蚀事故,如飞机因某一零部件破裂而坠毁;桥梁因钢梁产生裂缝而塌陷;油管因穿孔或裂缝而漏油,引起着火爆炸;化工厂中储酸槽穿孔泄漏,造成重大环境污染;管道和设备跑、冒、滴、漏,破坏生产环境,有毒气体如Cl2、H2S、HCN等的泄漏,更会危及工作人员和附近居民的生命安全。
面对这样惊人的数据
和金属腐蚀危害事实,
大家有没有想过,
铁怎么会被腐蚀?
怎样防腐?
看后:你有何感想?
