九上易错题整理4:氢氧化钠变质问题
图片预览

文档简介
中小学教育资源及组卷应用平台
氢氧化钠变质问题
知识梳理
氢氧化钠变质的原理是
。变质后溶液质量
。(填“变大”“不变”或“变小”)
如何检验氢氧化钠已经变质?(必须选用不同类型的试剂)
方法一:滴加
,若观察到
,说明氢氧化钠已经变质,原理是
。(用化学方程式表示,下同)
方法二:滴加
,若观察到
,说明氢氧化钠已经变质,原理是
。
方法三:滴加
,若观察到
,说明氢氧化钠已经变质,原理是
。
如何提纯已经变质的氢氧化钠?
方法:加入适量的
,过滤、蒸发、结晶。原理是
。(用化学方程式表示)
如何判断氢氧化钠是部分变质还是完全变质?
方法:先加入
量的
,静止后取上层清液,再滴加
,若观察到
,则说明是部分变质;若观察到
,则说明是完全变质。
二、练习题
1、某同学发现,上个月做实验用的氢氧化钠溶液忘记了盖瓶塞.对于该溶液的探究,同学们的实验设计合理的是( )21cnjy.com
A.取样,在溶液中加入过量的稀盐酸,如果有气泡产生,则可证明该溶液已变质
B.取样,在溶液中滴加酚酞,如酚酞呈无色,则溶液已完全变质
C.取样,在溶液中加入过量滴有酚酞的氯化钡溶液,如产生白色沉淀,且上层清液呈红色,则溶液已经完全变质
D.取样,在溶液中加入过量稀盐酸,则可除去氢氧化钠溶液中产生的杂质
2、为了证明长期暴露在空气中的氢氧化钠浓溶液已变质,某同学分别取2mL试样于试管中,而后进行如下实验,其中不能达到实验目的是( )
A.通适量CO2气体,观察现象
B.加入澄清石灰水,观察现象
C.加入氯化钡溶液,观察现象
D.加入足量盐酸,观察现象
3、露置在空气中的氢氧化钠因与二氧化碳反应而部分变质,要除去氢氧化钠中混有的杂质,应加入的适量物质是( )
A.HCl溶液
B.KOH溶液
C.Ca(OH)2溶液
D.NaCl溶液
4、为了探究实验室中久置的氢氧化钠固体的变质情况,同学们进行如下图所示的实验.下列分析和结论正确的是( )
A.若Ⅱ、Ⅲ均有明显现象,则说明样品一定完全变质
B.若D为白色固体,则溶液A是Na2CO3溶液.
C.若D为气体,则加入甲溶液的目的是证明样品已变质.
D.若D为白色固体,且溶液C为红色,则样品一定是部分变质.
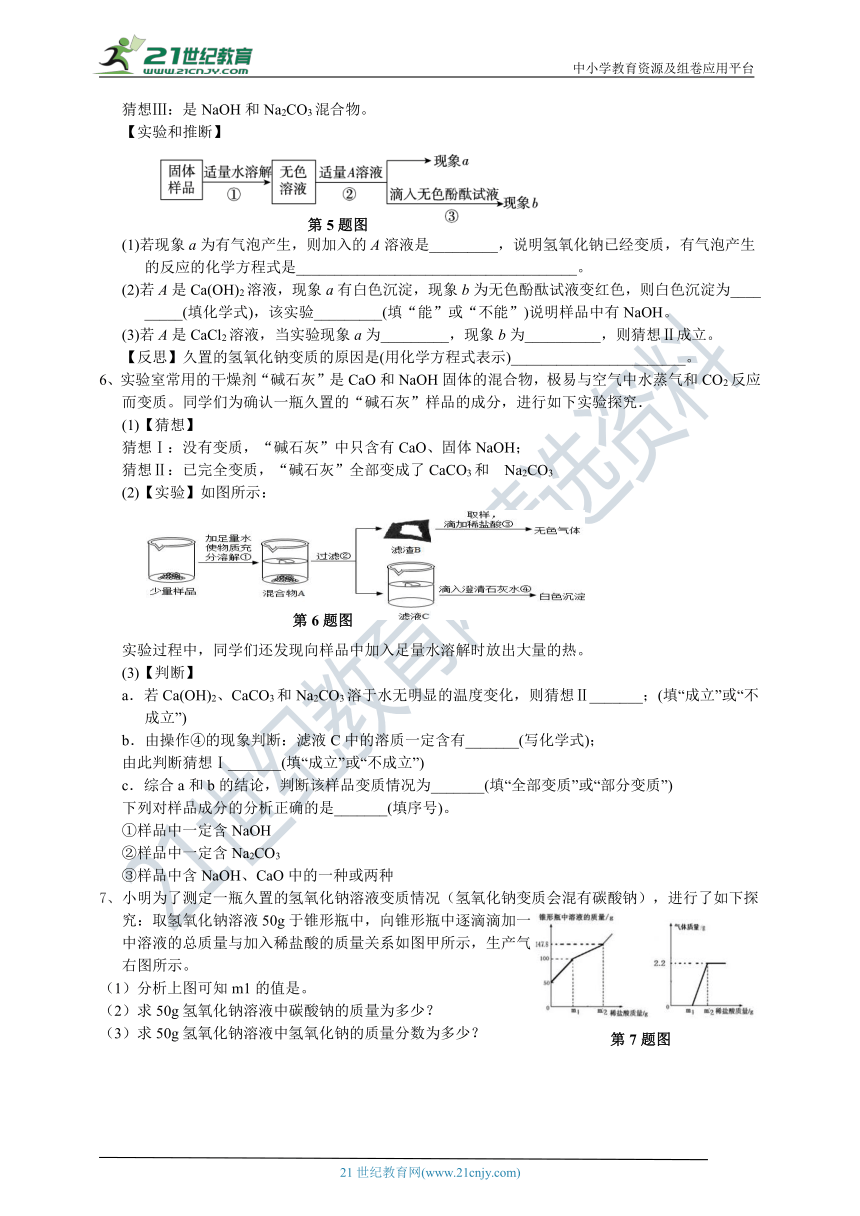
5、兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验如图。请你与他们一起完成以下探究活动:
【查阅资料】Na2CO3溶液的pH>7,与盐酸反应有气泡产生,与Ca(OH)2溶液反应有白色沉淀生成。
【对固体猜想】猜想Ⅰ:全部是NaOH;
猜想Ⅱ:全部是Na2CO3;
猜想Ⅲ:是NaOH和Na2CO3混合物。
【实验和推断】
(1)若现象a为有气泡产生,则加入的A溶液是_________,说明氢氧化钠已经变质,有气泡产生的反应的化学方程式是_____________________________________。
(2)若A是Ca(OH)2溶液,现象a有白色沉淀,现象b为无色酚酞试液变红色,则白色沉淀为_________(填化学式),该实验_________(填“能”或“不能”)说明样品中有NaOH。
(3)若A是CaCl2溶液,当实验现象a为_________,现象b为__________,则猜想Ⅱ成立。
【反思】久置的氢氧化钠变质的原因是(用化学方程式表示)_______________________。
6、实验室常用的干燥剂“碱石灰”是CaO和NaOH固体的混合物,极易与空气中水蒸气和CO2反应而变质。同学们为确认一瓶久置的“碱石灰”样品的成分,进行如下实验探究.
(1)【猜想】
猜想Ⅰ:没有变质,“碱石灰”中只含有CaO、固体NaOH;
猜想Ⅱ:已完全变质,“碱石灰”全部变成了CaCO3和 Na2CO3
(2)【实验】如图所示:
实验过程中,同学们还发现向样品中加入足量水溶解时放出大量的热。
(3)【判断】
a.若Ca(OH)2、CaCO3和Na2CO3溶于水无明显的温度变化,则猜想Ⅱ_______;(填“成立”或“不成立”)
b.由操作④的现象判断:滤液C中的溶质一定含有_______(写化学式);
由此判断猜想Ⅰ_______(填“成立”或“不成立”)
c.综合a和b的结论,判断该样品变质情况为_______(填“全部变质”或“部分变质”)
下列对样品成分的分析正确的是_______(填序号)。
①样品中一定含NaOH
②样品中一定含Na2CO3
③样品中含NaOH、CaO中的一种或两种
7、小明为了测定一瓶久置的氢氧化钠溶液变质情况(氢氧化钠变质会混有碳酸钠),进行了如下探究:取氢氧化钠溶液50g于锥形瓶中,向锥形瓶中逐滴滴加一定浓度的稀盐酸。实验测得锥形瓶中溶液的总质量与加入稀盐酸的质量关系如图甲所示,生产气体质量与加入稀盐酸的质量关系如右图所示。
分析上图可知m1的值是。
求50g氢氧化钠溶液中碳酸钠的质量为多少?
求50g氢氧化钠溶液中氢氧化钠的质量分数为多少?
8、小敏对实验室用石灰石和稀盐酸制取二氧化碳后的废液,进行溶质成分鉴定.取废液上层清液50克,逐滴加入质量分数为26.5%的碳酸钠溶液,出现气泡,滴加至10克后开始出现白色沉淀.继续滴加至沉淀不再产生,过滤,测得沉淀的质量为5克,并绘制了图象.
(1)滴加的溶液中溶质属于____(选填“盐”或“碱”).
(2)10克碳酸钠溶液中含有的溶质质量是______克.
(3)废液中含有的溶质是________(写化学式).
(4)图象中的a点数值是_______.
(5)通过计算说明,图象横坐标中的b点表示的溶液的质量是多少克?
答案
知识梳理
CO2+2NaOH===Na2CO3+H2O
变大
BaCl2/CaCl2/Ba(NO3)2/Ca(NO3)2
白色沉淀
BaCl2+Na2CO3=BaCO3↓+2NaCl(其他也可以)
Ba(OH)2/Ca(OH)2
白色沉淀
Ba(OH)2+Na2CO3=BaCO3↓+2NaOH(其他也可以)
过量的HCl
气泡
2HCl+Na2CO3=2NaCl+H2O+CO2↑(其他也可以)
3、Ba(OH)2/Ca(OH)2
Ba(OH)2+Na2CO3=BaCO3↓+2NaOH(其他也可以)
4、过
BaCl2/CaCl2/Ba(NO3)2/Ca(NO3)2
无色酚酞
溶液变红
溶液不变红
二、练习题
1——4
AACC
5、(1)
HCl,2HCl+Na2CO3===2NaCl+H2O+CO↑。
(2)
CaCO3
不能
(3)
有白色沉淀
不变色
【反思】
CO2+2NaOH===Na2CO3+H2O
。
6、a、不成立;
b、Na2CO3;不成立;
c、部分变质;②③;
7、(1)50g
(2)5.3g
(3)8%
8、(1)盐????
(2)2.65????
(3)1.1???
(4)HCl、CaCl2???
(5)设与氯化钙反应的碳酸钠溶液中溶质质量为x,????
CaCl2+Na2CO3=2NaCl+CaCO3↓????
106????????100????
x?????????5克???
?106∶100=x∶5克????
x=5.3克????
溶液质量是5.3克/26.5%=20克????
b点质量应标20克+10克=30克
第4题图
第5题图
第6题图
第7题图
第8题图
21世纪教育网
www.21cnjy.com
精品试卷·第
2
页
(共
2
页)
HYPERLINK
"http://21世纪教育网(www.21cnjy.com)
"
21世纪教育网(www.21cnjy.com)
氢氧化钠变质问题
知识梳理
氢氧化钠变质的原理是
。变质后溶液质量
。(填“变大”“不变”或“变小”)
如何检验氢氧化钠已经变质?(必须选用不同类型的试剂)
方法一:滴加
,若观察到
,说明氢氧化钠已经变质,原理是
。(用化学方程式表示,下同)
方法二:滴加
,若观察到
,说明氢氧化钠已经变质,原理是
。
方法三:滴加
,若观察到
,说明氢氧化钠已经变质,原理是
。
如何提纯已经变质的氢氧化钠?
方法:加入适量的
,过滤、蒸发、结晶。原理是
。(用化学方程式表示)
如何判断氢氧化钠是部分变质还是完全变质?
方法:先加入
量的
,静止后取上层清液,再滴加
,若观察到
,则说明是部分变质;若观察到
,则说明是完全变质。
二、练习题
1、某同学发现,上个月做实验用的氢氧化钠溶液忘记了盖瓶塞.对于该溶液的探究,同学们的实验设计合理的是( )21cnjy.com
A.取样,在溶液中加入过量的稀盐酸,如果有气泡产生,则可证明该溶液已变质
B.取样,在溶液中滴加酚酞,如酚酞呈无色,则溶液已完全变质
C.取样,在溶液中加入过量滴有酚酞的氯化钡溶液,如产生白色沉淀,且上层清液呈红色,则溶液已经完全变质
D.取样,在溶液中加入过量稀盐酸,则可除去氢氧化钠溶液中产生的杂质
2、为了证明长期暴露在空气中的氢氧化钠浓溶液已变质,某同学分别取2mL试样于试管中,而后进行如下实验,其中不能达到实验目的是( )
A.通适量CO2气体,观察现象
B.加入澄清石灰水,观察现象
C.加入氯化钡溶液,观察现象
D.加入足量盐酸,观察现象
3、露置在空气中的氢氧化钠因与二氧化碳反应而部分变质,要除去氢氧化钠中混有的杂质,应加入的适量物质是( )
A.HCl溶液
B.KOH溶液
C.Ca(OH)2溶液
D.NaCl溶液
4、为了探究实验室中久置的氢氧化钠固体的变质情况,同学们进行如下图所示的实验.下列分析和结论正确的是( )
A.若Ⅱ、Ⅲ均有明显现象,则说明样品一定完全变质
B.若D为白色固体,则溶液A是Na2CO3溶液.
C.若D为气体,则加入甲溶液的目的是证明样品已变质.
D.若D为白色固体,且溶液C为红色,则样品一定是部分变质.
5、兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验如图。请你与他们一起完成以下探究活动:
【查阅资料】Na2CO3溶液的pH>7,与盐酸反应有气泡产生,与Ca(OH)2溶液反应有白色沉淀生成。
【对固体猜想】猜想Ⅰ:全部是NaOH;
猜想Ⅱ:全部是Na2CO3;
猜想Ⅲ:是NaOH和Na2CO3混合物。
【实验和推断】
(1)若现象a为有气泡产生,则加入的A溶液是_________,说明氢氧化钠已经变质,有气泡产生的反应的化学方程式是_____________________________________。
(2)若A是Ca(OH)2溶液,现象a有白色沉淀,现象b为无色酚酞试液变红色,则白色沉淀为_________(填化学式),该实验_________(填“能”或“不能”)说明样品中有NaOH。
(3)若A是CaCl2溶液,当实验现象a为_________,现象b为__________,则猜想Ⅱ成立。
【反思】久置的氢氧化钠变质的原因是(用化学方程式表示)_______________________。
6、实验室常用的干燥剂“碱石灰”是CaO和NaOH固体的混合物,极易与空气中水蒸气和CO2反应而变质。同学们为确认一瓶久置的“碱石灰”样品的成分,进行如下实验探究.
(1)【猜想】
猜想Ⅰ:没有变质,“碱石灰”中只含有CaO、固体NaOH;
猜想Ⅱ:已完全变质,“碱石灰”全部变成了CaCO3和 Na2CO3
(2)【实验】如图所示:
实验过程中,同学们还发现向样品中加入足量水溶解时放出大量的热。
(3)【判断】
a.若Ca(OH)2、CaCO3和Na2CO3溶于水无明显的温度变化,则猜想Ⅱ_______;(填“成立”或“不成立”)
b.由操作④的现象判断:滤液C中的溶质一定含有_______(写化学式);
由此判断猜想Ⅰ_______(填“成立”或“不成立”)
c.综合a和b的结论,判断该样品变质情况为_______(填“全部变质”或“部分变质”)
下列对样品成分的分析正确的是_______(填序号)。
①样品中一定含NaOH
②样品中一定含Na2CO3
③样品中含NaOH、CaO中的一种或两种
7、小明为了测定一瓶久置的氢氧化钠溶液变质情况(氢氧化钠变质会混有碳酸钠),进行了如下探究:取氢氧化钠溶液50g于锥形瓶中,向锥形瓶中逐滴滴加一定浓度的稀盐酸。实验测得锥形瓶中溶液的总质量与加入稀盐酸的质量关系如图甲所示,生产气体质量与加入稀盐酸的质量关系如右图所示。
分析上图可知m1的值是。
求50g氢氧化钠溶液中碳酸钠的质量为多少?
求50g氢氧化钠溶液中氢氧化钠的质量分数为多少?
8、小敏对实验室用石灰石和稀盐酸制取二氧化碳后的废液,进行溶质成分鉴定.取废液上层清液50克,逐滴加入质量分数为26.5%的碳酸钠溶液,出现气泡,滴加至10克后开始出现白色沉淀.继续滴加至沉淀不再产生,过滤,测得沉淀的质量为5克,并绘制了图象.
(1)滴加的溶液中溶质属于____(选填“盐”或“碱”).
(2)10克碳酸钠溶液中含有的溶质质量是______克.
(3)废液中含有的溶质是________(写化学式).
(4)图象中的a点数值是_______.
(5)通过计算说明,图象横坐标中的b点表示的溶液的质量是多少克?
答案
知识梳理
CO2+2NaOH===Na2CO3+H2O
变大
BaCl2/CaCl2/Ba(NO3)2/Ca(NO3)2
白色沉淀
BaCl2+Na2CO3=BaCO3↓+2NaCl(其他也可以)
Ba(OH)2/Ca(OH)2
白色沉淀
Ba(OH)2+Na2CO3=BaCO3↓+2NaOH(其他也可以)
过量的HCl
气泡
2HCl+Na2CO3=2NaCl+H2O+CO2↑(其他也可以)
3、Ba(OH)2/Ca(OH)2
Ba(OH)2+Na2CO3=BaCO3↓+2NaOH(其他也可以)
4、过
BaCl2/CaCl2/Ba(NO3)2/Ca(NO3)2
无色酚酞
溶液变红
溶液不变红
二、练习题
1——4
AACC
5、(1)
HCl,2HCl+Na2CO3===2NaCl+H2O+CO↑。
(2)
CaCO3
不能
(3)
有白色沉淀
不变色
【反思】
CO2+2NaOH===Na2CO3+H2O
。
6、a、不成立;
b、Na2CO3;不成立;
c、部分变质;②③;
7、(1)50g
(2)5.3g
(3)8%
8、(1)盐????
(2)2.65????
(3)1.1???
(4)HCl、CaCl2???
(5)设与氯化钙反应的碳酸钠溶液中溶质质量为x,????
CaCl2+Na2CO3=2NaCl+CaCO3↓????
106????????100????
x?????????5克???
?106∶100=x∶5克????
x=5.3克????
溶液质量是5.3克/26.5%=20克????
b点质量应标20克+10克=30克
第4题图
第5题图
第6题图
第7题图
第8题图
21世纪教育网
www.21cnjy.com
精品试卷·第
2
页
(共
2
页)
HYPERLINK
"http://21世纪教育网(www.21cnjy.com)
"
21世纪教育网(www.21cnjy.com)
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
