人教版高二化学选修5第3章第1节 醇 酚(共50张PPT)
文档属性
| 名称 | 人教版高二化学选修5第3章第1节 醇 酚(共50张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 6.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-08-01 00:00:00 | ||
图片预览






文档简介
(共50张PPT)
第三章
烃的含氧衍生物
第一节
醇
酚
第1课时
酚
借
问
酒
家
何
处
有
?
牧
童
遥
指
杏
花
村。
明
月
几
时
有
?
把
酒
问
青
天
!
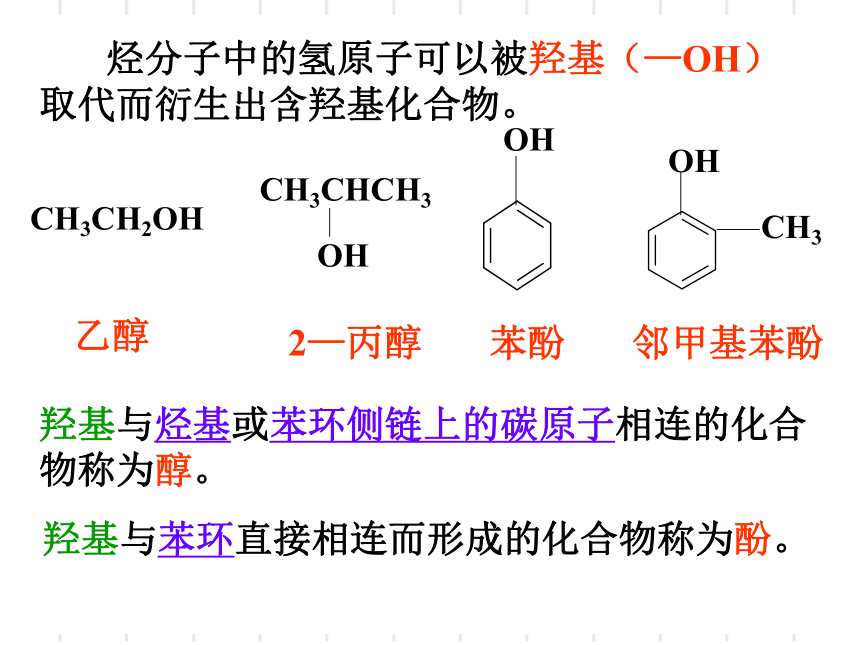
烃分子中的氢原子可以被羟基(—OH)取代而衍生出含羟基化合物。
羟基与烃基或苯环侧链上的碳原子相连的化合物称为醇。
CH3CH2OH
乙醇
2—丙醇
苯酚
邻甲基苯酚
羟基与苯环直接相连而形成的化合物称为酚。
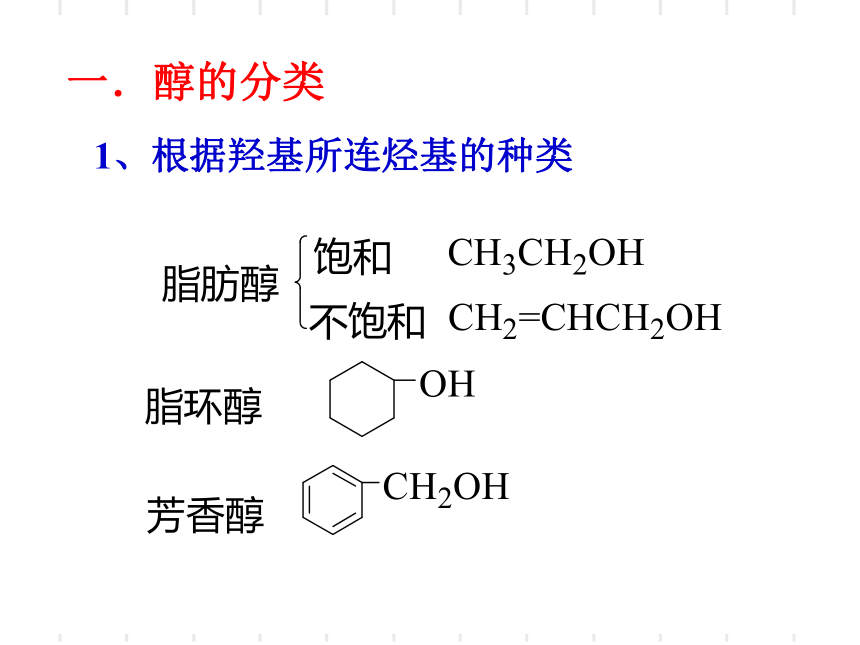
一.醇的分类
1、根据羟基所连烃基的种类
2、根据醇分子结构中羟基的数目,醇可分为一元醇、二元醇、三元醇……
CnH2n+1OH
或
CnH2n+2O
饱和一元醇通式:
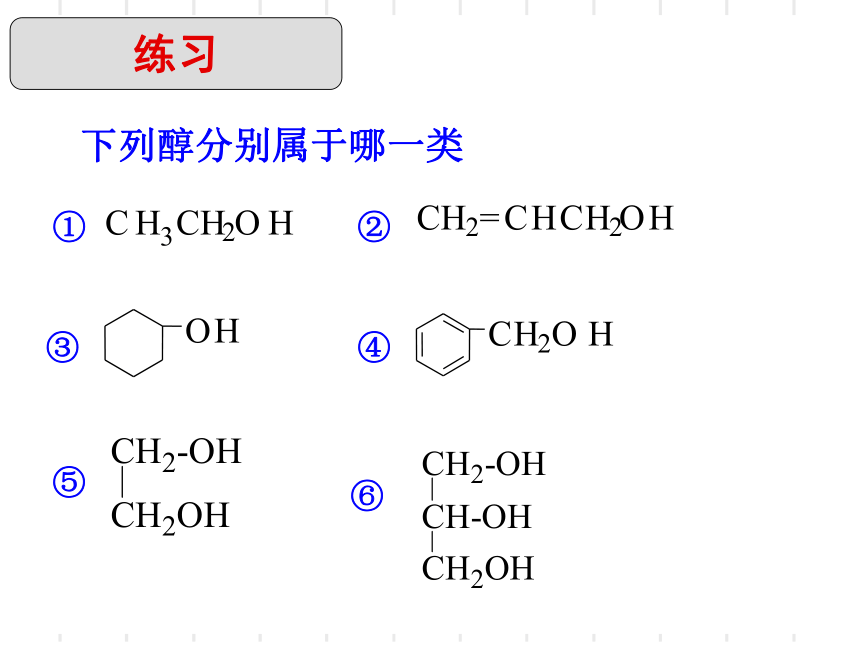
下列醇分别属于哪一类
练习
①
②
③
④
⑤
⑥
(2)编号
(1)选主链
(3)写名称
选含—OH的最长碳链为主链
从离—OH最近的一端起编号
取代基位置—
取代基名称
—
羟基位置—
某醇(羟基位置用阿拉伯数字表示;羟基的个数用“二”、“三”等表示。)
醇的命名
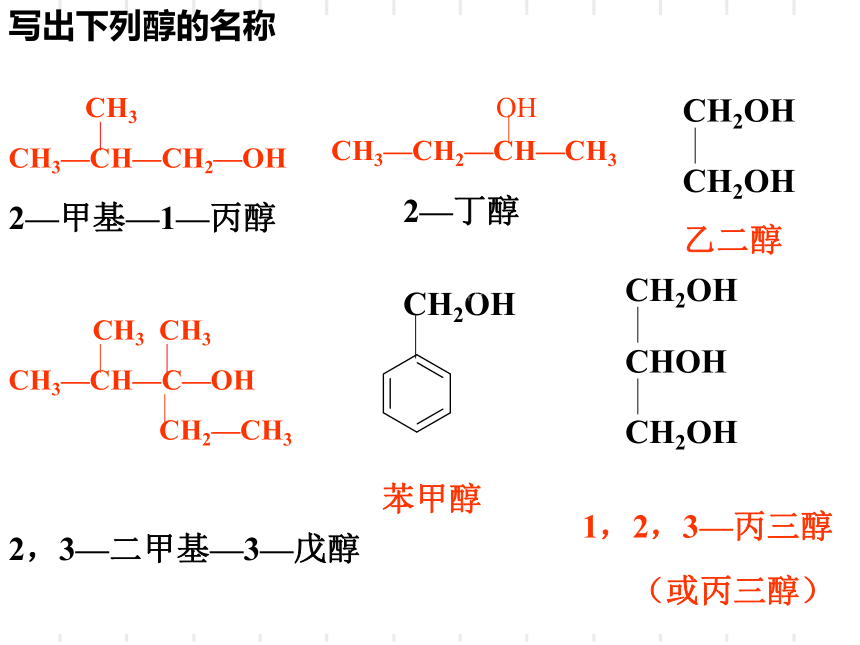
写出下列醇的名称
2—甲基—1—丙醇
2—丁醇
2,3—二甲基—3—戊醇
乙二醇
苯甲醇
1,2,3—丙三醇
(或丙三醇)
zxxkw
学.科.网
蒸馏
蒸馏
Mg粉
CaO
⑴甲醇
(3)乙二醇
(4)丙三醇
无色液体,有酒味,有毒,人饮用10ml就能使眼睛失明,再多则能致死。可作车用燃料,是新的可再生能源。
无色、黏稠有甜味的液体,易溶于水和乙醇。
俗称甘油,是无色、黏稠有甜味的液体,吸湿性强,具有护肤作用。能跟水、酒精以任意比混溶。
无色透明液体,具有特殊香味的液体,密度为0.789g/cm3,沸点78.5℃,易挥发,能与水以任意比互溶,能够溶解多种无机物和有机物,是一种良好的有机溶剂.
⑵乙醇
工业酒精(96%)
无水酒精(99.5%)
绝对酒精(100%)
酒精中是否含水的验证:用无水硫酸铜是否变蓝。
二、常见醇
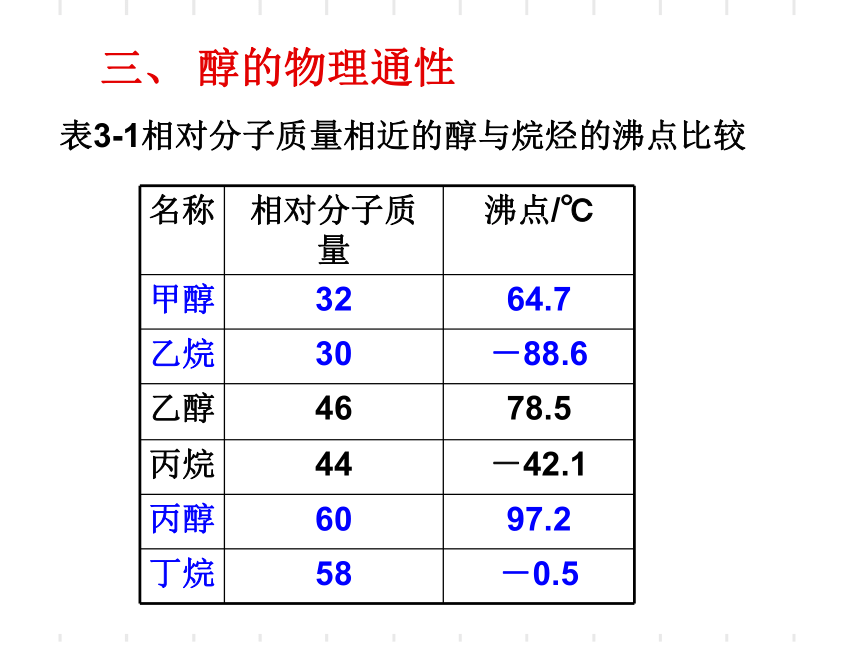
表3-1相对分子质量相近的醇与烷烃的沸点比较
三、
醇的物理通性
名称
相对分子质量
沸点/℃
甲醇
32
64.7
乙烷
30
-88.6
乙醇
46
78.5
丙烷
44
-42.1
丙醇
60
97.2
丁烷
58
-0.5
思考与交流
结论:
原因:
甲醇、乙醇、丙醇均可与水以任意比例混溶,这是因为甲醇、乙醇、丙醇与水形成了氢键。
相对分子质量相近的醇和烷烃相比,醇的沸点远远高于烷烃。
由于醇分子中羟基的氧原子与另一醇分子羟基的氢原子间存在着相互吸引作用,这种吸引作用叫氢键。
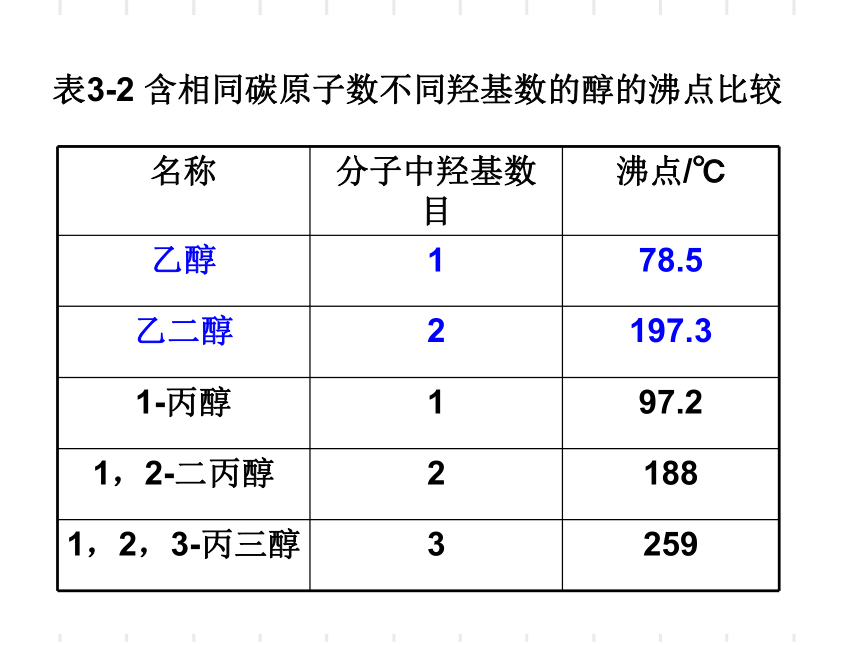
表3-2
含相同碳原子数不同羟基数的醇的沸点比较
名称
分子中羟基数目
沸点/℃
乙醇
1
78.5
乙二醇
2
197.3
1-丙醇
1
97.2
1,2-二丙醇
2
188
1,2,3-丙三醇
3
259
学与问
由于羟基数目增多,使得分子间形成的氢键增多增强。
结论:
原因:
乙二醇的沸点高于乙醇,1,2,3—丙三醇的沸点高于1,2—丙二醇,
1,2—丙二醇的沸点高于1—丙醇
沸点随分子内羟基数目的增多而增大
1)无色、透明、有特殊香味的液体;
2)沸点78.5℃;
3)易挥发;
4)密度比水小;
5)与水任意比互溶;
6)能溶解多种无机物和有机物。
乙醇的物理性质总结
●O
:
H
:
:
乙醇的结构
乙醇球棍模型
乙醇比例模型
1、与钠反应:置换反应
乙醇钠
呈强碱性
现象:
乙醇分子中羟基上的氢不如水分子中的氢活泼。
结论:
原因:
羟基受乙基的影响
四、醇类化学性质:以乙醇为例
回忆钠与水的反应
思考与交流
处理反应釜中金属钠的最安全、合理的方法是第(3)种方案,向反应釜中慢慢加入乙醇,由于乙醇与金属钠的反应比水与钠的反应缓和,热效应小,因此是比较安全,可行的处理方法。
请写出2-丙醇、乙二醇、丙三醇分别与钠反应的化学方程式
练习
2、消去反应
分子内脱水
学与问
CH3CH2OH
CH3CH2Br
反应条件
化学键的断裂
化学键的生成
反应产物
NaOH、乙醇溶液、加热
C—Br、C—H
C—O、C—H
C==C
C==C
CH2==CH2、HBr
CH2==CH2、H2O
浓硫酸、加热到170℃
学与问
卤代烃与醇都能发生消去反应,它们有什么异同点?
相同:
分子结构中都必须邻碳有氢。
不同点:
官能团不同、反应条件不同、断键不同、产物不同
3、取代反应
乙醚
写出乙醇与2-丙醇分子间脱水的化学方程式
(1)
分子间脱水(生成醚)
3、取代反应
乙酸乙酯
写出乙酸分别与2-丙醇、乙二醇、丙三醇酯化的化学方程式
(2)酯化反应
溴乙烷
写出浓氢溴酸分别与2-丙醇、乙二醇、丙三醇取代的化学方程式
(3)与浓HX反应(卤代)
3、取代反应
4、氧化反应
催化剂为铜或银
①燃烧
②催化氧化
乙醛
写出1-丙醇、2-丙醇、乙二醇与氧气催化氧化的方程式
规律
连-OH的C上有两个H则被催化氧化成醛
连-OH的C上只有一个H则被催化氧化成酮
连-OH的C上没有H则不能被催化氧化
练习
焊接银器、铜器时,表面会生成发黑的氧化膜
银匠说,可以先把铜、银在火上烧热,马上蘸一下酒精,铜银会光亮如初!这是何原理?
乙
醇
乙
醛
4.氧化反应
课本P51
学与问
2
③能被酸性KMnO4或酸性重铬酸钾(K2Cr2O7)溶液氧化
去氢或者加氧就是氧化
课本P52
资料卡片
加氢或者去氧就是还原
CH3CH2OH
CH3CHO
CH3COOH
氧化
氧化
乙醇
乙醛
乙酸
身边的化学Ⅰ
酒精的快速检测:让驾车人呼出的气体接触载有经过硫酸酸化处理的氧化剂重铬酸钾的硅胶,可测出呼出的气体中是否含有乙醇及乙醇含量的高低。
驾驶员正在接受酒精检查
小结
②
④
②
①
③
①
、②
①
①
反应
断键位置
与金属钠反应
Cu或Ag催化氧化
浓硫酸加热到170℃
浓硫酸加热到140℃
浓硫酸条件下与乙酸加热
与HX加热反应
1、下列物质属于醇类且能发生
消去反应的是(
)
A.CH3OH
B.C6H5—CH2OH
C.CH3CHOHCH3
D.HO—C6H4—CH3
C
课堂练习
2.下列各醇,能发生催化氧化的是(
)
CH3—C—CH2OH
CH3
CH3
CH3
∣
B.
CH3—C—OH
∣
CH3
C.CH3—CH—CH3
∣
OH
CH3
∣
D.C6H5—C—CH3
∣
OH
A.
AC
A.
作业布置
课本P55
第2题
Thank
you!
第三章
烃的含氧衍生物
第一节
醇
酚
第2课时
酚
或
C6H5O
H
一、苯酚的分子结构
C6H6O
比例模型
球棍模型
苯酚分子中除-OH上的H原子以外的所有原子都在同一平面上,且-OH上的H也可能出现在该平面
颜色:
无色
状态:
晶体
气味:
特殊气味
熔点:
43.6℃
沸点:
181.7℃
溶解性:
水中
二、苯酚的物理性质
易被氧气氧化而呈粉红色
常温溶解度为9.3g
65
℃以上混溶
有机溶剂中
易溶于乙醇等有机溶剂
特性:
有毒、有腐蚀性、易燃、易爆
1、苯酚的弱酸性
澄清
浑浊
三、苯酚的化学性质
结论:
苯环对侧链(羟基)的影响导致酚羟基中的氧氢键易断,显酸性
石炭酸
苯氧离子
苯酚酸性强弱的探究
结论:
苯酚酸性极弱,不使指示剂变色
酸性:H2CO3
>
C6H5OH
>
HCO3—
酸性极弱
变浑浊
变浑浊
不变色
颜色变浅
现象
原因或方程式
与盐酸反应
与CO2反应
与指示剂作用
Na2CO3反应
2.苯酚与溴水的反应
实验3-4
(白色)
观察现象并思考实验中应注意问题
此反应很灵敏,常用于苯酚的定性检验和定量测定。
(取代反应)
实验中苯酚不能过量,否则产生的三溴苯酚易溶于苯酚而观察不到白色沉淀。
注意:
结论:
侧链(羟基)对苯环的影响导致苯环上与羟基邻、对位的氢原子活泼,易被取代
一次取代苯环上三个氢原子
一次取代苯环
上一个氢原子
溴水与苯酚
不用催化剂
使用催化剂
液溴与苯
试比较苯、苯酚与溴反应的异同:
苯酚与溴取代反应比苯容易
受羟基的影响,苯酚中苯环上的H变得更活泼了
苯酚
苯
对溴的要求
反应条件
取代苯环上氢原子数
结论
解释
3.苯酚的显色反应
苯酚溶液
常用该反应来检验苯酚的存在;也可利用苯酚的这一性质检验FeCl3。
紫色
FeCl3
紫色
实验与观察现象
4、氧化反应
具有强还原性
苯酚易被空气中的氧气氧化而呈粉红色
思考:苯酚能否使高锰酸钾酸性溶液褪色?
对-苯醌
苯酚溶液
高锰酸钾酸性溶液
褪色
结论:
苯酚能使高锰酸钾酸性溶液褪色
5、加成反应
学与问
苯酚分子中苯环上连有一羟基,由于羟基对苯环的影响,使得苯酚分子中苯环上的氢原子比苯分子中的氢原子更活泼,因此苯酚比苯更易发生取代反应。
乙醇分子中—OH与乙基相连,—OH上H原子比水分子中H原子还难电离,因此乙醇不显酸性。而苯酚分子中的—OH与苯环相连,受苯环影响,—OH上H原子易电离,使苯酚显示一定酸性。
由此可见:不同的烃基与羟基相连,可以影响物质的化学性质。
(四)苯酚的用途
苯酚的用途
酚醛树脂
合成纤维
合成香料
医药
消毒剂
染料
农药
防腐剂
化学性质:
1.
酸性
酚羟基的性质
与Na,
NaOH
,
Na2
CO3反应,但不放出CO2,也不能使紫色石蕊变色。
4.加成反应
物理性质:
这节课我们学到了
酚的定义:
2.取代反应
3
.显色反应
酚中苯环的性质
酚的特性
常用于检验苯酚存在
酚中苯环的性质
羟基与苯环直接相连接的化合物是酚
有毒,如果不慎沾到皮肤上,
应立即用酒精洗涤。
5.氧化反应
1、怎样分离苯酚和苯的混合物
加入NaOH溶液→分液→在苯酚钠溶液中加酸或通入CO2
2、如何鉴别苯酚
B
利用与浓溴水生成三溴苯酚白色沉淀
A
利用与三价铁离子的显色反应
巩固练习
课堂练习
1.只用一试种剂把下列四种无色溶液鉴别开:苯酚、乙醇、NaOH、KSCN,现象分别怎样?
FeCl3溶液
紫色溶液
无现象
红褐色沉淀
血红色
物质
苯酚
乙醇
NaOH
KSCN
现象
2、下列物质久置于空气中,
颜色会发生变化的是(
)
A、Na2SO3
B、苯酚
C、Na2O2
D、CaO
B、C
第三章
烃的含氧衍生物
第一节
醇
酚
第1课时
酚
借
问
酒
家
何
处
有
?
牧
童
遥
指
杏
花
村。
明
月
几
时
有
?
把
酒
问
青
天
!
烃分子中的氢原子可以被羟基(—OH)取代而衍生出含羟基化合物。
羟基与烃基或苯环侧链上的碳原子相连的化合物称为醇。
CH3CH2OH
乙醇
2—丙醇
苯酚
邻甲基苯酚
羟基与苯环直接相连而形成的化合物称为酚。
一.醇的分类
1、根据羟基所连烃基的种类
2、根据醇分子结构中羟基的数目,醇可分为一元醇、二元醇、三元醇……
CnH2n+1OH
或
CnH2n+2O
饱和一元醇通式:
下列醇分别属于哪一类
练习
①
②
③
④
⑤
⑥
(2)编号
(1)选主链
(3)写名称
选含—OH的最长碳链为主链
从离—OH最近的一端起编号
取代基位置—
取代基名称
—
羟基位置—
某醇(羟基位置用阿拉伯数字表示;羟基的个数用“二”、“三”等表示。)
醇的命名
写出下列醇的名称
2—甲基—1—丙醇
2—丁醇
2,3—二甲基—3—戊醇
乙二醇
苯甲醇
1,2,3—丙三醇
(或丙三醇)
zxxkw
学.科.网
蒸馏
蒸馏
Mg粉
CaO
⑴甲醇
(3)乙二醇
(4)丙三醇
无色液体,有酒味,有毒,人饮用10ml就能使眼睛失明,再多则能致死。可作车用燃料,是新的可再生能源。
无色、黏稠有甜味的液体,易溶于水和乙醇。
俗称甘油,是无色、黏稠有甜味的液体,吸湿性强,具有护肤作用。能跟水、酒精以任意比混溶。
无色透明液体,具有特殊香味的液体,密度为0.789g/cm3,沸点78.5℃,易挥发,能与水以任意比互溶,能够溶解多种无机物和有机物,是一种良好的有机溶剂.
⑵乙醇
工业酒精(96%)
无水酒精(99.5%)
绝对酒精(100%)
酒精中是否含水的验证:用无水硫酸铜是否变蓝。
二、常见醇
表3-1相对分子质量相近的醇与烷烃的沸点比较
三、
醇的物理通性
名称
相对分子质量
沸点/℃
甲醇
32
64.7
乙烷
30
-88.6
乙醇
46
78.5
丙烷
44
-42.1
丙醇
60
97.2
丁烷
58
-0.5
思考与交流
结论:
原因:
甲醇、乙醇、丙醇均可与水以任意比例混溶,这是因为甲醇、乙醇、丙醇与水形成了氢键。
相对分子质量相近的醇和烷烃相比,醇的沸点远远高于烷烃。
由于醇分子中羟基的氧原子与另一醇分子羟基的氢原子间存在着相互吸引作用,这种吸引作用叫氢键。
表3-2
含相同碳原子数不同羟基数的醇的沸点比较
名称
分子中羟基数目
沸点/℃
乙醇
1
78.5
乙二醇
2
197.3
1-丙醇
1
97.2
1,2-二丙醇
2
188
1,2,3-丙三醇
3
259
学与问
由于羟基数目增多,使得分子间形成的氢键增多增强。
结论:
原因:
乙二醇的沸点高于乙醇,1,2,3—丙三醇的沸点高于1,2—丙二醇,
1,2—丙二醇的沸点高于1—丙醇
沸点随分子内羟基数目的增多而增大
1)无色、透明、有特殊香味的液体;
2)沸点78.5℃;
3)易挥发;
4)密度比水小;
5)与水任意比互溶;
6)能溶解多种无机物和有机物。
乙醇的物理性质总结
●O
:
H
:
:
乙醇的结构
乙醇球棍模型
乙醇比例模型
1、与钠反应:置换反应
乙醇钠
呈强碱性
现象:
乙醇分子中羟基上的氢不如水分子中的氢活泼。
结论:
原因:
羟基受乙基的影响
四、醇类化学性质:以乙醇为例
回忆钠与水的反应
思考与交流
处理反应釜中金属钠的最安全、合理的方法是第(3)种方案,向反应釜中慢慢加入乙醇,由于乙醇与金属钠的反应比水与钠的反应缓和,热效应小,因此是比较安全,可行的处理方法。
请写出2-丙醇、乙二醇、丙三醇分别与钠反应的化学方程式
练习
2、消去反应
分子内脱水
学与问
CH3CH2OH
CH3CH2Br
反应条件
化学键的断裂
化学键的生成
反应产物
NaOH、乙醇溶液、加热
C—Br、C—H
C—O、C—H
C==C
C==C
CH2==CH2、HBr
CH2==CH2、H2O
浓硫酸、加热到170℃
学与问
卤代烃与醇都能发生消去反应,它们有什么异同点?
相同:
分子结构中都必须邻碳有氢。
不同点:
官能团不同、反应条件不同、断键不同、产物不同
3、取代反应
乙醚
写出乙醇与2-丙醇分子间脱水的化学方程式
(1)
分子间脱水(生成醚)
3、取代反应
乙酸乙酯
写出乙酸分别与2-丙醇、乙二醇、丙三醇酯化的化学方程式
(2)酯化反应
溴乙烷
写出浓氢溴酸分别与2-丙醇、乙二醇、丙三醇取代的化学方程式
(3)与浓HX反应(卤代)
3、取代反应
4、氧化反应
催化剂为铜或银
①燃烧
②催化氧化
乙醛
写出1-丙醇、2-丙醇、乙二醇与氧气催化氧化的方程式
规律
连-OH的C上有两个H则被催化氧化成醛
连-OH的C上只有一个H则被催化氧化成酮
连-OH的C上没有H则不能被催化氧化
练习
焊接银器、铜器时,表面会生成发黑的氧化膜
银匠说,可以先把铜、银在火上烧热,马上蘸一下酒精,铜银会光亮如初!这是何原理?
乙
醇
乙
醛
4.氧化反应
课本P51
学与问
2
③能被酸性KMnO4或酸性重铬酸钾(K2Cr2O7)溶液氧化
去氢或者加氧就是氧化
课本P52
资料卡片
加氢或者去氧就是还原
CH3CH2OH
CH3CHO
CH3COOH
氧化
氧化
乙醇
乙醛
乙酸
身边的化学Ⅰ
酒精的快速检测:让驾车人呼出的气体接触载有经过硫酸酸化处理的氧化剂重铬酸钾的硅胶,可测出呼出的气体中是否含有乙醇及乙醇含量的高低。
驾驶员正在接受酒精检查
小结
②
④
②
①
③
①
、②
①
①
反应
断键位置
与金属钠反应
Cu或Ag催化氧化
浓硫酸加热到170℃
浓硫酸加热到140℃
浓硫酸条件下与乙酸加热
与HX加热反应
1、下列物质属于醇类且能发生
消去反应的是(
)
A.CH3OH
B.C6H5—CH2OH
C.CH3CHOHCH3
D.HO—C6H4—CH3
C
课堂练习
2.下列各醇,能发生催化氧化的是(
)
CH3—C—CH2OH
CH3
CH3
CH3
∣
B.
CH3—C—OH
∣
CH3
C.CH3—CH—CH3
∣
OH
CH3
∣
D.C6H5—C—CH3
∣
OH
A.
AC
A.
作业布置
课本P55
第2题
Thank
you!
第三章
烃的含氧衍生物
第一节
醇
酚
第2课时
酚
或
C6H5O
H
一、苯酚的分子结构
C6H6O
比例模型
球棍模型
苯酚分子中除-OH上的H原子以外的所有原子都在同一平面上,且-OH上的H也可能出现在该平面
颜色:
无色
状态:
晶体
气味:
特殊气味
熔点:
43.6℃
沸点:
181.7℃
溶解性:
水中
二、苯酚的物理性质
易被氧气氧化而呈粉红色
常温溶解度为9.3g
65
℃以上混溶
有机溶剂中
易溶于乙醇等有机溶剂
特性:
有毒、有腐蚀性、易燃、易爆
1、苯酚的弱酸性
澄清
浑浊
三、苯酚的化学性质
结论:
苯环对侧链(羟基)的影响导致酚羟基中的氧氢键易断,显酸性
石炭酸
苯氧离子
苯酚酸性强弱的探究
结论:
苯酚酸性极弱,不使指示剂变色
酸性:H2CO3
>
C6H5OH
>
HCO3—
酸性极弱
变浑浊
变浑浊
不变色
颜色变浅
现象
原因或方程式
与盐酸反应
与CO2反应
与指示剂作用
Na2CO3反应
2.苯酚与溴水的反应
实验3-4
(白色)
观察现象并思考实验中应注意问题
此反应很灵敏,常用于苯酚的定性检验和定量测定。
(取代反应)
实验中苯酚不能过量,否则产生的三溴苯酚易溶于苯酚而观察不到白色沉淀。
注意:
结论:
侧链(羟基)对苯环的影响导致苯环上与羟基邻、对位的氢原子活泼,易被取代
一次取代苯环上三个氢原子
一次取代苯环
上一个氢原子
溴水与苯酚
不用催化剂
使用催化剂
液溴与苯
试比较苯、苯酚与溴反应的异同:
苯酚与溴取代反应比苯容易
受羟基的影响,苯酚中苯环上的H变得更活泼了
苯酚
苯
对溴的要求
反应条件
取代苯环上氢原子数
结论
解释
3.苯酚的显色反应
苯酚溶液
常用该反应来检验苯酚的存在;也可利用苯酚的这一性质检验FeCl3。
紫色
FeCl3
紫色
实验与观察现象
4、氧化反应
具有强还原性
苯酚易被空气中的氧气氧化而呈粉红色
思考:苯酚能否使高锰酸钾酸性溶液褪色?
对-苯醌
苯酚溶液
高锰酸钾酸性溶液
褪色
结论:
苯酚能使高锰酸钾酸性溶液褪色
5、加成反应
学与问
苯酚分子中苯环上连有一羟基,由于羟基对苯环的影响,使得苯酚分子中苯环上的氢原子比苯分子中的氢原子更活泼,因此苯酚比苯更易发生取代反应。
乙醇分子中—OH与乙基相连,—OH上H原子比水分子中H原子还难电离,因此乙醇不显酸性。而苯酚分子中的—OH与苯环相连,受苯环影响,—OH上H原子易电离,使苯酚显示一定酸性。
由此可见:不同的烃基与羟基相连,可以影响物质的化学性质。
(四)苯酚的用途
苯酚的用途
酚醛树脂
合成纤维
合成香料
医药
消毒剂
染料
农药
防腐剂
化学性质:
1.
酸性
酚羟基的性质
与Na,
NaOH
,
Na2
CO3反应,但不放出CO2,也不能使紫色石蕊变色。
4.加成反应
物理性质:
这节课我们学到了
酚的定义:
2.取代反应
3
.显色反应
酚中苯环的性质
酚的特性
常用于检验苯酚存在
酚中苯环的性质
羟基与苯环直接相连接的化合物是酚
有毒,如果不慎沾到皮肤上,
应立即用酒精洗涤。
5.氧化反应
1、怎样分离苯酚和苯的混合物
加入NaOH溶液→分液→在苯酚钠溶液中加酸或通入CO2
2、如何鉴别苯酚
B
利用与浓溴水生成三溴苯酚白色沉淀
A
利用与三价铁离子的显色反应
巩固练习
课堂练习
1.只用一试种剂把下列四种无色溶液鉴别开:苯酚、乙醇、NaOH、KSCN,现象分别怎样?
FeCl3溶液
紫色溶液
无现象
红褐色沉淀
血红色
物质
苯酚
乙醇
NaOH
KSCN
现象
2、下列物质久置于空气中,
颜色会发生变化的是(
)
A、Na2SO3
B、苯酚
C、Na2O2
D、CaO
B、C
