苏教版高一化学必修1专题2第一单元 氯、溴、碘及其化合物(共23张PPT)
文档属性
| 名称 | 苏教版高一化学必修1专题2第一单元 氯、溴、碘及其化合物(共23张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-08-02 00:00:00 | ||
图片预览






文档简介
(共23张PPT)
氧化还原反应
思考:(1)上述反应中哪些是氧化还原反应?氧化还原反应的特征是什么?
属于氧化还原反应的有:①②③⑤
特征:有元素化合价的变化。
(2)氧化还原反应与四种基本反应类型之间有什么关系?
氧化还原反应
非氧化还原反应
小试牛刀
【针对训练1】(2008年江苏学业水平测试)下列反应属于氧化还原反应的是(
)
A.H2SO4+2NaOH
=
Na2SO4+2H2O
B.2NaHCO3
Na2CO3
+
CO2↑
+
H2O
C.NH3
+
HCl
=
NH4Cl
D.CuO
+
H2
Cu
+
H2O
D
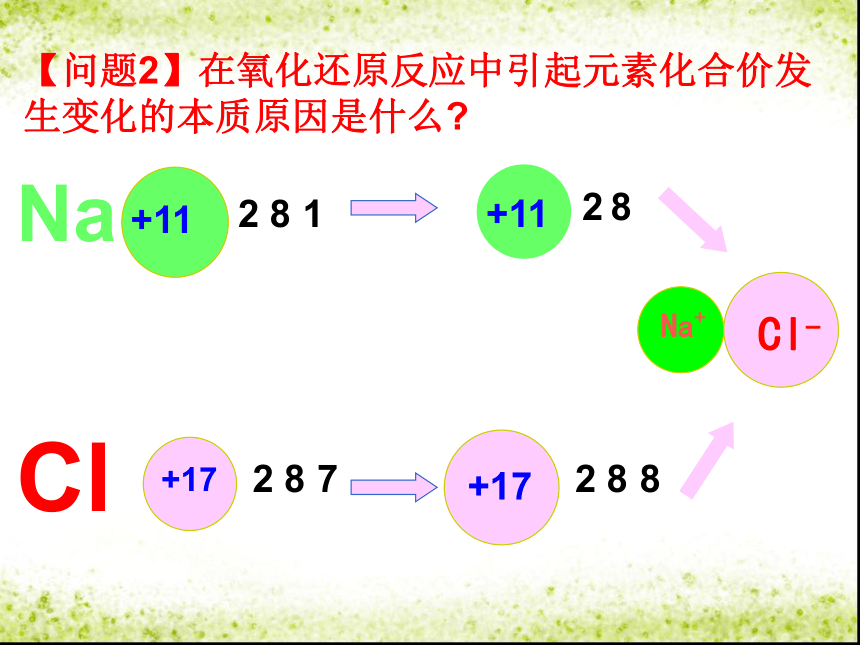
【问题2】在氧化还原反应中引起元素化合价发生变化的本质原因是什么?
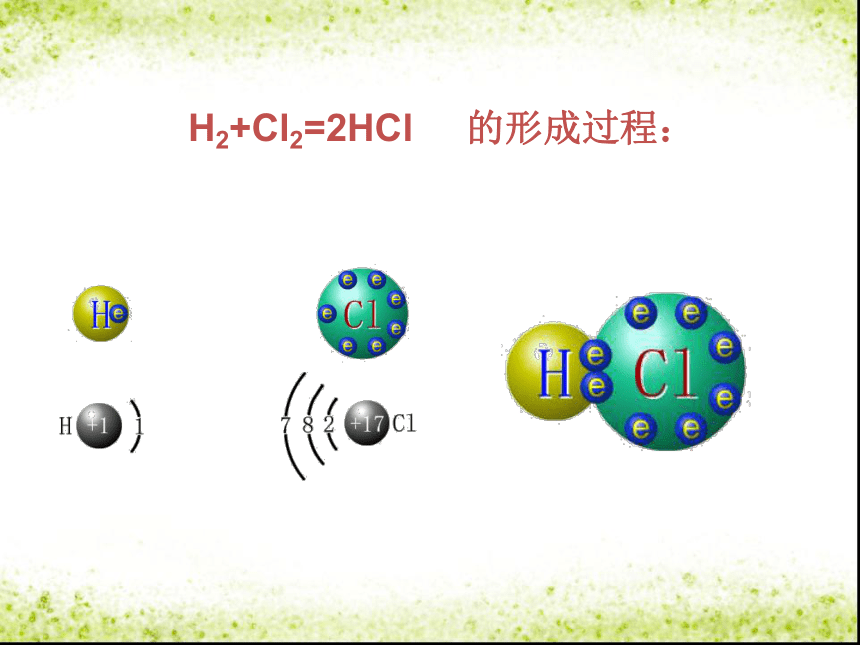
H2+Cl2=2HCl
的形成过程:
电子的转移,包括得失或偏移,
综上所述,可以给氧化还原反应下一个更为本质的定义:凡是有电子转移(得失或偏移)的反应都是氧化还原反应。
化合价升降的原因:
【针对训练2】写出下列变化中化合价发生变化的每个原子得到(或失去)电子数
①
Fe2O3
→
Fe
②C→CO2
③
SO2→S
④NH3→NO
小试牛刀
得到3e-
失去4e-
得到4e-
失去5e-
一、氧化还原反应
概念:
特征:
本质:
凡有电子转移(得失或偏移)的化学反应
电子转移
化合价发生了变化
(
判断依据)
【问题3】判断下列各反应中的氧化剂、还原剂,分别是什么?
思考:氧化还原反应包括氧化反应与还原反应两个部分,氧化剂与还原剂在反应中表现什么样的性质?
分别发生了什么反应?
与电子得失、化合价升降的关系?
(1)2Fe
+
3Cl2=2FeCl3
(2)3NO2
+
H2O
=
2HNO3+NO
(3)SO2
+
2
H2S
=3
S↓+2
H2O
还原剂
氧化剂
既是氧化剂又是还原剂
氧化剂
还原剂
氧化剂:
得到电子的物质
失去电子的物质
还原剂:
二、氧化剂和还原剂
口诀:升失氧化还原剂,降得还原氧化剂
【问题4】你能用双线桥法表示出下列氧化还原反应中电子转移的方向与数目吗?
2Na+Cl2
=
2NaCl
MnO2
+
4HCl(浓)
MnCl2
+
Cl2
↑
+
2H2O
双线桥法
+4
+2
-1
0
得2e-
失2e-
步骤:①标价态
MnO2
+
4HCl(浓)
=
MnCl2
+
Cl2
+
2H2O
三、氧化还原反应电子转移的表示方法
②连双线
③注得失
【问题5】配平下面的离子反应方程式。
四、氧化还原反应的基本规律--电子守恒规律
Fe2+
+
Cl2
=
Fe3+
+
Cl-
+2
0
+3
-1
2
2
2
失1e-
得2
×1e-
×2
五、生产生活中常见的氧化还原反应
【问题6】你知道日常生活中有哪些常见的氧化还原反应吗?
感受氧化还原反应的存在
刚削好的苹果
放置30分钟以后的苹果
刚泡好的绿茶
放置2小时后的绿茶
感受氧化还原反应的存在
感受氧化还原反应的存在
感受氧化还原反应的存在
好吃的月饼
感受氧化还原反应的存在
1.下列化学反应中,H2SO4作为氧化剂的是(
)
A.2NaOH+H2SO4=Na2SO4+2H2O
B.C+2H2SO4(浓)CO2↑+2SO2↑+2H2O
C.BaCl2+H2SO4=BaSO4↓+2HCl
D.CuO+H2SO4=CuSO4+H2O
练习:
2.高铁酸钾是一种新型、高效、多功能水处理剂。下列反应可制取:
对于该反应,下列说法正确的是(
)
A.该反应是置换反应
B.钾元素化合价降低
C.发生还原反应
D.是氧化剂
练习:
3.高铁的快速发展方便了人们的出行。工业上利用铝热反应焊接钢轨间的缝隙,反应方程式如下:2Al+Fe2O3=2Fe+Al2O3,其中Fe2O3是
(
)
A.氧化剂
B.还原剂
C.既是氧化剂又是还原剂
D.既不是氧化剂又不是还原剂
谋事在人,
成事在天!
氧化还原反应
思考:(1)上述反应中哪些是氧化还原反应?氧化还原反应的特征是什么?
属于氧化还原反应的有:①②③⑤
特征:有元素化合价的变化。
(2)氧化还原反应与四种基本反应类型之间有什么关系?
氧化还原反应
非氧化还原反应
小试牛刀
【针对训练1】(2008年江苏学业水平测试)下列反应属于氧化还原反应的是(
)
A.H2SO4+2NaOH
=
Na2SO4+2H2O
B.2NaHCO3
Na2CO3
+
CO2↑
+
H2O
C.NH3
+
HCl
=
NH4Cl
D.CuO
+
H2
Cu
+
H2O
D
【问题2】在氧化还原反应中引起元素化合价发生变化的本质原因是什么?
H2+Cl2=2HCl
的形成过程:
电子的转移,包括得失或偏移,
综上所述,可以给氧化还原反应下一个更为本质的定义:凡是有电子转移(得失或偏移)的反应都是氧化还原反应。
化合价升降的原因:
【针对训练2】写出下列变化中化合价发生变化的每个原子得到(或失去)电子数
①
Fe2O3
→
Fe
②C→CO2
③
SO2→S
④NH3→NO
小试牛刀
得到3e-
失去4e-
得到4e-
失去5e-
一、氧化还原反应
概念:
特征:
本质:
凡有电子转移(得失或偏移)的化学反应
电子转移
化合价发生了变化
(
判断依据)
【问题3】判断下列各反应中的氧化剂、还原剂,分别是什么?
思考:氧化还原反应包括氧化反应与还原反应两个部分,氧化剂与还原剂在反应中表现什么样的性质?
分别发生了什么反应?
与电子得失、化合价升降的关系?
(1)2Fe
+
3Cl2=2FeCl3
(2)3NO2
+
H2O
=
2HNO3+NO
(3)SO2
+
2
H2S
=3
S↓+2
H2O
还原剂
氧化剂
既是氧化剂又是还原剂
氧化剂
还原剂
氧化剂:
得到电子的物质
失去电子的物质
还原剂:
二、氧化剂和还原剂
口诀:升失氧化还原剂,降得还原氧化剂
【问题4】你能用双线桥法表示出下列氧化还原反应中电子转移的方向与数目吗?
2Na+Cl2
=
2NaCl
MnO2
+
4HCl(浓)
MnCl2
+
Cl2
↑
+
2H2O
双线桥法
+4
+2
-1
0
得2e-
失2e-
步骤:①标价态
MnO2
+
4HCl(浓)
=
MnCl2
+
Cl2
+
2H2O
三、氧化还原反应电子转移的表示方法
②连双线
③注得失
【问题5】配平下面的离子反应方程式。
四、氧化还原反应的基本规律--电子守恒规律
Fe2+
+
Cl2
=
Fe3+
+
Cl-
+2
0
+3
-1
2
2
2
失1e-
得2
×1e-
×2
五、生产生活中常见的氧化还原反应
【问题6】你知道日常生活中有哪些常见的氧化还原反应吗?
感受氧化还原反应的存在
刚削好的苹果
放置30分钟以后的苹果
刚泡好的绿茶
放置2小时后的绿茶
感受氧化还原反应的存在
感受氧化还原反应的存在
感受氧化还原反应的存在
好吃的月饼
感受氧化还原反应的存在
1.下列化学反应中,H2SO4作为氧化剂的是(
)
A.2NaOH+H2SO4=Na2SO4+2H2O
B.C+2H2SO4(浓)CO2↑+2SO2↑+2H2O
C.BaCl2+H2SO4=BaSO4↓+2HCl
D.CuO+H2SO4=CuSO4+H2O
练习:
2.高铁酸钾是一种新型、高效、多功能水处理剂。下列反应可制取:
对于该反应,下列说法正确的是(
)
A.该反应是置换反应
B.钾元素化合价降低
C.发生还原反应
D.是氧化剂
练习:
3.高铁的快速发展方便了人们的出行。工业上利用铝热反应焊接钢轨间的缝隙,反应方程式如下:2Al+Fe2O3=2Fe+Al2O3,其中Fe2O3是
(
)
A.氧化剂
B.还原剂
C.既是氧化剂又是还原剂
D.既不是氧化剂又不是还原剂
谋事在人,
成事在天!
