陕西省渭南市临渭区2019-2020学年高一下学期期末考试化学试题
文档属性
| 名称 | 陕西省渭南市临渭区2019-2020学年高一下学期期末考试化学试题 |

|
|
| 格式 | docx | ||
| 文件大小 | 482.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-08-03 00:00:00 | ||
图片预览




文档简介
1210310011264900临渭区 2019~ 2020学年度第二学期期末教学质量检测
高一化学试题
注意事项:
1. 本试卷全卷满分100 分,答题时间 90分钟:
2. 本试卷第I卷和第II卷两部分。 第 I卷为选择题, 用2B铅笔将正确答案徐写在答题卡上;第II卷为非选择题, 用 0. 5 mm黑色墨水签字笔完成在答题纸上;
3.答第I卷前,将姓名 、考号、考试科目、试卷类型按要求涂写在答题卡上;
4.答第II卷 前,将答题纸上装订线内栏目填写清楚。
可能用到的相对原子质量为:C一12 N一14 O一16 S 一 3 2 C l一35 . 5
K 一39 Fe-56 Cu一64
第 I 卷( 选 择 题 共 54 分)
— 、选择题(本大题共18 小题,每小题3 分.计54 分。每小题只有一个选项符合题意)
1.2019 年 l2 月以来,我国部分地区突发的新型冠状病毒肺炎威胁着人们的身体健康。以下是人们在面对“新型冠状病毒肺炎”时的一些认识,你认为符合科学道理的是
A. 家庭消毒时,消毒液越浓越好
B 吸烟、喝酒可以预防“新型冠状病毒”
C. 应经常保持室内清洁卫生和通风
D. 必须每天吃药,补充人体所需化学物质
2. 13C - NMR、15N- NMR可用于测定蛋白质、核酸等生物大分子的空间结构。下面叙述正确
的是
A. 13C 与15N有相同的中子数
B. 13C与 C60互为同位素
C. 15N与 14N 互为同位素
D. 15N和14N有不同的核外电子数
3.下列化学用语书写正确的是
A. 氯化镁的电于式:
B 乙烷的结构式是:
C.氯原子的结构示意图:
D . 中子数为7 的碳原子是:falseC
4.《后汉书? 郡国志》中记载:“石出泉水其水有肥、燃之极明,不可食,县人谓之石漆”; 《 西阳杂俎》一 书记载:“高奴且石脂水,水腻,浮上如漆,采以膏车及燃灯极明”。 下列说法正确的是
A. 上述材料所说“石漆”“石脂水”是石油,在工业上通过石油分馏可得纯净的苯
B. 以石油为原料可生产三大合成材料即合金、合成橡胶和合成纤维
C.石油的催化裂化属于物理变化
D. 塑料聚乙烯的单体可以由石油裂解得到
5. 下列关于物质性质变化的比较,正确的是
A.碱性强弱: KOH > NaOH> Mg(OH)2
B. 原子半径大小: Cl> Na> O
C. 稳定性:HI > HBr> HCl > HF
D. 还原性强弱: Cl-> Br-> I-
6.把纯净的甲烷与氯气混合物放在集气瓶中,用玻璃片盖好瓶口,放在光亮的地方一段时间后,下列说法中不正确的是
A. 气体发生爆炸
B. 瓶内气体的颜色变浅
C. 用一根蘸有浓氨水的玻璃棒伸入瓶内时有白烟产生
D. 集气瓶壁有油状液体生成
7.决定化学反应速率的主要因素是
A.参加反应的物质本身的性质 B. 催化剂
C. 温度、压强以及反应物的接触面 D. 反应物的浓度
8.相同条件下,分别测得反应 A(g) + 3 B(g) 2C(g) + 2 D( g ) 的速率如下:
① v( A) =0.15 mol ? L -1?s -1 ②v ( B) = 0.6 mol ? L -1?s -1
③v (C) =0.5 mol ? L -1?s -1 ④ v ( D) = 1.2 mol ? L -1?min -1
其中反应最快的是
A. ① B. ② C. ③ D. ④
9.如图是化学课外活动小组设计的用化学电源使 LED 灯发光的装置示意图。下列有关该装
置的说法正础的是
A.铜片为负极,其附近的溶液变蓝, 溶液中有 Cu2+ 产生
B. 如果将锌片换成铁片,电路中的电流方向将改变
C. 如果将稀硫酸换成拧檬汁、LED灯将不会发光
D. 其能量转化的形式主要是“化学能→ 电能→光能”
10.乙醇分子结构中各种化学键如图所示,下列说法正确的是
A.与金属钠反应时断裂 ②
B. 与乙酸反应时断裂①
C. 在铜丝催化下与O2反应断裂 ②③
D. 燃烧时断裂 ①③
11. 下列物质中属于离子化合物的是
A.CH3CH3 B. KOH C.CO2 D. H2SO4
12. 我国在砷化镓太阳能电池研究方面国际领。砷(As)和镓(Ga)都是第四周期元素,分别属于VA和IIIA族。下列说法中,不正确的是
A.原子半径;Ga > As > P
B.热稳定性:NH3> PH3> AsH3
C. G.a( OH )3可能是两性氢氧化物
D. 酸性:H3AsO4 > H2SO4> H3PO4
13. 下列图示的装置属说原电池的是
A. ①②⑥⑧ B.③④⑤⑦ C.③④⑥⑦ D.③④⑤⑥⑦⑧
14. 根据表1 信息,判断以下叙述正确的是
表 1 分短周期元素的原子半径及主要化合价
元素代号
L
M
Q
R
T
原子半径/ nm
0. 160
0.143
0.112
0. 104
0.066
主要化合价
+2
+3
+2
+6、-2
-2
A. M 与T 形成的化合物具有两性
B. 氢化物的沸点为:H2T< H2R
C. L2+与R2- 的核外电子数相等
D. 元素的金属性强弱程度为:L
高一化学试题
注意事项:
1. 本试卷全卷满分100 分,答题时间 90分钟:
2. 本试卷第I卷和第II卷两部分。 第 I卷为选择题, 用2B铅笔将正确答案徐写在答题卡上;第II卷为非选择题, 用 0. 5 mm黑色墨水签字笔完成在答题纸上;
3.答第I卷前,将姓名 、考号、考试科目、试卷类型按要求涂写在答题卡上;
4.答第II卷 前,将答题纸上装订线内栏目填写清楚。
可能用到的相对原子质量为:C一12 N一14 O一16 S 一 3 2 C l一35 . 5
K 一39 Fe-56 Cu一64
第 I 卷( 选 择 题 共 54 分)
— 、选择题(本大题共18 小题,每小题3 分.计54 分。每小题只有一个选项符合题意)
1.2019 年 l2 月以来,我国部分地区突发的新型冠状病毒肺炎威胁着人们的身体健康。以下是人们在面对“新型冠状病毒肺炎”时的一些认识,你认为符合科学道理的是
A. 家庭消毒时,消毒液越浓越好
B 吸烟、喝酒可以预防“新型冠状病毒”
C. 应经常保持室内清洁卫生和通风
D. 必须每天吃药,补充人体所需化学物质
2. 13C - NMR、15N- NMR可用于测定蛋白质、核酸等生物大分子的空间结构。下面叙述正确
的是
A. 13C 与15N有相同的中子数
B. 13C与 C60互为同位素
C. 15N与 14N 互为同位素
D. 15N和14N有不同的核外电子数
3.下列化学用语书写正确的是
A. 氯化镁的电于式:
B 乙烷的结构式是:
C.氯原子的结构示意图:
D . 中子数为7 的碳原子是:falseC
4.《后汉书? 郡国志》中记载:“石出泉水其水有肥、燃之极明,不可食,县人谓之石漆”; 《 西阳杂俎》一 书记载:“高奴且石脂水,水腻,浮上如漆,采以膏车及燃灯极明”。 下列说法正确的是
A. 上述材料所说“石漆”“石脂水”是石油,在工业上通过石油分馏可得纯净的苯
B. 以石油为原料可生产三大合成材料即合金、合成橡胶和合成纤维
C.石油的催化裂化属于物理变化
D. 塑料聚乙烯的单体可以由石油裂解得到
5. 下列关于物质性质变化的比较,正确的是
A.碱性强弱: KOH > NaOH> Mg(OH)2
B. 原子半径大小: Cl> Na> O
C. 稳定性:HI > HBr> HCl > HF
D. 还原性强弱: Cl-> Br-> I-
6.把纯净的甲烷与氯气混合物放在集气瓶中,用玻璃片盖好瓶口,放在光亮的地方一段时间后,下列说法中不正确的是
A. 气体发生爆炸
B. 瓶内气体的颜色变浅
C. 用一根蘸有浓氨水的玻璃棒伸入瓶内时有白烟产生
D. 集气瓶壁有油状液体生成
7.决定化学反应速率的主要因素是
A.参加反应的物质本身的性质 B. 催化剂
C. 温度、压强以及反应物的接触面 D. 反应物的浓度
8.相同条件下,分别测得反应 A(g) + 3 B(g) 2C(g) + 2 D( g ) 的速率如下:
① v( A) =0.15 mol ? L -1?s -1 ②v ( B) = 0.6 mol ? L -1?s -1
③v (C) =0.5 mol ? L -1?s -1 ④ v ( D) = 1.2 mol ? L -1?min -1
其中反应最快的是
A. ① B. ② C. ③ D. ④
9.如图是化学课外活动小组设计的用化学电源使 LED 灯发光的装置示意图。下列有关该装
置的说法正础的是
A.铜片为负极,其附近的溶液变蓝, 溶液中有 Cu2+ 产生
B. 如果将锌片换成铁片,电路中的电流方向将改变
C. 如果将稀硫酸换成拧檬汁、LED灯将不会发光
D. 其能量转化的形式主要是“化学能→ 电能→光能”
10.乙醇分子结构中各种化学键如图所示,下列说法正确的是
A.与金属钠反应时断裂 ②
B. 与乙酸反应时断裂①
C. 在铜丝催化下与O2反应断裂 ②③
D. 燃烧时断裂 ①③
11. 下列物质中属于离子化合物的是
A.CH3CH3 B. KOH C.CO2 D. H2SO4
12. 我国在砷化镓太阳能电池研究方面国际领。砷(As)和镓(Ga)都是第四周期元素,分别属于VA和IIIA族。下列说法中,不正确的是
A.原子半径;Ga > As > P
B.热稳定性:NH3> PH3> AsH3
C. G.a( OH )3可能是两性氢氧化物
D. 酸性:H3AsO4 > H2SO4> H3PO4
13. 下列图示的装置属说原电池的是
A. ①②⑥⑧ B.③④⑤⑦ C.③④⑥⑦ D.③④⑤⑥⑦⑧
14. 根据表1 信息,判断以下叙述正确的是
表 1 分短周期元素的原子半径及主要化合价
元素代号
L
M
Q
R
T
原子半径/ nm
0. 160
0.143
0.112
0. 104
0.066
主要化合价
+2
+3
+2
+6、-2
-2
A. M 与T 形成的化合物具有两性
B. 氢化物的沸点为:H2T< H2R
C. L2+与R2- 的核外电子数相等
D. 元素的金属性强弱程度为:L
15. 下列实验装置设计正确,且能达到目的的是
A. 石油的分馏 B. 制备乙酸乙酯 C.分离乙酸和乙醇 D.除甲烷中的乙烯
16. 下列反应中属于加成反应的是
A.CH4+ Cl2 CH3Cl + HCl
B. 2 CH3CH3+ 7O2 4CO2 + 6 H2O
C. CH3CH2OH + HBr CH3CH2Br + H2O
D. CH2 =CH2+HCl→ CH3CH2Cl
17.下列反应前后物质的总能量变化能用右图表示的是
A. 氢氧化钠和盐酸的反应
B. Ba(OH)2 ? 8H2O晶体和 NH4Cl 晶体的反应
C. 铝与NaOH溶液的反应
D. 甲烷在氧气中燃烧
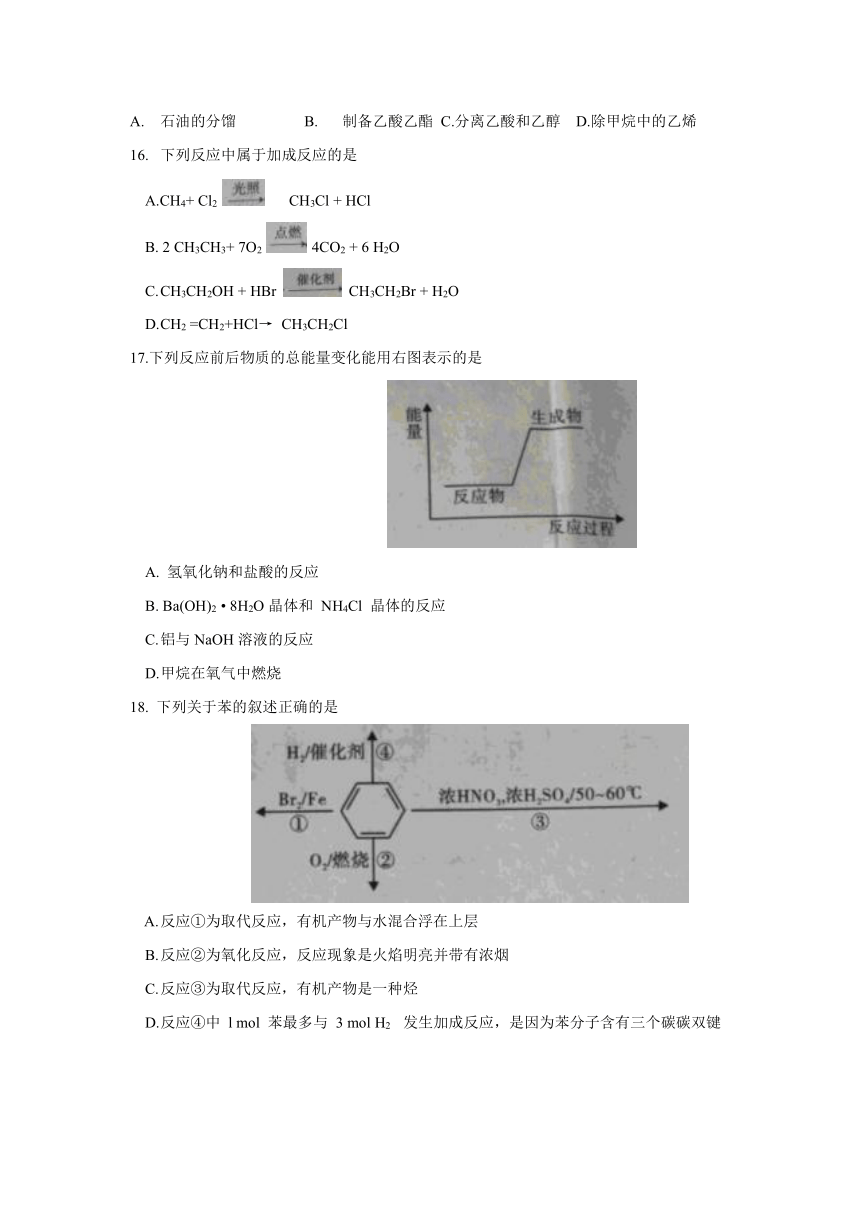
18. 下列关于苯的叙述正确的是
A. 反应①为取代反应,有机产物与水混合浮在上层
B. 反应②为氧化反应,反应现象是火焰明亮并带有浓烟
C. 反应③为取代反应,有机产物是一种烃
D. 反应④中 l mol 苯最多与 3 mol H2 发生加成反应,是因为苯分子含有三个碳碳双键
第 II 卷( 非选择题 共 46 分)
二、非选择题(本大题4 小题. ,计46 分 )
19. ( 6 分 )( 1) 下列3种不同粒子falseH、falseH、falseH 表示 种元素, 种核
素,falseH、falseH、falseH互称为 。
( 2 ) 写出第 2 周期VA 族元素单质的电子式: 。
( 3) 工业上以乙烯为原料可以生产一种重要的合成有机高分子化合物,其反应的化学方程式为 ,反应类型是 。
20. ( 12 分)下表元素周期表的一部分.针对表中的①~⑩种元素,请用化学用语问答下列
问题:
( 1) 在③~⑦元素中,原子半径最大的是 ( 填元素符号)。
( 2 ) ⑦ 元素的最高价氧化物对应的水化物与其氢化物能生成盐 M, M中含有的化学键类型有 。
( 3 ) 出写元素 ①和⑧的单质在加热杂件下反应生成的化合物的电子式: 。 ( 4 )③、⑤、⑦、⑨所形成的离子,其半径由小到大的顺序是 (填离子符号 )。
(5) ①~⑨中元素最高价氧化物对应的水化物中酸性最强的是 ( 填物质化学
式);呈两性的氢氧化物是 (填物质化学式).该化合物与 NuOH溶液反应的离子方程式为 。
( 6 ) 写出实验室制取元素⑨的单质的反应的离子方程式: 。
21. ( 12 分 )( 1 ) 新冠肺炎最明显的症状就是出现发热,体温枪能快速检测人体体温.该体温枪所用的电池为一种银锌电池(如下图所示),该电池的总反应式为:Zn+Ag2O+ H2O=-Zn(OH)2+ 2Ag。
回答下列问题:
①在测体温时,电池将 转化为 (填“化学能”或“电能”) 。
②电池中电子的流向:由 到 (填化学式),负极的电极反应式为 。
(2 ) 一定条件下铁可以和 CO2 发生反应 :Fe ( s ) + CO2 ( g ) Fe O( s ) + CO( g)。一定温度下,向某密闭容器中加入足量铁粉并充入一 定量的 CO2气体,反应过程中 CO2气体 和 CO气体的浓度与时间的关系如图所示:
①t1时 ,正、逆反应速率的大小关系为 v正 v逆(填“.”、“<”或“=”)
②4min 内 , CO的平均反应速率v ( CO) = 。
③下列条件的改变能减慢其反应速率的是 (填字母,下同)。
a. 降低温度 h. 减少铁粉的质量
c.保持压强不变,充入He使容器的体积增大
d. 保持容积不变 ,充入He使体系压强增大
(4)下列描述能说明上述反应已达到平衡状态的是 。
a . v ( CO2) == v ( CO)
b. 单位时间内生成 n mol CO2的同时生成 n mol CO2
c.容器中气体压强不随时间变化而变化
d. 容器中气体的平均相对分子质量不随时间变化而变化
22.( 1 6分)现有 7 瓶失去标签的试剂瓶,它们盛装的液体分别为①乙醇、②乙酸、③苯、④乙酸乙酯、⑤油脂、⑥葡萄糖溶液 、⑦蔗糖溶液中的一种。现通过如下实验来确定各试剂瓶中所装液体的名称。
实验步骤和方法
实验现象
a.把 7 瓶液体依次标号为 A 、B、C、D、E 、F、 G 后闻气味
只有F、G 两种液体没有气味
b. 各取少量 7 种液体于试管中,加水稀释
只有C、D 、E 三种液体与水分层,且位于上层
c. 各取少量 7 种液体于试管中,加新制的Cu(OH)2悬浊液并加热
只有 B 使沉淀溶解 ,F 中产生砖红色沉淀
d. 各取 C、D、E 适量于试管中,加足量NaOH并加热
只有 C 中有分层现象 ,D 的试管 中可闻到特殊香味
(1) 试写出下列标号代表的液体名称 :
A ,B ,C ,D , E ,
F. , C 。
( 2 ) 写出 A 与金属钠反应的化学方程式: 。
(3)已知乙醛发生银镜反应的方程式CH3CHO+2[Ag(NH3)2]OH CH3COONH4+H2O
+ 2Ag ↓+3NH3 。 试写出葡萄糖发生银镜反应的方程式: 。
( 1 ) 在实验室可以用右图所示的装置制取乙酸乙酯,请回答下列问题 。
①试管a中加入几块碎瓷片的目的是 。
②试管a中发生反应的化学方程式为 ,反应类型是 。
③反应开始前,试管b 中盛放的溶液是 。
④ 若要把制得的乙酸乙酯分离出来,应采用的实验橾作是
(填操作名称)
临渭区 2019~ 2020学年度第二学期期末教学质量检测
高一化学试题参考答案及评分标准
— 、选择题(本大题共18 小题悔 小题3 分.计54 分。每小题只有一个选项符合题意)
1.C 2.C 3 B 4 D 5.A 6.A 7.A 8.C 9.D 10.B
11.B 12. D 13. C 14.A 15 . B 16. D 17 . B 18. B
二、非选择题(本大题4 小题. ,计46 分 )
19. ( 6分)(每1空分)
(I) 1 3 同位素
(2)
(3)nCH2 =CH2 加聚反应
20. ( 12 分)(除标明外.每1空分)
(l)Ca
(2)离子键、共价键( 2 分)
( 3) ( 2 分)
( 4) Al3+ < Mg2+ < N3- < Cl-
(5 ) HClO4 Al(OH)3 Al(OH)3 + OH- = AlO2-+ 2 H2O ( 2 分)
( 6 ) MnO2+ 4H++ 2Cl Mn2++ Cl2↑+ 2H2O ( 2 分 )
2l. ( 12 分)(除标明外,每空1 分)
(1 )①化学能 电能
②Zn Ag2O Zn + 2OH-一2e-=Zn( OH)2 ( 2 分)
(2)① >
②0. 125 mol ? L-1? min-1
③ac( 2 分)
④bd( 2 分)
22. ( 16 分)(除标明外,每空1 分)
( 1 ) 乙醇 乙酸 苯 乙酸乙酯 油脂 葡萄糖溶液 蔗糖溶液
( 2 ) 2CH3CH2OH + 2Na→2CH3CH2ONa+ H2 ↑
( 3 ) HOCH2(CHOH)4CHO+2[Ag(NH3)2] OH HOCH2(CHOH)4COONH4+H2O +2Ag↓
+3NH3( 2 分)
( 4 )①防止暴沸
②CH3COOH +C2H5OH CH3COOC2H5 + H2O ( 2 分)酯化反应(或取代反应)
③饱和碳酸钠溶液
④分液
同课章节目录
