2011福建省重点高中新生入学选拔考试
文档属性
| 名称 | 2011福建省重点高中新生入学选拔考试 |  | |
| 格式 | zip | ||
| 文件大小 | 487.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2011-07-12 13:43:24 | ||
图片预览

文档简介
2011福建省重点高中新生入学选拔统一考试
<<化 学>> 试 题
(试卷满分:100分;考试时间:90分钟)
考生注意:1.本学科有两份试卷,一是答题卡,另一是本试题(共5页24题)。请将全部答案填在答题卡的相应答题栏内,否则不能得分!
2.可能用到的相对原子质量:H—1 C—12 O—16 K-39 Ca—40
一、选择题(本题15小题,共30分,每小题仅有一个正确选项,请在答题卡选择题栏内用黑色签字笔填写你的答案)
题记:化学此在我们身边,化学与我们息息相关
1.小明的食谱中有猪肉、米饭、食盐、矿泉水。从均衡营养的角度,小明还需增加摄入
A.蛋白质 B.糖类 C.无机盐 D.维生素
2.钙是人体不可缺少的重要元素,下列有关钙原子结构的说法正确的是
A.质子数为20 B.电子层数为3
C.最外层电子数为10 D.核外电子数为40
3.下列说法,你认为正确的是
A.人类利用的能量都是通过化学反应获得的
B.现代化学技术可在只有水的条件下生产汽油
C.CO2会使全球变暖,所以大气中CO2越少越好
D.在使用乙醇等新型燃料时,也要注意可能造成的环境污染
4.下列事故处理方法,不正确的是
A.电器着火,立即用水扑灭
B.炒菜时油锅着火,立即盖上锅盖
C.厨房煤气管道漏气,立即关闭阀门并开窗通风
D.图书馆内图书着火,立即用液态二氧化碳灭火器扑灭
5.常用抗生素“先锋Ⅵ”为粉末状固体,每瓶含“先锋Ⅵ”0.5g,注射时应配成质量分数不高于20%的溶液,则使用时每瓶至少需加入蒸馏水
A.1mL B. 2 mL C. 3mL D. 4 mL
题记:化学是二十一世纪最有用,最有创造力的中心学科
6.在厦参加国际磷化学会议的科学家认为无磷洗涤剂洗涤效果差,污染更严重,建议在建立磷回收机制后,重新使用加有磷化合物的含磷洗涤剂。对此的下列说法不正确的是
A.含磷洗涤剂含有磷元素 B.只要解决污染问题,可能重新使用含磷洗涤剂
C.含磷洗涤剂含有磷单质 D.研究高效无污染的洗涤剂仍是化学家的任务
7.我们看到“农家乐”灶炉膛中柴禾架空时烧得更旺。这是因为
A.散热更快 B.温度降低到着火点以下
C.使着火点降低 D.柴禾与空气中氧气接触更充分
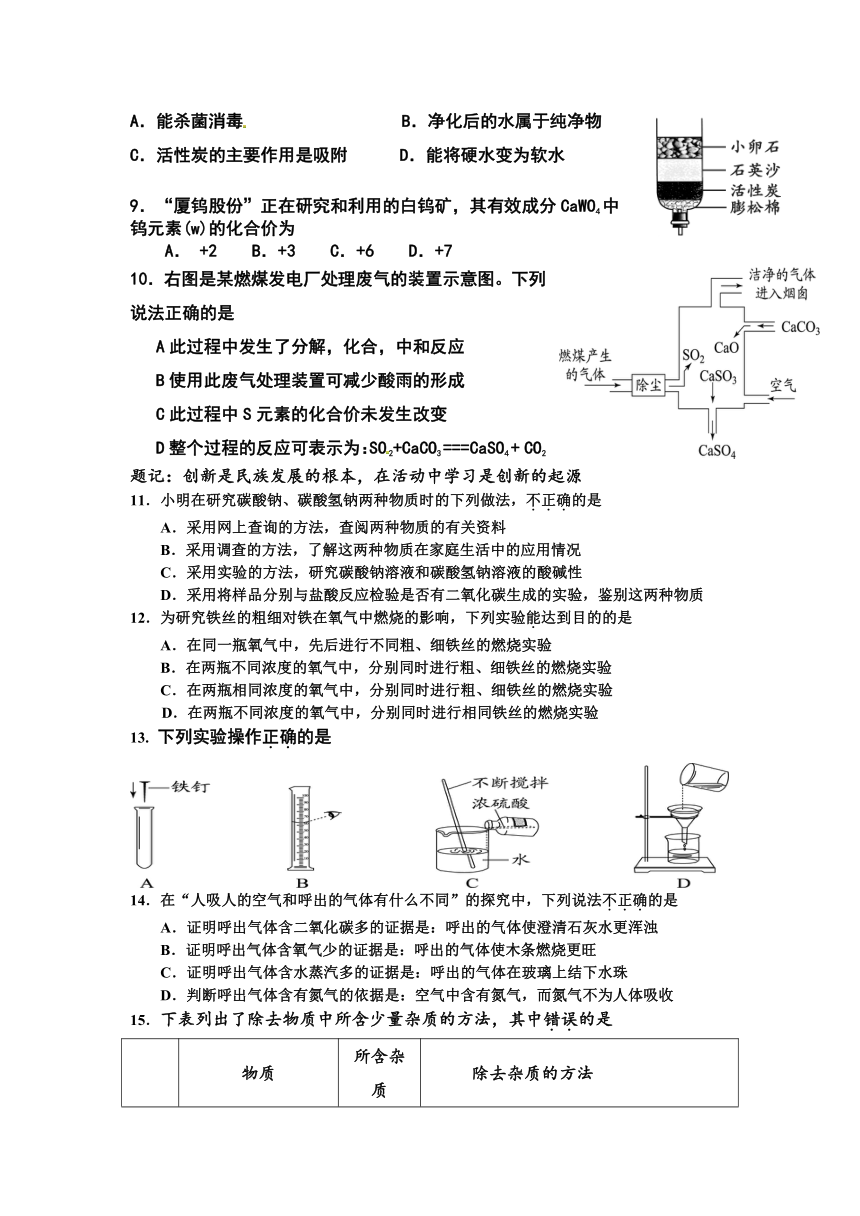
8用右图所示的简易净水器处理浑浊的河水,下面对该净水器分析正确的是
A.能杀菌消毒 B.净化后的水属于纯净物
C.活性炭的主要作用是吸附 D.能将硬水变为软水
9.“厦钨股份”正在研究和利用的白钨矿,其有效成分CaWO4中
钨元素(w)的化合价为
A. +2 B.+3 C.+6 D.+7
10.右图是某燃煤发电厂处理废气的装置示意图。下列说法正确的是
A此过程中发生了分解,化合,中和反应
B使用此废气处理装置可减少酸雨的形成
C此过程中S元素的化合价未发生改变
D整个过程的反应可表示为:SO2+CaCO3 ===CaSO4 + CO2
题记:创新是民族发展的根本,在活动中学习是创新的起源
11.小明在研究碳酸钠、碳酸氢钠两种物质时的下列做法,不正确的是
A.采用网上查询的方法,查阅两种物质的有关资料
B.采用调查的方法,了解这两种物质在家庭生活中的应用情况
C.采用实验的方法,研究碳酸钠溶液和碳酸氢钠溶液的酸碱性
D.采用将样品分别与盐酸反应检验是否有二氧化碳生成的实验,鉴别这两种物质
12.为研究铁丝的粗细对铁在氧气中燃烧的影响,下列实验能达到目的的是
A.在同一瓶氧气中,先后进行不同粗、细铁丝的燃烧实验
B.在两瓶不同浓度的氧气中,分别同时进行粗、细铁丝的燃烧实验
C.在两瓶相同浓度的氧气中,分别同时进行粗、细铁丝的燃烧实验
D.在两瓶不同浓度的氧气中,分别同时进行相同铁丝的燃烧实验
13. 下列实验操作正确的是
14.在“人吸人的空气和呼出的气体有什么不同”的探究中,下列说法不正确的是
A.证明呼出气体含二氧化碳多的证据是:呼出的气体使澄清石灰水更浑浊
B.证明呼出气体含氧气少的证据是:呼出的气体使木条燃烧更旺
C.证明呼出气体含水蒸汽多的证据是:呼出的气体在玻璃上结下水珠
D.判断呼出气体含有氮气的依据是:空气中含有氮气,而氮气不为人体吸收
15.下表列出了除去物质中所含少量杂质的方法,其中错误的是
物质 所含杂质 除去杂质的方法
A CO2 CO 点燃
B NaCl 泥沙 溶解、过滤、蒸发
C Cu(NO3)2溶液 AgNO3 加入过量的铜粉,过滤
D NaOH溶液 Na2CO3 加入适量的氢氧化钙溶液,过滤
二、填空与简答(本题共6小题,共40分)
16.(4分)请应用“物质性质决定用途”的规律,完成下表:
物质化学式 性 质 用 途
例子 CO2 在一定温度下能形成固体 制作干冰,用于人工降雨
(1) 在空气中可燃烧 可作为汽车燃料
(2)
17.(6分)写出下列反应的化学方程式:
(1)实验室制取氧气(写一个): ;
(2)碳酸氢钠受热分解生成碳酸钠、水和二氧化碳: 。
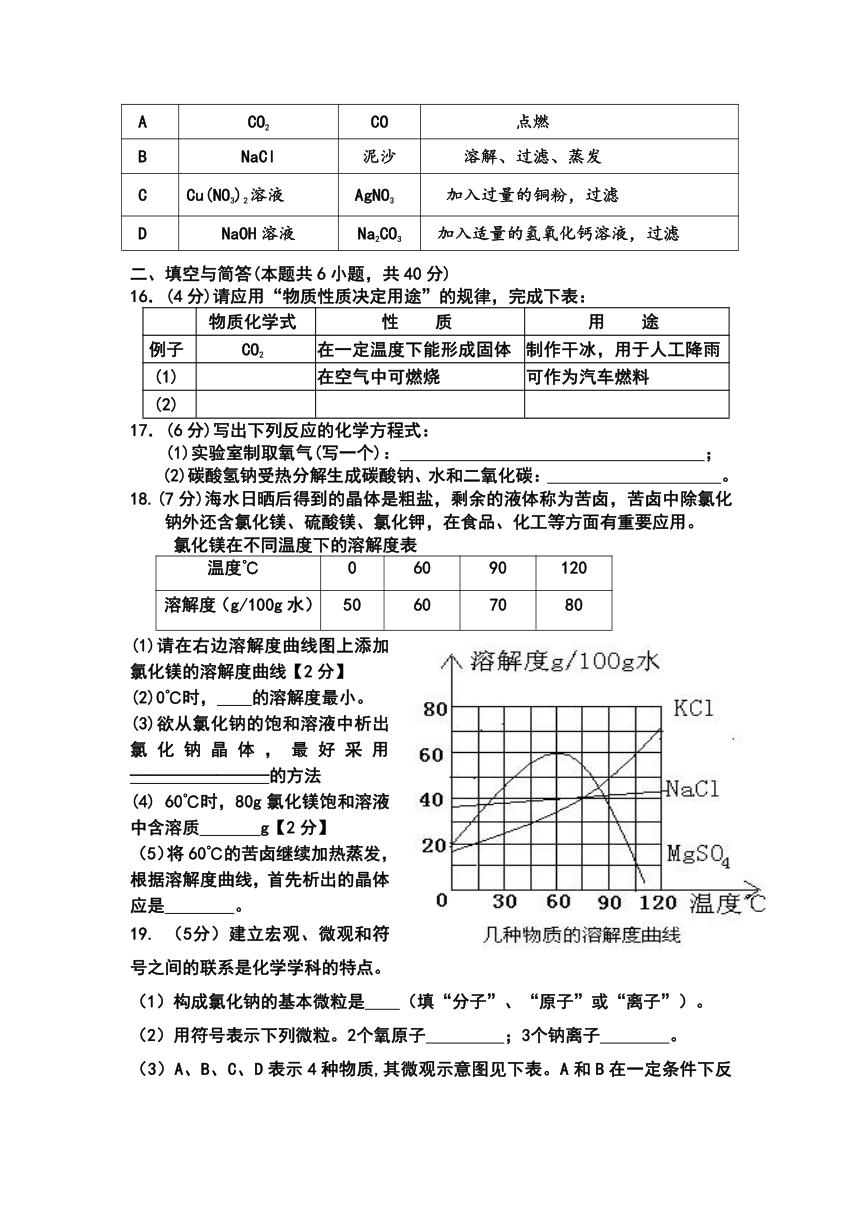
18.(7分)海水日晒后得到的晶体是粗盐,剩余的液体称为苦卤,苦卤中除氯化钠外还含氯化镁、硫酸镁、氯化钾,在食品、化工等方面有重要应用。
氯化镁在不同温度下的溶解度表
温度℃ 0 60 90 120
溶解度(g/100g水) 50 60 70 80
(1)请在右边溶解度曲线图上添加氯化镁的溶解度曲线【2分】
(2)0℃时, 的溶解度最小。
(3)欲从氯化钠的饱和溶液中析出氯化钠晶体,最好采用 ————————的方法
(4) 60℃时,80g氯化镁饱和溶液中含溶质 g【2分】
(5)将60℃的苦卤继续加热蒸发,根据溶解度曲线,首先析出的晶体应是 。
19. (5分)建立宏观、微观和符号之间的联系是化学学科的特点。
(1)构成氯化钠的基本微粒是 (填“分子”、“原子”或“离子”)。
(2)用符号表示下列微粒。2个氧原子 ;3个钠离子 。
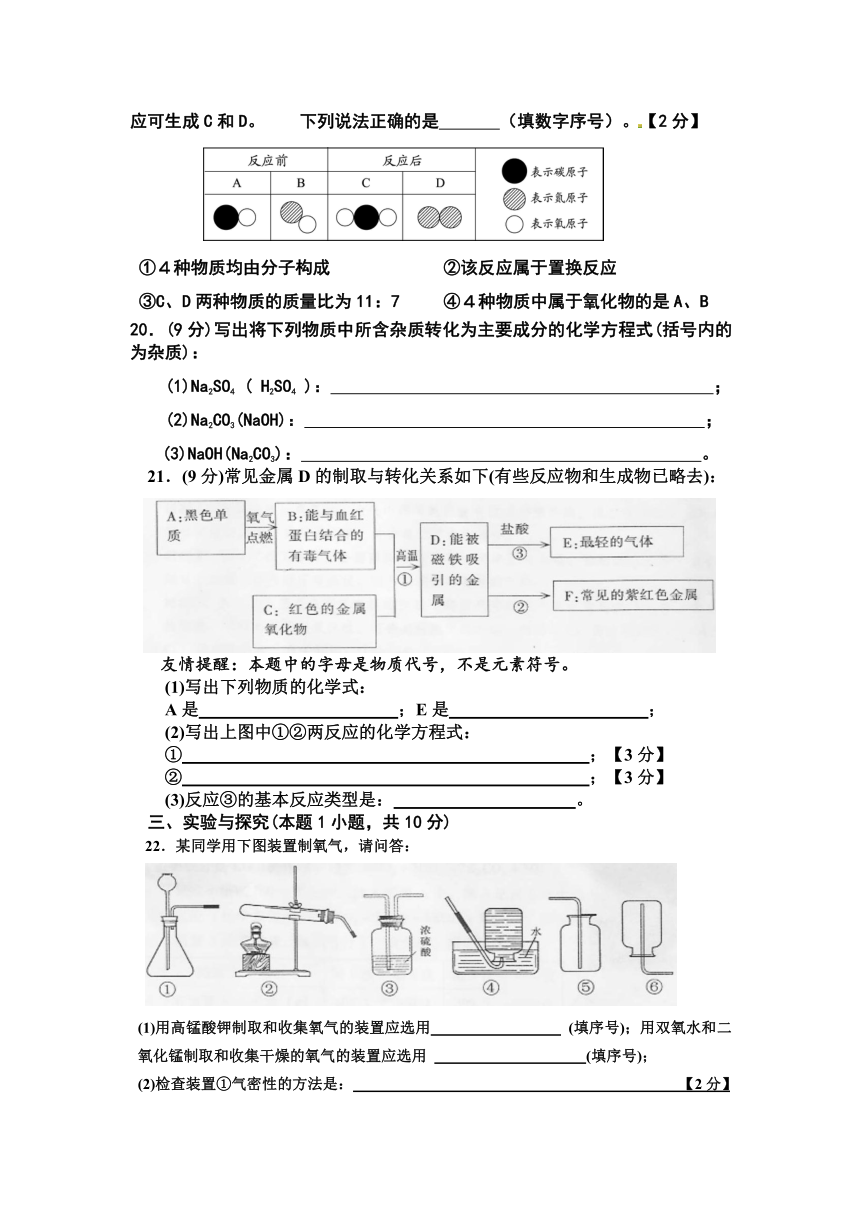
(3)A、B、C、D表示4种物质,其微观示意图见下表。A和B在一定条件下反应可生成C和D。 下列说法正确的是 (填数字序号)。【2分】
①4种物质均由分子构成 ②该反应属于置换反应
③C、D两种物质的质量比为11:7 ④4种物质中属于氧化物的是A、B
20.(9分)写出将下列物质中所含杂质转化为主要成分的化学方程式(括号内的为杂质):
(1)Na2SO4 ( H2SO4 ): ;
(2)Na2CO3(NaOH): ;
(3)NaOH(Na2CO3): 。
21.(9分)常见金属D的制取与转化关系如下(有些反应物和生成物已略去):
友情提醒:本题中的字母是物质代号,不是元素符号。
(1)写出下列物质的化学式:
A是 ;E是 ;
(2)写出上图中①②两反应的化学方程式:
① ;【3分】
② ;【3分】
(3)反应③的基本反应类型是: 。
三、实验与探究(本题1小题,共10分)
22.某同学用下图装置制氧气,请问答:
(1)用高锰酸钾制取和收集氧气的装置应选用 (填序号);用双氧水和二氧化锰制取和收集干燥的氧气的装置应选用 (填序号);
(2)检查装置①气密性的方法是: 【2分】
(3)装置②试管口要略向下倾斜的原因是:
(4)若用装置④收集的氧气不纯,其原因可能是(请写一种原因):【2分】
;
(5)有一种气体可以用装置1,3,6来制取,请写出反应方程式—————————【3分】
四、信息与分析(本题1小题,共10分)
23.阅读材料,回答问题:
材料1.臭氧是淡蓝色气体,大气中的臭氧层能有效阻挡紫外线,保护地球的生存环境,但目前南极出现了臭氧层空洞,并有继续扩大的趋势。
材料2.复印机在工作时,会因高压放电产生一定浓度的臭氧。长期吸入大量臭氧会引 起口干舌燥,咳嗽等不适症状,还可能诱发中毒性肺气肿。
材料3.臭氧发生器是在高压电极的作用下将空气中的氧气转化为臭氧(化学式为O3)的装置。利用臭氧的强氧化性,可将其应用于游泳池、生活用水、污水的杀菌和消毒。
(1)请总结臭氧的有关知识:①物理性质: ;
②化学性质: ;③用途: ;
(2)请从分子构成的角度,指出氧气和臭氧的不同点: ;
(3)写出材料3中氧气转化为臭氧的化学方程式: ;
(4)磷在臭氧中燃烧与在氧气中燃烧相似,请写出磷在臭氧中燃烧的化学方程式:
;
(5)请提出一个缩小臭氧层空洞的设想: 。
五、计算与应用(本题1小题,共10分)
24.食醋是家庭常用的调味品。某兴趣小组同学为探究食醋中醋酸(乙酸)的质量分数设计并进行了如下实验:取10%的氢氧化钠溶液(密度为1.2g/mL)逐滴加入到100g食醋中,当滴入25mL该氢氧化钠溶液时正好完全中和。已知反应化学方程式如下:CH3COOH + NaOH → CH3COONa + H2O,
请你完成探究实验中的相关计算:
⑴实验中消耗的25mL氢氧化钠溶液中溶质的物质的量是多少?
⑵食醋中醋酸的质量分数是多少
【友情提醒:试题结束,请认真检查。】
2011福建省重点高中新生入学选拔统一考试
化学试题参考答案
一、选择题【共30分】
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 D A D A B C D C C B D C C B D
二、填空与简答【共40分】【每空一分,除标明外】
16.C2H5OH CO 在空气中可燃烧 可作为气体燃料
17.(1) 或 2KMnO4 △ K2MnO4 + MnO2 + O2↑
(2)2NaHCO3 △ Na2CO3+H2O+CO2↑ 。【每个3分】
18. 1.曲线 【2分】 2。氯化钾 3.蒸发溶剂 4.30 【2分】 5.硫酸镁
19.1)离子 (2)2O 3Na+ (3)①⑤【2分】
20. (1) H2SO4 + 2NaOH = Na2SO4 + 2H2O 【每个3分】
(2) 2NaOH + CO2 = Na2CO3 + H2O
(3) Ca(OH)2 + Na2CO3 = CaCO3↓+ 2NaOH。
21. (1)C; H2 ; (2) ①3CO+ Fe2O3 高温 2Fe + 3CO2; ②Fe + CuSO4 === FeSO4 + Cu;【每个3分】
(3)置换反应。
三、实验与探【共10分】
22.
1.. ②⑤; ①③⑤;
(2)用弹簧夹夹紧橡皮管,向长颈漏斗中注入水至长颈漏斗下端管口浸没液面以下,继续加水,然后观察长颈漏斗管中的液面高度是否变化,如果液面不下降则说明气密性好;(合理叙述也给分)【2分】
(3)防止冷凝水倒流使试管炸裂;【2分】
(4) ①过早收集,没等导管口有连续且均匀的气泡冒出就开始收集;
②收集前集气瓶中的水没有装满,留有气泡。【答一种即可】
(5)如制取氢气【3分】
四、信息与分析【共10分】
23.(1)①淡蓝色气体;②具有强氧化性;③用于游泳池、生活用水、污水的杀菌和消毒;
(2)构成它们各自分子的氧原子的个数不同;
(3) 3O2 放电 2O3;
(4) 6P + 5O3 点燃 3P2O5
(5)言之有理即可【3~~~5每小题2分】
五、计算与应用【共10分】
24 【10分】 1。 3克 【4分】 2。 4.5%【6分】
2011福建省重点高中新生入学选拔统一考试
化学答题卷
题号 一 二 三 四 五 统计得分
得分
一、选择题【共30分】
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案
二、填空与简答【共40分】
16.(1)___________
(2)___________ __________________ ________________
17. (1)____________________________________
(2)____________________________________
18. (1)请画曲线
(2)_____________
(3)_____________
(4)_____________
(5)_____________
19. (1)______________
(2)_________ ____________
(3)_______________
20(1)___________________________________
(2)___________________________________
(3)___________________________________
21(1)_______________ _______________
(2)___________________________________
___________________________________
(3)_______________
三、实验与探究【10分】
22.(1)_______________ ______________
(2)___________________________________
(3)___________________________________
(4)___________________________________
(5)___________________________________
四、信息与分析【10分】
23.(1)_______________ ______________ ______________
(2)___________________________________
(3)___________________________________
(4)___________________________________
(5)___________________________________
五、计算与应用【10分】
24.此题请在本卷背面作答!!
【祝贺你成功完成了整卷,再认真检查一遍吧!】
<<化 学>> 试 题
(试卷满分:100分;考试时间:90分钟)
考生注意:1.本学科有两份试卷,一是答题卡,另一是本试题(共5页24题)。请将全部答案填在答题卡的相应答题栏内,否则不能得分!
2.可能用到的相对原子质量:H—1 C—12 O—16 K-39 Ca—40
一、选择题(本题15小题,共30分,每小题仅有一个正确选项,请在答题卡选择题栏内用黑色签字笔填写你的答案)
题记:化学此在我们身边,化学与我们息息相关
1.小明的食谱中有猪肉、米饭、食盐、矿泉水。从均衡营养的角度,小明还需增加摄入
A.蛋白质 B.糖类 C.无机盐 D.维生素
2.钙是人体不可缺少的重要元素,下列有关钙原子结构的说法正确的是
A.质子数为20 B.电子层数为3
C.最外层电子数为10 D.核外电子数为40
3.下列说法,你认为正确的是
A.人类利用的能量都是通过化学反应获得的
B.现代化学技术可在只有水的条件下生产汽油
C.CO2会使全球变暖,所以大气中CO2越少越好
D.在使用乙醇等新型燃料时,也要注意可能造成的环境污染
4.下列事故处理方法,不正确的是
A.电器着火,立即用水扑灭
B.炒菜时油锅着火,立即盖上锅盖
C.厨房煤气管道漏气,立即关闭阀门并开窗通风
D.图书馆内图书着火,立即用液态二氧化碳灭火器扑灭
5.常用抗生素“先锋Ⅵ”为粉末状固体,每瓶含“先锋Ⅵ”0.5g,注射时应配成质量分数不高于20%的溶液,则使用时每瓶至少需加入蒸馏水
A.1mL B. 2 mL C. 3mL D. 4 mL
题记:化学是二十一世纪最有用,最有创造力的中心学科
6.在厦参加国际磷化学会议的科学家认为无磷洗涤剂洗涤效果差,污染更严重,建议在建立磷回收机制后,重新使用加有磷化合物的含磷洗涤剂。对此的下列说法不正确的是
A.含磷洗涤剂含有磷元素 B.只要解决污染问题,可能重新使用含磷洗涤剂
C.含磷洗涤剂含有磷单质 D.研究高效无污染的洗涤剂仍是化学家的任务
7.我们看到“农家乐”灶炉膛中柴禾架空时烧得更旺。这是因为
A.散热更快 B.温度降低到着火点以下
C.使着火点降低 D.柴禾与空气中氧气接触更充分
8用右图所示的简易净水器处理浑浊的河水,下面对该净水器分析正确的是
A.能杀菌消毒 B.净化后的水属于纯净物
C.活性炭的主要作用是吸附 D.能将硬水变为软水
9.“厦钨股份”正在研究和利用的白钨矿,其有效成分CaWO4中
钨元素(w)的化合价为
A. +2 B.+3 C.+6 D.+7
10.右图是某燃煤发电厂处理废气的装置示意图。下列说法正确的是
A此过程中发生了分解,化合,中和反应
B使用此废气处理装置可减少酸雨的形成
C此过程中S元素的化合价未发生改变
D整个过程的反应可表示为:SO2+CaCO3 ===CaSO4 + CO2
题记:创新是民族发展的根本,在活动中学习是创新的起源
11.小明在研究碳酸钠、碳酸氢钠两种物质时的下列做法,不正确的是
A.采用网上查询的方法,查阅两种物质的有关资料
B.采用调查的方法,了解这两种物质在家庭生活中的应用情况
C.采用实验的方法,研究碳酸钠溶液和碳酸氢钠溶液的酸碱性
D.采用将样品分别与盐酸反应检验是否有二氧化碳生成的实验,鉴别这两种物质
12.为研究铁丝的粗细对铁在氧气中燃烧的影响,下列实验能达到目的的是
A.在同一瓶氧气中,先后进行不同粗、细铁丝的燃烧实验
B.在两瓶不同浓度的氧气中,分别同时进行粗、细铁丝的燃烧实验
C.在两瓶相同浓度的氧气中,分别同时进行粗、细铁丝的燃烧实验
D.在两瓶不同浓度的氧气中,分别同时进行相同铁丝的燃烧实验
13. 下列实验操作正确的是
14.在“人吸人的空气和呼出的气体有什么不同”的探究中,下列说法不正确的是
A.证明呼出气体含二氧化碳多的证据是:呼出的气体使澄清石灰水更浑浊
B.证明呼出气体含氧气少的证据是:呼出的气体使木条燃烧更旺
C.证明呼出气体含水蒸汽多的证据是:呼出的气体在玻璃上结下水珠
D.判断呼出气体含有氮气的依据是:空气中含有氮气,而氮气不为人体吸收
15.下表列出了除去物质中所含少量杂质的方法,其中错误的是
物质 所含杂质 除去杂质的方法
A CO2 CO 点燃
B NaCl 泥沙 溶解、过滤、蒸发
C Cu(NO3)2溶液 AgNO3 加入过量的铜粉,过滤
D NaOH溶液 Na2CO3 加入适量的氢氧化钙溶液,过滤
二、填空与简答(本题共6小题,共40分)
16.(4分)请应用“物质性质决定用途”的规律,完成下表:
物质化学式 性 质 用 途
例子 CO2 在一定温度下能形成固体 制作干冰,用于人工降雨
(1) 在空气中可燃烧 可作为汽车燃料
(2)
17.(6分)写出下列反应的化学方程式:
(1)实验室制取氧气(写一个): ;
(2)碳酸氢钠受热分解生成碳酸钠、水和二氧化碳: 。
18.(7分)海水日晒后得到的晶体是粗盐,剩余的液体称为苦卤,苦卤中除氯化钠外还含氯化镁、硫酸镁、氯化钾,在食品、化工等方面有重要应用。
氯化镁在不同温度下的溶解度表
温度℃ 0 60 90 120
溶解度(g/100g水) 50 60 70 80
(1)请在右边溶解度曲线图上添加氯化镁的溶解度曲线【2分】
(2)0℃时, 的溶解度最小。
(3)欲从氯化钠的饱和溶液中析出氯化钠晶体,最好采用 ————————的方法
(4) 60℃时,80g氯化镁饱和溶液中含溶质 g【2分】
(5)将60℃的苦卤继续加热蒸发,根据溶解度曲线,首先析出的晶体应是 。
19. (5分)建立宏观、微观和符号之间的联系是化学学科的特点。
(1)构成氯化钠的基本微粒是 (填“分子”、“原子”或“离子”)。
(2)用符号表示下列微粒。2个氧原子 ;3个钠离子 。
(3)A、B、C、D表示4种物质,其微观示意图见下表。A和B在一定条件下反应可生成C和D。 下列说法正确的是 (填数字序号)。【2分】
①4种物质均由分子构成 ②该反应属于置换反应
③C、D两种物质的质量比为11:7 ④4种物质中属于氧化物的是A、B
20.(9分)写出将下列物质中所含杂质转化为主要成分的化学方程式(括号内的为杂质):
(1)Na2SO4 ( H2SO4 ): ;
(2)Na2CO3(NaOH): ;
(3)NaOH(Na2CO3): 。
21.(9分)常见金属D的制取与转化关系如下(有些反应物和生成物已略去):
友情提醒:本题中的字母是物质代号,不是元素符号。
(1)写出下列物质的化学式:
A是 ;E是 ;
(2)写出上图中①②两反应的化学方程式:
① ;【3分】
② ;【3分】
(3)反应③的基本反应类型是: 。
三、实验与探究(本题1小题,共10分)
22.某同学用下图装置制氧气,请问答:
(1)用高锰酸钾制取和收集氧气的装置应选用 (填序号);用双氧水和二氧化锰制取和收集干燥的氧气的装置应选用 (填序号);
(2)检查装置①气密性的方法是: 【2分】
(3)装置②试管口要略向下倾斜的原因是:
(4)若用装置④收集的氧气不纯,其原因可能是(请写一种原因):【2分】
;
(5)有一种气体可以用装置1,3,6来制取,请写出反应方程式—————————【3分】
四、信息与分析(本题1小题,共10分)
23.阅读材料,回答问题:
材料1.臭氧是淡蓝色气体,大气中的臭氧层能有效阻挡紫外线,保护地球的生存环境,但目前南极出现了臭氧层空洞,并有继续扩大的趋势。
材料2.复印机在工作时,会因高压放电产生一定浓度的臭氧。长期吸入大量臭氧会引 起口干舌燥,咳嗽等不适症状,还可能诱发中毒性肺气肿。
材料3.臭氧发生器是在高压电极的作用下将空气中的氧气转化为臭氧(化学式为O3)的装置。利用臭氧的强氧化性,可将其应用于游泳池、生活用水、污水的杀菌和消毒。
(1)请总结臭氧的有关知识:①物理性质: ;
②化学性质: ;③用途: ;
(2)请从分子构成的角度,指出氧气和臭氧的不同点: ;
(3)写出材料3中氧气转化为臭氧的化学方程式: ;
(4)磷在臭氧中燃烧与在氧气中燃烧相似,请写出磷在臭氧中燃烧的化学方程式:
;
(5)请提出一个缩小臭氧层空洞的设想: 。
五、计算与应用(本题1小题,共10分)
24.食醋是家庭常用的调味品。某兴趣小组同学为探究食醋中醋酸(乙酸)的质量分数设计并进行了如下实验:取10%的氢氧化钠溶液(密度为1.2g/mL)逐滴加入到100g食醋中,当滴入25mL该氢氧化钠溶液时正好完全中和。已知反应化学方程式如下:CH3COOH + NaOH → CH3COONa + H2O,
请你完成探究实验中的相关计算:
⑴实验中消耗的25mL氢氧化钠溶液中溶质的物质的量是多少?
⑵食醋中醋酸的质量分数是多少
【友情提醒:试题结束,请认真检查。】
2011福建省重点高中新生入学选拔统一考试
化学试题参考答案
一、选择题【共30分】
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 D A D A B C D C C B D C C B D
二、填空与简答【共40分】【每空一分,除标明外】
16.C2H5OH CO 在空气中可燃烧 可作为气体燃料
17.(1) 或 2KMnO4 △ K2MnO4 + MnO2 + O2↑
(2)2NaHCO3 △ Na2CO3+H2O+CO2↑ 。【每个3分】
18. 1.曲线 【2分】 2。氯化钾 3.蒸发溶剂 4.30 【2分】 5.硫酸镁
19.1)离子 (2)2O 3Na+ (3)①⑤【2分】
20. (1) H2SO4 + 2NaOH = Na2SO4 + 2H2O 【每个3分】
(2) 2NaOH + CO2 = Na2CO3 + H2O
(3) Ca(OH)2 + Na2CO3 = CaCO3↓+ 2NaOH。
21. (1)C; H2 ; (2) ①3CO+ Fe2O3 高温 2Fe + 3CO2; ②Fe + CuSO4 === FeSO4 + Cu;【每个3分】
(3)置换反应。
三、实验与探【共10分】
22.
1.. ②⑤; ①③⑤;
(2)用弹簧夹夹紧橡皮管,向长颈漏斗中注入水至长颈漏斗下端管口浸没液面以下,继续加水,然后观察长颈漏斗管中的液面高度是否变化,如果液面不下降则说明气密性好;(合理叙述也给分)【2分】
(3)防止冷凝水倒流使试管炸裂;【2分】
(4) ①过早收集,没等导管口有连续且均匀的气泡冒出就开始收集;
②收集前集气瓶中的水没有装满,留有气泡。【答一种即可】
(5)如制取氢气【3分】
四、信息与分析【共10分】
23.(1)①淡蓝色气体;②具有强氧化性;③用于游泳池、生活用水、污水的杀菌和消毒;
(2)构成它们各自分子的氧原子的个数不同;
(3) 3O2 放电 2O3;
(4) 6P + 5O3 点燃 3P2O5
(5)言之有理即可【3~~~5每小题2分】
五、计算与应用【共10分】
24 【10分】 1。 3克 【4分】 2。 4.5%【6分】
2011福建省重点高中新生入学选拔统一考试
化学答题卷
题号 一 二 三 四 五 统计得分
得分
一、选择题【共30分】
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案
二、填空与简答【共40分】
16.(1)___________
(2)___________ __________________ ________________
17. (1)____________________________________
(2)____________________________________
18. (1)请画曲线
(2)_____________
(3)_____________
(4)_____________
(5)_____________
19. (1)______________
(2)_________ ____________
(3)_______________
20(1)___________________________________
(2)___________________________________
(3)___________________________________
21(1)_______________ _______________
(2)___________________________________
___________________________________
(3)_______________
三、实验与探究【10分】
22.(1)_______________ ______________
(2)___________________________________
(3)___________________________________
(4)___________________________________
(5)___________________________________
四、信息与分析【10分】
23.(1)_______________ ______________ ______________
(2)___________________________________
(3)___________________________________
(4)___________________________________
(5)___________________________________
五、计算与应用【10分】
24.此题请在本卷背面作答!!
【祝贺你成功完成了整卷,再认真检查一遍吧!】
同课章节目录
