鲁科版(2019)高中化学 选择性必修一 第1章 微项目 设计载人航天器用化学电池与氧气再生方案 导学课件(31张ppt)
文档属性
| 名称 | 鲁科版(2019)高中化学 选择性必修一 第1章 微项目 设计载人航天器用化学电池与氧气再生方案 导学课件(31张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-08-04 00:00:00 | ||
图片预览











文档简介
※微项目※
设计载人航天器用化学电池与氧气再生方案
——化学反应中能量及物质的转化利用
知识铺垫
必备知识
正误判断
1.请写出碱性氢氧燃料电池的电极反应和电池反应。
?
?
?
2.实验室如何将CO2转化为O2?载人航天器中人员呼吸需要的O2从何而来?
提示:负极反应为:2H2+4OH--4e- === 4H2O,正极反应为:O2+2H2O+4e- === 4OH-,电池反应为2H2+O2 === 2H2O。
提示:实验室利用Na2O2与CO2反应可生成O2;通过化学反应将航天器内人体产生的CO2转化为O2,从而为航天人员提供O2。
知识铺垫
必备知识
正误判断
1.氢氧燃料电池分为酸性和碱性两种
2H2-4e- === 4H+
2H2+4OH--4e- === 4H2O
O2+4e-+4H+ === 2H2O
O2+2H2O+4e- === 4OH-
2.“神舟”飞船中的镍镉电池工作原理
镉镍电池中Cd作为负极,NiOOH作为正极,通过放电反应释放能量,总反应: 。?
知识铺垫
必备知识
正误判断
判断下列说法是否正确,正确的打“√”,错误的打“×”。
(1)理论上说,任何可燃物气体与氧气都可设计成燃料电池。 ( )
(2)在燃料电池中,发生氧化反应的一极一定是可燃气体。( )
(3)用Pt作为电极,用KOH溶液作为电解质溶液构成燃料电池,通入氧气的一极一定是正极。( )
(4)飞船中电池工作时,KOH溶液中的阳离子向负极移动。( )
(5)氢氧燃料电池能量比氢气直接燃烧产生的能量效率高。 ( )
(6)镍镉电池工作时,当电路中转移0.1 mol电子时,负极增重1.7 g。( )
√
√
√
×
√
√
探究一
探究二
随堂检测
尝试设计载人航天器用化学电池
问题探究
航天器中经常使用的化学电池有哪些?哪种更适合做短寿命载人航天器的电源?
?
?
?
提示:航天器中经常使用的化学电池有镍镉电池、镍氢电池、氢氧燃料电池等。与其他化学电池相比,氢氧燃料电池具有单位质量输出电能较高、反应生成的水可作为航天员的饮用水、氧气可以作为备用氧源供给航天员呼吸等优点,因此更适合做短寿命载人航天器的电源。
探究一
探究二
随堂检测
深化拓展
1.“阿波罗”飞船燃料电池的工作原理
(1)“阿波罗”飞船燃料电池(离子导体为KOH溶液)
负极反应为:2H2+4OH--4e- === 4H2O,正极反应为:O2+2H2O+4e- === 4OH-
(2)“阿波罗”登月飞船一代燃料电池(离子导体为H2SO4溶液)
负极反应为:2H2-4e- === 4H+,正极反应为:O2+4H++4e- === 2H2O
2.“神舟”飞船中的化学电池的工作原理
镍镉碱性蓄电池电极反应为:
负极 Cd+2OH--2e- === Cd(OH)2
正极 2NiOOH+2H2O+2e- === 2Ni(OH)2+2OH-
总反应式 Cd+2NiOOH+2H2O 2Ni(OH)2+Cd(OH)2
探究一
探究二
随堂检测
素能应用
典例1镉镍可充电电池的充、放电反应原理如下:Cd+2NiOOH+2H2O Cd(OH)2+2Ni(OH)2。下列说法错误的是( )
A.放电时,Cd作为负极
B.放电时,NiOOH作为负极
C.电解质溶液为碱性溶液
D.放电时,负极反应为Cd+2OH--2e- === Cd(OH)2
答案:B
解析:镉镍电池放电时,Cd作为负极,电极反应为Cd+2OH--2e- === Cd(OH)2;NiOOH作为正极,电解质溶液为碱性溶液,B项错误。
探究一
探究二
随堂检测
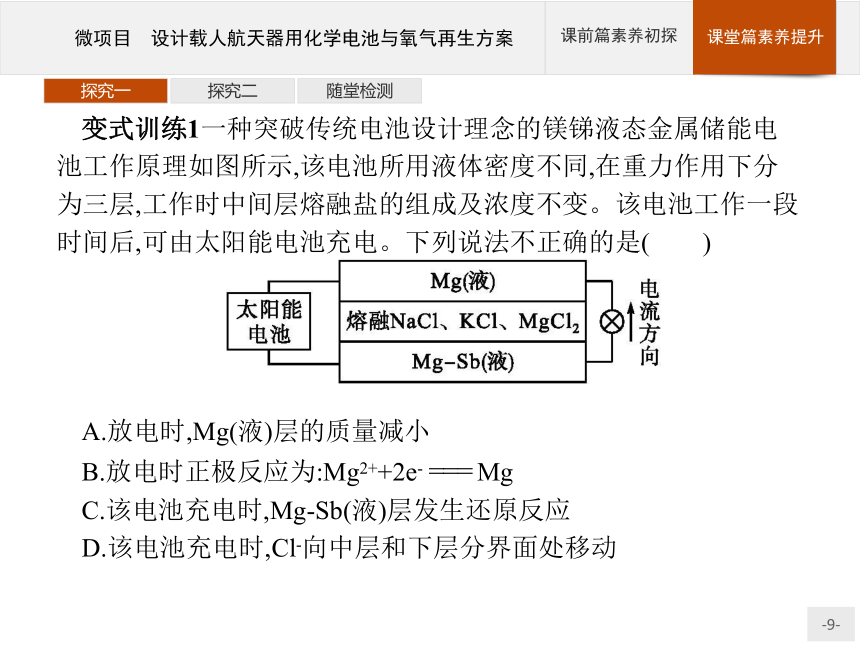
变式训练1一种突破传统电池设计理念的镁锑液态金属储能电池工作原理如图所示,该电池所用液体密度不同,在重力作用下分为三层,工作时中间层熔融盐的组成及浓度不变。该电池工作一段时间后,可由太阳能电池充电。下列说法不正确的是( )
A.放电时,Mg(液)层的质量减小
B.放电时正极反应为:Mg2++2e- === Mg
C.该电池充电时,Mg-Sb(液)层发生还原反应
D.该电池充电时,Cl-向中层和下层分界面处移动
探究一
探究二
随堂检测
答案:C
解析:放电时,负极Mg失电子生成镁离子,则Mg(液)层的质量减小,A项正确;正极镁离子得电子得到Mg,则放电时正极反应为:Mg2++2e- === Mg,B项正确;该电池充电时,Mg-Sb(液)层为阳极,阳极发生失电子的氧化反应,C项错误;该电池充电时,阴离子向阳极移动,即Cl-向中层和下层分界面处移动,D项正确。
探究一
探究二
随堂检测
尝试设计载人航天器的氧气再生方案
问题探究
在设计航天器中氧气的获取方案时,应注意什么?
?
?
提示:载人航天器中的物质和能量资源都十分宝贵。在设计氧气的获取方案时,要尽可能地将人体代谢物中的氧元素转化为氧气,从而保证氧元素的持续循环。
探究一
探究二
随堂检测
深化拓展
1.计算萨巴蒂尔反应的焓变
探究一
探究二
随堂检测
2.利用萨巴蒂尔反应再生氧气的大体流程
3.项目成果展示
(1)探究载人航天器的化学电源和氧气再生办法。
探究一
探究二
随堂检测
(2)书写新型电池电极反应的一般步骤。
探究一
探究二
随堂检测
素能应用
典例2为了实现空间站的零排放,循环利用人体呼出的CO2来提供O2,我国科学家设计了如图装置。反应后,电解质溶液的pH保持不变。下列说法正确的是 ( )
A.图中N型半导体为正极,P型半导体为负极
B.Y电极的反应:4OH--4e- === 2H2O+O2↑
C.图中离子交换膜为阳离子交换膜
D.该装置实现了“太阳能→化学能→电能”的转化
探究一
探究二
随堂检测
答案:B
解析:根据装置图中电荷移动的方向可知,N型半导体为负极,P型半导体为正极,A项错误;Y电极连接电源的正极,作为阳极,根据电解原理,电极反应为4OH--4e- === 2H2O+O2↑,B项正确;反应后,电解质溶液的pH保持不变,离子交换膜应为阴离子交换膜,C项错误;该装置实现了“太阳能→电能→化学能”的转化,D项错误。
探究一
探究二
随堂检测
变式训练2为循环利用人体呼出的CO2并提供氧气,我国科学家设计了一种装置(如图所示),实现“太阳能→电能→化学能”的转化,总反应为2CO2 === 2CO+O2,下列有关说法不正确的是( )
A.该装置属于电解池
B.X极发生氧化反应,Y极发生还原反应
C.人体呼出的水蒸气参与Y极反应:CO2+H2O+2e- === CO+2OH-
D.X极每产生标准状况下22.4 L气体,有2 mol的OH-从Y极移向X极
探究一
探究二
随堂检测
答案:D
解析:题给装置实现“太阳能—电能—化学能”的转化,将电能转化为化学能的装置为电解池,A项正确;根据图中电子的流向“X→Y”可知,X极为阳极,失电子发生氧化反应,Y为阴极,得电子发生还原反应,B项正确;Y为阴极,根据总反应可知,阴极为CO2得电子生成CO,电极反应为CO2+H2O+2e- === CO+2OH-,C项正确;X极为阳极,OH-放电生成氧气,电极反应为4OH--4e- === 2H2O+O2↑,生成1 mol O2,阳极有4 mol OH-放电,根据溶液电中性原理,X电极区阴离子减少,则会有4 mol OH-从Y极透过阴离子交换膜移向X极,使得溶液保持电中性,D项错误。
探究一
探究二
随堂检测
1.(2019安徽宿州高二质检)太阳能光电池具有可靠稳定、寿命长、安装维护简便等优点,现已得到广泛应用。氮化镓(GaN)光电池的结构如图所示。下列说法中正确的是( )
A.该装置系统中只存在光能与电能之间的转化
B.Cu电极上的电极反应为CO2+8H+-8e- === CH4+2H2O
C.工作时,产生的O2、CH4体积比为1∶1(同温同压)
D.离子交换膜为质子交换膜,H+从左池移向右池
探究一
探究二
随堂检测
答案:D
解析:由题图可知,该装置系统中存在太阳能与化学能、化学能与电能等的转化,A错误;CO2在Cu电极上发生还原反应生成CH4,则电极反应为CO2+8H++8e- === CH4+2H2O,B错误;H2O在GaN电极上发生氧化反应生成O2,电极反应为2H2O-4e- === 4H++O2↑,根据得失电子守恒可知,产生O2和CH4的物质的量之比为2∶1,即在同温同压下的体积比为2∶1,C错误;由上述分析可知左池产生H+,右池消耗H+,则离子交换膜为质子交换膜,H+向正极移动,即H+从左池移向右池,D正确。
探究一
探究二
随堂检测
2.(2019黑龙江哈尔滨高三月考)一种熔融碳酸盐燃料电池原理示意如图。有关该电池的说法正确的是( )
探究一
探究二
随堂检测
答案:B
探究一
探究二
随堂检测
3.(2019北京朝阳区高二测试)我国科研人员借助太阳能,将光解水制H2与脱硫结合起来,既能大幅度提高光解水制H2的效率,又能脱除SO2,工作原理如图所示。下列说法不正确的是( )
A.该装置可将太阳能转化为化学能
B.催化剂a表面发生还原反应,产生H2
C.催化剂b附近的溶液pH增大
D.吸收1 mol SO2,理论上能产生1 mol H2
探究一
探究二
随堂检测
答案:C
解析:在光解水的过程中,存在将太阳能转化为化学能的过程,A项正确;根据示意图,a电极为得到电子的一极,发生还原反应。电解水的反应为2H2O 2H2↑+O2↑,得到电子一极产生氢气,B项正确;b电极为电子流出的一极,发生氧化反应,电极反应为2H2O-4e- === O2↑+4H+,则b极附近溶液pH减小,C项错误;在b极附近,氧气、二氧化硫,以及水生成硫酸,1 mol SO2生成H2SO4时转移2 mol电子,根据得失电子守恒,同时会产生1 mol氢气,D项正确。
探究一
探究二
随堂检测
4.(2019湖南岳阳高二质检)一种“全氢电池”的工作原理如图所示。下列说法不正确的是( )
探究一
探究二
随堂检测
A.电子流向是从吸附层M通过导线到吸附层N
B.Na+从左边穿过离子交换膜向右边移动
C.离子交换膜可用质子交换膜
D.负极的电极反应是:H2-2e-+2OH- === 2H2O
答案:C
解析:根据图示分析,电子流动方向是从M通过导线到N,故A项正确;原电池中,阳离子从负极移向正极,所以Na+从左边穿过离子交换膜向右边移动,故B项正确;离子交换膜可阻止左边的碱性溶液和右边的酸性溶液发生中和,不能用质子交换膜,故C项错误;原电池的负极发生氧化反应,由于负极为碱性溶液,所以负极的电极反应是H2-2e-+2OH- === 2H2O,故D项正确。
探究一
探究二
随堂检测
5.(2019陕西西安长安区第五中学高三期中)一种钌(Ru)基配合物光敏染料敏化太阳能电池的工作原理及电池中发生的主要反应如图所示。下列说法正确的是( )
A.镀铂导电玻璃的作用是传递I-
B.电池工作时,光能转变为电能,X为电池的正极
C.电池的电解质溶液中I-和 的浓度均不断减小
D.电解质溶液中发生反应2Ru3++3I- === 2Ru2++
探究一
探究二
随堂检测
答案:D
探究一
探究二
随堂检测
6.科学家们发明了一种能够给电子设备提供动力的生物燃料电池。该电池包括两个涂覆着酶的电极,它们处于充满空气和少量氢气的玻璃槽中。由于气体可以混合从而省去了昂贵的燃料隔离膜,其工作原理如图所示。下列说法正确的是( )
A.左边为该电池的负极
B.该电池可在高温环境下使用
C.该电池负极反应为H2-2e- === 2H+
D.该电池正极反应为O2+4e- === 2O2-
答案:C
解析:由电池示意图可知,H2→H+是H2被氧化的过程,通入H2的一极为原电池的负极,发生反应:H2-2e- === 2H+;O2→H2O是O2被还原的过程,通入O2的一极为原电池的正极,发生反应:O2+4H++4e- === 2H2O,故A、D错误,C正确;该电池包括两个涂覆着酶的电极,高温下会使酶变性,不能在高温下使用,B错误。
探究一
探究二
随堂检测
7.氨氧燃料电池具有很大的发展潜力。氨氧燃料电池工作原理如下图所示。
(1)a电极的电极反应为 ;?
(2)为了使碱溶液浓度不变,一段时间后,需向装置中补充KOH,请依据反应原理解释原因: 。?
探究一
探究二
随堂检测
答案:(1)2NH3+6OH--6e- === N2+6H2O
(2)发生反应4NH3+3O2 === 2N2+6H2O,有水生成,使得溶液逐渐变稀,所以要补充KOH
解析:(1)a电极是通入NH3的电极,NH3失去电子发生氧化反应,所以该电极为负极,电极反应是2NH3+6OH--6e- === N2+6H2O。
(2)一段时间后,需向装置中补充KOH,原因是发生反应4NH3+3O2 === 2N2+6H2O,有水生成,使得溶液逐渐变稀,为了维持碱溶液的浓度不变,所以要补充KOH。
设计载人航天器用化学电池与氧气再生方案
——化学反应中能量及物质的转化利用
知识铺垫
必备知识
正误判断
1.请写出碱性氢氧燃料电池的电极反应和电池反应。
?
?
?
2.实验室如何将CO2转化为O2?载人航天器中人员呼吸需要的O2从何而来?
提示:负极反应为:2H2+4OH--4e- === 4H2O,正极反应为:O2+2H2O+4e- === 4OH-,电池反应为2H2+O2 === 2H2O。
提示:实验室利用Na2O2与CO2反应可生成O2;通过化学反应将航天器内人体产生的CO2转化为O2,从而为航天人员提供O2。
知识铺垫
必备知识
正误判断
1.氢氧燃料电池分为酸性和碱性两种
2H2-4e- === 4H+
2H2+4OH--4e- === 4H2O
O2+4e-+4H+ === 2H2O
O2+2H2O+4e- === 4OH-
2.“神舟”飞船中的镍镉电池工作原理
镉镍电池中Cd作为负极,NiOOH作为正极,通过放电反应释放能量,总反应: 。?
知识铺垫
必备知识
正误判断
判断下列说法是否正确,正确的打“√”,错误的打“×”。
(1)理论上说,任何可燃物气体与氧气都可设计成燃料电池。 ( )
(2)在燃料电池中,发生氧化反应的一极一定是可燃气体。( )
(3)用Pt作为电极,用KOH溶液作为电解质溶液构成燃料电池,通入氧气的一极一定是正极。( )
(4)飞船中电池工作时,KOH溶液中的阳离子向负极移动。( )
(5)氢氧燃料电池能量比氢气直接燃烧产生的能量效率高。 ( )
(6)镍镉电池工作时,当电路中转移0.1 mol电子时,负极增重1.7 g。( )
√
√
√
×
√
√
探究一
探究二
随堂检测
尝试设计载人航天器用化学电池
问题探究
航天器中经常使用的化学电池有哪些?哪种更适合做短寿命载人航天器的电源?
?
?
?
提示:航天器中经常使用的化学电池有镍镉电池、镍氢电池、氢氧燃料电池等。与其他化学电池相比,氢氧燃料电池具有单位质量输出电能较高、反应生成的水可作为航天员的饮用水、氧气可以作为备用氧源供给航天员呼吸等优点,因此更适合做短寿命载人航天器的电源。
探究一
探究二
随堂检测
深化拓展
1.“阿波罗”飞船燃料电池的工作原理
(1)“阿波罗”飞船燃料电池(离子导体为KOH溶液)
负极反应为:2H2+4OH--4e- === 4H2O,正极反应为:O2+2H2O+4e- === 4OH-
(2)“阿波罗”登月飞船一代燃料电池(离子导体为H2SO4溶液)
负极反应为:2H2-4e- === 4H+,正极反应为:O2+4H++4e- === 2H2O
2.“神舟”飞船中的化学电池的工作原理
镍镉碱性蓄电池电极反应为:
负极 Cd+2OH--2e- === Cd(OH)2
正极 2NiOOH+2H2O+2e- === 2Ni(OH)2+2OH-
总反应式 Cd+2NiOOH+2H2O 2Ni(OH)2+Cd(OH)2
探究一
探究二
随堂检测
素能应用
典例1镉镍可充电电池的充、放电反应原理如下:Cd+2NiOOH+2H2O Cd(OH)2+2Ni(OH)2。下列说法错误的是( )
A.放电时,Cd作为负极
B.放电时,NiOOH作为负极
C.电解质溶液为碱性溶液
D.放电时,负极反应为Cd+2OH--2e- === Cd(OH)2
答案:B
解析:镉镍电池放电时,Cd作为负极,电极反应为Cd+2OH--2e- === Cd(OH)2;NiOOH作为正极,电解质溶液为碱性溶液,B项错误。
探究一
探究二
随堂检测
变式训练1一种突破传统电池设计理念的镁锑液态金属储能电池工作原理如图所示,该电池所用液体密度不同,在重力作用下分为三层,工作时中间层熔融盐的组成及浓度不变。该电池工作一段时间后,可由太阳能电池充电。下列说法不正确的是( )
A.放电时,Mg(液)层的质量减小
B.放电时正极反应为:Mg2++2e- === Mg
C.该电池充电时,Mg-Sb(液)层发生还原反应
D.该电池充电时,Cl-向中层和下层分界面处移动
探究一
探究二
随堂检测
答案:C
解析:放电时,负极Mg失电子生成镁离子,则Mg(液)层的质量减小,A项正确;正极镁离子得电子得到Mg,则放电时正极反应为:Mg2++2e- === Mg,B项正确;该电池充电时,Mg-Sb(液)层为阳极,阳极发生失电子的氧化反应,C项错误;该电池充电时,阴离子向阳极移动,即Cl-向中层和下层分界面处移动,D项正确。
探究一
探究二
随堂检测
尝试设计载人航天器的氧气再生方案
问题探究
在设计航天器中氧气的获取方案时,应注意什么?
?
?
提示:载人航天器中的物质和能量资源都十分宝贵。在设计氧气的获取方案时,要尽可能地将人体代谢物中的氧元素转化为氧气,从而保证氧元素的持续循环。
探究一
探究二
随堂检测
深化拓展
1.计算萨巴蒂尔反应的焓变
探究一
探究二
随堂检测
2.利用萨巴蒂尔反应再生氧气的大体流程
3.项目成果展示
(1)探究载人航天器的化学电源和氧气再生办法。
探究一
探究二
随堂检测
(2)书写新型电池电极反应的一般步骤。
探究一
探究二
随堂检测
素能应用
典例2为了实现空间站的零排放,循环利用人体呼出的CO2来提供O2,我国科学家设计了如图装置。反应后,电解质溶液的pH保持不变。下列说法正确的是 ( )
A.图中N型半导体为正极,P型半导体为负极
B.Y电极的反应:4OH--4e- === 2H2O+O2↑
C.图中离子交换膜为阳离子交换膜
D.该装置实现了“太阳能→化学能→电能”的转化
探究一
探究二
随堂检测
答案:B
解析:根据装置图中电荷移动的方向可知,N型半导体为负极,P型半导体为正极,A项错误;Y电极连接电源的正极,作为阳极,根据电解原理,电极反应为4OH--4e- === 2H2O+O2↑,B项正确;反应后,电解质溶液的pH保持不变,离子交换膜应为阴离子交换膜,C项错误;该装置实现了“太阳能→电能→化学能”的转化,D项错误。
探究一
探究二
随堂检测
变式训练2为循环利用人体呼出的CO2并提供氧气,我国科学家设计了一种装置(如图所示),实现“太阳能→电能→化学能”的转化,总反应为2CO2 === 2CO+O2,下列有关说法不正确的是( )
A.该装置属于电解池
B.X极发生氧化反应,Y极发生还原反应
C.人体呼出的水蒸气参与Y极反应:CO2+H2O+2e- === CO+2OH-
D.X极每产生标准状况下22.4 L气体,有2 mol的OH-从Y极移向X极
探究一
探究二
随堂检测
答案:D
解析:题给装置实现“太阳能—电能—化学能”的转化,将电能转化为化学能的装置为电解池,A项正确;根据图中电子的流向“X→Y”可知,X极为阳极,失电子发生氧化反应,Y为阴极,得电子发生还原反应,B项正确;Y为阴极,根据总反应可知,阴极为CO2得电子生成CO,电极反应为CO2+H2O+2e- === CO+2OH-,C项正确;X极为阳极,OH-放电生成氧气,电极反应为4OH--4e- === 2H2O+O2↑,生成1 mol O2,阳极有4 mol OH-放电,根据溶液电中性原理,X电极区阴离子减少,则会有4 mol OH-从Y极透过阴离子交换膜移向X极,使得溶液保持电中性,D项错误。
探究一
探究二
随堂检测
1.(2019安徽宿州高二质检)太阳能光电池具有可靠稳定、寿命长、安装维护简便等优点,现已得到广泛应用。氮化镓(GaN)光电池的结构如图所示。下列说法中正确的是( )
A.该装置系统中只存在光能与电能之间的转化
B.Cu电极上的电极反应为CO2+8H+-8e- === CH4+2H2O
C.工作时,产生的O2、CH4体积比为1∶1(同温同压)
D.离子交换膜为质子交换膜,H+从左池移向右池
探究一
探究二
随堂检测
答案:D
解析:由题图可知,该装置系统中存在太阳能与化学能、化学能与电能等的转化,A错误;CO2在Cu电极上发生还原反应生成CH4,则电极反应为CO2+8H++8e- === CH4+2H2O,B错误;H2O在GaN电极上发生氧化反应生成O2,电极反应为2H2O-4e- === 4H++O2↑,根据得失电子守恒可知,产生O2和CH4的物质的量之比为2∶1,即在同温同压下的体积比为2∶1,C错误;由上述分析可知左池产生H+,右池消耗H+,则离子交换膜为质子交换膜,H+向正极移动,即H+从左池移向右池,D正确。
探究一
探究二
随堂检测
2.(2019黑龙江哈尔滨高三月考)一种熔融碳酸盐燃料电池原理示意如图。有关该电池的说法正确的是( )
探究一
探究二
随堂检测
答案:B
探究一
探究二
随堂检测
3.(2019北京朝阳区高二测试)我国科研人员借助太阳能,将光解水制H2与脱硫结合起来,既能大幅度提高光解水制H2的效率,又能脱除SO2,工作原理如图所示。下列说法不正确的是( )
A.该装置可将太阳能转化为化学能
B.催化剂a表面发生还原反应,产生H2
C.催化剂b附近的溶液pH增大
D.吸收1 mol SO2,理论上能产生1 mol H2
探究一
探究二
随堂检测
答案:C
解析:在光解水的过程中,存在将太阳能转化为化学能的过程,A项正确;根据示意图,a电极为得到电子的一极,发生还原反应。电解水的反应为2H2O 2H2↑+O2↑,得到电子一极产生氢气,B项正确;b电极为电子流出的一极,发生氧化反应,电极反应为2H2O-4e- === O2↑+4H+,则b极附近溶液pH减小,C项错误;在b极附近,氧气、二氧化硫,以及水生成硫酸,1 mol SO2生成H2SO4时转移2 mol电子,根据得失电子守恒,同时会产生1 mol氢气,D项正确。
探究一
探究二
随堂检测
4.(2019湖南岳阳高二质检)一种“全氢电池”的工作原理如图所示。下列说法不正确的是( )
探究一
探究二
随堂检测
A.电子流向是从吸附层M通过导线到吸附层N
B.Na+从左边穿过离子交换膜向右边移动
C.离子交换膜可用质子交换膜
D.负极的电极反应是:H2-2e-+2OH- === 2H2O
答案:C
解析:根据图示分析,电子流动方向是从M通过导线到N,故A项正确;原电池中,阳离子从负极移向正极,所以Na+从左边穿过离子交换膜向右边移动,故B项正确;离子交换膜可阻止左边的碱性溶液和右边的酸性溶液发生中和,不能用质子交换膜,故C项错误;原电池的负极发生氧化反应,由于负极为碱性溶液,所以负极的电极反应是H2-2e-+2OH- === 2H2O,故D项正确。
探究一
探究二
随堂检测
5.(2019陕西西安长安区第五中学高三期中)一种钌(Ru)基配合物光敏染料敏化太阳能电池的工作原理及电池中发生的主要反应如图所示。下列说法正确的是( )
A.镀铂导电玻璃的作用是传递I-
B.电池工作时,光能转变为电能,X为电池的正极
C.电池的电解质溶液中I-和 的浓度均不断减小
D.电解质溶液中发生反应2Ru3++3I- === 2Ru2++
探究一
探究二
随堂检测
答案:D
探究一
探究二
随堂检测
6.科学家们发明了一种能够给电子设备提供动力的生物燃料电池。该电池包括两个涂覆着酶的电极,它们处于充满空气和少量氢气的玻璃槽中。由于气体可以混合从而省去了昂贵的燃料隔离膜,其工作原理如图所示。下列说法正确的是( )
A.左边为该电池的负极
B.该电池可在高温环境下使用
C.该电池负极反应为H2-2e- === 2H+
D.该电池正极反应为O2+4e- === 2O2-
答案:C
解析:由电池示意图可知,H2→H+是H2被氧化的过程,通入H2的一极为原电池的负极,发生反应:H2-2e- === 2H+;O2→H2O是O2被还原的过程,通入O2的一极为原电池的正极,发生反应:O2+4H++4e- === 2H2O,故A、D错误,C正确;该电池包括两个涂覆着酶的电极,高温下会使酶变性,不能在高温下使用,B错误。
探究一
探究二
随堂检测
7.氨氧燃料电池具有很大的发展潜力。氨氧燃料电池工作原理如下图所示。
(1)a电极的电极反应为 ;?
(2)为了使碱溶液浓度不变,一段时间后,需向装置中补充KOH,请依据反应原理解释原因: 。?
探究一
探究二
随堂检测
答案:(1)2NH3+6OH--6e- === N2+6H2O
(2)发生反应4NH3+3O2 === 2N2+6H2O,有水生成,使得溶液逐渐变稀,所以要补充KOH
解析:(1)a电极是通入NH3的电极,NH3失去电子发生氧化反应,所以该电极为负极,电极反应是2NH3+6OH--6e- === N2+6H2O。
(2)一段时间后,需向装置中补充KOH,原因是发生反应4NH3+3O2 === 2N2+6H2O,有水生成,使得溶液逐渐变稀,为了维持碱溶液的浓度不变,所以要补充KOH。
同课章节目录
- 第1章 化学反应与能量转化
- 第1节 化学反应的热效应
- 第2节 化学能转化为电能——电池
- 第3节 电能转化为化学能——电解
- 第4节 金属的腐蚀与防护
- 微项目 设计载人航天器用化学电池与氧气再生方案——化学反应中能量及物质的转化利用
- 第2章 化学反应的方向、 限度与速率
- 第1节 化学反应的方向
- 第2节 化学反应的限度
- 第3节 化学反应的速率
- 第4节 化学反应条件的优化——工业合成氨
- 微项目 探讨如何利用工业废气中的二氧化碳合成甲醇——化学反应选择与反应条件优化
- 第3章 物质在水溶液中的行为
- 第1节 水与水溶液
- 第2节 弱电解质的电离 盐类的水解
- 第3节 沉淀溶解平衡
- 第4节 离子反应
- 微项目 揭秘索尔维制碱法和侯氏制碱法——化学平衡思想的创造性应用
