科粤版九年级上册化学2.4 辨别物质的元素组成 课件 (共18张PPT建议WPS打开)
文档属性
| 名称 | 科粤版九年级上册化学2.4 辨别物质的元素组成 课件 (共18张PPT建议WPS打开) |  | |
| 格式 | zip | ||
| 文件大小 | 4.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-08-04 22:45:39 | ||
图片预览





文档简介
(共18张PPT)
2.4
辨别物质的组成元素
新课导学
缺“钙”吃什么好呢?
想一想:几种名称中的“钙”、“锌”指的是什么?分子、原子,还是……?
元素
利用化学方法分析众多的物质,发现组成它们的基本成分—元素其实只有一百多种,就像可拼写出数十万个英文单词的字母只有26个一样。例如,水中的氧原子、二氧化碳中的氧原子、氧气中的氧原子,以及其他物质中的氧原子,其核电荷数都是8,就是核电荷数为8的一类原子,这一类原子就总称为氧元素。
元素是指具有相同核电荷数(即核内质子数)的一类原子的总称
注意:(1)具有相同核电荷数(即核内质子数)是是同种元素的依据。
(2)“一类原子”指的是其核电荷数相同而核内所含中子数并不一定相同的一类原子。之所以把它们归成一类,是因为它们的化学性质相同。
(3)元素是一个描逑原子种类的概念,只讲种类,不讲个数。
1.元素的定义
元素
2.原子和元素的比较
原子
元素
定义
化学变化中的最小粒子
具有相同核电荷数(即核内质子数)的一类原子的总称
区别
①微观概念,表示物质的微观构成
②既表示种类,又表示个数
③化学反应中原子不会发生改变
①宏观概念,表示物质的宏观组成
②只表示种类,不表示个数
③化学反应中元素的种类不会发生改变
联系
只要是核电荷数相同的一类原子就是同一种元素。原子是元素的最小单位,而元素则是原子的一个归类“集体”。即元素和原子是总体和个体的关系。
元素
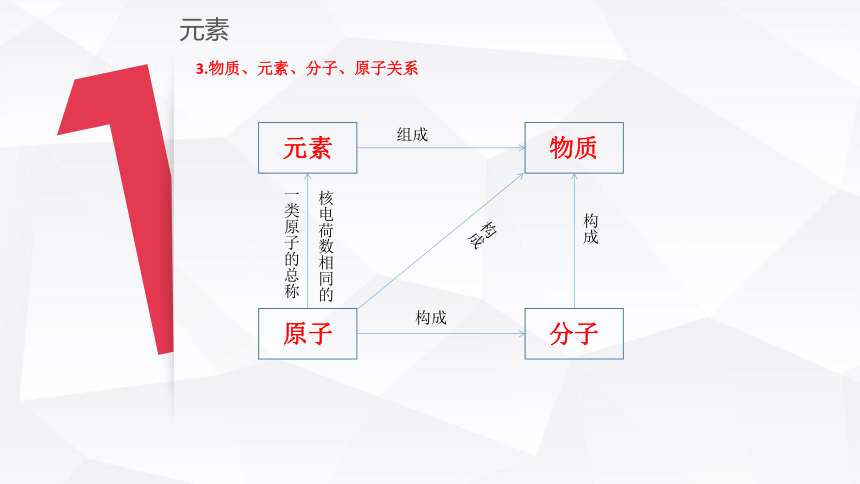
3.物质、元素、分子、原子关系
元素
分子
原子
物质
核电荷数相同的
一类原子的总称
组成
构成
构成
构成
元素
4.元素在地壳中和生物体细胞中的含量
地壳中各元素的质量分数
生物赖以生存的元素
元素的名称和符号
铁
Fe
铜
Cu
钙
Ca
钾
K
钠
Na
碳
C
硅
Si
硫
S
磷
P
硼
B
氢
H
氧
O
氟
F
氯
Cl
氦
He
溴
Br
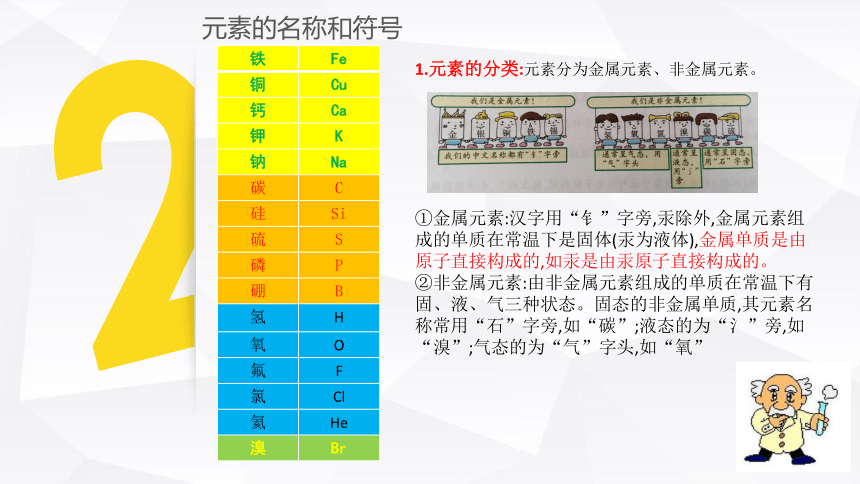
1.元素的分类:元素分为金属元素、非金属元素。
①金属元素:汉字用“钅”字旁,汞除外,金属元素组成的单质在常温下是固体(汞为液体),金属单质是由原子直接构成的,如汞是由汞原子直接构成的。
②非金属元素:由非金属元素组成的单质在常温下有固、液、气三种状态。固态的非金属单质,其元素名称常用“石”字旁,如“碳”;液态的为“氵”旁,如“溴”;气态的为“气”字头,如“氧”
元素的名称和符号
2.元素符号的表示方法
在国际上统一采用元素拉丁文名称的第一个大写字母来表示,如果几种元素名和
的第一个字母相同时,可再附加一个或两个小写字母来区别。
3.书写方法
(1)由一个字母表示的元素符号要大写。如H、O、C、N、P、K等。
(2)由两个字母表示的元素符号,第一个字母要大写,第二个字母要小写,即“一大二小”。如:Na、Ca、Mg、Si等。
4.元素符号表示的意义
(1)表示一种元素;
(2)表示该元素的一个原子。如“H”可以表示的意义有:①氢元素;②一个氢原子。
对于单质是由原子直接构成的物质,其元素符号还可以表示这种单质,如“Fe”表示的意义有:①铁元素;②一个铁原子;③铁单质。
说明:在元素符号前面加数字可表示多个原子,如“3H"表示3个氢原子。
元素周期表
1829年,德国J.W.德贝赖纳在研究元素的原子量与化学性质的关系
时,发现有几个相似的元素组:①锂、钠、钾。②钙、锶、钡。
③氯、溴、碘。④硫、硒、碲。⑤锰、铬、铁。同组元素的性
质相似,中间元素的化学性质介于前后两个元素之间,它的原
子量也差不多是前后两个元素的平均值。
1862年,法国尚古多提出元素性质有周期性重复出现的规律,他
创造了一种螺旋图,将62个元素按原子量大小循序标记在绕着圆
柱体上升的螺线上,可以清楚地看出某些性质相近的元素都出现
在同一条母线上。
1864年,英国W.奥德林发表了一张比较详细的周期表,表中的元
素基本上按原子量递增的顺序排列,体现了元素性质随原子量递增会出现周期性的变化。他还在表中留下空位,认识到它们是尚未被发现但性质与同一横列元素相似的元素。
1865年,英国J.A.R.纽兰兹把当时已发现的元素按原子量大小顺序排列,发现从任意一个元素算起,每到第八个元素,就和第一个元素的性质相似,他把这个规律称为八音律。
对元素周期律的发展贡献最大的当推俄国D.I.门捷列夫和德国J.L.迈尔。门捷列夫曾经收集了许多元素性质的数据,并加以整理,在这一过程中,他紧紧抓住元素的基本特征——原子量,探索原子量与元素性质的关系。他发现,如果把所有当时已知的元素按照原子量递增的顺序排列起来,经过一定的间隔,元素的性质会呈现明显的周期性。1869年,他发表了第一张元素周期表。
根据元素的结构和性质,把现在已知的100多种元素按原子序数(核电荷数)科学有序地排列起来,得到的表叫元素周期表。
元素周期表
1.元素周期表的结构
(1)在元素周期表中,每一种元素都占据一格,对于每一格都包含元素的原子序数、元素符号、元素名称、相对原子质原子质量等内容,如图所示。
(2)元素周期表的每一横行叫做一个周期,共有7个横行即有7个周期
(3)元素周期表中共有18个纵行,其中第8、9、10三个纵行共同组成一个族,其余每一纵行叫做一个族,共16个族。
元素周期表
2.元素周期表的规律
(1)元素周期表每周期(除第一周期外)开头都是金属元素,靠近尾部的是非金属元素,最后以稀有气体元素结尾。
(2)同一周期(横行)的元素的原子电子层数相同,从左到右,随着原子序数的递增,最外层电子数依次递增。
3)同一族(纵行)的元素的原子最外层电子数相同,从上而下,电子层数依次递增。
3.元素周期表的意义
(1)是学习和研究化学知识的重要工具
(2)在元素周期表中,位置越靠近的元素性质越相似,可以启发人们在元素周期表的一定区域内寻找新物质。
单质和化合物
根据纯净物中所含元素的种类可分为单质和化合物。
理解:首先两者都属于纯净物,再从组成元素的种类或构成分子的原子种类分析,含有同种元素或原子的为单质,含有多种元素或原子的为化合物。
单质和化合物
1.定义
单质:由同种元素组成的纯净物叫单质,如氧气(O2)、氮气(N2)、铁(Fe)等都是单质
化合物:由不同种元素组成的纯净物叫化合物,如二氧化碳(CO2)、高锰酸钾(KMnO4)等。
氧化物:由两种元素组成,其中一种是氧元素的纯净物为氧化物,如二氧化硫(SO2)、四氧化三铁(Fe3O4)等。
2.单质和化合物的比较
单质
化合物
概念
由同种元素组成的纯净物
由不同种元素组成的纯净物
区别
由同种元素组成
由不同种元素组成
举例
氧气(O2)、氮气(N2)、铁(Fe)
高锰酸钾(KMnO4)、水(H2O)
联系
都是纯净物
单质和化合物
3.氧化物和含氧化合物的关系
氧化物
含氧化合物
不同点
仅由两种元素组成,其中一种是氧元素的化合物
含两种或两种以上元素,其中一种是氧元素的化合物
相同点
都属于化合物,都含有氧元素
联系
氧化物属于含氧化合物,含氧化合物不一定是氧化物
4.各类物质间的关系
单质和化合物
混合物:由两种或两种以上物质组成。
纯净物:只由一种物质组成。
混合物
纯净物
化合物
单质
氧化物
基础练习
【典型例题1】二氧化碳是由碳、氧两种元素组成的,这两种元素的本质区别是(
)
A.质子数不同
B.中子数不同
C.电子数不同
D.相对原子质量不同
【典型例题2】(2018湖南衡阳中考改编)下列符号,既能表示一种元素,又能表示这种元素的一个原子,还能表示一种物质的是()
A.S
B.
C60
C.H
D
Fe2O3
【典型例题3】元素符号“Cd”不能表示()
A.镉元素
B.金属镉
C.一个镉原子
D.一个镉分子
【典型例题4】(多选)丽丽同学对元素周期表的认识正确的是()
A.元素周期表中共有七个周期十八个族
B.元素的原子序数等于该元素原子的核内质子数目
C.同一周期元素原子的电子层数相同
D.元素周期表中的金属元素中文名称都有“钅”字旁
【典型例题5】下列物质中属于混合物的是
属于纯净物的是
,属于单质的是
属于化合物的是
属于氧化物的是
。
①硫粉;②液态空气;③高锰酸钾受热完全分解所残留的固体;④氮气;⑤铜;⑥水;⑦氯酸钾;⑧四氧化三铁。
【典型例题6】现有以下几种物质:氧气、红磷,蒸馏水、二氧化碳、食盐水、空气、高锰酸钾。根据物质的分类知识,完成物质分类的网络图,并将上述几种物质按不同类别填入网络图中。
(1)其中属于氧化物的有
。
(2)网络图中的分类标准,请从以下提供的物质分类标准中找出正确对应关系的序号填入空格中。
A为
;B为
。
①按由同种物质还是不同物质组成来分
②按由同种元素还是不同种元素组成来分
③按物质的性质相同或不同来分
【典型例题7】类推是化学常见的学习方法,下列类推正确的是(
)
A.氧化物含氧元素,含氧元素的化合物一定是氧化物
B.化合物含有不同元素,由不同元素组成的物质一定是化合物
C.元素有不同的存在状态,液氧和氧气是同种物质
D.单质由一种元素组成,由一种元素组成的物质一定是纯净物
【典型例题7】下图是以原子为中心的知识网络,它帮助我们建立了物质的宏观组成和微观结构之间的联系。
(1)在上图方框A、B、C处分别填入“元素”“分子”“离子”,使这个知识
网络关系图正确
(2)仿照方框R处的示例,在方框D处填入不同种微粒构成的物质,使知识网络关系图更完善。
基础练习
【典型例题7】下图是以原子为中心的知识网络,它帮助我们建立了物质的宏观组成和微观结构之间的联系。
(1)在上图方框A、B、C处分别填入“元素”“分子”“离子”,使这个知识
网络关系图正确
(2)仿照方框R处的示例,在方框D处填入不同种微粒构成的物质,使知识网络关系图更完善。
【典型例题8】构建知识网络是一种重要的学习方法。
将“分子”“原子”“元素”填入如图序号所对应的
横线上。
①
,②
,③
。
【典型例题9】在①Cu、Mg、s、K,②2CO2、CuO、P2O3、H2O,③3H2、O2、N2、C三组物质中,均有一种物质与组内其他物质存在明显的不同,这三种物质分别是()
A.Cu、P2O、H
B.K、CO2、O2
C.Mg、H2O、O2
D.S、CuO、C
【典型例题10】掌握化学用语和物质的分类是学习化学的基础,请按要求回答下列问题。
(1)填写下列表格。
(2)将下列物质的名称填写在对应类别空格上(注:未提供对应类别物质
的,可不填)。物质:金刚石,氮气,三氧化硫,氧化铝,铜,氦气
中考题型专练
1.(2018海南中考)某地温泉中富含硫、铜、锌等,可以治疗皮肤病。这里的“硫、铜、锌”指的是()
A.分子
B.原子
C.元素
D.单质
2.(2018湖南株洲中考)碘元素在元素周期表中的信息如下。下列说法正确的是()
A.1个碘原子中含有53个中子
B.碘元素属于金属元素
C.1个I2分子中含有53个电子
D.碘的相对原子质量为126.9
3.(天津中考)地壳中含量最多的元素是()
A
.Si
B.
Fe
C.O
D.AI
4.(浙江金华中考)下列各选项中,物质的分类均正确的是()
5.(山东莱芜中考)氯元素在自然界中广泛存在,下列说法不正确的是()
A.氯元素属于非金属元素
B海水中含量最高的元素是氯元素
C.氯原子易得电子形成氯离子(Cl-)
D.氯气(Cl2)是由氯分子构成的
6.(山东威海中考)古希腊学者曾经提出过一个学说:复杂的物质世界是由“水、木、火和空气”四种基本成分组成的,也称“四元素学说”。18世纪末,科学家通过实验证明了空气中含有氧气和氮气及通电分解水能产生氧气和氢气,该学说被彻底否定。
(1)从现代物质组成的理论看,在水、火和空气中,属于纯净物的是
属于混合物的是
,火
(填“属于”或“不属于”)物质。
(2)从化学变化的理论看,组成物质世界的基本成分是
。
7.(福建泉州中考)我国探月工程已经发现月球中含有种类繁多的矿物,其中有的是在地球上未曾发现过的矿产。下列月球矿物中属于单质的是()
A.钛铁矿
B.铁锡合金
C.纯铁颗粒
D.硫化银颗粒
8.(广东佛山中考)自然界中相多种多样的物质,如下图:
(1)构成物质的微粒有
等。
(2)上图物质中常温下呈液的金属单质是
。
2.4
辨别物质的组成元素
新课导学
缺“钙”吃什么好呢?
想一想:几种名称中的“钙”、“锌”指的是什么?分子、原子,还是……?
元素
利用化学方法分析众多的物质,发现组成它们的基本成分—元素其实只有一百多种,就像可拼写出数十万个英文单词的字母只有26个一样。例如,水中的氧原子、二氧化碳中的氧原子、氧气中的氧原子,以及其他物质中的氧原子,其核电荷数都是8,就是核电荷数为8的一类原子,这一类原子就总称为氧元素。
元素是指具有相同核电荷数(即核内质子数)的一类原子的总称
注意:(1)具有相同核电荷数(即核内质子数)是是同种元素的依据。
(2)“一类原子”指的是其核电荷数相同而核内所含中子数并不一定相同的一类原子。之所以把它们归成一类,是因为它们的化学性质相同。
(3)元素是一个描逑原子种类的概念,只讲种类,不讲个数。
1.元素的定义
元素
2.原子和元素的比较
原子
元素
定义
化学变化中的最小粒子
具有相同核电荷数(即核内质子数)的一类原子的总称
区别
①微观概念,表示物质的微观构成
②既表示种类,又表示个数
③化学反应中原子不会发生改变
①宏观概念,表示物质的宏观组成
②只表示种类,不表示个数
③化学反应中元素的种类不会发生改变
联系
只要是核电荷数相同的一类原子就是同一种元素。原子是元素的最小单位,而元素则是原子的一个归类“集体”。即元素和原子是总体和个体的关系。
元素
3.物质、元素、分子、原子关系
元素
分子
原子
物质
核电荷数相同的
一类原子的总称
组成
构成
构成
构成
元素
4.元素在地壳中和生物体细胞中的含量
地壳中各元素的质量分数
生物赖以生存的元素
元素的名称和符号
铁
Fe
铜
Cu
钙
Ca
钾
K
钠
Na
碳
C
硅
Si
硫
S
磷
P
硼
B
氢
H
氧
O
氟
F
氯
Cl
氦
He
溴
Br
1.元素的分类:元素分为金属元素、非金属元素。
①金属元素:汉字用“钅”字旁,汞除外,金属元素组成的单质在常温下是固体(汞为液体),金属单质是由原子直接构成的,如汞是由汞原子直接构成的。
②非金属元素:由非金属元素组成的单质在常温下有固、液、气三种状态。固态的非金属单质,其元素名称常用“石”字旁,如“碳”;液态的为“氵”旁,如“溴”;气态的为“气”字头,如“氧”
元素的名称和符号
2.元素符号的表示方法
在国际上统一采用元素拉丁文名称的第一个大写字母来表示,如果几种元素名和
的第一个字母相同时,可再附加一个或两个小写字母来区别。
3.书写方法
(1)由一个字母表示的元素符号要大写。如H、O、C、N、P、K等。
(2)由两个字母表示的元素符号,第一个字母要大写,第二个字母要小写,即“一大二小”。如:Na、Ca、Mg、Si等。
4.元素符号表示的意义
(1)表示一种元素;
(2)表示该元素的一个原子。如“H”可以表示的意义有:①氢元素;②一个氢原子。
对于单质是由原子直接构成的物质,其元素符号还可以表示这种单质,如“Fe”表示的意义有:①铁元素;②一个铁原子;③铁单质。
说明:在元素符号前面加数字可表示多个原子,如“3H"表示3个氢原子。
元素周期表
1829年,德国J.W.德贝赖纳在研究元素的原子量与化学性质的关系
时,发现有几个相似的元素组:①锂、钠、钾。②钙、锶、钡。
③氯、溴、碘。④硫、硒、碲。⑤锰、铬、铁。同组元素的性
质相似,中间元素的化学性质介于前后两个元素之间,它的原
子量也差不多是前后两个元素的平均值。
1862年,法国尚古多提出元素性质有周期性重复出现的规律,他
创造了一种螺旋图,将62个元素按原子量大小循序标记在绕着圆
柱体上升的螺线上,可以清楚地看出某些性质相近的元素都出现
在同一条母线上。
1864年,英国W.奥德林发表了一张比较详细的周期表,表中的元
素基本上按原子量递增的顺序排列,体现了元素性质随原子量递增会出现周期性的变化。他还在表中留下空位,认识到它们是尚未被发现但性质与同一横列元素相似的元素。
1865年,英国J.A.R.纽兰兹把当时已发现的元素按原子量大小顺序排列,发现从任意一个元素算起,每到第八个元素,就和第一个元素的性质相似,他把这个规律称为八音律。
对元素周期律的发展贡献最大的当推俄国D.I.门捷列夫和德国J.L.迈尔。门捷列夫曾经收集了许多元素性质的数据,并加以整理,在这一过程中,他紧紧抓住元素的基本特征——原子量,探索原子量与元素性质的关系。他发现,如果把所有当时已知的元素按照原子量递增的顺序排列起来,经过一定的间隔,元素的性质会呈现明显的周期性。1869年,他发表了第一张元素周期表。
根据元素的结构和性质,把现在已知的100多种元素按原子序数(核电荷数)科学有序地排列起来,得到的表叫元素周期表。
元素周期表
1.元素周期表的结构
(1)在元素周期表中,每一种元素都占据一格,对于每一格都包含元素的原子序数、元素符号、元素名称、相对原子质原子质量等内容,如图所示。
(2)元素周期表的每一横行叫做一个周期,共有7个横行即有7个周期
(3)元素周期表中共有18个纵行,其中第8、9、10三个纵行共同组成一个族,其余每一纵行叫做一个族,共16个族。
元素周期表
2.元素周期表的规律
(1)元素周期表每周期(除第一周期外)开头都是金属元素,靠近尾部的是非金属元素,最后以稀有气体元素结尾。
(2)同一周期(横行)的元素的原子电子层数相同,从左到右,随着原子序数的递增,最外层电子数依次递增。
3)同一族(纵行)的元素的原子最外层电子数相同,从上而下,电子层数依次递增。
3.元素周期表的意义
(1)是学习和研究化学知识的重要工具
(2)在元素周期表中,位置越靠近的元素性质越相似,可以启发人们在元素周期表的一定区域内寻找新物质。
单质和化合物
根据纯净物中所含元素的种类可分为单质和化合物。
理解:首先两者都属于纯净物,再从组成元素的种类或构成分子的原子种类分析,含有同种元素或原子的为单质,含有多种元素或原子的为化合物。
单质和化合物
1.定义
单质:由同种元素组成的纯净物叫单质,如氧气(O2)、氮气(N2)、铁(Fe)等都是单质
化合物:由不同种元素组成的纯净物叫化合物,如二氧化碳(CO2)、高锰酸钾(KMnO4)等。
氧化物:由两种元素组成,其中一种是氧元素的纯净物为氧化物,如二氧化硫(SO2)、四氧化三铁(Fe3O4)等。
2.单质和化合物的比较
单质
化合物
概念
由同种元素组成的纯净物
由不同种元素组成的纯净物
区别
由同种元素组成
由不同种元素组成
举例
氧气(O2)、氮气(N2)、铁(Fe)
高锰酸钾(KMnO4)、水(H2O)
联系
都是纯净物
单质和化合物
3.氧化物和含氧化合物的关系
氧化物
含氧化合物
不同点
仅由两种元素组成,其中一种是氧元素的化合物
含两种或两种以上元素,其中一种是氧元素的化合物
相同点
都属于化合物,都含有氧元素
联系
氧化物属于含氧化合物,含氧化合物不一定是氧化物
4.各类物质间的关系
单质和化合物
混合物:由两种或两种以上物质组成。
纯净物:只由一种物质组成。
混合物
纯净物
化合物
单质
氧化物
基础练习
【典型例题1】二氧化碳是由碳、氧两种元素组成的,这两种元素的本质区别是(
)
A.质子数不同
B.中子数不同
C.电子数不同
D.相对原子质量不同
【典型例题2】(2018湖南衡阳中考改编)下列符号,既能表示一种元素,又能表示这种元素的一个原子,还能表示一种物质的是()
A.S
B.
C60
C.H
D
Fe2O3
【典型例题3】元素符号“Cd”不能表示()
A.镉元素
B.金属镉
C.一个镉原子
D.一个镉分子
【典型例题4】(多选)丽丽同学对元素周期表的认识正确的是()
A.元素周期表中共有七个周期十八个族
B.元素的原子序数等于该元素原子的核内质子数目
C.同一周期元素原子的电子层数相同
D.元素周期表中的金属元素中文名称都有“钅”字旁
【典型例题5】下列物质中属于混合物的是
属于纯净物的是
,属于单质的是
属于化合物的是
属于氧化物的是
。
①硫粉;②液态空气;③高锰酸钾受热完全分解所残留的固体;④氮气;⑤铜;⑥水;⑦氯酸钾;⑧四氧化三铁。
【典型例题6】现有以下几种物质:氧气、红磷,蒸馏水、二氧化碳、食盐水、空气、高锰酸钾。根据物质的分类知识,完成物质分类的网络图,并将上述几种物质按不同类别填入网络图中。
(1)其中属于氧化物的有
。
(2)网络图中的分类标准,请从以下提供的物质分类标准中找出正确对应关系的序号填入空格中。
A为
;B为
。
①按由同种物质还是不同物质组成来分
②按由同种元素还是不同种元素组成来分
③按物质的性质相同或不同来分
【典型例题7】类推是化学常见的学习方法,下列类推正确的是(
)
A.氧化物含氧元素,含氧元素的化合物一定是氧化物
B.化合物含有不同元素,由不同元素组成的物质一定是化合物
C.元素有不同的存在状态,液氧和氧气是同种物质
D.单质由一种元素组成,由一种元素组成的物质一定是纯净物
【典型例题7】下图是以原子为中心的知识网络,它帮助我们建立了物质的宏观组成和微观结构之间的联系。
(1)在上图方框A、B、C处分别填入“元素”“分子”“离子”,使这个知识
网络关系图正确
(2)仿照方框R处的示例,在方框D处填入不同种微粒构成的物质,使知识网络关系图更完善。
基础练习
【典型例题7】下图是以原子为中心的知识网络,它帮助我们建立了物质的宏观组成和微观结构之间的联系。
(1)在上图方框A、B、C处分别填入“元素”“分子”“离子”,使这个知识
网络关系图正确
(2)仿照方框R处的示例,在方框D处填入不同种微粒构成的物质,使知识网络关系图更完善。
【典型例题8】构建知识网络是一种重要的学习方法。
将“分子”“原子”“元素”填入如图序号所对应的
横线上。
①
,②
,③
。
【典型例题9】在①Cu、Mg、s、K,②2CO2、CuO、P2O3、H2O,③3H2、O2、N2、C三组物质中,均有一种物质与组内其他物质存在明显的不同,这三种物质分别是()
A.Cu、P2O、H
B.K、CO2、O2
C.Mg、H2O、O2
D.S、CuO、C
【典型例题10】掌握化学用语和物质的分类是学习化学的基础,请按要求回答下列问题。
(1)填写下列表格。
(2)将下列物质的名称填写在对应类别空格上(注:未提供对应类别物质
的,可不填)。物质:金刚石,氮气,三氧化硫,氧化铝,铜,氦气
中考题型专练
1.(2018海南中考)某地温泉中富含硫、铜、锌等,可以治疗皮肤病。这里的“硫、铜、锌”指的是()
A.分子
B.原子
C.元素
D.单质
2.(2018湖南株洲中考)碘元素在元素周期表中的信息如下。下列说法正确的是()
A.1个碘原子中含有53个中子
B.碘元素属于金属元素
C.1个I2分子中含有53个电子
D.碘的相对原子质量为126.9
3.(天津中考)地壳中含量最多的元素是()
A
.Si
B.
Fe
C.O
D.AI
4.(浙江金华中考)下列各选项中,物质的分类均正确的是()
5.(山东莱芜中考)氯元素在自然界中广泛存在,下列说法不正确的是()
A.氯元素属于非金属元素
B海水中含量最高的元素是氯元素
C.氯原子易得电子形成氯离子(Cl-)
D.氯气(Cl2)是由氯分子构成的
6.(山东威海中考)古希腊学者曾经提出过一个学说:复杂的物质世界是由“水、木、火和空气”四种基本成分组成的,也称“四元素学说”。18世纪末,科学家通过实验证明了空气中含有氧气和氮气及通电分解水能产生氧气和氢气,该学说被彻底否定。
(1)从现代物质组成的理论看,在水、火和空气中,属于纯净物的是
属于混合物的是
,火
(填“属于”或“不属于”)物质。
(2)从化学变化的理论看,组成物质世界的基本成分是
。
7.(福建泉州中考)我国探月工程已经发现月球中含有种类繁多的矿物,其中有的是在地球上未曾发现过的矿产。下列月球矿物中属于单质的是()
A.钛铁矿
B.铁锡合金
C.纯铁颗粒
D.硫化银颗粒
8.(广东佛山中考)自然界中相多种多样的物质,如下图:
(1)构成物质的微粒有
等。
(2)上图物质中常温下呈液的金属单质是
。
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
