金属复习导学案
图片预览
文档简介
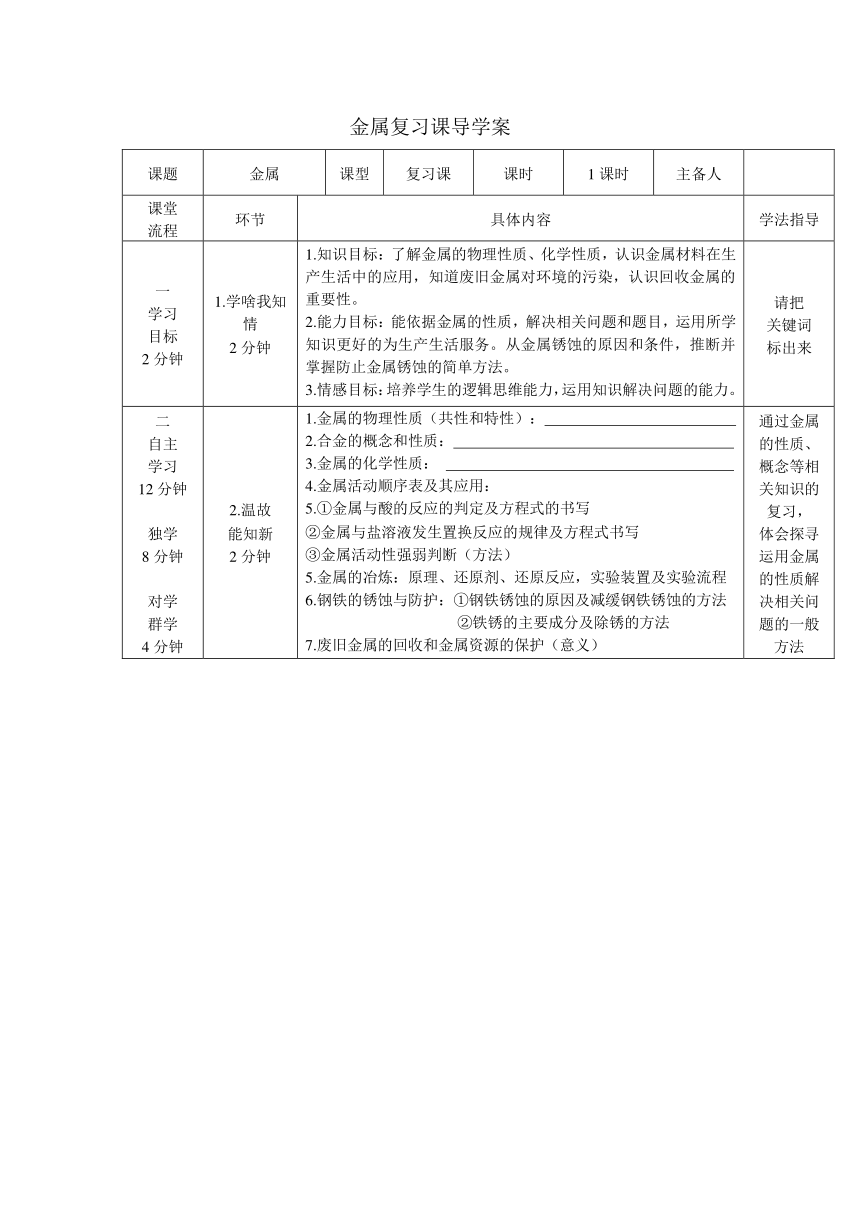
金属复习课导学案
课题 金属 课型 复习课 课时 1课时 主备人
课堂流程 环节 具体内容 学法指导
一学习目标2分钟 学啥我知情2分钟 1.知识目标:了解金属的物理性质、化学性质,认识金属材料在生产生活中的应用,知道废旧金属对环境的污染,认识回收金属的重要性。2.能力目标:能依据金属的性质,解决相关问题和题目,运用所学知识更好的为生产生活服务。从金属锈蚀的原因和条件,推断并掌握防止金属锈蚀的简单方法。3.情感目标:培养学生的逻辑思维能力,运用知识解决问题的能力。 请把关键词标出来
二自主学习12分钟独学8分钟对学群学4分钟 温故能知新2分钟 金属的物理性质(共性和特性): 合金的概念和性质: 金属的化学性质: 金属活动顺序表及其应用:①金属与酸的反应的判定及方程式的书写②金属与盐溶液发生置换反应的规律及方程式书写③金属活动性强弱判断(方法)5.金属的冶炼:原理、还原剂、还原反应,实验装置及实验流程6.钢铁的锈蚀与防护:①钢铁锈蚀的原因及减缓钢铁锈蚀的方法 ②铁锈的主要成分及除锈的方法7.废旧金属的回收和金属资源的保护(意义) 通过金属的性质、概念等相关知识的复习,体会探寻运用金属的性质解决相关问题的一般方法
基础我能行4分钟 1.地壳中含量最多的元素与含量最多的金属元素组成的物质的化学式是 ;2.下列关于合金的叙述:①合金中至少有两种金属②合金中元素以化合物形式存在③合金中一定含有非金属④合金一定为混合物⑤合金依然具有金属特性,⑥合金的熔点变得更高,硬度变得更大了。其中正确的是( ) A、④⑤⑥ B、①②③ C、④⑤ D、③④⑤3.实验室有一包混有铁粉的铜粉,请你用两种不同方法除去铁粉(简述操作过程)(1)物理方法: (2)化学方法: 4.有X、Y、Z三种金属,把Y投入X(N03)2溶液中,Y表面有X析出, 把X投入Z(N03)2溶液中,X表面有Z析出。X、Y、Z三种金属的活动性由强到弱的顺序是:( )A.Z﹥Y﹥X B.Y﹥X﹥Z C.X﹥Y﹥Z D.X﹥Z﹥Y5.将锌粒放入下列物质的溶液里,溶液质量减少的是( )A、HCl B、FeSO4 C、AgNO3 D、CuCl26.铝与氧气反应生成的氧化铝能起到保护内层铝的作用。铁锈是否也能保护内层的铁呢? 请注意化学语言和化学符号的严密和规范理解关系提升能力从条件和已知入手尝试解决问题
拓展我解决6分钟 1.下列有关金属的说法中,正确的是( )A.生铁是纯铁B. 铝合金硬度大、密度小,用于飞机制造C.铜在潮湿的空气中也不生锈D.钢铁制品表面涂油是为了更美观2.利用废弃的定影液可回收银。原理是Fe+2AgNO3=2Ag+Fe(NO3)2,反应属( )A.化合反应B.置换反应C.分解反应D.复分解反应3.室温下,等质量的镁片和铝片分别与足量的稀硫酸反应,产生氢气的质量(m)与时间(t)的关系图正确的是 ( )在Cu(NO3)2和AgNO3 混合溶液中加入一定量铁粉充分反应后过滤,①向滤液中滴加盐酸有白色沉淀,则滤出的固体有 ,滤液中存在的物质是 ②若滤出的固体加盐酸有可燃性气体产生,则滤出的固体有 ,滤液中存在的物质 .5.除去Cu粉中混有的少量Fe粉,可以选用的试剂是 6.现有10吨含Fe2O380%的赤铁矿在高温下完全被CO还原,试问能得到多少吨含杂质40%的生铁? 运用基础知识解决拓展问题提升新能力
三 展示 交流 20分钟 5.展示 我精彩 板演讲解 20分钟 先讨论交流,解疑释难,然后板演展示并讲解。看哪个小组写的又快又好,讲解的清晰明白。环节一:1—6代表板演并讲解 基础我能行环节二:1—6代表板演并讲解 拓展我解决 烂熟于心才能享受脱稿展示的潇洒
四 总结 升华 6分钟 6. 总结 我提升 6分钟 通过本节课的学习,我的收获是: 只有善于总结知识才能学到家
五课堂作业7分钟 7.作业当堂请7分钟 1.等质量的两种金属A、B与足量稀硫酸反应时都产生了+2价的硫酸盐,其中产生H2与反应时间的关系如下图:(1)A、B两金属的活动性强弱是 。(2)A、B相对原子质量的大小是 。(3)在Mg和Fe、Fe和Zn、Zn和Cu中A、B可能是 。2.下列物质可以用金属与稀盐酸直接反应制得的是( )A FeCl3 B FeCl2 C CuCl2 D AgCl 独立用5分钟完成,然后用2分钟小组反馈
8.挑战我接招附加题 如图所示,在一根等到臂棒的两端,用细线分别吊住质量相等的铁块和铜块,并使之浸入甲、乙烧杯中。问一段时间后,观察者可能观察到哪些现象? 你能独占鳌头!真能耐!
t
Mg
A
m
Al
m
B
Mg
t
Al
Al
m
t
Mg
C
t
Mg
m
Al
D
t
B
A
Fe
Cu
H2SO4
甲
Hg(NO3)2
乙
课题 金属 课型 复习课 课时 1课时 主备人
课堂流程 环节 具体内容 学法指导
一学习目标2分钟 学啥我知情2分钟 1.知识目标:了解金属的物理性质、化学性质,认识金属材料在生产生活中的应用,知道废旧金属对环境的污染,认识回收金属的重要性。2.能力目标:能依据金属的性质,解决相关问题和题目,运用所学知识更好的为生产生活服务。从金属锈蚀的原因和条件,推断并掌握防止金属锈蚀的简单方法。3.情感目标:培养学生的逻辑思维能力,运用知识解决问题的能力。 请把关键词标出来
二自主学习12分钟独学8分钟对学群学4分钟 温故能知新2分钟 金属的物理性质(共性和特性): 合金的概念和性质: 金属的化学性质: 金属活动顺序表及其应用:①金属与酸的反应的判定及方程式的书写②金属与盐溶液发生置换反应的规律及方程式书写③金属活动性强弱判断(方法)5.金属的冶炼:原理、还原剂、还原反应,实验装置及实验流程6.钢铁的锈蚀与防护:①钢铁锈蚀的原因及减缓钢铁锈蚀的方法 ②铁锈的主要成分及除锈的方法7.废旧金属的回收和金属资源的保护(意义) 通过金属的性质、概念等相关知识的复习,体会探寻运用金属的性质解决相关问题的一般方法
基础我能行4分钟 1.地壳中含量最多的元素与含量最多的金属元素组成的物质的化学式是 ;2.下列关于合金的叙述:①合金中至少有两种金属②合金中元素以化合物形式存在③合金中一定含有非金属④合金一定为混合物⑤合金依然具有金属特性,⑥合金的熔点变得更高,硬度变得更大了。其中正确的是( ) A、④⑤⑥ B、①②③ C、④⑤ D、③④⑤3.实验室有一包混有铁粉的铜粉,请你用两种不同方法除去铁粉(简述操作过程)(1)物理方法: (2)化学方法: 4.有X、Y、Z三种金属,把Y投入X(N03)2溶液中,Y表面有X析出, 把X投入Z(N03)2溶液中,X表面有Z析出。X、Y、Z三种金属的活动性由强到弱的顺序是:( )A.Z﹥Y﹥X B.Y﹥X﹥Z C.X﹥Y﹥Z D.X﹥Z﹥Y5.将锌粒放入下列物质的溶液里,溶液质量减少的是( )A、HCl B、FeSO4 C、AgNO3 D、CuCl26.铝与氧气反应生成的氧化铝能起到保护内层铝的作用。铁锈是否也能保护内层的铁呢? 请注意化学语言和化学符号的严密和规范理解关系提升能力从条件和已知入手尝试解决问题
拓展我解决6分钟 1.下列有关金属的说法中,正确的是( )A.生铁是纯铁B. 铝合金硬度大、密度小,用于飞机制造C.铜在潮湿的空气中也不生锈D.钢铁制品表面涂油是为了更美观2.利用废弃的定影液可回收银。原理是Fe+2AgNO3=2Ag+Fe(NO3)2,反应属( )A.化合反应B.置换反应C.分解反应D.复分解反应3.室温下,等质量的镁片和铝片分别与足量的稀硫酸反应,产生氢气的质量(m)与时间(t)的关系图正确的是 ( )在Cu(NO3)2和AgNO3 混合溶液中加入一定量铁粉充分反应后过滤,①向滤液中滴加盐酸有白色沉淀,则滤出的固体有 ,滤液中存在的物质是 ②若滤出的固体加盐酸有可燃性气体产生,则滤出的固体有 ,滤液中存在的物质 .5.除去Cu粉中混有的少量Fe粉,可以选用的试剂是 6.现有10吨含Fe2O380%的赤铁矿在高温下完全被CO还原,试问能得到多少吨含杂质40%的生铁? 运用基础知识解决拓展问题提升新能力
三 展示 交流 20分钟 5.展示 我精彩 板演讲解 20分钟 先讨论交流,解疑释难,然后板演展示并讲解。看哪个小组写的又快又好,讲解的清晰明白。环节一:1—6代表板演并讲解 基础我能行环节二:1—6代表板演并讲解 拓展我解决 烂熟于心才能享受脱稿展示的潇洒
四 总结 升华 6分钟 6. 总结 我提升 6分钟 通过本节课的学习,我的收获是: 只有善于总结知识才能学到家
五课堂作业7分钟 7.作业当堂请7分钟 1.等质量的两种金属A、B与足量稀硫酸反应时都产生了+2价的硫酸盐,其中产生H2与反应时间的关系如下图:(1)A、B两金属的活动性强弱是 。(2)A、B相对原子质量的大小是 。(3)在Mg和Fe、Fe和Zn、Zn和Cu中A、B可能是 。2.下列物质可以用金属与稀盐酸直接反应制得的是( )A FeCl3 B FeCl2 C CuCl2 D AgCl 独立用5分钟完成,然后用2分钟小组反馈
8.挑战我接招附加题 如图所示,在一根等到臂棒的两端,用细线分别吊住质量相等的铁块和铜块,并使之浸入甲、乙烧杯中。问一段时间后,观察者可能观察到哪些现象? 你能独占鳌头!真能耐!
t
Mg
A
m
Al
m
B
Mg
t
Al
Al
m
t
Mg
C
t
Mg
m
Al
D
t
B
A
Fe
Cu
H2SO4
甲
Hg(NO3)2
乙
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
