人教版高一化学必修二第二节-来自煤和石油的化工原料(38张PPT)
文档属性
| 名称 | 人教版高一化学必修二第二节-来自煤和石油的化工原料(38张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-08-06 00:00:00 | ||
图片预览








文档简介
(共66张PPT)
第二节
来自石油和煤的两种基本化工原料
第三章
有机化合物
我们常说煤是工业的粮食,石油是现在工业的血液,从煤和石油不仅可以得到多种常用燃料,而且可以从中获取大量的基本化工原料。
在前面我们已经知道,在有机化学的学习中,常常是根据某一物质的结构和性质可推导出一类结构相似的物质的性质,只要我们抓住了一类物质的结构特点,那么掌握它们的性质也就比较容易了.这节课我们就来推导又一类结构相似的物质的化学性质。
乙烯
思考:
1、你知道石油是怎么形成的?石油中有些什么物质?
2、石油可以为我们提供什么化工原料呢?
3、我们怎么从石油中得到化工原料呢?
动物的尸体经几万年的地质变化形成;石油中主要含有烷烃、环烷烃、芳香烃等稳定的烃。
烷烃、环烷烃、芳香烃等,经加工后还可以得到烯烃、炔烃。
通过蒸馏、分馏将石油分离成多个组分,在通过裂化、裂解得到各种化工原料
4、石油化工原料我们又能制造什么呢?
你知道衡量一个国家化工产业发展水平的标志是什么?
乙烯的产量
思考:
请大家写出乙烷的分子式、电子式、结构式和结构简式
C2H6
H
H
|
|
H-C-C-H
|
|
H
H
乙烷
CH3CH3
如果把乙烷分子中每个碳原子的氢原子都去掉一个,有会形成什么分子呢?
C2H4
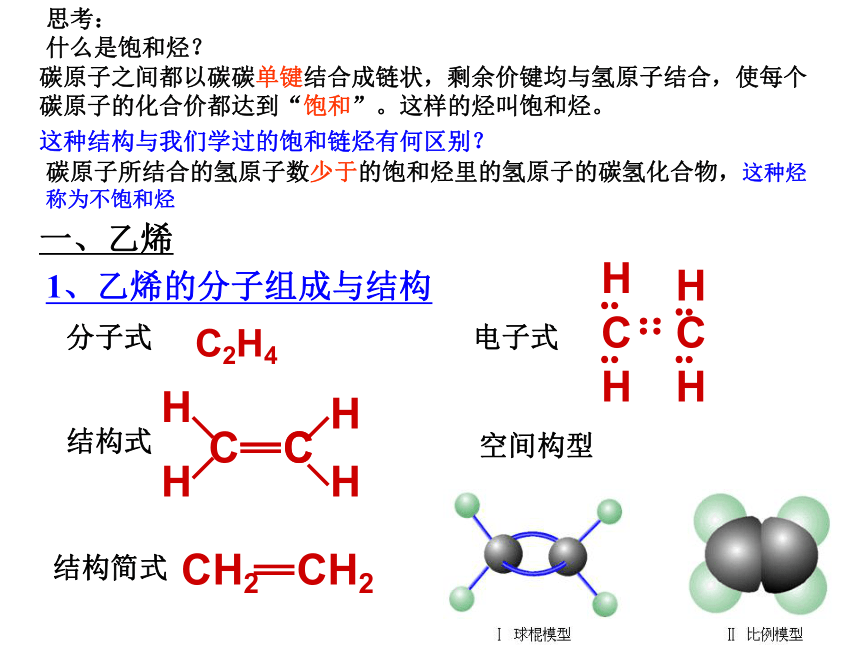
这种结构与我们学过的饱和链烃有何区别?
碳原子所结合的氢原子数少于的饱和烃里的氢原子的碳氢化合物,这种烃称为不饱和烃
1、乙烯的分子组成与结构
一、乙烯
分子式
结构式
电子式
结构简式
C2H4
空间构型
思考:
什么是饱和烃?
碳原子之间都以碳碳单键结合成链状,剩余价键均与氢原子结合,使每个碳原子的化合价都达到“饱和”。这样的烃叫饱和烃。
乙烷和乙烯结构比较
碳碳单键
碳碳双键
109
°28
?
120°
384
612
2个碳原子和6
个氢
所有原子处于同一
不在同一平面内
平面内
H
H
|
|
H-C-C-H
|
|
H
H
分子式
C2H6
C2H4
结构式
键类别
键角
键kJ/mol
分子的中各原子在空间的相对位置
分子结构的特点:
a、乙烯是平面结构,所有的原子处于同一平面。
b、碳原子间以双键结合,其中有一个键不稳定。
c、碳氢键角为120°
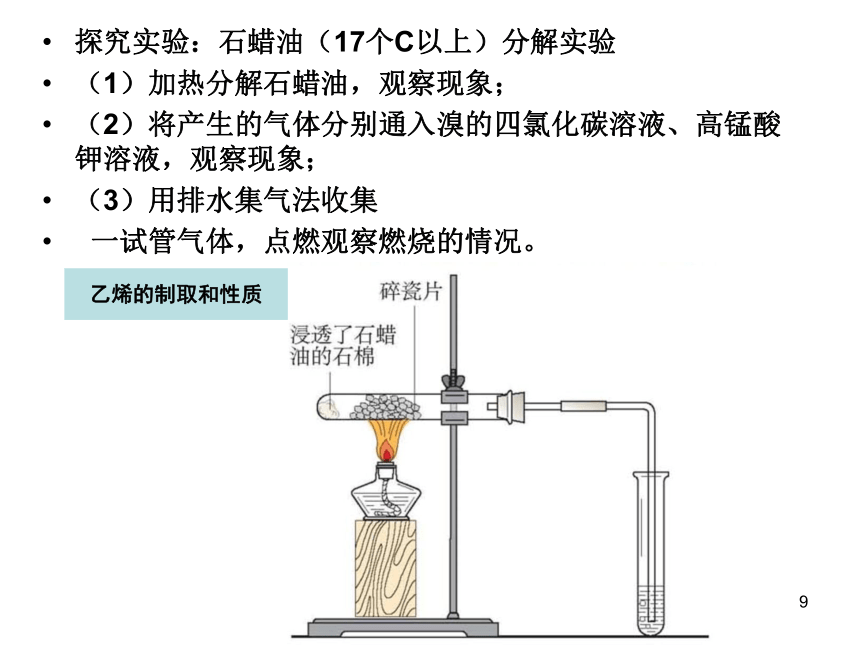
探究实验:石蜡油(17个C以上)分解实验
(1)加热分解石蜡油,观察现象;
(2)将产生的气体分别通入溴的四氯化碳溶液、高锰酸钾溶液,观察现象;
(3)用排水集气法收集
一试管气体,点燃观察燃烧的情况。
乙烯的制取和性质
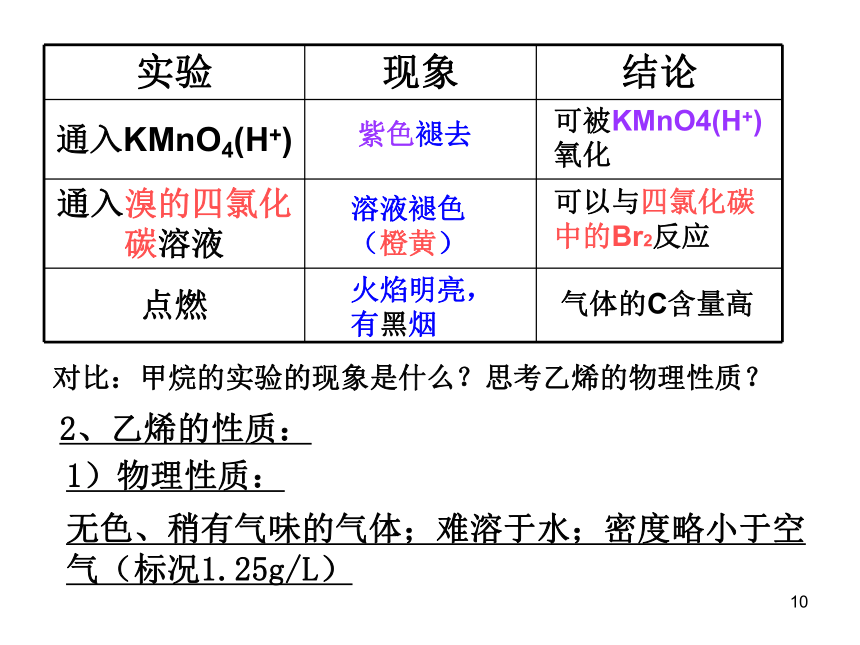
紫色褪去
溶液褪色
(橙黄)
可被KMnO4(H+)氧化
可以与四氯化碳中的Br2反应
火焰明亮,有黑烟
气体的C含量高
对比:甲烷的实验的现象是什么?思考乙烯的物理性质?
2、乙烯的性质:
无色、稍有气味的气体;难溶于水;密度略小于空气(标况1.25g/L)
1)物理性质:
实验
现象
结论
通入KMnO4(H+)
通入溴的四氯化碳溶液
点燃
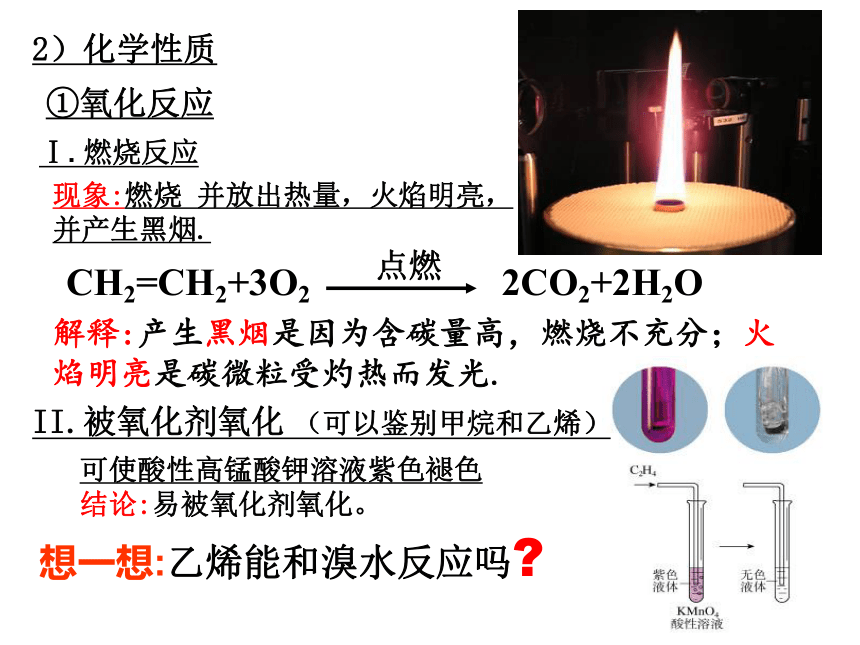
现象:燃烧
并放出热量,火焰明亮,并产生黑烟.
解释:产生黑烟是因为含碳量高,燃烧不充分;火焰明亮是碳微粒受灼热而发光.
①氧化反应
Ⅰ.
燃烧反应
2)化学性质
II.被氧化剂氧化
(可以鉴别甲烷和乙烯)
可使酸性高锰酸钾溶液紫色褪色
结论:易被氧化剂氧化。
想一想:乙烯能和溴水反应吗?
乙烯分子内碳碳双键的键能(615KJ/mol)小于碳碳单键键能(348KJ/mol)的二倍,说明其中有一条碳碳键键能小,容易断裂。
实验现象:
溴水的黄色很快褪去
将乙烯气体通入溴水中,观察现象
回忆乙烯的结构:
②加成反应:
有机物分子中的不饱和碳原子(双键或三键)与其它原子或原子团直接结合生成新的化合物的反应。
注意:乙烯与卤素单质的溶液反应,与烷烃不同;
乙烯与卤素单质溶液的加成没有反应条件;
双键中只断一条;
不饱和键与加成试剂分子之比为1:1;
产物为纯净物。
(1、2-二溴乙烷)
(无色液体)
乙烯与溴水(或溴的四氯化碳溶液)的反应
(特点:只进不出,断键加入)
根据上面的反应想想看:除去乙烷中混入的少量乙烯,最佳方法是
用足量的稀溴水洗气
练一练
1.乙烯与氢气反应:
2.乙烯与氯化氢反应:
3.乙烯与水反应:
4.乙烯与氯气反应:
思考:
如果要生产一溴乙烷,可用乙烷和溴蒸气光照取代生成,也可将乙烯通入溴水来制取,你认为用哪种方法合适?
(3)聚合反应
小分子有机物变大分子有机物——聚合反应
以加成的方式聚合为加成聚合反应,简称加聚反应
说明:1、聚乙烯无固定熔沸点。
2、聚乙烯、聚氯乙烯等白色塑料废弃物,微生物不能降解,是白色污染物。现在用可降解塑料聚乳酸来代替,它可以被乳酸菌分解为无毒物质。
链节
聚合度
单体
3.乙烯的用途
催熟剂
调节剂
⑴石油化学工业最重要的基础原料
⑵植物生长调节剂
乙烯常用作果实催熟剂
烯烃(单烯烃)
1.概念:
2.通式:
3.烯烃同系物的物理性质:
CnH2n
(n≥2)
4.烯烃的化学性质:
氧化反应:
加成反应:
分子中含有碳碳双键的不饱和链烃。
加聚反应:
1、能用于鉴别甲烷和乙烯的试剂是
(
)
A.溴水
B.酸性高锰酸钾溶液
C.苛性钠溶液
D.四氯化碳溶液
2.
既可以使溴水褪色,又可以使酸性高锰酸钾溶液褪色的气体有
(
)
A.
CO
B.
CO2
C.
C2H4
D.
C2H6
AB
C
3.
乙烯发生的下列反应中,不属于加成反
应的是
(
)
A.
与氢气反应生成乙烷
B.
与水反应生成乙醇
C.
与溴水反应使之褪色
D.
与氧气反应生成二氧化碳和水
D
4.实验室常用CH3CH2OH和浓硫酸共热到170℃制备CH2=CH2,同时得到H2O,制取乙烯的反应常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计下列实验确认上述混合气体中有乙烯和二氧化硫。A:品红溶液,B:NaOH溶液,C:浓硫酸,D:酸性高锰酸钾溶液。试回答下列问题:
(1)图3—1中①②③④装置可盛放的试剂是:①
,②
,③
,④
。(将有关试剂的序号填入空格内)
(2)能说明SO2存在的现象是
。
(3)使用装置②的目的是
。
(4)使用装置③的目的是
。
(5)确证乙烯存在的现象是
。
5.1mol乙烯与氯气完全加成,再与氯气彻底取代,两个过程中共有氯气(
)
A、2mol
B、4mol
C、5mol
D、6mol
19世纪欧洲许多国家都使用煤气照明,煤气通常是压缩在桶里贮运的,人们发现这种桶里总有一种油状液体,但长时间无人问津。英国科学家法拉第对这种液体产生了浓厚兴趣,他花了整整五年时间提取这种液体,从中得到了苯——一种无色
油状液体。
Michael
Faraday
(1791-1867)
二、苯
苯是重要的化工原料,分子式是C6H6,它是一种环状有机化合物,其结构式.
学与问P69:苯是否含有双键,如何证明?
实验3-1
上层橙色,
下层几乎无色。
萃取(物理现象)
没有发生加成反应,
苯无C=C存在。
溶液不褪色。
苯中无C=C存在。
苯加溴水
苯加酸性高
锰酸钾溶液
现
象
结
论
(1)无色、有特殊气味的液体,有毒,不溶于水,密度比水的小,常用作有机溶剂;
(2)苯的熔点为5.5℃
,用冰冷却可凝结成无色晶体。
苯的化学性质:
苯也是烃类,可以燃烧,但产生较多的黑烟。原因?
反应见课本P69。
苯的物理性质:
结论:苯中不存在双键,6个碳碳键完全相同,是一
种介于单键和双键之间的独特的键,比烯烃稳定。
资料卡片P69——芳香烃
凯库勒式
结构特点:
a、平面结构;
b、碳碳键是一种介于单键和
双键之间的独特的键。
①溴代反应
(1)
取代反应
无色液体,密度大于水
②硝化反应
纯净的硝基苯:无色而有苦杏仁气味的油状液体,不溶于水,密度比水大。硝基苯蒸气有毒性。
硝基苯
注意:苯不能与溴水发生加成反应(但能萃取溴而使水层褪色),说明它比烯烃、炔烃难进行加成反应。
跟H2在镍的存在下加热可生成环己烷:
180℃-250
℃
(2)加成反应
总结苯的化学性质(较稳定):
1.
难氧化(但可燃);
2.
易取代,难加成。
3.
苯兼有饱和烃和不饱和烃的性质,但没有饱和烃稳定,比不饱和烃稳定.
第二节
来自石油和煤的两种基本化工原料
第三章
有机化合物
我们常说煤是工业的粮食,石油是现在工业的血液,从煤和石油不仅可以得到多种常用燃料,而且可以从中获取大量的基本化工原料。
在前面我们已经知道,在有机化学的学习中,常常是根据某一物质的结构和性质可推导出一类结构相似的物质的性质,只要我们抓住了一类物质的结构特点,那么掌握它们的性质也就比较容易了.这节课我们就来推导又一类结构相似的物质的化学性质。
乙烯
思考:
1、你知道石油是怎么形成的?石油中有些什么物质?
2、石油可以为我们提供什么化工原料呢?
3、我们怎么从石油中得到化工原料呢?
动物的尸体经几万年的地质变化形成;石油中主要含有烷烃、环烷烃、芳香烃等稳定的烃。
烷烃、环烷烃、芳香烃等,经加工后还可以得到烯烃、炔烃。
通过蒸馏、分馏将石油分离成多个组分,在通过裂化、裂解得到各种化工原料
4、石油化工原料我们又能制造什么呢?
你知道衡量一个国家化工产业发展水平的标志是什么?
乙烯的产量
思考:
请大家写出乙烷的分子式、电子式、结构式和结构简式
C2H6
H
H
|
|
H-C-C-H
|
|
H
H
乙烷
CH3CH3
如果把乙烷分子中每个碳原子的氢原子都去掉一个,有会形成什么分子呢?
C2H4
这种结构与我们学过的饱和链烃有何区别?
碳原子所结合的氢原子数少于的饱和烃里的氢原子的碳氢化合物,这种烃称为不饱和烃
1、乙烯的分子组成与结构
一、乙烯
分子式
结构式
电子式
结构简式
C2H4
空间构型
思考:
什么是饱和烃?
碳原子之间都以碳碳单键结合成链状,剩余价键均与氢原子结合,使每个碳原子的化合价都达到“饱和”。这样的烃叫饱和烃。
乙烷和乙烯结构比较
碳碳单键
碳碳双键
109
°28
?
120°
384
612
2个碳原子和6
个氢
所有原子处于同一
不在同一平面内
平面内
H
H
|
|
H-C-C-H
|
|
H
H
分子式
C2H6
C2H4
结构式
键类别
键角
键kJ/mol
分子的中各原子在空间的相对位置
分子结构的特点:
a、乙烯是平面结构,所有的原子处于同一平面。
b、碳原子间以双键结合,其中有一个键不稳定。
c、碳氢键角为120°
探究实验:石蜡油(17个C以上)分解实验
(1)加热分解石蜡油,观察现象;
(2)将产生的气体分别通入溴的四氯化碳溶液、高锰酸钾溶液,观察现象;
(3)用排水集气法收集
一试管气体,点燃观察燃烧的情况。
乙烯的制取和性质
紫色褪去
溶液褪色
(橙黄)
可被KMnO4(H+)氧化
可以与四氯化碳中的Br2反应
火焰明亮,有黑烟
气体的C含量高
对比:甲烷的实验的现象是什么?思考乙烯的物理性质?
2、乙烯的性质:
无色、稍有气味的气体;难溶于水;密度略小于空气(标况1.25g/L)
1)物理性质:
实验
现象
结论
通入KMnO4(H+)
通入溴的四氯化碳溶液
点燃
现象:燃烧
并放出热量,火焰明亮,并产生黑烟.
解释:产生黑烟是因为含碳量高,燃烧不充分;火焰明亮是碳微粒受灼热而发光.
①氧化反应
Ⅰ.
燃烧反应
2)化学性质
II.被氧化剂氧化
(可以鉴别甲烷和乙烯)
可使酸性高锰酸钾溶液紫色褪色
结论:易被氧化剂氧化。
想一想:乙烯能和溴水反应吗?
乙烯分子内碳碳双键的键能(615KJ/mol)小于碳碳单键键能(348KJ/mol)的二倍,说明其中有一条碳碳键键能小,容易断裂。
实验现象:
溴水的黄色很快褪去
将乙烯气体通入溴水中,观察现象
回忆乙烯的结构:
②加成反应:
有机物分子中的不饱和碳原子(双键或三键)与其它原子或原子团直接结合生成新的化合物的反应。
注意:乙烯与卤素单质的溶液反应,与烷烃不同;
乙烯与卤素单质溶液的加成没有反应条件;
双键中只断一条;
不饱和键与加成试剂分子之比为1:1;
产物为纯净物。
(1、2-二溴乙烷)
(无色液体)
乙烯与溴水(或溴的四氯化碳溶液)的反应
(特点:只进不出,断键加入)
根据上面的反应想想看:除去乙烷中混入的少量乙烯,最佳方法是
用足量的稀溴水洗气
练一练
1.乙烯与氢气反应:
2.乙烯与氯化氢反应:
3.乙烯与水反应:
4.乙烯与氯气反应:
思考:
如果要生产一溴乙烷,可用乙烷和溴蒸气光照取代生成,也可将乙烯通入溴水来制取,你认为用哪种方法合适?
(3)聚合反应
小分子有机物变大分子有机物——聚合反应
以加成的方式聚合为加成聚合反应,简称加聚反应
说明:1、聚乙烯无固定熔沸点。
2、聚乙烯、聚氯乙烯等白色塑料废弃物,微生物不能降解,是白色污染物。现在用可降解塑料聚乳酸来代替,它可以被乳酸菌分解为无毒物质。
链节
聚合度
单体
3.乙烯的用途
催熟剂
调节剂
⑴石油化学工业最重要的基础原料
⑵植物生长调节剂
乙烯常用作果实催熟剂
烯烃(单烯烃)
1.概念:
2.通式:
3.烯烃同系物的物理性质:
CnH2n
(n≥2)
4.烯烃的化学性质:
氧化反应:
加成反应:
分子中含有碳碳双键的不饱和链烃。
加聚反应:
1、能用于鉴别甲烷和乙烯的试剂是
(
)
A.溴水
B.酸性高锰酸钾溶液
C.苛性钠溶液
D.四氯化碳溶液
2.
既可以使溴水褪色,又可以使酸性高锰酸钾溶液褪色的气体有
(
)
A.
CO
B.
CO2
C.
C2H4
D.
C2H6
AB
C
3.
乙烯发生的下列反应中,不属于加成反
应的是
(
)
A.
与氢气反应生成乙烷
B.
与水反应生成乙醇
C.
与溴水反应使之褪色
D.
与氧气反应生成二氧化碳和水
D
4.实验室常用CH3CH2OH和浓硫酸共热到170℃制备CH2=CH2,同时得到H2O,制取乙烯的反应常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计下列实验确认上述混合气体中有乙烯和二氧化硫。A:品红溶液,B:NaOH溶液,C:浓硫酸,D:酸性高锰酸钾溶液。试回答下列问题:
(1)图3—1中①②③④装置可盛放的试剂是:①
,②
,③
,④
。(将有关试剂的序号填入空格内)
(2)能说明SO2存在的现象是
。
(3)使用装置②的目的是
。
(4)使用装置③的目的是
。
(5)确证乙烯存在的现象是
。
5.1mol乙烯与氯气完全加成,再与氯气彻底取代,两个过程中共有氯气(
)
A、2mol
B、4mol
C、5mol
D、6mol
19世纪欧洲许多国家都使用煤气照明,煤气通常是压缩在桶里贮运的,人们发现这种桶里总有一种油状液体,但长时间无人问津。英国科学家法拉第对这种液体产生了浓厚兴趣,他花了整整五年时间提取这种液体,从中得到了苯——一种无色
油状液体。
Michael
Faraday
(1791-1867)
二、苯
苯是重要的化工原料,分子式是C6H6,它是一种环状有机化合物,其结构式.
学与问P69:苯是否含有双键,如何证明?
实验3-1
上层橙色,
下层几乎无色。
萃取(物理现象)
没有发生加成反应,
苯无C=C存在。
溶液不褪色。
苯中无C=C存在。
苯加溴水
苯加酸性高
锰酸钾溶液
现
象
结
论
(1)无色、有特殊气味的液体,有毒,不溶于水,密度比水的小,常用作有机溶剂;
(2)苯的熔点为5.5℃
,用冰冷却可凝结成无色晶体。
苯的化学性质:
苯也是烃类,可以燃烧,但产生较多的黑烟。原因?
反应见课本P69。
苯的物理性质:
结论:苯中不存在双键,6个碳碳键完全相同,是一
种介于单键和双键之间的独特的键,比烯烃稳定。
资料卡片P69——芳香烃
凯库勒式
结构特点:
a、平面结构;
b、碳碳键是一种介于单键和
双键之间的独特的键。
①溴代反应
(1)
取代反应
无色液体,密度大于水
②硝化反应
纯净的硝基苯:无色而有苦杏仁气味的油状液体,不溶于水,密度比水大。硝基苯蒸气有毒性。
硝基苯
注意:苯不能与溴水发生加成反应(但能萃取溴而使水层褪色),说明它比烯烃、炔烃难进行加成反应。
跟H2在镍的存在下加热可生成环己烷:
180℃-250
℃
(2)加成反应
总结苯的化学性质(较稳定):
1.
难氧化(但可燃);
2.
易取代,难加成。
3.
苯兼有饱和烃和不饱和烃的性质,但没有饱和烃稳定,比不饱和烃稳定.
