沪科版高中化 2.1-以食盐为原料的化工产品(共31张PPT)
文档属性
| 名称 | 沪科版高中化 2.1-以食盐为原料的化工产品(共31张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-08-10 00:00:00 | ||
图片预览











文档简介
(共31张PPT)
以食盐为原料的化工产品
一、海水晒盐
海水晒盐
海洋中含氯化钠高达
4×1016
t,可用盐田法取得固体氯化钠。
盐田法:
利用太阳能,蒸发浓缩海水使食盐结晶出来
问题:如何从海水中得到食盐
盐田
我国是海水晒盐产量最多的国家,也是盐田面积最大的国家,我国有盐田37.6万公顷,年产海盐1500万吨左右(其中
100万吨出口)约占全国原盐产量的
70%,目前,我国的海盐产量位居世界之首。
晒盐
思考与讨论
为了使得到的粗盐中除氯化钠外含杂质较少,实际生产中卤水(析出了盐类的海水称为卤水)
的密度范围应控制在什么范围内?
1.21-1.26
g/ml
思考与讨论
经结晶法得到的粗盐,除氯化钠外还含有哪些物质?
怎样提纯呢?
含
MgCl2
MgSO4
KCl
MgBr2和难溶性物质等
再重结晶
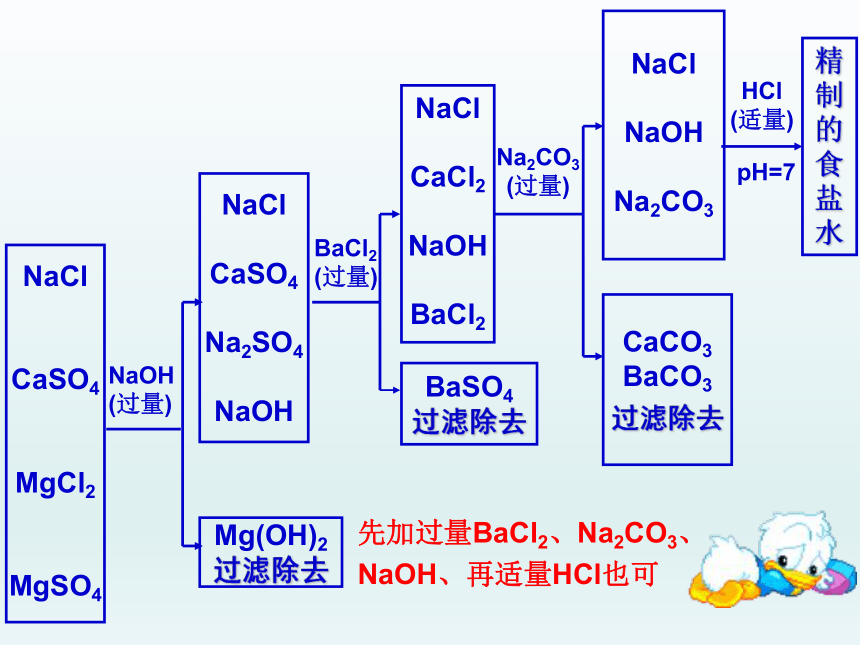
如何精制食盐水,以除去硫酸钙、硫酸镁、氯化镁等杂质?
难溶物过滤
NaCl
CaSO4
MgCl2
MgSO4
先加过量BaCl2、Na2CO3、
NaOH、再适量HCl也可
粗盐的提纯
-走进实验室
所用的仪器?
实验步骤?
溶解、过滤、蒸发、洗涤
过滤的目的是?
洗涤晶体的目的是?
除去不溶性杂质
除去晶体表面少量可溶性杂质。
烧杯、玻璃棒、量筒、过滤组件装置、蒸发组件装置。
思考与讨论
为什么10g
粗盐要量取
30
ml
左右水来
溶解?
35.9g/100gH2O
过滤操作中要注意些什么?
蒸发到即将干时,为什么要停止加热或用小火加热?
200C时氯化钠溶解度
一贴
二低
三靠
防止晶体飞溅
思考与讨论
为什么用少量水洗涤结晶物能除去其中少量的可溶性杂质?
粗盐提纯中几次用到玻棒,每次使用的作用各是什么?
三次使用;1.溶解(搅拌)
2.过滤(引流)3.蒸发(搅拌)
可溶性杂质能溶解在洗涤水中,随洗涤水的流动而离开晶体
你知道海水里前十位元素的含量吗
思考与讨论
两瓶无色液体:氯化钠和水怎样鉴别?
①
测密度
②
测沸点
③
用硝酸银溶液
④蒸发
⑤焰色反应
……
氯、钠、镁、硫、钙;
钾、溴、锶、硼、锂。
【本课要点】
电解饱和食盐水的化学原理
工业上如何精制食盐水
实验室电解饱和食盐水的装置
电离方程式
中国现代化工之母—氯碱工业
电解饱和食盐水(氯碱工业)
通过结晶得到的粗盐还含有可溶性杂质,如:MgCl2、MgSO4、CaSO4、KCl、MgBr2
等
杂质,在氯碱工业中电解
饱和食盐水,需进一步提
纯粗盐以除去钙离子、镁
离子
、硫酸根离子
。
电解饱和的食盐水可以得
到氯气、氢气和氢氧化
钠,大部分食盐用来制氯气、氢气、烧碱和纯碱。
上海氯碱总厂离子膜电解车间
实验与观察
电解饱和食盐水有关的化学方程式2NaCl+2H2O
2NaOH
+
Cl2
↑+
H2
↑
阴极:
阳极:
有气泡;滴入酚酞后阴极附近溶液呈红色。
有气泡;滴入酚酞后阳极附近溶液仍无色,湿润的淀粉碘化钾试纸变蓝色。
动手做一做
1.
用湿润的淀粉碘化钾试纸检验阳极生成的气体
2.
用小试管收集阴极生成的气体,作点燃试验。
现象
淀粉碘化钾试纸变蓝
Cl2
+2KI
→
2KCl
+
I2
现象
发出轻微的“卟”声,管内有淡蓝色的火焰
思考
某直流电源失去正负极标志,如何用化学的方法检出其正负极?
用该直流电源电解氯化钠水溶液,并在两极附近滴入酚酞溶液,变红的一极所接的电源为负极
介绍电离方程式的写法
1.可用电离方程式表示酸、碱、盐的电离
2.强酸(硫酸、盐酸、硝酸等)、强碱(氢氧化钠、氢氧化钾、氢氧化钙、氢氧化钡等)、盐在水溶液中完全电离用“→”表示(强碱、盐在熔融时也能电离)
3.除上述物质以外的酸、碱(即弱酸、弱碱)部分电离用“ ”表示
练习
写出下列物质的电离方程式
硫酸、醋酸、硫酸铝、氯化镁、
氢氧化钠、氢氧化钡、溴化钠、
水、*碳酸、
*碳酸氢钠、
答案
【本课要点】
氯化氢的性质
氯化氢气体的工业及实验室制法
实验室制、取氯化氢气体的装置
实验室制、取气体的装置
气体的净化装置及吸收装置
检验极易溶于水的气体的装置
工业上用氢气在氯气中燃烧制备氯化氢。
盐酸
——氯化氢的水溶液
易挥发的一元强酸,在水中氯化氢全部电离
电离方程式:
HCl
→
H+
+
Cl-
重要的化工基本原料——盐酸和烧碱
实验与观察
1.
观察一瓶氯化氢气体的颜色和状态
2.
打开集气瓶上的玻璃盖,小心嗅闻它的气味,并观察瓶口有什么现象发生
记录
___________________________
3.用一条湿润的蓝石磊试纸接近瓶口,观察现象
记录
____________________________
有刺激性气味,瓶口有白雾
氯化氢的物理性质
蓝石蕊试纸变红
4.氯化氢的水溶性实验
现象
___________
___________________
解释
____________
__________________
_______________
___________________
_________________
_________________
_________________
_________________
___________________
_______________
_________________
_________________
由于氯化氢极易溶于水,当胶头滴管里的水射入烧瓶中后,瓶中的氯化氢迅速溶解在水中,使瓶内的压强瞬间减小,烧杯里的水在大气压力的作用下被压入烧瓶中,形成喷泉;烧瓶中的液体含盐酸,盐酸能使紫石蕊试液变红。
氯化氢的物理性质
形成喷泉;紫石蕊试液变红
探究与实践
实验室制氯化氢气体
反应原理
NaCl
+
H2SO4
NaHSO4
+
HCl
(
NaCl
+
NaHSO4
Na2SO4
+
HCl
)
(
工业上制氯化氢的化学方程式
H2+CI2
2HCI
)
(浓)
设计实验室制氯化氢的装置
固
+
固
加热
固
+
液
常温
固
+
液
加热
提供装置见后
反应物状态
反应条件
实验室制氧气
实验室制二氧化碳
实验室制氯化氢
固+固
加热型
固+液
常温型
固+液
或
液+液
加热型
气体收集装置
气体的净化装置
气体的吸收装置
氢氧化钠
一元强碱,在水中全部电离成钠离子和氢氧根离子
NaOH→Na++OH-
氢氧化钠的用途
以食盐为原料的化工产品
一、海水晒盐
海水晒盐
海洋中含氯化钠高达
4×1016
t,可用盐田法取得固体氯化钠。
盐田法:
利用太阳能,蒸发浓缩海水使食盐结晶出来
问题:如何从海水中得到食盐
盐田
我国是海水晒盐产量最多的国家,也是盐田面积最大的国家,我国有盐田37.6万公顷,年产海盐1500万吨左右(其中
100万吨出口)约占全国原盐产量的
70%,目前,我国的海盐产量位居世界之首。
晒盐
思考与讨论
为了使得到的粗盐中除氯化钠外含杂质较少,实际生产中卤水(析出了盐类的海水称为卤水)
的密度范围应控制在什么范围内?
1.21-1.26
g/ml
思考与讨论
经结晶法得到的粗盐,除氯化钠外还含有哪些物质?
怎样提纯呢?
含
MgCl2
MgSO4
KCl
MgBr2和难溶性物质等
再重结晶
如何精制食盐水,以除去硫酸钙、硫酸镁、氯化镁等杂质?
难溶物过滤
NaCl
CaSO4
MgCl2
MgSO4
先加过量BaCl2、Na2CO3、
NaOH、再适量HCl也可
粗盐的提纯
-走进实验室
所用的仪器?
实验步骤?
溶解、过滤、蒸发、洗涤
过滤的目的是?
洗涤晶体的目的是?
除去不溶性杂质
除去晶体表面少量可溶性杂质。
烧杯、玻璃棒、量筒、过滤组件装置、蒸发组件装置。
思考与讨论
为什么10g
粗盐要量取
30
ml
左右水来
溶解?
35.9g/100gH2O
过滤操作中要注意些什么?
蒸发到即将干时,为什么要停止加热或用小火加热?
200C时氯化钠溶解度
一贴
二低
三靠
防止晶体飞溅
思考与讨论
为什么用少量水洗涤结晶物能除去其中少量的可溶性杂质?
粗盐提纯中几次用到玻棒,每次使用的作用各是什么?
三次使用;1.溶解(搅拌)
2.过滤(引流)3.蒸发(搅拌)
可溶性杂质能溶解在洗涤水中,随洗涤水的流动而离开晶体
你知道海水里前十位元素的含量吗
思考与讨论
两瓶无色液体:氯化钠和水怎样鉴别?
①
测密度
②
测沸点
③
用硝酸银溶液
④蒸发
⑤焰色反应
……
氯、钠、镁、硫、钙;
钾、溴、锶、硼、锂。
【本课要点】
电解饱和食盐水的化学原理
工业上如何精制食盐水
实验室电解饱和食盐水的装置
电离方程式
中国现代化工之母—氯碱工业
电解饱和食盐水(氯碱工业)
通过结晶得到的粗盐还含有可溶性杂质,如:MgCl2、MgSO4、CaSO4、KCl、MgBr2
等
杂质,在氯碱工业中电解
饱和食盐水,需进一步提
纯粗盐以除去钙离子、镁
离子
、硫酸根离子
。
电解饱和的食盐水可以得
到氯气、氢气和氢氧化
钠,大部分食盐用来制氯气、氢气、烧碱和纯碱。
上海氯碱总厂离子膜电解车间
实验与观察
电解饱和食盐水有关的化学方程式2NaCl+2H2O
2NaOH
+
Cl2
↑+
H2
↑
阴极:
阳极:
有气泡;滴入酚酞后阴极附近溶液呈红色。
有气泡;滴入酚酞后阳极附近溶液仍无色,湿润的淀粉碘化钾试纸变蓝色。
动手做一做
1.
用湿润的淀粉碘化钾试纸检验阳极生成的气体
2.
用小试管收集阴极生成的气体,作点燃试验。
现象
淀粉碘化钾试纸变蓝
Cl2
+2KI
→
2KCl
+
I2
现象
发出轻微的“卟”声,管内有淡蓝色的火焰
思考
某直流电源失去正负极标志,如何用化学的方法检出其正负极?
用该直流电源电解氯化钠水溶液,并在两极附近滴入酚酞溶液,变红的一极所接的电源为负极
介绍电离方程式的写法
1.可用电离方程式表示酸、碱、盐的电离
2.强酸(硫酸、盐酸、硝酸等)、强碱(氢氧化钠、氢氧化钾、氢氧化钙、氢氧化钡等)、盐在水溶液中完全电离用“→”表示(强碱、盐在熔融时也能电离)
3.除上述物质以外的酸、碱(即弱酸、弱碱)部分电离用“ ”表示
练习
写出下列物质的电离方程式
硫酸、醋酸、硫酸铝、氯化镁、
氢氧化钠、氢氧化钡、溴化钠、
水、*碳酸、
*碳酸氢钠、
答案
【本课要点】
氯化氢的性质
氯化氢气体的工业及实验室制法
实验室制、取氯化氢气体的装置
实验室制、取气体的装置
气体的净化装置及吸收装置
检验极易溶于水的气体的装置
工业上用氢气在氯气中燃烧制备氯化氢。
盐酸
——氯化氢的水溶液
易挥发的一元强酸,在水中氯化氢全部电离
电离方程式:
HCl
→
H+
+
Cl-
重要的化工基本原料——盐酸和烧碱
实验与观察
1.
观察一瓶氯化氢气体的颜色和状态
2.
打开集气瓶上的玻璃盖,小心嗅闻它的气味,并观察瓶口有什么现象发生
记录
___________________________
3.用一条湿润的蓝石磊试纸接近瓶口,观察现象
记录
____________________________
有刺激性气味,瓶口有白雾
氯化氢的物理性质
蓝石蕊试纸变红
4.氯化氢的水溶性实验
现象
___________
___________________
解释
____________
__________________
_______________
___________________
_________________
_________________
_________________
_________________
___________________
_______________
_________________
_________________
由于氯化氢极易溶于水,当胶头滴管里的水射入烧瓶中后,瓶中的氯化氢迅速溶解在水中,使瓶内的压强瞬间减小,烧杯里的水在大气压力的作用下被压入烧瓶中,形成喷泉;烧瓶中的液体含盐酸,盐酸能使紫石蕊试液变红。
氯化氢的物理性质
形成喷泉;紫石蕊试液变红
探究与实践
实验室制氯化氢气体
反应原理
NaCl
+
H2SO4
NaHSO4
+
HCl
(
NaCl
+
NaHSO4
Na2SO4
+
HCl
)
(
工业上制氯化氢的化学方程式
H2+CI2
2HCI
)
(浓)
设计实验室制氯化氢的装置
固
+
固
加热
固
+
液
常温
固
+
液
加热
提供装置见后
反应物状态
反应条件
实验室制氧气
实验室制二氧化碳
实验室制氯化氢
固+固
加热型
固+液
常温型
固+液
或
液+液
加热型
气体收集装置
气体的净化装置
气体的吸收装置
氢氧化钠
一元强碱,在水中全部电离成钠离子和氢氧根离子
NaOH→Na++OH-
氢氧化钠的用途
