鲁教版九年级上册化学6.3-到实验去:二氧化碳的实验室制取和性质(共21张PPT)
文档属性
| 名称 | 鲁教版九年级上册化学6.3-到实验去:二氧化碳的实验室制取和性质(共21张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-08-09 00:00:00 | ||
图片预览




文档简介
(共21张PPT)
二氧化碳发展史
“千凿万凿出深山,烈火焚烧若等闲。”
公元300年以前,我国发现了二氧化碳的存在。
17世纪,比利时科学家发现了二氧化碳的存在。
1755年,英国科学家发现二氧化碳的存在。
1772年,法国科学家证明其碳、氧原子比为1:2。
历时1500年
二氧化碳的循环与制取
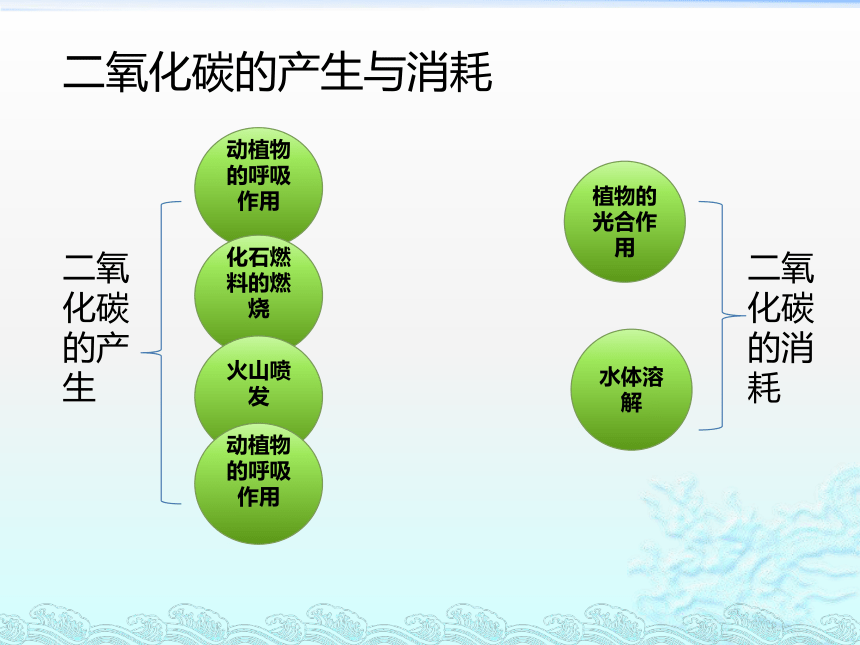
植物的光合作用
水体溶解
动植物的呼吸作用
化石燃料的燃烧
二氧化碳的产生
二氧化碳的消耗
二氧化碳的产生与消耗
火山喷发
动植物的呼吸作用
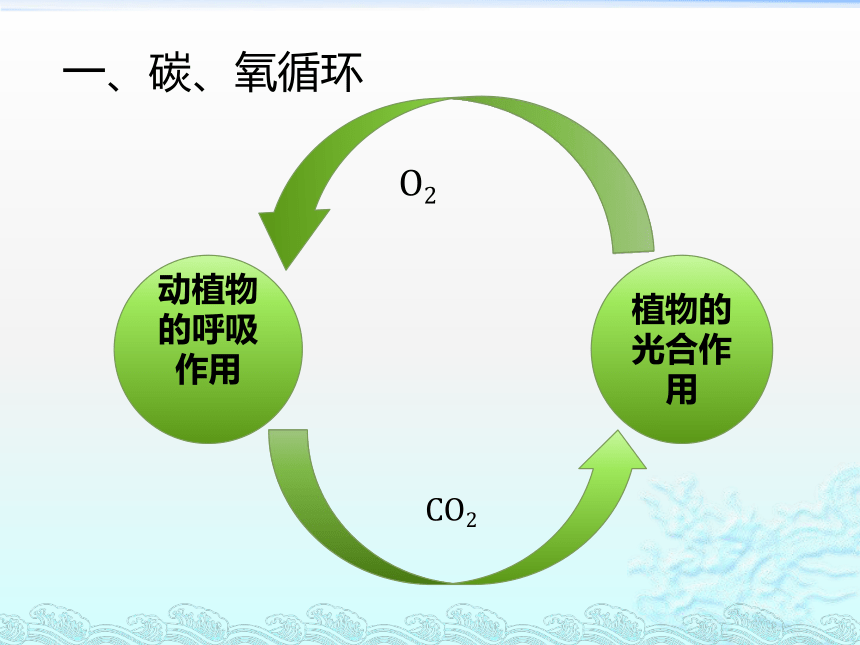
植物的光合作用
动植物的呼吸作用
O2
CO2
一、碳、氧循环
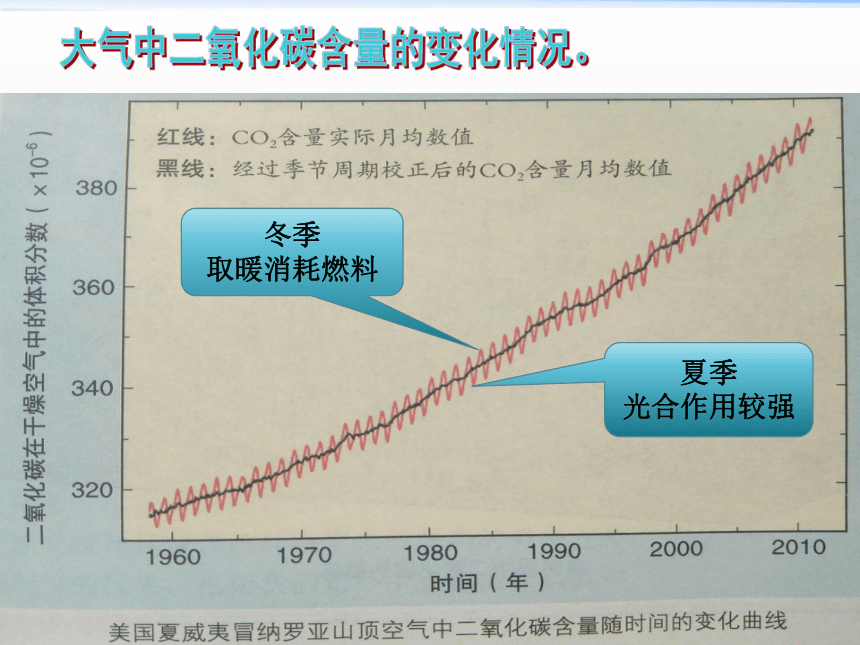
大气中二氧化碳含量的变化情况。
冬季
取暖消耗燃料
夏季
光合作用较强
二氧化碳的影响
二氧化碳含量上升
“温室效应”
缓解温室效应
1、减少化石燃料的燃烧。
2、多植树造林,保护植被。
3、低碳生活。
回顾:用过氧化氢制取氧气流程
1、反应药品:过氧化氢和二氧化锰
2、反应原理:2H2O2
==
2H2O+O2
3、发生装置:固液常温型
4、收集装置:向上排空气法、排水法
5、气体验满:带火星木条放在集气瓶口,观察现象
6、检验气体:带火星木条伸入集气瓶中,观察现象
7、操作步骤:①连接仪器;
②检查装置气密性;
③装药品;
④收集气体;
⑤气体验满;⑥检验气体;
MnO2
回忆:制取氧气的药品有什么特点?
那么制取二氧化碳的药品呢?
氧元素——O
碳、氧元素——C、O
O2
CO2
元素守恒
二、实验室制取二氧化碳
Na2CO3+稀盐酸
迅速产生大量气泡,速率极快
Na2CO3+稀硫酸
迅速产生大量气泡,速率极快
CaCO3+稀盐酸
持续冒出气泡,速率适中
CaCO3+稀硫酸
较快的冒出气泡,但反应一会儿后停止
探究:药品搭配
药品
现象
CaCO3+2HCl==
CaCl2+H2O+CO2↑
1、反应药品
大理石(石灰石)和稀盐酸
2、反应原理
二氧化碳的实验室制取
反应物状态
反应条件
固+液
不需加热
固
加热
固+液
不需加热
装置图
3、制取二氧化碳的发生装置
依据:反应物状态和反应条件
制O2
制CO2
难溶、不易溶或不溶于水,且不与水反应
比空气大,且不与空气中成分反应
向上排空气法
向下排空气法
排水法
比空气小,且不与空气中成分反应
4、气体收集
O2
CO2
装置图
密度
水溶性
常温下,CO2密度比空气大,能溶于水
要求
5、气体的验满
将燃着的木条放在集气瓶口,若木条熄灭,则气体收集满。
将带火星的木条放在集气瓶口,若木条复燃,则气体收集满。
O2
CO2
1、如何检验收集的气体为二氧化碳?
将该气体通入澄清的石灰水中,若澄清石灰水变浑浊,则该气体为二氧化碳。
2、能否用燃着的木条去检验气体是否为二氧化碳?
6、气体的检验
澄清石灰水
变浑浊
不能
7、制取与收集二氧化碳操作步骤:
4、收集气体
2、检查气密性
3、装药品
1、连接仪器
5、气体验满与检验
6、拆除仪器
1、导管刚露出胶塞,便于气体排出。
8、注意事项:
2、长颈漏斗必须伸入液面以下,防止气体从长颈漏斗口逸出。
实验室制取气体的一般思路
小结
定药品
选装置
验气体
石灰石和稀盐酸
元素守恒;
反应条件容易达到;
装置、操作简单;
反应速度适中;
反应物状态;
反应条件;
气体密度;
气体水溶性;
气体的性质
澄清石灰水
CaSO4微溶于水
强烈挥发性,挥发出HCl
反应速率太快
C
导管刚露出胶塞
长颈漏斗必须伸入液面以下
应用向上排空气法收集气体
课后作业:
练习册155-156页,1-6(1)题
谢谢,
再见!
二氧化碳发展史
“千凿万凿出深山,烈火焚烧若等闲。”
公元300年以前,我国发现了二氧化碳的存在。
17世纪,比利时科学家发现了二氧化碳的存在。
1755年,英国科学家发现二氧化碳的存在。
1772年,法国科学家证明其碳、氧原子比为1:2。
历时1500年
二氧化碳的循环与制取
植物的光合作用
水体溶解
动植物的呼吸作用
化石燃料的燃烧
二氧化碳的产生
二氧化碳的消耗
二氧化碳的产生与消耗
火山喷发
动植物的呼吸作用
植物的光合作用
动植物的呼吸作用
O2
CO2
一、碳、氧循环
大气中二氧化碳含量的变化情况。
冬季
取暖消耗燃料
夏季
光合作用较强
二氧化碳的影响
二氧化碳含量上升
“温室效应”
缓解温室效应
1、减少化石燃料的燃烧。
2、多植树造林,保护植被。
3、低碳生活。
回顾:用过氧化氢制取氧气流程
1、反应药品:过氧化氢和二氧化锰
2、反应原理:2H2O2
==
2H2O+O2
3、发生装置:固液常温型
4、收集装置:向上排空气法、排水法
5、气体验满:带火星木条放在集气瓶口,观察现象
6、检验气体:带火星木条伸入集气瓶中,观察现象
7、操作步骤:①连接仪器;
②检查装置气密性;
③装药品;
④收集气体;
⑤气体验满;⑥检验气体;
MnO2
回忆:制取氧气的药品有什么特点?
那么制取二氧化碳的药品呢?
氧元素——O
碳、氧元素——C、O
O2
CO2
元素守恒
二、实验室制取二氧化碳
Na2CO3+稀盐酸
迅速产生大量气泡,速率极快
Na2CO3+稀硫酸
迅速产生大量气泡,速率极快
CaCO3+稀盐酸
持续冒出气泡,速率适中
CaCO3+稀硫酸
较快的冒出气泡,但反应一会儿后停止
探究:药品搭配
药品
现象
CaCO3+2HCl==
CaCl2+H2O+CO2↑
1、反应药品
大理石(石灰石)和稀盐酸
2、反应原理
二氧化碳的实验室制取
反应物状态
反应条件
固+液
不需加热
固
加热
固+液
不需加热
装置图
3、制取二氧化碳的发生装置
依据:反应物状态和反应条件
制O2
制CO2
难溶、不易溶或不溶于水,且不与水反应
比空气大,且不与空气中成分反应
向上排空气法
向下排空气法
排水法
比空气小,且不与空气中成分反应
4、气体收集
O2
CO2
装置图
密度
水溶性
常温下,CO2密度比空气大,能溶于水
要求
5、气体的验满
将燃着的木条放在集气瓶口,若木条熄灭,则气体收集满。
将带火星的木条放在集气瓶口,若木条复燃,则气体收集满。
O2
CO2
1、如何检验收集的气体为二氧化碳?
将该气体通入澄清的石灰水中,若澄清石灰水变浑浊,则该气体为二氧化碳。
2、能否用燃着的木条去检验气体是否为二氧化碳?
6、气体的检验
澄清石灰水
变浑浊
不能
7、制取与收集二氧化碳操作步骤:
4、收集气体
2、检查气密性
3、装药品
1、连接仪器
5、气体验满与检验
6、拆除仪器
1、导管刚露出胶塞,便于气体排出。
8、注意事项:
2、长颈漏斗必须伸入液面以下,防止气体从长颈漏斗口逸出。
实验室制取气体的一般思路
小结
定药品
选装置
验气体
石灰石和稀盐酸
元素守恒;
反应条件容易达到;
装置、操作简单;
反应速度适中;
反应物状态;
反应条件;
气体密度;
气体水溶性;
气体的性质
澄清石灰水
CaSO4微溶于水
强烈挥发性,挥发出HCl
反应速率太快
C
导管刚露出胶塞
长颈漏斗必须伸入液面以下
应用向上排空气法收集气体
课后作业:
练习册155-156页,1-6(1)题
谢谢,
再见!
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
