人教版九年级化学第四单元课题4化学式与化合价(共59张PPT)
文档属性
| 名称 | 人教版九年级化学第四单元课题4化学式与化合价(共59张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 816.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-08-15 00:00:00 | ||
图片预览







文档简介
第四单元 物质构成的奥秘
课题4 化学式和化合价
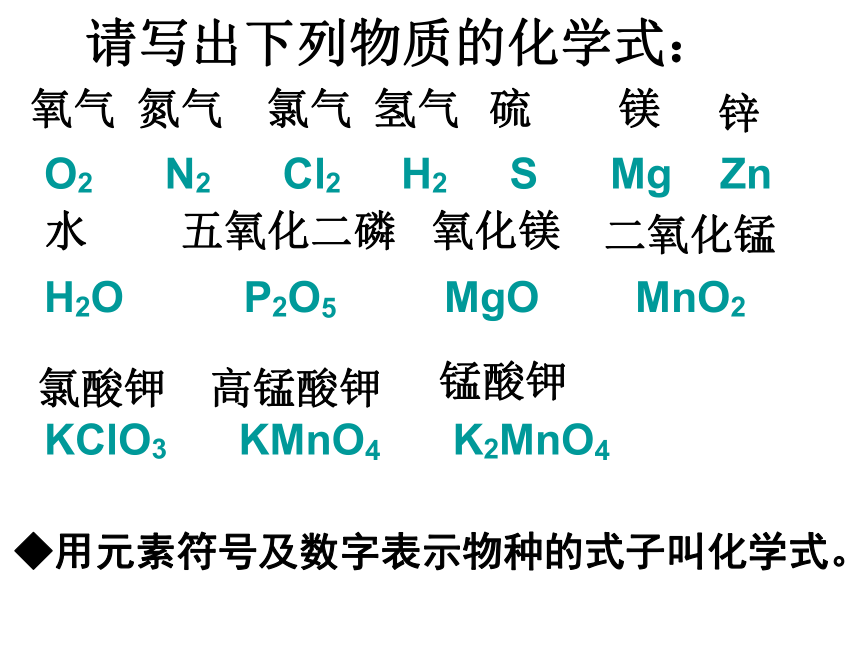
请写出下列物质的化学式:
O2 N2 Cl2 H2 S Mg Zn
H2O P2O5 MgO MnO2
KClO3 KMnO4 K2MnO4
氧气
氮气
氯气
氢气
硫
镁
锌
水
五氧化二磷
氧化镁
二氧化锰
氯酸钾
高锰酸钾
锰酸钾
◆用元素符号及数字表示物种的式子叫化学式。
(1)用元素符号及数字表示物质的式子叫化学式。
如:O2、H2、H2O、KMnO4。
(2)一个化学式表示一种物质。
(3)混合物的化学式用最主要成分的物质的化学式代替。
如:澄清石灰水:Ca(OH)2
稀盐酸:HCl
一.化学式一.化学式
化合价口诀:
K Na H Ag +1价,Ca Mg Ba Zn +2价
F Cl Br I -1价,通常 O是-2价,
亚 Cu+1; Cu +2,亚 Fe+2; Fe +3,
+3金属Au和Al ,
C 有+2和+4,S 有-2,+4和+6。
-1价硝酸根NO3、氢氧根OH,
-2价硫酸根SO4 、碳酸根CO3
-3价磷酸根PO4,+1价铵根NH4
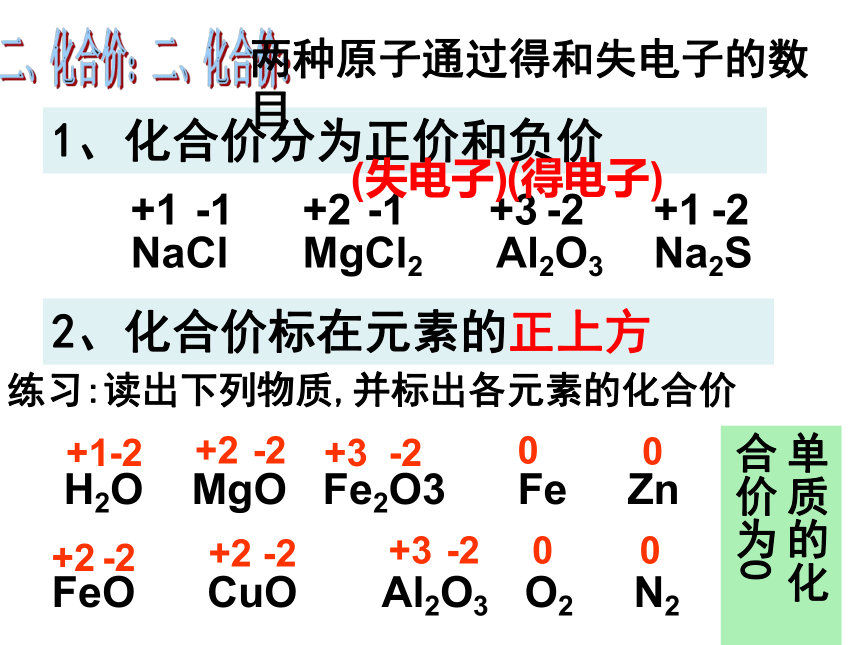
1、化合价分为正价和负价
二、化合价:二、化合价:
NaCl
+1
-1
MgCl2
+2
-1
Al2O3
-2
+1
-2
+3
Na2S
2、化合价标在元素的正上方
两种原子通过得和失电子的数目.
(失电子)
(得电子)
练习:读出下列物质,并标出各元素的化合价
H2O MgO Fe2O3 Fe Zn
FeO CuO Al2O3 O2 N2
+1
-2
-2
+2
+3
-2
+2
-2
+2
-2
+3
-2
0
0
0
0
单质的化合价为0
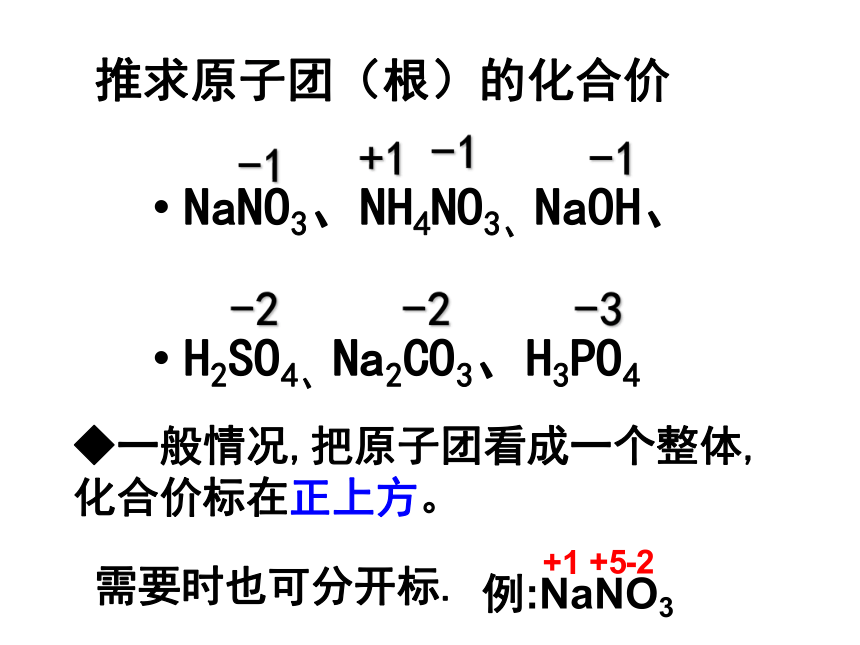
推求原子团(根)的化合价
NaNO3、NH4NO3、NaOH、
H2SO4、Na2CO3、H3PO4
-1
-1
+1
-1
-2
-2
-3
◆一般情况,把原子团看成一个整体,化合价标在正上方。
例:NaNO3
+1
+5
-2
需要时也可分开标.
根据下列化合物的化学式找规律
Al O
S O
P O
Al Cl
Si O
Ca S
+4 -2
+5 -2
+6-2
+3 -1
+3 -2
+2 -2
2 3
2 5
3
3
2
正左负右,约简交叉
3
1
2
1
1
1
分析:分析:
----交叉法
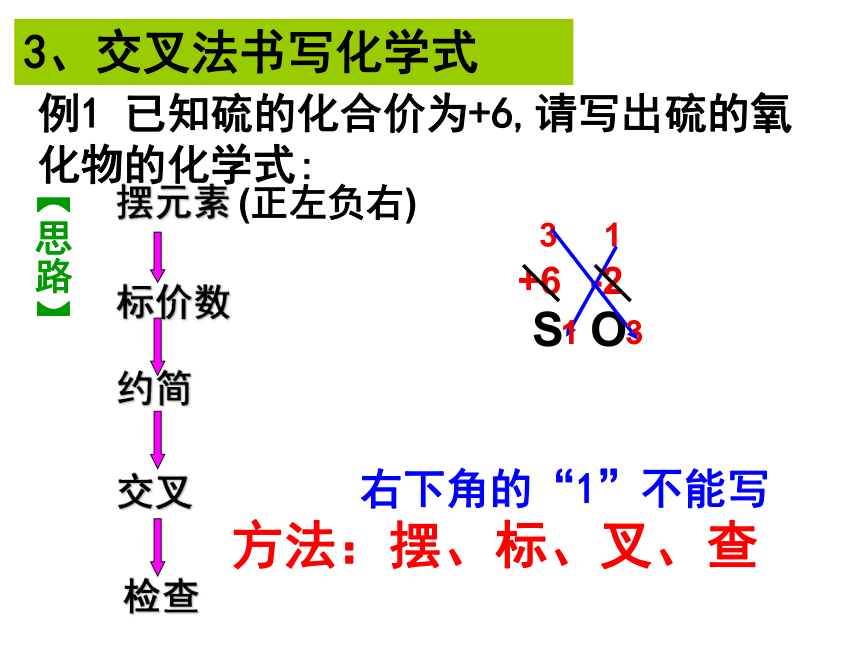
例1 已知硫的化合价为+6,请写出硫的氧化物的化学式:
摆元素
标价数
交叉
检查
约简
【思路】
(正左负右)
S O
+6
-2
3
1
3
1
右下角的“1”不能写
方法:摆、标、叉、查
3、交叉法书写化学式
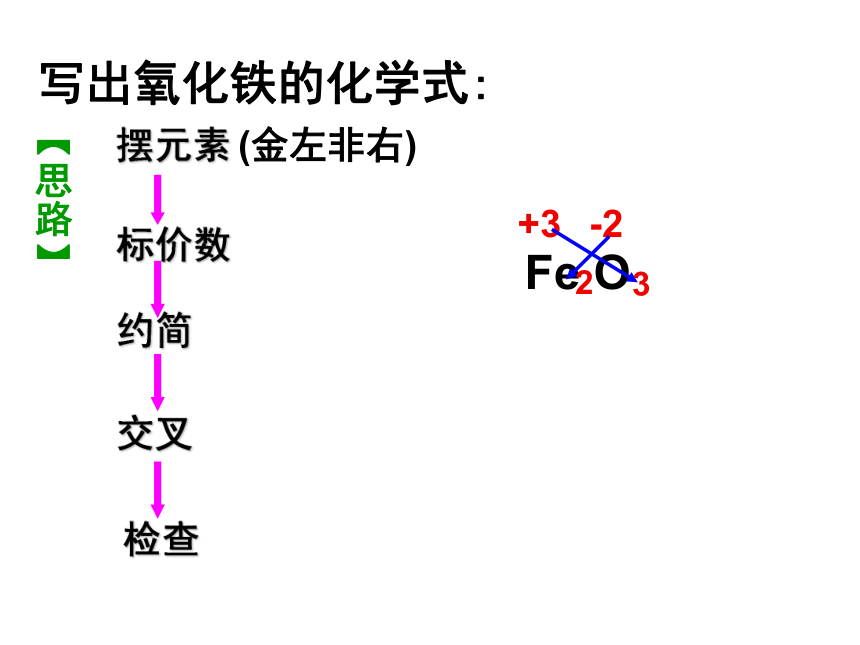
写出氧化铁的化学式:
摆元素
标价数
交叉
检查
约简
【思路】
(金左非右)
Fe O
+3
-2
3
2
写出硫酸铁的化学式:
摆元素
标价数
交叉
检查
约简
【思路】
(金左非右)
Fe SO4
+3
-2
3
2
( )
看一看,找一找,你知哪里错吗?
AlO ; NaO ; KSO4 ; CuNO3
C2O4 ; S2O4 ; S2O6 ; Cu2O2
(K)2SO4 ; Fe(Cl)3 ; (Na)2CO3
Na2O1 ; C1O2 ; K1Cl1 ; H2O1
K(OH) ; Na(NO3) ; Ba(CO3)
+1
+1
+2
+3
+4
+4
+6
+2
-2
-2
-2
-1
-2
-2
-2
-2
CuNO32 Fe2SO43 CaOH2
+2
+3
+2
-1
-1
-2
错的原因:
只排出元素,没有用化合价交叉
右下角的1不写.
化合价没有约简.
单一元素不能有括号
右下角没有数字的原子团,不能加上括号.
右下角要写数字的原子团必需先括号
更正下列化学式中的错误
Fe3O2
Mn2O4
Cl2Ca
Ca2(PO4)3
+4 -2
+3 -2
-1 +2
+2 -3
MnO2
Fe2O3
CaCl2
Ca3(PO4)2
7、利用交叉法,写出下列物质的化学式:
硫酸 ;硝酸 ;碳酸 ;
氧化亚铁 ;氧化镁 ;氧化钾 ;氧化铜 ;
氢氧化钡 ;氢氧化钠 ;氢氧化钙 ;氢氧化镁
氯化镁 ;氯化铝 ;氯化银 ;氯化亚铁 ;
硫酸铁 ;硫酸钠 ;硫酸钡 ;硫酸亚铁 ;
硝酸钙 ;硝酸钠 ;硝酸铜 ;硝酸银 ;
碳酸钾 ; 碳酸钠 ;碳酸钙 ;碳酸银 .
MgO
FeO
H2CO3
H2SO4
HNO3
NaOH
Ba(OH)2
Ca(OH)2
CuO
K2O
Mg(OH)2
MgCl2
AlCl3
FeCl2
AgCl
Na2SO4
BaSO4
FeSO4
Fe2(SO4)3
NaNO3
Ca(NO3)2
Cu(NO3)2
AgNO3
K2CO3
Na2CO3
CaCO3
Ag2CO3
常错的化学式:
氦气 ;氖气 ;氩气 ;
氧化铁 ;氧化亚铁 ;氧化铝 ;
氧化钠 ;氧化钾 ;亚硫酸 ;
氢氧化铁 ;氢氧化亚铁 ;
氯化铁 ;氯化亚铁 ;
硝酸铁 ;硝酸亚铁 ;
硫酸钾 ;硫酸钠 ;
硫酸铝 ;硫酸铁 ;
碳酸钾 ;碳酸钠 ;氨气 ;
碳酸银 ;碳酸氢钠 ;氨水 .
He
Ne
Ar
Fe2O3
FeO
H2SO3
Fe(OH)3
NH3?H2O
Al2O3
K2O
Na2O
Fe(OH)2
FeCl2
FeCl3
Fe(NO3)2
Fe(NO3)3
K2SO4
Na2SO4
Al2(SO4)3
Fe2(SO4)3
K2CO3
Na2CO3
Ag2CO3
NaHCO3
NH3
你一定要会哟!
4、化合价的有关规律
①在化合物中,正负化合价分别乘于右下角数字相加等于0
②单质里元素的化合价为零
③同种元素在不同的化合物里可显不同的化合价
④同种元素在同一化合物里也可能显不同的化合价
如NH4NO3
-3
+5
+2
+3
如FeO,Fe2O3
比较并找规律
NaCl
MgCl2
Al2O3
HF
CO
Na+
Mg2+
Al3+
F-
O2-
+1
+2
+3
-1
-2
5、化合价与离子所带电荷数值和正负相同,但
离子
化合价
书写的位置不同.
数值和符号相反.
钾离子 ;钙离子 ;氧离子 ;氯离子 ;硫离子 ;
硝酸根离子 ;氢氧根离子 ;硫酸根离子 ;碳酸根离子 ;磷酸根离子 ;铵根离子 。
K+
O2-
Ca2+
Cl-
S2-
NO3-
OH-
SO42-
CO32-
PO43-
NH4+
练习:利用化合价书写离子符号练习:利用化合价书写离子符号
(必考)
例1 试确定氯酸钾中氯元素的化合价
【思路】
写
K Cl O3
设
列
+1+X+(-2) ×3=0
验
X=+5
+1
-2
X
标
(写化学式)
(设X)
(标定价)
(利用正负化合价分别乘以右下角数字相加等于0来列算式)
(检验正负化合价分别乘以右下角数字相加是否为0)
6、求化合物中某元素的化合价
如:SO3
X
-2
+
X=+6
X ?1
(-2)
?3
=O
如:H2SO4
X
-2
X ?1
(-2)
?2
=O
+
X=+6
+1
(+1)?2
+
Fe(NO3) 3
X
-1
X
+
(-1)
?3
=0
X
=
+3
练习:求下列有横线的元素的化合价
Fe2O3 H2SO3 Cu(OH) 2 K2MnO4
O2 Zn
H2RO3 H2RO4 HmROm+2 R(NO3) 3
+3
+5
+2
+6
0
+4
+6
m+4
+3
0
RO42-
+6
1、A原子的最外层有7个电子,B原子的最外层上有2个电子,由A和B组成的化合物的化学式是 。
2、X粒子的结构示意图为 ,Y
粒子的结构示意图为 ,X、Y组
成物质的化学式 。
BA2
X2Y3
7、根据最外层电子数,确定化合价,再写化学式
三、化学式表示的意义三、化学式表示的意义
①表示这种物质.
②表示该物质由什么元组成.
③表示一个分子.
④表示一个分子由几个什么原子构成.
化学式CO2的意义
化学式的意义
宏观意义
宏观意义
微观意义
微观意义
④表示一个分子由几个什么原子构成。
①表示这种物质
③表示一个分子
②表示该物质由什么元组成
练习练习
①表示二氧化碳这种物质.
②表示二氧化碳由碳元素和氧元素组成.
③表示一个二氧化碳分子.
④表示一个二氧化碳分子由一个碳原子和两个氧原子构成.
①二氧化硫这种物质。
②二氧化硫由硫元素和氧元素组成。
③一个二氧化硫分子。
④一个二氧化硫分子由一个硫原子和两个氧原子构成。
如:SO2
H
2H
H2
2H2
氢元素
1个氢原子
2个氢原子
2个氢分子
1个氢分子
1个氢分子含有2个氢原子
符号H、2H、H2、2H2各具有什么意义?
R
b
c
a
+
-
b
+
-
①多少个分子、多少个原子、多少个离子
②每个什么分子含有几个什么原子
③每个什么离子带多少个单位正或负电荷
④某物质中,什么元素的化合价为多少
四、化学符号周围数字表示的意义四、化学符号周围数字表示的意义
练习:判断下列带横线符号中,哪些是原子,哪些是分子,哪些是离子?
N, 3S, 4O , 8Hg
2O2 ,5SO2 ,N2 , 3Cl2
O2-,5Na+, Mg2+ , 7Cl-, 2SO42-
(原子)
(分子)
(离子)
练习:写出下列“2”的意义:
2H2O
2K+ :
2N:
①2个水分子,②每个水分子中含有2个氢原子.
2个钾离子
2个氮原子
3Cl2
4P2O5
每个五氧化二磷分子中含有2个磷原子。
每个氯分子中含有2个氯原子。
Ca2+
每个镁离子带2个单位正电荷。
Mg2+
每个钙离子带2个单位正电荷。
在氧化钙中,钙元素化合价为+2。
①在三氧化二铝中,氧元素化合价为-2。
+2
CaO
-2
Al2O3
②每个三氧化二铝分子含有2个铝原子.
练习:写出下列“3”的意义:
每个三氧化硫分子中含有3个氧原子。
每个钙离子带2个单位正电荷。
在三氧化二铁中,铁元素化合价为+3。
3个三氧化硫分子
3Al3+
+3
Fe2O3
3SO3
3个铝离子
每个氧化铁分子中含有3个氧原子。
1.写出下列的化学符号:
①2个氢分子 ;②4个钙离子 ; ③2个磷原子 ; ④4个磷原子构成的白磷分子 ; ⑤由60个碳原子构成的碳分子 ; ⑥由1个硫原子和2个氧原子构成的二氧化硫分子 .
2.写出下列的化学符号或意义:
2个铁原子
5个水分子
+3价的铝元素
由3个氧原子构成的一个臭氧分子
一氧化碳中碳元素显+2价
2P2O5
Al3+
2H2
4Ca2+
2P
P4
C60
SO2
2Fe
5H2O
Al2O3
+3
O3
CO
+2
2个五氧化二磷分子
3个铝离子
五、有关相对分子质量的计算五、有关相对分子质量的计算
1、计算原子数比1、计算原子数比
2、计算元素质量比2、计算元素质量比
3、计算相对分子质量3、计算相对分子质量
4、计算某元素质量分数4、计算某元素质量分数
5、计算一定质量化合物中某元素质量5、计算一定质量化合物中某元素质量
6、计算含一定量某元素的化合物质量6、计算含一定量某元素的化合物质量
7、有关杂质计算7、有关杂质计算
关键—先写出化学式!
P2O5 MgO Fe2O3 Ba(OH) 2 Ca(OH) 2
Al(OH)3 Mg(NO3)2 Al(NO3)3 Al2 (SO4)3
Fe2 (SO4)3 Cu2 (OH) 2 CO3 NH4NO3
谁最快:谁最快:
说出下列物质中氧原子个数
5个O
1个O
3个O
2个O
2个O
3个O
6个O
9个O
12个O
12个O
5个O
3个O
1、计算原子数比1、计算原子数比
(1)K2Cr2O7中钾原子和铬原子和氧原子个数比 .
练一练:氯酸钾中各原子个数比 。
2:2:7
KClO3
看成
K1C1O3
1:1:3
(化学式右下角数字比)
(2)Cu2(OH)2CO3中各种原子个数比 。
(3)碳酸氢钙[Ca(HCO3)2]中钙元素、氢元素
、碳元素、氧元素的最简原子个数比是
( )
2:5:2:1
(Cu、O、H、C)
A.1:1:1:3 B.20:1:12:48 C.1:1:1:6 D.1:2:2:6
D
(1)、二氧化碳中各种元素质量比 。
2、计算元素质量比2、计算元素质量比
(相对原子质量×右下角数字之比)
查:C-12,
O-16
CO2
12
=
=3:8
12:32
:
16
x
2
(2).氯酸钾中各种元素质量比 .
KClO3
=3:8
练
39:35.5:48
(3)、Cu2(OH)2CO3中Cu、H、C、O的质量比
。
(4)、葡萄糖(C6H12O6)是一种重要的营养物质.求出葡萄糖中各元素的质量最简比为
.
测一测测一测
127:2:12:80
18:3:24
(1)O2的相对分子质量=
3、计算相对分子质量3、计算相对分子质量
16
X
2
=32
查:O-16; H-1
32
(各相对原子质量×右下角数字之和)
1
X
2
+
16
=18
18
(2)H2O的相对分子质量=
试一试:
1.二氧化碳CO2的相对分子质量 。
2.油炸食物中可能会含有微量的丙烯醛(C3H4O)等有毒物质,求这种物质的相对分子质 .
44
56
C-12,O-16,H-1
(3)氢氧化钙的相对分子质量 。
Ca(OH) 2
练一练:
1、氢氧化铜的相对分子质量 。
2、 Al2(SO4)3的相对分子质量 。
Ca-40,0-16,H-1, Cu-64,S-32,Al-27
74
98
342
(4) CuSO4?5H2O的相对分子质量 。
练习:
1、 Na2CO3?10H2O的相对分子质量 。
64
+
32
+
16X4
↓
+
5
(
1X2
+16
)
=250
=250
Cu-64,S-32,O-16,H-1, Na-23,C-12
268
(5)CO2相对分子质量总和 。
练一练
1、5 SO3相对分子质量总和 。
2、2HCl相对分子质量总和 。
3、3 H2SO4相对分子质量总和 。
132
400
71
294
4、计算某元素质量分数4、计算某元素质量分数
(1)H20
2H
H%=
2H
H20
×100%
=
2×1
1×2+16
×100%
=11.1%
氢元素占水的质量分数?氢元素占水的质量分数?
某元素质量分数=
该原子×右下角数字
化学式
×100%
(1) H2O
4、计算某元素质量分数4、计算某元素质量分数
→
2H
2H
氢元素质量分数
=
————
H2O
X100%
=
2X1
————
1X2+16
X100%
H-1,O-16
氢元素占水的质量分数?氢元素占水的质量分数?
某元素质量分数=
该原子×右下角数字
化学式
(
)
=
11.1%
____________
→
2N
氮元素质量分数
=
2N
————
NH4NO3
X100%
=
2X14
14+1X4+14+16X3
X100%
=35%
1、求氧化铁Fe2O3中铁元素的质量分数?
2、计算二氧化硫中硫元素的质量分数?
50%
70%
计算化肥硝酸铵(NH4NO3)中氮元素的质量分数。
NH4NO3
例:求160g三氧化硫中氧元素的质量?
SO3
5、计算一定质量化合物中某元素质量5、计算一定质量化合物中某元素质量
1.求32g氧化铁中铁元素的质量。
32g
2.8g
分析题目列比例
2.求180g葡萄糖(C6H12O6)中含碳元素的质量
144g
3O
160g
x
32+16x3
3x16
=
160g
x=96g
x3x16
=
x
80
例:求多少克三氧化硫中含32g氧元素?
SO3
80g
1、求多少克二氧化碳中含g碳元素?
22g
2、求多少克硫酸中含2g氢元素?
98g
6、计算含一定量某元素的化合物质量6、计算含一定量某元素的化合物质量
3O
x
32g
32+16x3
3x16
=
x
x=53.3g
·3x16
=
32g
80·
分析题目列比例
2、98g硫酸溶液(含H2SO410%)中含硫元素多少克?
例:求100g赤铁矿(含Fe2O3 75%)中铁元素质量?
7、有关杂质计算7、有关杂质计算
19.5g
1、100g盐酸(含氯化氢20%)中含氯元素多少克?
52.5g
100gX75%=75g
Fe2O3
3.3g
2Fe
75g
x
56x2+16x3
2x56
=
75g
x=52.5g
x2x56
=
x
160
分析题目列比例
计算类型
计算方法
1.计算原子个数
2.计算元素质量比
3.计算相对分子质量
4.计算某元素质量分数
5.计算一定质量化合物中某元素质量
6.计算含一定质量某元素的化合物质量
7.有关杂质计算
(化学式右下角数字比)
相对原子质量×右下角数字之比)
(相对原子质量×右下角数字之和)
该原子×右下角数字
质量分数=
化学式
分析题目列比例
分析题目列比例
分析题目列比例
下图中“ ”和“ ”表示两种不同原子,下列方框中表示混合物的是( )
A
B
C
B
B
想一想
根据给出的信息,写出下列有关物质的化学式
H2
K2O
H2O
KClO3
HCl
用H、K、Cl、O、Cl等元素符号写出化学式
①单质 ;②金属氧化物 ; ③非金属氧化物 ;④酸 ; ⑤制取氧气的物质 ;
+1
+1
-1
-2
+5
3.写出下列的化学符号:
①氢氧化钙在水中存在的离子是 ; ②氢氧化钠溶液中的阳离子是 ; ③氢氧化钾溶液中能使酚酞溶液变红色,其原因是溶液中含有大量 的缘故. ④氯化钠溶液中存在的粒子 .
Ca2+
OH-
Na+
OH-
OH-
Na+
H2O
根据给出的信息,写出下列有关物质的化学式
①抢救非典肺炎病人的呼吸机输入的单质气体 ; ②海水中含量最多的氧化物 ; ③空气中含量最多的气体 ; ④实验室常用来制取氧气的一种暗紫色固体 ; ⑤温度中常用的一种液体(水银温度计中的液体) ; ⑥地壳总含量最高的金属元素组成的氧化物 .
O2
H2O
N2
KMnO4
Hg
Al2O3
1、下列物质中氯元素化合价最低的是( )
A Cl2 B HCl C HClO D KClO3
2、石棉的熔点高,以不易燃烧,可制作石棉网,石棉的化学式可表示为CaMg3Si4O12,其中硅元素的化合价为( )
A +1 B +2 C +3 D +4
3、钛铁矿主要成分的化学式为FeTiOx,其中铁元素和钛元素的化合价均显+3价,则X为( )
A 2 B 3 C 4 D 6
4、酸根阴离子RO42-中R的化合价是( )
A -2 B 0 C +4 D +6
练练:你能对多少?练练:你能对多少?
B
D
B
D
1.味精是人们熟悉的食品助鲜剂,其化学式为C5NH8O4Na,它是由 种元素组成,其是,碳元素、氮元素及氢元素的原子个数比是 ;氧元素与钠元素的质量比是 ;169g该物质是含钠元素的质量是 ; g该物质中含有32g氧元素.
看你掌握了多少!
5
5:1:8
64:23
23g
84.5
2.目前市场上的补钙药剂很多,右图是某品牌补钙药品的部分说明书.如果按用量服用,则每天补充钙元素的质量为( ) A.0.5gB.1gC.1.25gD.0.25g
XX钙片
[药品规格]
每片含CaCO3
0.625g
[用法用量]
每次一片,
每天2次
A
1、计算Cu2 (OH) 2 CO3中氧元素的质量分数。
2、求106g碳酸钠中含多少克氧元素?
3、求葡萄糖[C6H12O6]中碳元素的质量分数 ,180g葡萄糖中含有 g碳元素?
4、求多少克氧化铝中含48g氧元素?
5、100g石灰石(含杂质 10%)中含钙元素多少克?(石灰石中主要成分CaCO3 )
36%
40%
48g
72
102g
36g
练一练:
铁 Fe 镁 Mg 锌 Zn 铝 Al 硫 S 红磷 P 白磷 P 碳 C 氦气 He 氖气 Ne 氩气 Ar
单质:
氧气 O2 氮气 N2 氯气 Cl2 氢气 H2
1.双原子分子单质的化学式:(4个)
2.金属、非金属、稀有气体单质的化学式:
在元素符号右下角加2
用元素符号直接表示化学式.
二、简单化学式的写法和读法二、简单化学式的写法和读法
二氧化碳 CO2;一氧化碳 CO; 二氧化硫SO2 ;
三氧化硫 SO3;五氧化二磷 P2O5;二氧化锰 MnO2; 二氧化氮NO2;四氧化三铁Fe3O4;三氧化二铁Fe2O3;
氧化物:
氧化铁 Fe2O3;氧化亚铁 FeO;氧化镁 MgO;
氧化铜 CuO; 氧化铝 Al2O3; 氧化钙CaO; 氧化钾 K2O;氧化钠Na2O:氧化钡BaO;水H2O;
3.名称中有数字的物质的化学式:
4.名称中没有数字的物质的化学式:
用交叉法,读作“氧化某”
后读先写,读作“几氧化几某”
盐酸 HCl;硫酸 H2SO4;硝酸 HNO3;
碳酸 H2CO3;亚硫酸 H2SO3;磷酸 H3PO4;
酸:
5.酸的化学式:
氢氧化钠 NaOH; 氢氧化钾 KOH;
氢氧化钡 Ba(OH)2;氢氧化钙 Ca(OH)2; 氢氧化镁 Mg(OH)2;氢氧化铝 Al(OH)3; 氢氧化铁 Fe(OH)3;氢氧化铜 Cu(OH)2; 氢氧化锌 Zn(OH)2;氨气 NH3
碱:
6.碱的化学式:
要OH结尾,再用交叉法(氨气NH3除外),读作“氢氧化某”.
要H开头,再用交叉法.读作“某酸”
小结:化学式的写法和读法小结:化学式的写法和读法
(1)双原子分子单质的化学式:在元素符号右下角加2
(2)除双原子分子外的单质的化学式:用元素符号直接表示.
(5)酸的化学式:要H开头,再用交叉法.读作“某酸”
(6)碱的化学式:要OH结尾,再用交叉法(氨气NH3除外),读作“氢氧化某”.
(3)名称中有数字的物质的化学式:后读先写;读作“几氧化几某”
(4)名称中没有数字的物质的化学式:用交叉法,读作“氧化某”
课题4 化学式和化合价
请写出下列物质的化学式:
O2 N2 Cl2 H2 S Mg Zn
H2O P2O5 MgO MnO2
KClO3 KMnO4 K2MnO4
氧气
氮气
氯气
氢气
硫
镁
锌
水
五氧化二磷
氧化镁
二氧化锰
氯酸钾
高锰酸钾
锰酸钾
◆用元素符号及数字表示物种的式子叫化学式。
(1)用元素符号及数字表示物质的式子叫化学式。
如:O2、H2、H2O、KMnO4。
(2)一个化学式表示一种物质。
(3)混合物的化学式用最主要成分的物质的化学式代替。
如:澄清石灰水:Ca(OH)2
稀盐酸:HCl
一.化学式一.化学式
化合价口诀:
K Na H Ag +1价,Ca Mg Ba Zn +2价
F Cl Br I -1价,通常 O是-2价,
亚 Cu+1; Cu +2,亚 Fe+2; Fe +3,
+3金属Au和Al ,
C 有+2和+4,S 有-2,+4和+6。
-1价硝酸根NO3、氢氧根OH,
-2价硫酸根SO4 、碳酸根CO3
-3价磷酸根PO4,+1价铵根NH4
1、化合价分为正价和负价
二、化合价:二、化合价:
NaCl
+1
-1
MgCl2
+2
-1
Al2O3
-2
+1
-2
+3
Na2S
2、化合价标在元素的正上方
两种原子通过得和失电子的数目.
(失电子)
(得电子)
练习:读出下列物质,并标出各元素的化合价
H2O MgO Fe2O3 Fe Zn
FeO CuO Al2O3 O2 N2
+1
-2
-2
+2
+3
-2
+2
-2
+2
-2
+3
-2
0
0
0
0
单质的化合价为0
推求原子团(根)的化合价
NaNO3、NH4NO3、NaOH、
H2SO4、Na2CO3、H3PO4
-1
-1
+1
-1
-2
-2
-3
◆一般情况,把原子团看成一个整体,化合价标在正上方。
例:NaNO3
+1
+5
-2
需要时也可分开标.
根据下列化合物的化学式找规律
Al O
S O
P O
Al Cl
Si O
Ca S
+4 -2
+5 -2
+6-2
+3 -1
+3 -2
+2 -2
2 3
2 5
3
3
2
正左负右,约简交叉
3
1
2
1
1
1
分析:分析:
----交叉法
例1 已知硫的化合价为+6,请写出硫的氧化物的化学式:
摆元素
标价数
交叉
检查
约简
【思路】
(正左负右)
S O
+6
-2
3
1
3
1
右下角的“1”不能写
方法:摆、标、叉、查
3、交叉法书写化学式
写出氧化铁的化学式:
摆元素
标价数
交叉
检查
约简
【思路】
(金左非右)
Fe O
+3
-2
3
2
写出硫酸铁的化学式:
摆元素
标价数
交叉
检查
约简
【思路】
(金左非右)
Fe SO4
+3
-2
3
2
( )
看一看,找一找,你知哪里错吗?
AlO ; NaO ; KSO4 ; CuNO3
C2O4 ; S2O4 ; S2O6 ; Cu2O2
(K)2SO4 ; Fe(Cl)3 ; (Na)2CO3
Na2O1 ; C1O2 ; K1Cl1 ; H2O1
K(OH) ; Na(NO3) ; Ba(CO3)
+1
+1
+2
+3
+4
+4
+6
+2
-2
-2
-2
-1
-2
-2
-2
-2
CuNO32 Fe2SO43 CaOH2
+2
+3
+2
-1
-1
-2
错的原因:
只排出元素,没有用化合价交叉
右下角的1不写.
化合价没有约简.
单一元素不能有括号
右下角没有数字的原子团,不能加上括号.
右下角要写数字的原子团必需先括号
更正下列化学式中的错误
Fe3O2
Mn2O4
Cl2Ca
Ca2(PO4)3
+4 -2
+3 -2
-1 +2
+2 -3
MnO2
Fe2O3
CaCl2
Ca3(PO4)2
7、利用交叉法,写出下列物质的化学式:
硫酸 ;硝酸 ;碳酸 ;
氧化亚铁 ;氧化镁 ;氧化钾 ;氧化铜 ;
氢氧化钡 ;氢氧化钠 ;氢氧化钙 ;氢氧化镁
氯化镁 ;氯化铝 ;氯化银 ;氯化亚铁 ;
硫酸铁 ;硫酸钠 ;硫酸钡 ;硫酸亚铁 ;
硝酸钙 ;硝酸钠 ;硝酸铜 ;硝酸银 ;
碳酸钾 ; 碳酸钠 ;碳酸钙 ;碳酸银 .
MgO
FeO
H2CO3
H2SO4
HNO3
NaOH
Ba(OH)2
Ca(OH)2
CuO
K2O
Mg(OH)2
MgCl2
AlCl3
FeCl2
AgCl
Na2SO4
BaSO4
FeSO4
Fe2(SO4)3
NaNO3
Ca(NO3)2
Cu(NO3)2
AgNO3
K2CO3
Na2CO3
CaCO3
Ag2CO3
常错的化学式:
氦气 ;氖气 ;氩气 ;
氧化铁 ;氧化亚铁 ;氧化铝 ;
氧化钠 ;氧化钾 ;亚硫酸 ;
氢氧化铁 ;氢氧化亚铁 ;
氯化铁 ;氯化亚铁 ;
硝酸铁 ;硝酸亚铁 ;
硫酸钾 ;硫酸钠 ;
硫酸铝 ;硫酸铁 ;
碳酸钾 ;碳酸钠 ;氨气 ;
碳酸银 ;碳酸氢钠 ;氨水 .
He
Ne
Ar
Fe2O3
FeO
H2SO3
Fe(OH)3
NH3?H2O
Al2O3
K2O
Na2O
Fe(OH)2
FeCl2
FeCl3
Fe(NO3)2
Fe(NO3)3
K2SO4
Na2SO4
Al2(SO4)3
Fe2(SO4)3
K2CO3
Na2CO3
Ag2CO3
NaHCO3
NH3
你一定要会哟!
4、化合价的有关规律
①在化合物中,正负化合价分别乘于右下角数字相加等于0
②单质里元素的化合价为零
③同种元素在不同的化合物里可显不同的化合价
④同种元素在同一化合物里也可能显不同的化合价
如NH4NO3
-3
+5
+2
+3
如FeO,Fe2O3
比较并找规律
NaCl
MgCl2
Al2O3
HF
CO
Na+
Mg2+
Al3+
F-
O2-
+1
+2
+3
-1
-2
5、化合价与离子所带电荷数值和正负相同,但
离子
化合价
书写的位置不同.
数值和符号相反.
钾离子 ;钙离子 ;氧离子 ;氯离子 ;硫离子 ;
硝酸根离子 ;氢氧根离子 ;硫酸根离子 ;碳酸根离子 ;磷酸根离子 ;铵根离子 。
K+
O2-
Ca2+
Cl-
S2-
NO3-
OH-
SO42-
CO32-
PO43-
NH4+
练习:利用化合价书写离子符号练习:利用化合价书写离子符号
(必考)
例1 试确定氯酸钾中氯元素的化合价
【思路】
写
K Cl O3
设
列
+1+X+(-2) ×3=0
验
X=+5
+1
-2
X
标
(写化学式)
(设X)
(标定价)
(利用正负化合价分别乘以右下角数字相加等于0来列算式)
(检验正负化合价分别乘以右下角数字相加是否为0)
6、求化合物中某元素的化合价
如:SO3
X
-2
+
X=+6
X ?1
(-2)
?3
=O
如:H2SO4
X
-2
X ?1
(-2)
?2
=O
+
X=+6
+1
(+1)?2
+
Fe(NO3) 3
X
-1
X
+
(-1)
?3
=0
X
=
+3
练习:求下列有横线的元素的化合价
Fe2O3 H2SO3 Cu(OH) 2 K2MnO4
O2 Zn
H2RO3 H2RO4 HmROm+2 R(NO3) 3
+3
+5
+2
+6
0
+4
+6
m+4
+3
0
RO42-
+6
1、A原子的最外层有7个电子,B原子的最外层上有2个电子,由A和B组成的化合物的化学式是 。
2、X粒子的结构示意图为 ,Y
粒子的结构示意图为 ,X、Y组
成物质的化学式 。
BA2
X2Y3
7、根据最外层电子数,确定化合价,再写化学式
三、化学式表示的意义三、化学式表示的意义
①表示这种物质.
②表示该物质由什么元组成.
③表示一个分子.
④表示一个分子由几个什么原子构成.
化学式CO2的意义
化学式的意义
宏观意义
宏观意义
微观意义
微观意义
④表示一个分子由几个什么原子构成。
①表示这种物质
③表示一个分子
②表示该物质由什么元组成
练习练习
①表示二氧化碳这种物质.
②表示二氧化碳由碳元素和氧元素组成.
③表示一个二氧化碳分子.
④表示一个二氧化碳分子由一个碳原子和两个氧原子构成.
①二氧化硫这种物质。
②二氧化硫由硫元素和氧元素组成。
③一个二氧化硫分子。
④一个二氧化硫分子由一个硫原子和两个氧原子构成。
如:SO2
H
2H
H2
2H2
氢元素
1个氢原子
2个氢原子
2个氢分子
1个氢分子
1个氢分子含有2个氢原子
符号H、2H、H2、2H2各具有什么意义?
R
b
c
a
+
-
b
+
-
①多少个分子、多少个原子、多少个离子
②每个什么分子含有几个什么原子
③每个什么离子带多少个单位正或负电荷
④某物质中,什么元素的化合价为多少
四、化学符号周围数字表示的意义四、化学符号周围数字表示的意义
练习:判断下列带横线符号中,哪些是原子,哪些是分子,哪些是离子?
N, 3S, 4O , 8Hg
2O2 ,5SO2 ,N2 , 3Cl2
O2-,5Na+, Mg2+ , 7Cl-, 2SO42-
(原子)
(分子)
(离子)
练习:写出下列“2”的意义:
2H2O
2K+ :
2N:
①2个水分子,②每个水分子中含有2个氢原子.
2个钾离子
2个氮原子
3Cl2
4P2O5
每个五氧化二磷分子中含有2个磷原子。
每个氯分子中含有2个氯原子。
Ca2+
每个镁离子带2个单位正电荷。
Mg2+
每个钙离子带2个单位正电荷。
在氧化钙中,钙元素化合价为+2。
①在三氧化二铝中,氧元素化合价为-2。
+2
CaO
-2
Al2O3
②每个三氧化二铝分子含有2个铝原子.
练习:写出下列“3”的意义:
每个三氧化硫分子中含有3个氧原子。
每个钙离子带2个单位正电荷。
在三氧化二铁中,铁元素化合价为+3。
3个三氧化硫分子
3Al3+
+3
Fe2O3
3SO3
3个铝离子
每个氧化铁分子中含有3个氧原子。
1.写出下列的化学符号:
①2个氢分子 ;②4个钙离子 ; ③2个磷原子 ; ④4个磷原子构成的白磷分子 ; ⑤由60个碳原子构成的碳分子 ; ⑥由1个硫原子和2个氧原子构成的二氧化硫分子 .
2.写出下列的化学符号或意义:
2个铁原子
5个水分子
+3价的铝元素
由3个氧原子构成的一个臭氧分子
一氧化碳中碳元素显+2价
2P2O5
Al3+
2H2
4Ca2+
2P
P4
C60
SO2
2Fe
5H2O
Al2O3
+3
O3
CO
+2
2个五氧化二磷分子
3个铝离子
五、有关相对分子质量的计算五、有关相对分子质量的计算
1、计算原子数比1、计算原子数比
2、计算元素质量比2、计算元素质量比
3、计算相对分子质量3、计算相对分子质量
4、计算某元素质量分数4、计算某元素质量分数
5、计算一定质量化合物中某元素质量5、计算一定质量化合物中某元素质量
6、计算含一定量某元素的化合物质量6、计算含一定量某元素的化合物质量
7、有关杂质计算7、有关杂质计算
关键—先写出化学式!
P2O5 MgO Fe2O3 Ba(OH) 2 Ca(OH) 2
Al(OH)3 Mg(NO3)2 Al(NO3)3 Al2 (SO4)3
Fe2 (SO4)3 Cu2 (OH) 2 CO3 NH4NO3
谁最快:谁最快:
说出下列物质中氧原子个数
5个O
1个O
3个O
2个O
2个O
3个O
6个O
9个O
12个O
12个O
5个O
3个O
1、计算原子数比1、计算原子数比
(1)K2Cr2O7中钾原子和铬原子和氧原子个数比 .
练一练:氯酸钾中各原子个数比 。
2:2:7
KClO3
看成
K1C1O3
1:1:3
(化学式右下角数字比)
(2)Cu2(OH)2CO3中各种原子个数比 。
(3)碳酸氢钙[Ca(HCO3)2]中钙元素、氢元素
、碳元素、氧元素的最简原子个数比是
( )
2:5:2:1
(Cu、O、H、C)
A.1:1:1:3 B.20:1:12:48 C.1:1:1:6 D.1:2:2:6
D
(1)、二氧化碳中各种元素质量比 。
2、计算元素质量比2、计算元素质量比
(相对原子质量×右下角数字之比)
查:C-12,
O-16
CO2
12
=
=3:8
12:32
:
16
x
2
(2).氯酸钾中各种元素质量比 .
KClO3
=3:8
练
39:35.5:48
(3)、Cu2(OH)2CO3中Cu、H、C、O的质量比
。
(4)、葡萄糖(C6H12O6)是一种重要的营养物质.求出葡萄糖中各元素的质量最简比为
.
测一测测一测
127:2:12:80
18:3:24
(1)O2的相对分子质量=
3、计算相对分子质量3、计算相对分子质量
16
X
2
=32
查:O-16; H-1
32
(各相对原子质量×右下角数字之和)
1
X
2
+
16
=18
18
(2)H2O的相对分子质量=
试一试:
1.二氧化碳CO2的相对分子质量 。
2.油炸食物中可能会含有微量的丙烯醛(C3H4O)等有毒物质,求这种物质的相对分子质 .
44
56
C-12,O-16,H-1
(3)氢氧化钙的相对分子质量 。
Ca(OH) 2
练一练:
1、氢氧化铜的相对分子质量 。
2、 Al2(SO4)3的相对分子质量 。
Ca-40,0-16,H-1, Cu-64,S-32,Al-27
74
98
342
(4) CuSO4?5H2O的相对分子质量 。
练习:
1、 Na2CO3?10H2O的相对分子质量 。
64
+
32
+
16X4
↓
+
5
(
1X2
+16
)
=250
=250
Cu-64,S-32,O-16,H-1, Na-23,C-12
268
(5)CO2相对分子质量总和 。
练一练
1、5 SO3相对分子质量总和 。
2、2HCl相对分子质量总和 。
3、3 H2SO4相对分子质量总和 。
132
400
71
294
4、计算某元素质量分数4、计算某元素质量分数
(1)H20
2H
H%=
2H
H20
×100%
=
2×1
1×2+16
×100%
=11.1%
氢元素占水的质量分数?氢元素占水的质量分数?
某元素质量分数=
该原子×右下角数字
化学式
×100%
(1) H2O
4、计算某元素质量分数4、计算某元素质量分数
→
2H
2H
氢元素质量分数
=
————
H2O
X100%
=
2X1
————
1X2+16
X100%
H-1,O-16
氢元素占水的质量分数?氢元素占水的质量分数?
某元素质量分数=
该原子×右下角数字
化学式
(
)
=
11.1%
____________
→
2N
氮元素质量分数
=
2N
————
NH4NO3
X100%
=
2X14
14+1X4+14+16X3
X100%
=35%
1、求氧化铁Fe2O3中铁元素的质量分数?
2、计算二氧化硫中硫元素的质量分数?
50%
70%
计算化肥硝酸铵(NH4NO3)中氮元素的质量分数。
NH4NO3
例:求160g三氧化硫中氧元素的质量?
SO3
5、计算一定质量化合物中某元素质量5、计算一定质量化合物中某元素质量
1.求32g氧化铁中铁元素的质量。
32g
2.8g
分析题目列比例
2.求180g葡萄糖(C6H12O6)中含碳元素的质量
144g
3O
160g
x
32+16x3
3x16
=
160g
x=96g
x3x16
=
x
80
例:求多少克三氧化硫中含32g氧元素?
SO3
80g
1、求多少克二氧化碳中含g碳元素?
22g
2、求多少克硫酸中含2g氢元素?
98g
6、计算含一定量某元素的化合物质量6、计算含一定量某元素的化合物质量
3O
x
32g
32+16x3
3x16
=
x
x=53.3g
·3x16
=
32g
80·
分析题目列比例
2、98g硫酸溶液(含H2SO410%)中含硫元素多少克?
例:求100g赤铁矿(含Fe2O3 75%)中铁元素质量?
7、有关杂质计算7、有关杂质计算
19.5g
1、100g盐酸(含氯化氢20%)中含氯元素多少克?
52.5g
100gX75%=75g
Fe2O3
3.3g
2Fe
75g
x
56x2+16x3
2x56
=
75g
x=52.5g
x2x56
=
x
160
分析题目列比例
计算类型
计算方法
1.计算原子个数
2.计算元素质量比
3.计算相对分子质量
4.计算某元素质量分数
5.计算一定质量化合物中某元素质量
6.计算含一定质量某元素的化合物质量
7.有关杂质计算
(化学式右下角数字比)
相对原子质量×右下角数字之比)
(相对原子质量×右下角数字之和)
该原子×右下角数字
质量分数=
化学式
分析题目列比例
分析题目列比例
分析题目列比例
下图中“ ”和“ ”表示两种不同原子,下列方框中表示混合物的是( )
A
B
C
B
B
想一想
根据给出的信息,写出下列有关物质的化学式
H2
K2O
H2O
KClO3
HCl
用H、K、Cl、O、Cl等元素符号写出化学式
①单质 ;②金属氧化物 ; ③非金属氧化物 ;④酸 ; ⑤制取氧气的物质 ;
+1
+1
-1
-2
+5
3.写出下列的化学符号:
①氢氧化钙在水中存在的离子是 ; ②氢氧化钠溶液中的阳离子是 ; ③氢氧化钾溶液中能使酚酞溶液变红色,其原因是溶液中含有大量 的缘故. ④氯化钠溶液中存在的粒子 .
Ca2+
OH-
Na+
OH-
OH-
Na+
H2O
根据给出的信息,写出下列有关物质的化学式
①抢救非典肺炎病人的呼吸机输入的单质气体 ; ②海水中含量最多的氧化物 ; ③空气中含量最多的气体 ; ④实验室常用来制取氧气的一种暗紫色固体 ; ⑤温度中常用的一种液体(水银温度计中的液体) ; ⑥地壳总含量最高的金属元素组成的氧化物 .
O2
H2O
N2
KMnO4
Hg
Al2O3
1、下列物质中氯元素化合价最低的是( )
A Cl2 B HCl C HClO D KClO3
2、石棉的熔点高,以不易燃烧,可制作石棉网,石棉的化学式可表示为CaMg3Si4O12,其中硅元素的化合价为( )
A +1 B +2 C +3 D +4
3、钛铁矿主要成分的化学式为FeTiOx,其中铁元素和钛元素的化合价均显+3价,则X为( )
A 2 B 3 C 4 D 6
4、酸根阴离子RO42-中R的化合价是( )
A -2 B 0 C +4 D +6
练练:你能对多少?练练:你能对多少?
B
D
B
D
1.味精是人们熟悉的食品助鲜剂,其化学式为C5NH8O4Na,它是由 种元素组成,其是,碳元素、氮元素及氢元素的原子个数比是 ;氧元素与钠元素的质量比是 ;169g该物质是含钠元素的质量是 ; g该物质中含有32g氧元素.
看你掌握了多少!
5
5:1:8
64:23
23g
84.5
2.目前市场上的补钙药剂很多,右图是某品牌补钙药品的部分说明书.如果按用量服用,则每天补充钙元素的质量为( ) A.0.5gB.1gC.1.25gD.0.25g
XX钙片
[药品规格]
每片含CaCO3
0.625g
[用法用量]
每次一片,
每天2次
A
1、计算Cu2 (OH) 2 CO3中氧元素的质量分数。
2、求106g碳酸钠中含多少克氧元素?
3、求葡萄糖[C6H12O6]中碳元素的质量分数 ,180g葡萄糖中含有 g碳元素?
4、求多少克氧化铝中含48g氧元素?
5、100g石灰石(含杂质 10%)中含钙元素多少克?(石灰石中主要成分CaCO3 )
36%
40%
48g
72
102g
36g
练一练:
铁 Fe 镁 Mg 锌 Zn 铝 Al 硫 S 红磷 P 白磷 P 碳 C 氦气 He 氖气 Ne 氩气 Ar
单质:
氧气 O2 氮气 N2 氯气 Cl2 氢气 H2
1.双原子分子单质的化学式:(4个)
2.金属、非金属、稀有气体单质的化学式:
在元素符号右下角加2
用元素符号直接表示化学式.
二、简单化学式的写法和读法二、简单化学式的写法和读法
二氧化碳 CO2;一氧化碳 CO; 二氧化硫SO2 ;
三氧化硫 SO3;五氧化二磷 P2O5;二氧化锰 MnO2; 二氧化氮NO2;四氧化三铁Fe3O4;三氧化二铁Fe2O3;
氧化物:
氧化铁 Fe2O3;氧化亚铁 FeO;氧化镁 MgO;
氧化铜 CuO; 氧化铝 Al2O3; 氧化钙CaO; 氧化钾 K2O;氧化钠Na2O:氧化钡BaO;水H2O;
3.名称中有数字的物质的化学式:
4.名称中没有数字的物质的化学式:
用交叉法,读作“氧化某”
后读先写,读作“几氧化几某”
盐酸 HCl;硫酸 H2SO4;硝酸 HNO3;
碳酸 H2CO3;亚硫酸 H2SO3;磷酸 H3PO4;
酸:
5.酸的化学式:
氢氧化钠 NaOH; 氢氧化钾 KOH;
氢氧化钡 Ba(OH)2;氢氧化钙 Ca(OH)2; 氢氧化镁 Mg(OH)2;氢氧化铝 Al(OH)3; 氢氧化铁 Fe(OH)3;氢氧化铜 Cu(OH)2; 氢氧化锌 Zn(OH)2;氨气 NH3
碱:
6.碱的化学式:
要OH结尾,再用交叉法(氨气NH3除外),读作“氢氧化某”.
要H开头,再用交叉法.读作“某酸”
小结:化学式的写法和读法小结:化学式的写法和读法
(1)双原子分子单质的化学式:在元素符号右下角加2
(2)除双原子分子外的单质的化学式:用元素符号直接表示.
(5)酸的化学式:要H开头,再用交叉法.读作“某酸”
(6)碱的化学式:要OH结尾,再用交叉法(氨气NH3除外),读作“氢氧化某”.
(3)名称中有数字的物质的化学式:后读先写;读作“几氧化几某”
(4)名称中没有数字的物质的化学式:用交叉法,读作“氧化某”
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
