鲁教版九年级化学上册到实验室去:二氧化碳的实验室制取与性质(14张ppt)
文档属性
| 名称 | 鲁教版九年级化学上册到实验室去:二氧化碳的实验室制取与性质(14张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 366.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-08-16 00:00:00 | ||
图片预览




文档简介
(共14张PPT)
二氧化碳的实验室制取与性质
一、导入新课
以下图片中,都用到了哪种物质?
固态二氧化碳俗称干冰,可用于人工降雨,除此之外,还有许多其他的用途,是一种非常重要的物质。那么,实验室是如何制取二氧化碳的呢?
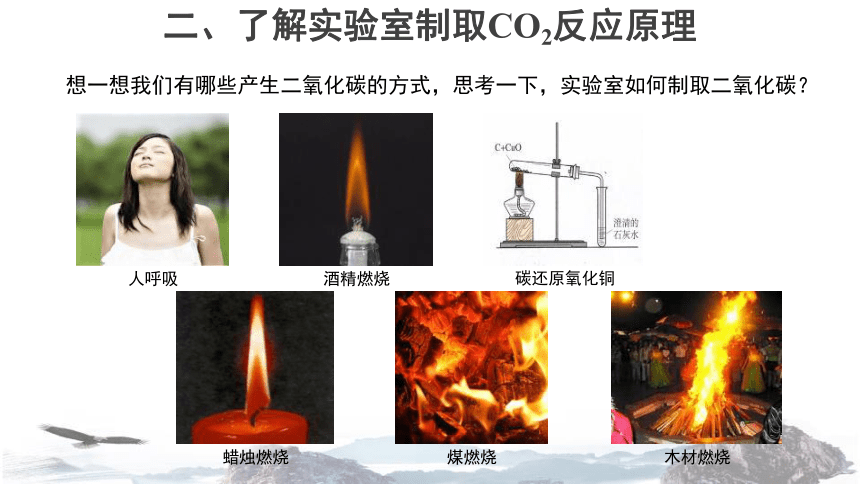
二、了解实验室制取CO2反应原理
想一想我们有哪些产生二氧化碳的方式,思考一下,实验室如何制取二氧化碳?
煤燃烧
木材燃烧
人呼吸
酒精燃烧
碳还原氧化铜
蜡烛燃烧
二、了解实验室制取CO2反应原理
CaCO3
+
2HCl=CaCl2
+
H3CO2
实验室制取二氧化碳的正确原理:
碳酸不稳定,容易分解成二氧化碳和水:
H3CO2
=
H2O
+CO2↑
总的化学方程式是:
CaCO3
+
2HCl=CaCl2
+
H2O
+
CO2↑
实验室制法的条件是:
1.制取应简便迅速。
2.所制得的气体纯度高,符合演示实验的需要。
3.操作简单、安全,易于实现。
三、装置的设计与选择
根据O2的实验室制法,找出实验室制取CO2气体应选择哪种发生装置和收集装置?
【资料展示】
①空气的平均相对分子质量为29,CO2的相对分子质量为44,由此可推出CO2的密度比空气大。
②CO2能溶于水,在标准情况下,1体积水可溶解0.88体积CO2;且与水反应,CO2溶于水生成碳酸,碳酸很不稳定,很容易分解成CO2和水。
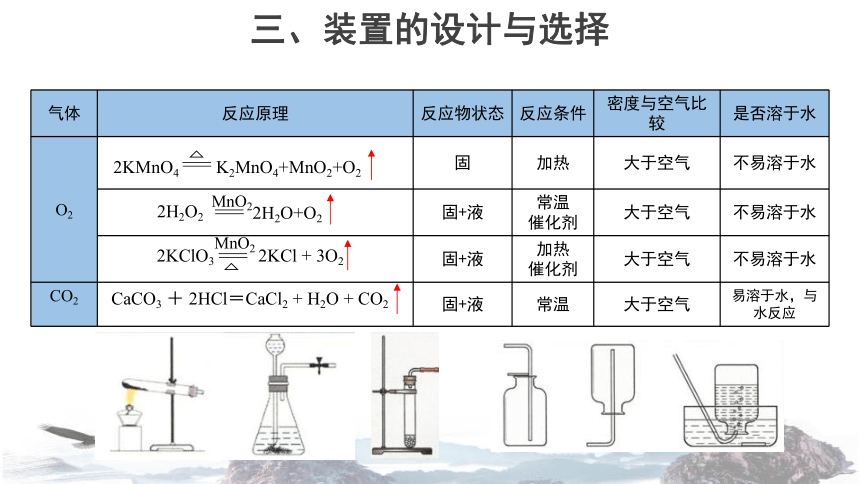
三、装置的设计与选择
气体
反应原理
反应物状态
反应条件
密度与空气比较
是否溶于水
O2
固
加热
大于空气
不易溶于水
固+液
常温
催化剂
大于空气
不易溶于水
固+液
加热
催化剂
大于空气
不易溶于水
CO2
固+液
常温
大于空气
易溶于水,与水反应
2H2O2
MnO2
2H2O+O2
2KMnO4
K2MnO4+MnO2+O2
2KClO3
MnO2
2KCl
+
3O2
CaCO3
+
2HCl=CaCl2
+
H2O
+
CO2
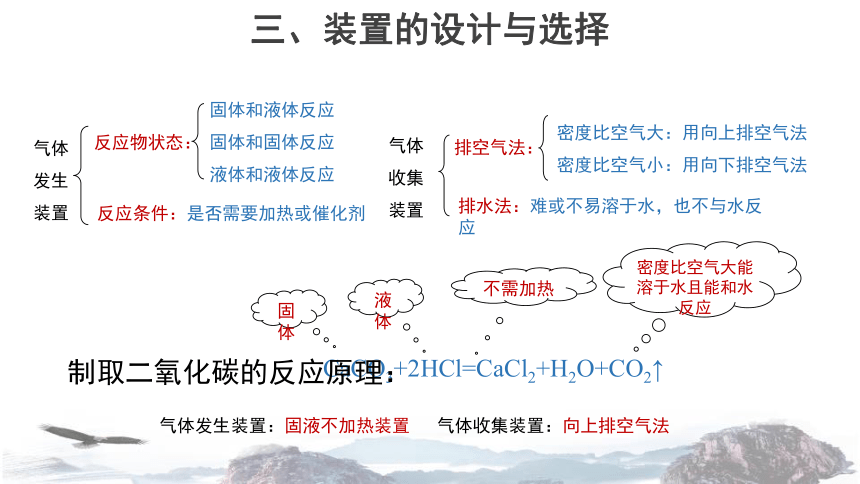
三、装置的设计与选择
气体
发生
装置
气体
收集
装置
反应物状态:
反应条件:是否需要加热或催化剂
固体和液体反应
固体和固体反应
液体和液体反应
排空气法:
密度比空气大:用向上排空气法
密度比空气小:用向下排空气法
排水法:难或不易溶于水,也不与水反应
CaCO3+2HCl=CaCl2+H2O+CO2↑
制取二氧化碳的反应原理:
固体
液体
不需加热
密度比空气大能溶于水且能和水反应
气体发生装置:固液不加热装置
气体收集装置:向上排空气法
三、装置的设计与选择
复杂装置
优点:方便随时添加稀盐酸
简易装置
优点:仪器装配简单易操作
注意事项
目的
长颈漏斗必须液封
导管应在橡皮塞下少许
导管应接近集气瓶底部
防止气体从长颈漏斗口逸出
便于排出气体
充分排走集气瓶中空气
四、实验室制取CO2的步骤与检验
连接仪器
检查气密性
加大理石
加稀盐酸
收集气体
燃着的木条
熄灭
澄清石灰水
变浑浊
检验方法:
验满方法:
四、实验室制取CO2的步骤与检验
【反思与交流】
①将块状大理石改为粉末状合适吗,为什么?
②为什么不能使用浓盐酸?
③为什么不能使用硫酸与块状大理石反应?
④为什么不能用碳酸钠?
碳酸钙粉末与稀盐酸反应太快,来不及收集气体。
不能用浓盐酸。因为浓盐酸易挥发,氯化氢气体易混入产生的二氧化碳内。
不能用硫酸。虽然硫酸也能跟碳酸钙反应生成二氧化碳:但由于产物硫酸钙微溶于水,会附着在块状大理石或石灰石的表面,阻碍反应的继续进行。
不能用碳酸钠,因为碳酸钠与酸反应速率太快,不利于收集。
五、验证二氧化碳的性质
(1)二氧化碳的物理性质
①在托盘天平两边各放一只250mL的烧杯,调节天平平衡。然后向其中一只烧杯中慢慢倾倒集气瓶中的二氧化碳气体。(或自行设计实验方案比较二氧化碳和空气的密度)。
现象
结论
②向盛有二氧化碳的塑料瓶A中加入适量的蒸馏水,迅速拧紧瓶盖,振荡,观察现象。
现象
结论
塑料瓶变瘪了
CO2能溶于水
天枰向二氧化碳一端倾斜
CO2密度比空气大
五、验证二氧化碳的性质
(2)二氧化碳的化学性质
①向上述盛有二氧化碳水溶液的塑料瓶A中滴入1~2滴紫色石蕊试液,拧紧瓶盖,振荡,观察现象。
现象
结论
②向盛有二氧化碳的塑料瓶B中倒入适量澄清石灰水,振荡,观察现象。
现象
结论
③将准备好的两支蜡烛放入500mL烧杯中,分别点燃。然后慢慢倒入塑料瓶C中的二氧化碳气体,观察现象。
现象
结论
紫色石蕊试剂变红
CO2溶于水生成碳酸
澄清石灰水变浑浊
CO2能澄清石灰水变浑浊。
下层阶梯上的蜡烛先熄灭,上层蜡烛后熄灭。
二氧化碳不能燃烧也不能支持燃烧。
六、课堂小结
一、药品及反应原理
药品:石灰石和稀盐酸
原理:
二、装置的确定
固体加热型
固液常温型
向上排空气法(收集密度比空气大的气体)
向下排空气法(收集密度比空气小的气体)
排水法(收集不易溶于水且不与水发生反应的气体)
CaCO3
+
2HCl=CaCl2
+
H2O
+
CO2↑
气体发生装置
气体收集装置
三、二氧化碳性质的验证
再
见
二氧化碳的实验室制取与性质
一、导入新课
以下图片中,都用到了哪种物质?
固态二氧化碳俗称干冰,可用于人工降雨,除此之外,还有许多其他的用途,是一种非常重要的物质。那么,实验室是如何制取二氧化碳的呢?
二、了解实验室制取CO2反应原理
想一想我们有哪些产生二氧化碳的方式,思考一下,实验室如何制取二氧化碳?
煤燃烧
木材燃烧
人呼吸
酒精燃烧
碳还原氧化铜
蜡烛燃烧
二、了解实验室制取CO2反应原理
CaCO3
+
2HCl=CaCl2
+
H3CO2
实验室制取二氧化碳的正确原理:
碳酸不稳定,容易分解成二氧化碳和水:
H3CO2
=
H2O
+CO2↑
总的化学方程式是:
CaCO3
+
2HCl=CaCl2
+
H2O
+
CO2↑
实验室制法的条件是:
1.制取应简便迅速。
2.所制得的气体纯度高,符合演示实验的需要。
3.操作简单、安全,易于实现。
三、装置的设计与选择
根据O2的实验室制法,找出实验室制取CO2气体应选择哪种发生装置和收集装置?
【资料展示】
①空气的平均相对分子质量为29,CO2的相对分子质量为44,由此可推出CO2的密度比空气大。
②CO2能溶于水,在标准情况下,1体积水可溶解0.88体积CO2;且与水反应,CO2溶于水生成碳酸,碳酸很不稳定,很容易分解成CO2和水。
三、装置的设计与选择
气体
反应原理
反应物状态
反应条件
密度与空气比较
是否溶于水
O2
固
加热
大于空气
不易溶于水
固+液
常温
催化剂
大于空气
不易溶于水
固+液
加热
催化剂
大于空气
不易溶于水
CO2
固+液
常温
大于空气
易溶于水,与水反应
2H2O2
MnO2
2H2O+O2
2KMnO4
K2MnO4+MnO2+O2
2KClO3
MnO2
2KCl
+
3O2
CaCO3
+
2HCl=CaCl2
+
H2O
+
CO2
三、装置的设计与选择
气体
发生
装置
气体
收集
装置
反应物状态:
反应条件:是否需要加热或催化剂
固体和液体反应
固体和固体反应
液体和液体反应
排空气法:
密度比空气大:用向上排空气法
密度比空气小:用向下排空气法
排水法:难或不易溶于水,也不与水反应
CaCO3+2HCl=CaCl2+H2O+CO2↑
制取二氧化碳的反应原理:
固体
液体
不需加热
密度比空气大能溶于水且能和水反应
气体发生装置:固液不加热装置
气体收集装置:向上排空气法
三、装置的设计与选择
复杂装置
优点:方便随时添加稀盐酸
简易装置
优点:仪器装配简单易操作
注意事项
目的
长颈漏斗必须液封
导管应在橡皮塞下少许
导管应接近集气瓶底部
防止气体从长颈漏斗口逸出
便于排出气体
充分排走集气瓶中空气
四、实验室制取CO2的步骤与检验
连接仪器
检查气密性
加大理石
加稀盐酸
收集气体
燃着的木条
熄灭
澄清石灰水
变浑浊
检验方法:
验满方法:
四、实验室制取CO2的步骤与检验
【反思与交流】
①将块状大理石改为粉末状合适吗,为什么?
②为什么不能使用浓盐酸?
③为什么不能使用硫酸与块状大理石反应?
④为什么不能用碳酸钠?
碳酸钙粉末与稀盐酸反应太快,来不及收集气体。
不能用浓盐酸。因为浓盐酸易挥发,氯化氢气体易混入产生的二氧化碳内。
不能用硫酸。虽然硫酸也能跟碳酸钙反应生成二氧化碳:但由于产物硫酸钙微溶于水,会附着在块状大理石或石灰石的表面,阻碍反应的继续进行。
不能用碳酸钠,因为碳酸钠与酸反应速率太快,不利于收集。
五、验证二氧化碳的性质
(1)二氧化碳的物理性质
①在托盘天平两边各放一只250mL的烧杯,调节天平平衡。然后向其中一只烧杯中慢慢倾倒集气瓶中的二氧化碳气体。(或自行设计实验方案比较二氧化碳和空气的密度)。
现象
结论
②向盛有二氧化碳的塑料瓶A中加入适量的蒸馏水,迅速拧紧瓶盖,振荡,观察现象。
现象
结论
塑料瓶变瘪了
CO2能溶于水
天枰向二氧化碳一端倾斜
CO2密度比空气大
五、验证二氧化碳的性质
(2)二氧化碳的化学性质
①向上述盛有二氧化碳水溶液的塑料瓶A中滴入1~2滴紫色石蕊试液,拧紧瓶盖,振荡,观察现象。
现象
结论
②向盛有二氧化碳的塑料瓶B中倒入适量澄清石灰水,振荡,观察现象。
现象
结论
③将准备好的两支蜡烛放入500mL烧杯中,分别点燃。然后慢慢倒入塑料瓶C中的二氧化碳气体,观察现象。
现象
结论
紫色石蕊试剂变红
CO2溶于水生成碳酸
澄清石灰水变浑浊
CO2能澄清石灰水变浑浊。
下层阶梯上的蜡烛先熄灭,上层蜡烛后熄灭。
二氧化碳不能燃烧也不能支持燃烧。
六、课堂小结
一、药品及反应原理
药品:石灰石和稀盐酸
原理:
二、装置的确定
固体加热型
固液常温型
向上排空气法(收集密度比空气大的气体)
向下排空气法(收集密度比空气小的气体)
排水法(收集不易溶于水且不与水发生反应的气体)
CaCO3
+
2HCl=CaCl2
+
H2O
+
CO2↑
气体发生装置
气体收集装置
三、二氧化碳性质的验证
再
见
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
