人教版化学高中必修一第二节:富集在海水中的元素——氯(35张ppt)
文档属性
| 名称 | 人教版化学高中必修一第二节:富集在海水中的元素——氯(35张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-08-20 00:00:00 | ||
图片预览











文档简介
(共35张PPT)
第四章
非金属及其化合物
第二节
富集在海水中的元素——氯
本课以资料卡片海洋中含有大量的氯导入,氯元素的学习以结构决定性质、性质决定用途的思路进行。课件用一则新闻材料让学生自己归纳出氯气的理化性质,然后再按先物理性质后化学性质展开,重点突出氯气的化学性质。氯气的化学性质讲解顺序:与金属反应(Na、Fe、Cu)、与非金属反应H2、与水反应、与碱反应。其中重点介绍氯气与水反应、与碱的反应。在介绍时采用与实际生活相联系的方式。并用对比的方式进行学习,氯气有毒但可以消毒自来水事实,对学生进行辩证法的培养。最后采用思维导图的方式帮助学生构建知识网络。
氯气的性质采用播放视频的方式,提高学生的学习兴趣。最后设计了适量的练习帮助学生,巩固应用知识。
海洋—巨大的资源宝库
如果将海洋中的盐全部提取出来,铺在地球的陆地上,可使陆地平均升高150m。
1、氯元素(Cl)
以化合态形式存在,主要是NaCl
(1)原子结构示意图
氯元素性质很活泼,表现为典型的非金属性。
(2)存在
京沪高速公路淮安路段液氯的泄漏
新华网报道:2005年3月29日,京沪高速公路淮安路段一辆满载液氯的液罐车和对面来车相撞
,大量液氯外泄。据目击者描述
:
“一股黄绿色的气体就像探照灯光一样,‘唰’地射向空中,并有刺鼻的味道,眼睛也熏得睁不开
。”
事发后消防队员不断地用水枪喷射,但还是造成350
人中毒进医院救治,
28人中毒死亡,附近居民采取应急措施,疏散到高坡上。
颜色
气味
溶解性
密度
毒性
根据上述材料,得出氯气的哪些物理性质?
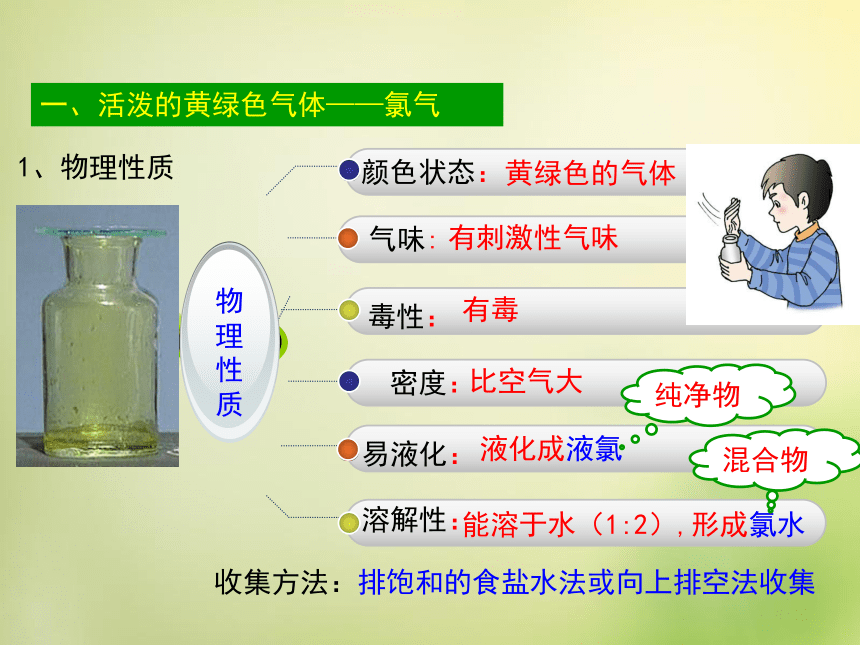
一、活泼的黄绿色气体——氯气
气味:
密度:比空气大
毒性:
密度:
有刺激性气味
易液化:
溶解性:
颜色状态:
物理性质
黄绿色的气体
有毒
比空气大
液化成液氯
能溶于水(1:2),形成氯水
1、物理性质
纯净物
混合物
收集方法:排饱和的食盐水法或向上排空法收集
闻气体的方法
用手轻轻的在瓶口煽动,仅使极少量的气体飘进鼻孔
这是闻各种气体气味的方法
请根据氯原子的结构示意图分析和猜测氯气可能具有的化学性质
得e-
易得到电子,化合价降低;氯是活泼非金属元素,氯气的化学性质非常活泼。表现出强氧化性(典型的非金属性)
结构决定性质
2、化学性质
Cl2是很活泼的非金属单质,具有很强的氧化性。
(1)、与金属反应
①与Na反应
剧烈燃烧,火焰呈黄色,产生大量白烟。
现象:
2Na
+
Cl2
2
NaCl
点燃
铁丝剧烈燃烧,产生棕褐色烟,加少量水形成棕黄色溶液。
②与铁反应
现象:
2Fe
+
3
Cl2
2
FeCl3
点燃
铜丝剧烈燃烧,产生棕黄色烟。
③与铜反应:
现象:
Cu
+
Cl2
CuCl2
点燃
反应规律:氯气可跟绝大多数金属反应,生成高价金属的氯化物。
FeCl3和CuCl2能用它们的金属与盐酸反应制取吗?可以一步反应制取吗?
不能,但可以用金属单质与氯气反应一步制取
(2)、与非金属反应
【实验4-3】
现象
化学方程式
安静地燃烧,发出苍白色火焰,放出大量的热,瓶口有大量白雾产生。
H2
+
Cl2
2HCl
点燃
H2与Cl2通过点燃和光照都能发生反应生成HCl。
爆炸
H2
+
Cl2
2HCl
光照
HCl溶于水形成盐酸
工业制盐酸原理
注意:点燃前,必须验纯。
通过氢气在氯气中燃烧的实验,你对燃烧的条件及其本质有什么新的认识?
①燃烧不一定有O2参加
②燃烧的本质是氧化还原反应
③任何发光发热的剧烈的化学反应都称为燃烧
描述反应现象要注意的事项:
烟-固体小颗粒分散在空气中
雾-小液滴分散在空气中
2.
不要把现象和结果混淆
不要说成是:有氯化铜生成。
(这是反应的结果)
1.
区分烟和雾
Cl2与Cu反应的现象是:有棕黄色的烟产生
你是否遇到过打开自来水,会闻到一股刺激性的气味?这是什么原因?
(3)、与水反应
氯气能溶于水(常温常压下,1体积水约溶解2体积的氯气,1:2),氯气的水溶液叫氯水。
H2O
+
Cl2
=
HCl
+
HClO
(一元弱酸)
(次氯酸)
2、用氧化还原知识分析上述反应,标明电子转移的数目和方向,并指出其中的氧化剂、还原剂。
1、写出上述反应的离子方程式
次氯酸(HClO)的性质
A、弱酸性,为一元弱酸
电离方程式:
B、不稳定性,见光易分解
C、具有强氧化性
氧化性比Cl2还强,具有杀菌性能,还具有漂白性。氯水也因为含有次氯酸而具有漂白作用。
根据氯气与水反应方程式推测新制氯水中可能存在哪些粒子?
分子:
Cl2、H2O、HClO
离子:
H+、Cl-、ClO-、
OH-(极少量)
新制氯水可能具有哪些性质?
H+
酸性
Cl2
氧化性
HClO
漂白性
Cl-
遇硝酸银产生白色沉淀
氯水性质具有多样性,试指出下列各现象主要是何种微粒所表现出来的性质:
①氯水呈浅黄绿色______
②使湿润的紫色石蕊试纸先变红
后褪色
。
③滴加AgNO3溶液后生成白色沉淀
.
Cl2
H+
HClO
Cl-
④加入石灰石粉末逐渐溶解,并放出气体______
⑤往含有Fe2+溶液中滴加KSCN溶液无明显现象,再滴加氯水后呈红色
。
H+
Cl2
氯水的漂白作用
【实验4-4、5】将有色纸条分别放入①干燥氯气瓶和②盛有1/3体积新制氯水的广口瓶中,盖上玻璃片,观察现象。
现象
结论
与解释
①有色布条不褪色
②有色布条褪色
①干燥的氯气无漂白作用
②氯水中起漂白作用的是HClO
——HClO起漂白作用
1、在氯水中滴入紫色石蕊试液,会观察到什么变化?
2、久置氯水中又有哪些粒子,具有怎样的性质?
2、新制氯水久置后酸性如何变化?
3、氯水应该怎样保存?
H+
、Cl-、H2O、OH—(少量)
久置氯水相当于盐酸
酸性增大
阴凉处,避光保存
紫色石蕊试纸先变红,后褪色
新制、久置氯水以及液氯比较
新制氯水
久置氯水
液氯
物质种类
成分
性质
混合物
混合物
纯净物
分子:Cl2,
H2O,
HClO
离子:H+,
Cl-,
ClO-,
OH-(极少量)
分子:H2O
离子:Cl-,H+
Cl2
三分子、四离子
氯水只能现配现用,并保存在棕色试剂瓶内,至于阴暗处。
强氧化性、酸性、漂白性
酸性
强氧化性
1、下列关于氯的说法正确的是(
)
A.
液氯和氯水是同一物质
B
.
氯水久置后酸性将减弱
C
.
新制氯水可使蓝色石蕊试纸先变红后褪色
D
.
光照氯水有气泡逸出,该气体为Cl2
E.
新制氯水中滴加硝酸银溶液,没有任何现象
F.
新制氯水可以使干燥的布条褪色
C、F
2、现在你知道养金鱼时,为什么要先将自来水在阳光下暴晒1-2天吗?
问题1:既然氯气可用来杀菌消毒,那么游泳池中是直接使
用氯气消毒的吗?
问题2
:既然氯水中真正起消毒杀菌作用的物质是次氯酸,
而次氯酸又不稳定,那么工业上又是如何解决存放和运输
问题的呢?
(提示:碳酸不稳定,碳酸盐稳定吗?)
思考:如何得到次氯酸盐?
(4)、与碱反应
①与NaOH溶液反应
2NaOH+Cl2=NaClO+NaCl+H2O
有效成分:NaClO
漂白液
Cl2尾气吸收处理
此反应离子方程式,用单线桥注明电子转移情况
——工业制备漂白液
漂白粉
①禽流感消毒:可用5%漂白粉溶液喷洒于动物圈舍、笼架、饲槽及车辆等进行消毒。
②非典型肺炎污染对象的消毒方法:物品、家具可用漂白粉配成溶液进行浸泡、喷洒或擦洗。
③洪涝灾害饮水问题:可用漂白粉或漂粉精对水进行消毒。
说明书
漂白粉(次氯酸钙)
化学式(Ca(ClO)2)
性状:漂白粉为白色粉
末固体,
主要用作染
料、医药、矿业行业的
水处理;自来水消毒、
游泳池、鱼塘杀菌,蔬
菜、饲养场的消毒、净
水
漂白粉、漂粉精主要成分
有效成分:Ca(ClO)2
用途:既可做漂白棉、麻、纸张的漂白剂,又可做游泳池及环境的消毒剂。
②与Ca(OH)2溶液反应
2Cl2+2Ca(OH)2=
CaCl
2+Ca(ClO)2+2H2O
——工业制备漂白粉
此反应离子方程式,用单线桥注明电子转移情况
提示:与澄清石灰水反应:
与石灰乳反应:
氯气跟碱反应的化学方程式有规律吗?
氯气+碱
氯化物+次氯酸盐+水
Cl2既是氧化剂,又是还原剂
漂白粉中的成分并没有杀菌、消毒的作用,那它是怎样发挥杀菌、消毒作用的?
日常
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO
工业
Ca(ClO)2+2HCl=CaCl2+2HClO
漂白原理:
(反应原理:强酸制取弱酸)
氯水、漂白液、漂白粉、漂粉精的漂白作用都是因反应生成的HClO
漂白粉敞放在潮湿的空气中会失效吗?又应该如何保存?
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO
失效原理:
密封、干燥、避光保存。
3、用途
1)、用于自来水的杀菌、消毒;
3)、工业制盐酸。
2)、制取漂白粉、消毒液等;
4)、氯气是合成塑料、橡胶、人造纤维、
农药、染料和药品的重要原料
任何事物都有两面性,化学技术和化学品也不例外。氯气是有毒气体,但它可以用于自来水消毒,而且是重要的化工原料。近来也有研究表明,使用氯气给自来水消毒时,会产生有致癌作用的物质如三氯甲烷,在一些发达国家已经使用更好的替代品如二氧化氯、臭氧等。所以,我们应该认真学好知识,正确运用,让自然资源更好地为人类服务。
氯气是一种有毒气体,但在工农业生产和日常生活中却有着广泛的应用,从中你得到什么启示?
氯及其化合物
Cl2
物理性质
化学性质
黄绿色气体
与金属单质反应
与非金属单质反应
与水反应
与碱反应
HClO
化学性质
弱酸性、强氧化性、不稳定性
含氧酸盐
NaClO
、Ca(ClO)2
用途
消毒液,漂白粉
1、可以用氯气灌洞的方法来消灭田鼠,这是利用了氯气的哪些性质?(
)
①密度比空气大
②易液化
③能溶于水
④有毒
A、
①
②
B、
③
④
C、
①
③
④
D、
①
④
D
2、下列氯化物中,既能由金属和氯气直接反应制得,又能由金属和盐酸反应制得的是(
)
A、CuCl2
B、FeCl2
C、FeCl3
D、AlCl3
D
3.下列关于氯水的说法中正确的是(
)
A.新制氯水中只含有Cl2和H2O分子
B.新制氯水能杀菌消毒是因为Cl2有毒,能毒杀细菌
C.光照氯水有气泡逸出,该气体是Cl2
D.氯水放置数天后酸性增强
D
4、洪灾过后,饮用水的消毒杀菌成为一只大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为
。
2)漂白粉的有效成分是
(填化学式)。
3)漂白粉溶于水后,受空气中CO2作用,即产生有漂白、杀菌作用的次氯酸,发生化学反应的离子方程式为
4)反应1)和3)中属于氧化还原反应的是(填编号)
。
5)瓶装漂白粉久置于空气中会呈稀粥状而失效。试用化学方程式表示漂白粉在空气中失效的原因是
。
2Cl2+2Ca(OH)2=
CaCl
2+Ca(ClO)2+2H2O
Ca(ClO)2
Ca2+
+2ClO-+CO2+H2O=CaCO3↓+2HClO
1)
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO
第四章
非金属及其化合物
第二节
富集在海水中的元素——氯
本课以资料卡片海洋中含有大量的氯导入,氯元素的学习以结构决定性质、性质决定用途的思路进行。课件用一则新闻材料让学生自己归纳出氯气的理化性质,然后再按先物理性质后化学性质展开,重点突出氯气的化学性质。氯气的化学性质讲解顺序:与金属反应(Na、Fe、Cu)、与非金属反应H2、与水反应、与碱反应。其中重点介绍氯气与水反应、与碱的反应。在介绍时采用与实际生活相联系的方式。并用对比的方式进行学习,氯气有毒但可以消毒自来水事实,对学生进行辩证法的培养。最后采用思维导图的方式帮助学生构建知识网络。
氯气的性质采用播放视频的方式,提高学生的学习兴趣。最后设计了适量的练习帮助学生,巩固应用知识。
海洋—巨大的资源宝库
如果将海洋中的盐全部提取出来,铺在地球的陆地上,可使陆地平均升高150m。
1、氯元素(Cl)
以化合态形式存在,主要是NaCl
(1)原子结构示意图
氯元素性质很活泼,表现为典型的非金属性。
(2)存在
京沪高速公路淮安路段液氯的泄漏
新华网报道:2005年3月29日,京沪高速公路淮安路段一辆满载液氯的液罐车和对面来车相撞
,大量液氯外泄。据目击者描述
:
“一股黄绿色的气体就像探照灯光一样,‘唰’地射向空中,并有刺鼻的味道,眼睛也熏得睁不开
。”
事发后消防队员不断地用水枪喷射,但还是造成350
人中毒进医院救治,
28人中毒死亡,附近居民采取应急措施,疏散到高坡上。
颜色
气味
溶解性
密度
毒性
根据上述材料,得出氯气的哪些物理性质?
一、活泼的黄绿色气体——氯气
气味:
密度:比空气大
毒性:
密度:
有刺激性气味
易液化:
溶解性:
颜色状态:
物理性质
黄绿色的气体
有毒
比空气大
液化成液氯
能溶于水(1:2),形成氯水
1、物理性质
纯净物
混合物
收集方法:排饱和的食盐水法或向上排空法收集
闻气体的方法
用手轻轻的在瓶口煽动,仅使极少量的气体飘进鼻孔
这是闻各种气体气味的方法
请根据氯原子的结构示意图分析和猜测氯气可能具有的化学性质
得e-
易得到电子,化合价降低;氯是活泼非金属元素,氯气的化学性质非常活泼。表现出强氧化性(典型的非金属性)
结构决定性质
2、化学性质
Cl2是很活泼的非金属单质,具有很强的氧化性。
(1)、与金属反应
①与Na反应
剧烈燃烧,火焰呈黄色,产生大量白烟。
现象:
2Na
+
Cl2
2
NaCl
点燃
铁丝剧烈燃烧,产生棕褐色烟,加少量水形成棕黄色溶液。
②与铁反应
现象:
2Fe
+
3
Cl2
2
FeCl3
点燃
铜丝剧烈燃烧,产生棕黄色烟。
③与铜反应:
现象:
Cu
+
Cl2
CuCl2
点燃
反应规律:氯气可跟绝大多数金属反应,生成高价金属的氯化物。
FeCl3和CuCl2能用它们的金属与盐酸反应制取吗?可以一步反应制取吗?
不能,但可以用金属单质与氯气反应一步制取
(2)、与非金属反应
【实验4-3】
现象
化学方程式
安静地燃烧,发出苍白色火焰,放出大量的热,瓶口有大量白雾产生。
H2
+
Cl2
2HCl
点燃
H2与Cl2通过点燃和光照都能发生反应生成HCl。
爆炸
H2
+
Cl2
2HCl
光照
HCl溶于水形成盐酸
工业制盐酸原理
注意:点燃前,必须验纯。
通过氢气在氯气中燃烧的实验,你对燃烧的条件及其本质有什么新的认识?
①燃烧不一定有O2参加
②燃烧的本质是氧化还原反应
③任何发光发热的剧烈的化学反应都称为燃烧
描述反应现象要注意的事项:
烟-固体小颗粒分散在空气中
雾-小液滴分散在空气中
2.
不要把现象和结果混淆
不要说成是:有氯化铜生成。
(这是反应的结果)
1.
区分烟和雾
Cl2与Cu反应的现象是:有棕黄色的烟产生
你是否遇到过打开自来水,会闻到一股刺激性的气味?这是什么原因?
(3)、与水反应
氯气能溶于水(常温常压下,1体积水约溶解2体积的氯气,1:2),氯气的水溶液叫氯水。
H2O
+
Cl2
=
HCl
+
HClO
(一元弱酸)
(次氯酸)
2、用氧化还原知识分析上述反应,标明电子转移的数目和方向,并指出其中的氧化剂、还原剂。
1、写出上述反应的离子方程式
次氯酸(HClO)的性质
A、弱酸性,为一元弱酸
电离方程式:
B、不稳定性,见光易分解
C、具有强氧化性
氧化性比Cl2还强,具有杀菌性能,还具有漂白性。氯水也因为含有次氯酸而具有漂白作用。
根据氯气与水反应方程式推测新制氯水中可能存在哪些粒子?
分子:
Cl2、H2O、HClO
离子:
H+、Cl-、ClO-、
OH-(极少量)
新制氯水可能具有哪些性质?
H+
酸性
Cl2
氧化性
HClO
漂白性
Cl-
遇硝酸银产生白色沉淀
氯水性质具有多样性,试指出下列各现象主要是何种微粒所表现出来的性质:
①氯水呈浅黄绿色______
②使湿润的紫色石蕊试纸先变红
后褪色
。
③滴加AgNO3溶液后生成白色沉淀
.
Cl2
H+
HClO
Cl-
④加入石灰石粉末逐渐溶解,并放出气体______
⑤往含有Fe2+溶液中滴加KSCN溶液无明显现象,再滴加氯水后呈红色
。
H+
Cl2
氯水的漂白作用
【实验4-4、5】将有色纸条分别放入①干燥氯气瓶和②盛有1/3体积新制氯水的广口瓶中,盖上玻璃片,观察现象。
现象
结论
与解释
①有色布条不褪色
②有色布条褪色
①干燥的氯气无漂白作用
②氯水中起漂白作用的是HClO
——HClO起漂白作用
1、在氯水中滴入紫色石蕊试液,会观察到什么变化?
2、久置氯水中又有哪些粒子,具有怎样的性质?
2、新制氯水久置后酸性如何变化?
3、氯水应该怎样保存?
H+
、Cl-、H2O、OH—(少量)
久置氯水相当于盐酸
酸性增大
阴凉处,避光保存
紫色石蕊试纸先变红,后褪色
新制、久置氯水以及液氯比较
新制氯水
久置氯水
液氯
物质种类
成分
性质
混合物
混合物
纯净物
分子:Cl2,
H2O,
HClO
离子:H+,
Cl-,
ClO-,
OH-(极少量)
分子:H2O
离子:Cl-,H+
Cl2
三分子、四离子
氯水只能现配现用,并保存在棕色试剂瓶内,至于阴暗处。
强氧化性、酸性、漂白性
酸性
强氧化性
1、下列关于氯的说法正确的是(
)
A.
液氯和氯水是同一物质
B
.
氯水久置后酸性将减弱
C
.
新制氯水可使蓝色石蕊试纸先变红后褪色
D
.
光照氯水有气泡逸出,该气体为Cl2
E.
新制氯水中滴加硝酸银溶液,没有任何现象
F.
新制氯水可以使干燥的布条褪色
C、F
2、现在你知道养金鱼时,为什么要先将自来水在阳光下暴晒1-2天吗?
问题1:既然氯气可用来杀菌消毒,那么游泳池中是直接使
用氯气消毒的吗?
问题2
:既然氯水中真正起消毒杀菌作用的物质是次氯酸,
而次氯酸又不稳定,那么工业上又是如何解决存放和运输
问题的呢?
(提示:碳酸不稳定,碳酸盐稳定吗?)
思考:如何得到次氯酸盐?
(4)、与碱反应
①与NaOH溶液反应
2NaOH+Cl2=NaClO+NaCl+H2O
有效成分:NaClO
漂白液
Cl2尾气吸收处理
此反应离子方程式,用单线桥注明电子转移情况
——工业制备漂白液
漂白粉
①禽流感消毒:可用5%漂白粉溶液喷洒于动物圈舍、笼架、饲槽及车辆等进行消毒。
②非典型肺炎污染对象的消毒方法:物品、家具可用漂白粉配成溶液进行浸泡、喷洒或擦洗。
③洪涝灾害饮水问题:可用漂白粉或漂粉精对水进行消毒。
说明书
漂白粉(次氯酸钙)
化学式(Ca(ClO)2)
性状:漂白粉为白色粉
末固体,
主要用作染
料、医药、矿业行业的
水处理;自来水消毒、
游泳池、鱼塘杀菌,蔬
菜、饲养场的消毒、净
水
漂白粉、漂粉精主要成分
有效成分:Ca(ClO)2
用途:既可做漂白棉、麻、纸张的漂白剂,又可做游泳池及环境的消毒剂。
②与Ca(OH)2溶液反应
2Cl2+2Ca(OH)2=
CaCl
2+Ca(ClO)2+2H2O
——工业制备漂白粉
此反应离子方程式,用单线桥注明电子转移情况
提示:与澄清石灰水反应:
与石灰乳反应:
氯气跟碱反应的化学方程式有规律吗?
氯气+碱
氯化物+次氯酸盐+水
Cl2既是氧化剂,又是还原剂
漂白粉中的成分并没有杀菌、消毒的作用,那它是怎样发挥杀菌、消毒作用的?
日常
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO
工业
Ca(ClO)2+2HCl=CaCl2+2HClO
漂白原理:
(反应原理:强酸制取弱酸)
氯水、漂白液、漂白粉、漂粉精的漂白作用都是因反应生成的HClO
漂白粉敞放在潮湿的空气中会失效吗?又应该如何保存?
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO
失效原理:
密封、干燥、避光保存。
3、用途
1)、用于自来水的杀菌、消毒;
3)、工业制盐酸。
2)、制取漂白粉、消毒液等;
4)、氯气是合成塑料、橡胶、人造纤维、
农药、染料和药品的重要原料
任何事物都有两面性,化学技术和化学品也不例外。氯气是有毒气体,但它可以用于自来水消毒,而且是重要的化工原料。近来也有研究表明,使用氯气给自来水消毒时,会产生有致癌作用的物质如三氯甲烷,在一些发达国家已经使用更好的替代品如二氧化氯、臭氧等。所以,我们应该认真学好知识,正确运用,让自然资源更好地为人类服务。
氯气是一种有毒气体,但在工农业生产和日常生活中却有着广泛的应用,从中你得到什么启示?
氯及其化合物
Cl2
物理性质
化学性质
黄绿色气体
与金属单质反应
与非金属单质反应
与水反应
与碱反应
HClO
化学性质
弱酸性、强氧化性、不稳定性
含氧酸盐
NaClO
、Ca(ClO)2
用途
消毒液,漂白粉
1、可以用氯气灌洞的方法来消灭田鼠,这是利用了氯气的哪些性质?(
)
①密度比空气大
②易液化
③能溶于水
④有毒
A、
①
②
B、
③
④
C、
①
③
④
D、
①
④
D
2、下列氯化物中,既能由金属和氯气直接反应制得,又能由金属和盐酸反应制得的是(
)
A、CuCl2
B、FeCl2
C、FeCl3
D、AlCl3
D
3.下列关于氯水的说法中正确的是(
)
A.新制氯水中只含有Cl2和H2O分子
B.新制氯水能杀菌消毒是因为Cl2有毒,能毒杀细菌
C.光照氯水有气泡逸出,该气体是Cl2
D.氯水放置数天后酸性增强
D
4、洪灾过后,饮用水的消毒杀菌成为一只大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为
。
2)漂白粉的有效成分是
(填化学式)。
3)漂白粉溶于水后,受空气中CO2作用,即产生有漂白、杀菌作用的次氯酸,发生化学反应的离子方程式为
4)反应1)和3)中属于氧化还原反应的是(填编号)
。
5)瓶装漂白粉久置于空气中会呈稀粥状而失效。试用化学方程式表示漂白粉在空气中失效的原因是
。
2Cl2+2Ca(OH)2=
CaCl
2+Ca(ClO)2+2H2O
Ca(ClO)2
Ca2+
+2ClO-+CO2+H2O=CaCO3↓+2HClO
1)
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO
