人教版(2019)化学选择性必修三 4.2~4.3 蛋白质、核酸 小节自测(A)卷(含解析)
文档属性
| 名称 | 人教版(2019)化学选择性必修三 4.2~4.3 蛋白质、核酸 小节自测(A)卷(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 551.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-08-21 17:52:13 | ||
图片预览




文档简介
2020—2021学年人教版(2019)选择性必修三章节自我强化训练第四章生物大分子 第二、三节蛋白质、核酸 小节自测(A)卷
1.将甘氨酸和丙氨酸混合后,在一定条件下发生成肽反应,能生成的二肽有(?? )
A.1种????????B.2种????????
C.3种????????D.4种
2.据美国《农业研究》杂志报道,美国的科学家发现半胱氨酸能增强艾滋病毒感染者的免疫力,对控制艾滋病毒的蔓延有奇效。已知半胱氨酸的结构简式为,则下列说法错误的是( )
A.两分子半胱氨酸脱水形成的二肽结构简式为:
B.半胱氨酸是一种两性物质
C.可与过量NaOH溶液反应放出氨气
D.天然蛋白质水解产物均为α﹣氨基酸
3.欲将蛋白质从水中析出而又不改变它的性质, 应加入(?? )
A.(NH4)2SO4溶液 B.75%的酒精溶液 C.CuSO4溶液 D.NaOH浓溶液
4.在有机化合物中,若一个碳原子连有4个不同的原子或原子团,则这个碳原子称为"手性碳原子"。有手性碳原子的物质具有光学活性。下列物质中不具有光学活性的是(?? )
A.
B.氨基乙酸
C.α-氨基丙酸
D.
5.构成下列结构片段蛋白质的氨基酸的种类数目为(?? )
A.2种 B.3种 C.4种 D.5种
6.三国时代,诸葛亮领兵南征孟获,遇到了"哑泉",士兵饮后致哑,腹痛,甚至死亡。又有一"安乐泉"饮后可解"哑泉"之毒。1995年10月国内某报刊报道,经科研人员研究,“哑泉”水中溶有CuSO4,"安乐泉"水质偏碱性。下列有关说法符合题意的是(?? )
①"哑泉"之毒是由于水中的Cu2+使人体中的蛋白质变性引起
②"哑泉"之毒是由于水中的使人体中的蛋白质变性引起
③"哑泉"之毒是由于水中的Cu2+水解显酸性使人体中的蛋白质变性引起
④"安乐泉"能解“哑泉”之毒的离子方程式为Cu2++2OH-Cu(OH)2↓
①④???????B.②④???????
C.③?????????D.均不正确
7.有关核酸的叙述正确的是(?? )
A.核酸对生物体的生长繁殖、遗传变异等起着决定性作用,是生命活动的控制者,大量存在于细胞核中
B.核酸指挥控制着蛋白质的合成,细胞的分裂,主要存在于细胞质中
C.生物体遗传信息的载体DNA,大量存在于细胞核中,决定蛋白质的合成
D.生物体遗传信息的载体RNA,大量存在于细胞质?中,控制蛋白质的合成
8.在亚洲地区肆虐的禽流感又称为真性鸡瘟,亚洲的一些国家和地区发现了人类因感染禽流感死亡的病例。据专家分析,该病毒中有70%~75%的化学组成为蛋白质,因此要重视高温杀毒,在56℃时加热30分钟,60℃时加热10分钟,70℃时加热数分钟,阳光直射40到48小时均可杀死禽流感病毒。专家的上述建议是利用了蛋白质性质中的(?? )
A.盐析???????B.变性???????
C.水解???????D.颜色反应
9.三国时代,诸葛亮领兵南征孟获,遇到了“哑泉”,士兵饮后致哑,腹痛,甚至死亡。又有一“安乐泉”饮后可解“哑泉”之毒。1995年10月国内某报刊报道,经科研人员研究,“哑泉”水中溶有CuSO4,“安乐泉”水质偏碱性。下列有关说法中可能符合题意的是( )
A.“哑泉”之毒是由于水中的Cu2+使人体中的蛋白质变性
B.“哑泉”之毒是由于水中的使人体中的蛋白质变性
C.“哑泉”之毒是由于水中的Cu2+水解显酸性使人体中的蛋白质变性
D.“安乐泉”能解“哑泉”之毒的离子方程式为H++OH-=H2O
10."克隆羊"的关键技术之一是找到一些特殊的酶,这些酶能激活普通体细胞,使之能像生殖细胞一样发育成个体。下列说法不正确的是(?? )
A.酶具有催化作用
B.酶的催化作用具有选择性和专一性
C.高温或重金属盐能降低酶的活性
D.酶只有在强酸性或强碱性条件下才能发挥作用
11.下列对氨基酸和蛋白质的描述中正确的是(?? )
A.加热能杀死流感病毒是因为蛋白质受热变性
B.氨基酸和蛋白质遇重金属离子均会变性
C.α-氨基丙酸与α-氨基苯丙酸混合物脱水成肽,只生成2种二肽
D.氨基酸溶于过量氢氧化钠溶液中,生成的离子在电场作用下向负极移动
12.DNA复制是按半保留方式进行的。如果一个完全放射标记的双链DNA分子在不含有放射标记的溶液中,进行两轮复制。如此产生的4个DNA分子的放射活性将会出现(?? )
A.半数分子没有放射性
B.所有分子都有放射性
C.半数分子的两条链都有放射性
D.—个分子的两条链都有放射性
13.青霉素是重要的抗生素,其在体内经酸性水解后得到一种有机物R。R的结构如图所示,下列有关R的说法正确的是(?? )
A.R的分子式为C5H10NO2S B.R只能发生取代反应
C.R既可以与酸反应也可与碱反应 D.R属于烃的含氧衍生物
14.糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质。以下叙述正确的是(?? )
A.植物油不能使溴的四氯化碳溶液褪色
B.淀粉水解的最终产物是葡萄糖
C.葡萄糖能发生氧化反应和水解反应
D.蛋白质溶液遇硫酸铜后产生的沉淀能重新溶于水
15.有一分子式为的二肽,经水解得丙氨酸和另一种氨基酸X,则X的化学式可能是(?? )
A.C3H7NO3?????B.C5H9NO4?????C.C5H11NO5?????D.C5H7NO4
16.A是某天然蛋白质在一定条件下发生水解得到的产物之一。经测定:A的相对分子质量不超过200,其中氧元素所占质量分数约为26.5%;等物质的量的A分别与NaOH、Na充分反应,消耗两者的物质的量之比为1:2;经仪器分析A分子中含有苯环,不含-CH2-和-CH3基团。
(1)测定A的相对分子质量的仪器是__________,A的摩尔质量为__________。
(2)一定条件下A分子间发生反应生成聚酯的化学方程式为__________。
(3)A的同分异构体有多种,写出符合下列条件的所有异构体的结构简式:__________。
① 与A具有相同的官能团,是二取代苯,且苯环上的一溴代物有两种
② 催化氧化产物能发生银镜反应
③ 分子中氨基与羧基的位置关系与A分子中的氨基与羧基的位置关系不同
17.某有机物含碳、氢、氧、氮四种元素。如图是该有机物的球棍模型(其中黑点表示原子,短线表示原子之间的共价键):
(1).则该有机物的化学式为__________,结构简式为__________。
(2).该有机物可能发生的化学反应有__________(填编号)。
①水解 ②加聚 ③取代 ④消去 ⑤酯化
(3).该有机物发生水解反应的化学方程式:__________
(4).写出该有机物的一种同分异构体,它的分子中含有两个,且是天然蛋白质水解的最终产物之一,则该同分异构体的结构简式为__________
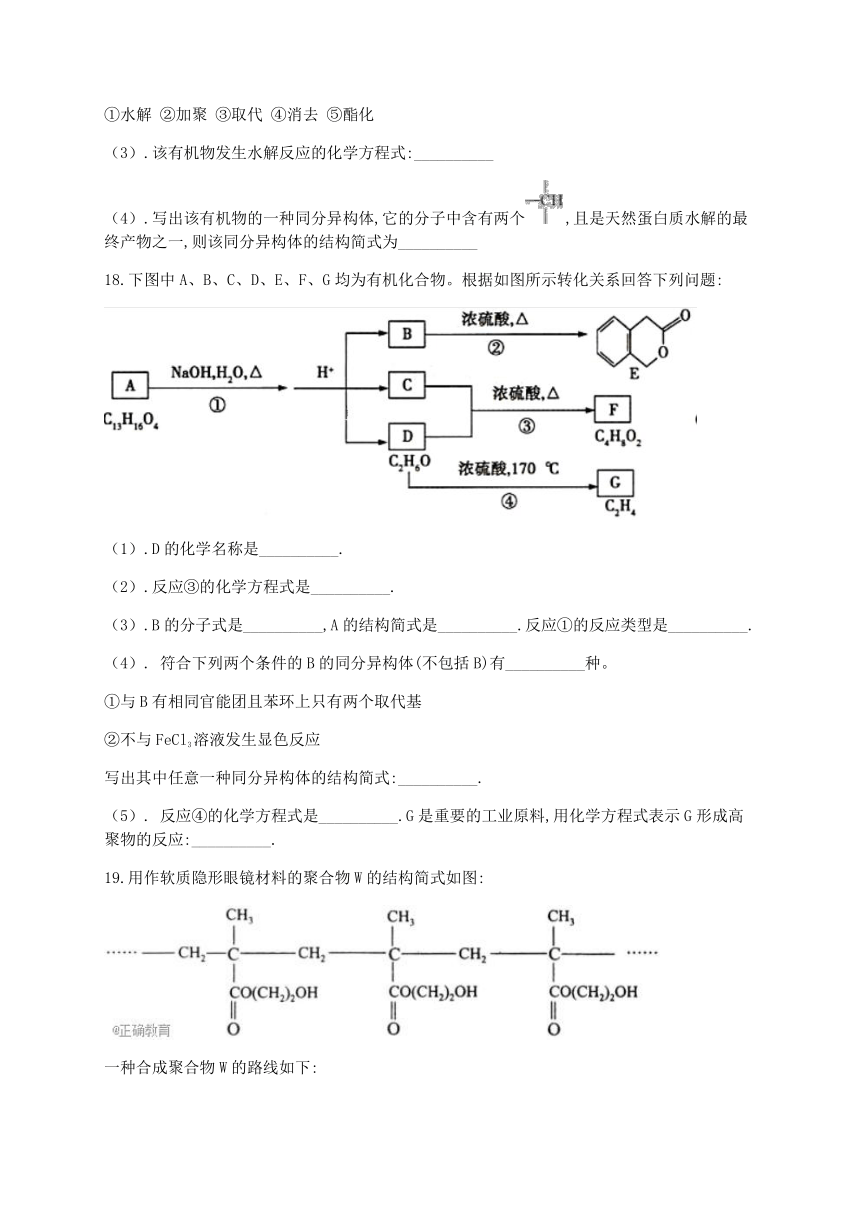
18.下图中A、B、C、D、E、F、G均为有机化合物。根据如图所示转化关系回答下列问题:
(1).D的化学名称是__________.
(2).反应③的化学方程式是__________.
(3).B的分子式是__________,A的结构简式是__________.反应①的反应类型是__________.
(4). 符合下列两个条件的B的同分异构体(不包括B)有__________种。
①与B有相同官能团且苯环上只有两个取代基
②不与FeCl3溶液发生显色反应
写出其中任意一种同分异构体的结构简式:__________.
(5). 反应④的化学方程式是__________.G是重要的工业原料,用化学方程式表示G形成高聚物的反应:__________.
19.用作软质隐形眼镜材料的聚合物W的结构简式如图:
一种合成聚合物W的路线如下:
已知:①的质谱图表明其相对分子质量为58;
②常用作果实催熟剂;
③
根据以上信息,回答下列问题:
(1). 中含有的官能团名称是__________。
(2). 的结构简式为__________,的反应类型是__________反应。
(3).写出下列反应的化学方程式:①:__________,
②:__________。
(4). 有多种同分异构体。属于酯类且含有碳碳双键的同分异构体共有__________(不考虑顺反异构)种,写出其中核磁共振氢谱峰面积之比为1:1:1:3的同分异构体的结构简式:__________。
20.某课外小组设计的实验室制取乙酸乙酯的装置如图所示,其中A中盛有浓硫酸,B中盛有乙醇、无水醋酸,D中盛有饱和碳酸钠溶液。
已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH;②有关有机物的沸点如下:
试剂
乙醚
乙醇
乙酸
乙酸乙酯
沸点/℃
34.6
78.3
117.9
77
请回答下列问题:
(1).若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示18O位置的化学方程式:__________.
(2). 球形干燥管C的作用是__________。若反应前向D中加入几滴酚酞,溶液呈红色,产生此现象的原因是__________(用离子方程式表示),反应结束后D中的现象是__________.
(3).从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出__________,再加__________(填序号),然后进行蒸馏,收集77℃左右的馏分,以得到较纯净的乙酸乙酯。
A.五氧化二磷?
B.碱石灰?
C.无水硫酸钠?
D.生石灰
21.实验小组测定某蛋白质的组成(假定只含C、H、O、N元素),设计如下实验(夹持装置略去)。
I.样品中碳、氢含量的测定
(1).仪器a的名称为__________
(2).导管g的作用为__________
(3).选择上述装置,按气流从左到右的方向,合理的连接顺序为__________(填大写字母,仪器可重复使用)→排水法收集气体装置。
(4).称取4.65g蛋白质样品,用上述连接好的装置进行实验。
①充分反应后,熄灭D处酒精灯之前,需继续通入O2至硬质玻璃管冷却,原因为__________
②充分反应后,测得用于接收气体产物的碱石灰和P2O5分别增重7.7g、2.25g
(5).样品中氮元素含量的测定已知:在催化剂存在下,浓硫酸能将样品中的氮元素转化为铵盐。i.重新称取4.65g蛋白质样品,将其中的氮元素全部转化为铵盐;ii.所得铵盐与足量NaOH溶液反应,并用100mL 1mol·L-1 盐酸将生成的氨气全部吸收;iii.将吸收液稀释至500mL;iv.取25.00mL稀释后的溶液,用0.1000mol·L-1 的NaOH 溶液平行滴定,平均消耗标准液25.00mL。
蛋白质样品中C、H、N、O的原子数目之比为__________。若步骤iii 中定容时仰视容量瓶刻度线,则所测氮元素含量__________(填“偏高”“偏低”或“无影响”)。
有同学认为,通过3中收集到的气体体积即可得到氮元素的含量,你认为其观点__________(填“正确”或“不正确”),理由为__________
参考答案
1.答案:D
解析:甘氨酸与丙氨酸混合发生成肽反应,若是两者间的成肽反应,可生成2中二肽;若是自身间的成肽反应,也可得到2中二肽,故共生成4中二肽。
2.答案:A
解析:一个半胱氨酸分子中的羧基与另一个半胱氨酸分子中的氨基发生脱水缩合,生成二肽的结构简式应为,故A错误;半膀氨酸分子中含有羧基和氨基,羧基显酸性,氨基显碱性,因此半胱氨酸是一种两性物质,故B正确;中含有,加入过量NaOH溶液,能产生,故C正确;天然蛋白质水解的最终产物是α-氨基酸,故D正确。
3.答案:A
解析:(NH4)2SO4溶液能够降低蛋白质的溶解度,向蛋白质溶液中加入(NH4)2SO4溶液会使蛋白质从水中析出而又不改变它的性质,故A符合题意;酒精、CuSO4、NaOH均会使蛋白质失活,改变了它的性质,故B、C、D不符合题意。
4.答案:B
解析:氨基乙酸的α碳上有两个氢原子,不满足"手性碳原子"的结构条件。
5.答案:B
解析:两个氨基酸分子在酸或碱的存在下加热,通过一分子的氨基和另一分子的羧基间脱去一分子水缩合形成含有肽键的化合物,称为成肽反应,蛋白质水解断裂的是肽键,生成相应的氨基酸,故该片断蛋白质水解生成的氨基酸的结构简式依次为H2NCH(CH3)COOH、H2NCH2COOH、H2NCH(CH3)COOH、H2NCH(C2H5)COOH、H2NCH2COOH,可见共3种氨基酸,B正确。
6.答案:A
解析:Cu2+是重金属离子,可以使"生命的基石"----蛋白质变性而失去生理活性。OH-可以使Cu2+转变成不溶性的Cu(OH)2而失去作用
7.答案:C
解析:根据五碳糖不同可以将核酸分为DNA和RNA,核酸是遗传信息的携带者,对于生物的遗传变异及蛋白质的生物合成具有重要作用。RNA主要存在于细胞质中,DNA大量存在于细胞核中,A错误;RNA主要存在于细胞质中,根据DNA提供的信息控制体内蛋白质的合成,B错误;DNA大量存在于细胞核中,是生物体遗传信息的载体,决定蛋白质的合成,C正确;生物体遗传信息的载体是DNA,D错误。
8.答案:B
解析:题干中信息是使蛋白质失去活性,即变性。
9.答案:A
解析:“哑泉”有毒是因为其含有的CuSO4电离出的Cu2+为重金属离子,重金属离子能使蛋白质变性,不能使人体中的蛋白质变性,A符合题意,B、C不符合题意;要解“哑泉”之毒就要使可溶性的Cu2+转变成沉淀,离子方程式为Cu2++2OH-=Cu(OH)2↓,D不符合题意。
10.答案:D
解析:酶在强酸性或强碱性条件下才会发生变性。
11.答案:A
解析:A项,加热能使蛋白质发生变性,杀死流感病毒,正确;B项,蛋白质遇重金属离子会变性,氨基酸与重金属离子的作用不属于变性,错误;C项,α-氨基丙酸与α-氨基苯丙酸混合物脱水成肽可生成4种二肽,自身脱水可形成2种二肽,不同分子间脱水可形成2种二肽(α-氨基丙酸的羧基脱羟基与α-氨基苯丙酸的氨基脱氢或α-氨基丙酸的氨基脱氢与α-氨基苯丙酸的羧基脱羟基),错误;D项,氨基酸溶于过量NaOH溶液,其中羧基与NaOH反应生成酸根阴离子,在电场作用下向正极移动,错误。
12.答案:A
解析:第一轮复制时,旧DNA分子的双螺旋结构在某些蛋白质的作用下解旋,2条链中间的碱基对分开,成为2条具有放射标记的单链,然后每条链按照碱基互补配对原则从不含有放射标记的溶液中吸收核苷酸,生成均具有放射标记的两个新的DNA分子,但是都是一条链上有放射标记。第二轮复制时,两个新的DNA分子解旋得到4条单链,2条有放射标记,2条没有,然后各自吸收没有放射标记的核苷酸形成4个DNA分子。很显然,4个DNA分子只有2个有放射标记,且都是只有一条链上有放射标记。
13.答案:C
解析:由有机物R的键线式可知,其分子式为C5H11NO2S,故A错误;R除了能发生取代反应外,还可以发生氧化反应(如燃烧、氨基被氧化)、还原反应(羧基被LiAlH4还原)等,故B错误;R分子中既含有氨基也含有羧基,所以既可以与酸反应也可以与碱反应,故C正确;R的组成中除了C、H、O元素之外还含有N、S元素,不属于烃的含氧衍生物,故D错误。
14.答案:B
解析:植物油中含有碳碳不饱和键,可使溴的四氯化碳溶液褪色;葡萄糖为单糖,不能发生水解反应;蛋白质遇重金属盐溶液发生变性,是不可逆过程。
15.答案:B
解析:水解方程式为+X,根据质量守恒可得X的化学式。
16.答案:(1)质谱仪;181g·mol-1
(2)
(3)
解析:(1)测定有机物的相对分子质量的仪器是质谱仪。A的相对分子质量不超过200,其中氧元素所占质量分数约为26.5%,由可知,A中最多可有3个氧原子,A是天然蛋白质的水解产物,则A为α-氨基酸,分子中含有-NH2、-COOH,由等物质的量的A分别与NaOH、Na充分反应,消耗两者的物质的量之比为1:2,可知分子中还含有-OH,-COOH与-OH个数之比为1:1,即分子中含有1个-COOH和1个-OH,则A分子中含有3个氧原子,A的摩尔质量为。
(2)根据上述分析,A分子中含有苯环、-NH2、-COOH、-OH,不含-CH2-和-CH3,可推得A的结构简式为;A分子中含-OH和-COOH,一定条件下可发生缩聚反应生成聚酯。
(3)满足条件:①与A具有相同的官能团,是二取代苯,且苯环上的一溴代物有两种,说明含有-NH2、-OH、-COOH,两取代基在苯环上是对位位置关系;②催化氧化产物能发生银镜反应,说明分子中含有-CH2OH结构;③分子中氨基与羧基的位置关系与A分子中的氨基与羧基的位置关系不同,符合条件的有机物的结构简式为。
17.答案:(1).C5H11O2N;?? CH3CH2CONHCH2CH2OH
(2).①③④⑤; (3).CH3CH2CONHCH2CH2OH+H2O→CH3CH2COOH+H2NCH2CH2OH
(4).
解析:(1).形成一个共价键的为氢原子,形成两个共价键的为氧原子,形成三个共价键的为氮原子,形成四个共价键的为碳原子。
(4).所写物质为天然蛋白质水解产物即为α-氨基酸,故可表示为。由题意知, 中应含有一个,故只能为
18.答案:(1).乙醇; (2).CH3COOH+C2H5OHCH3COOC2H5+H2O
(3). ;;水解反应
(4).11;
(5).C2H5OHCH2=CH2↑+H2O;nCH2=CH2
解析:(1). B在浓硫酸、加热条件下反应生成E,则B中含有羧基和羟基,由此可知B的结构简式为。D在浓硫酸、170℃下反应生成乙烯,结合D的分子式,可知D是乙醇.C和乙醇在浓硫酸、加热条件下发生酯化反应生成F,结合F的分子式可知C的结构简式为CH3COOH,则A的结构简式为.
(4). 由①可知其结构中含有羟基和羧基,由②可知其苯环上无羟基,故其含有的取代基为-CH2COOH和-CH2OH、-COOH和-CHOHCH3、-COOH和-CH2CH2OH、-CH3和-CHOHCOOH,两个取代基在苯环上有三种位置关系,故符合条件的同分异构体(不包括B)共有11种.
19.答案:(1).碳碳双键、醛基; (2). ;加聚
(3).①
②
(4).5;
解析:(1).结合信息知, 生成是先醛、醛加成然后失水生成烯醛的反应,由于式量为58,所以为丙醛, 为2-甲基丙烯醛, 为2-甲基丙烯酸,根据的结构知, 为乙二醇,所以为乙烯, 为1,2-二溴乙烷。
由于为2-甲基丙烯醛,所以中含碳碳双键和醛基。
(2). 为丙醛, 生成是中双键发生加聚形成高分子。
(3). 生成为乙烯与溴单质加成的反应, 与生成为酯化反应。
(4). 为2-甲基丙烯酸,含双键含酯基的异构体中,甲酸酯3种,乙酸酯1种,丙烯酸酯1种,共5种,符合核磁共振氢谱要求的结构只有。
20.答案:(1).
(2).冷凝蒸气,防止倒吸; ;溶液分层,上层为无色油状液体,下层溶液颜色变浅
(3).乙醇; C
解析:(1).考查利用同位素示踪法表示酯化反应的机理.酯化反应中羧酸提供羟基,醇提供氢原子,据此可写出该反应的化学方程式。
(2).考查盐类的水解、酯化反应的可逆性及饱和Na2CO3溶液在制取乙酸乙酯时的作用.由于生成的乙酸乙酯中含有乙酸和乙醇,二者都与水互溶,所以球形干燥管C的作用除了起到冷凝蒸气的作用外,还起到防止倒吸的作用.碳酸钠水解,溶液显碱性,因此滴加酚酞溶液显红色。乙酸乙酯不溶于水,而乙酸能和碳酸钠反应,所以反应结束后D中的现象是溶液分层,上层为无色油状液体,下层溶液颜色变浅.
(3).根据题给信息“①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH",说明加入无水氯化钙可除去乙醇,之后加入的物质既要吸收水,又要与乙酸乙酯不反应,C项符合题意.
21.答案:(1).长颈漏斗; (2).平衡压强,使分液漏斗中的水容易滴下;(3).BEDECC; (4).将装置中残留的的水蒸气和CO2全部吹入吸收剂被吸收
(5).7:10:2:4; 偏高; 不正确; 收集的氮气中混有未参加反应的氧气
解析:(1).仪器a的名称为长颈漏斗
(2).导管g的作用为平衡压强,使分液漏斗中的水容易滴下
(3).选择上述装置,按气流从左到右的方向,合理的连接顺序为BEDECC(填大写字母,仪器可重复使用)→排水法收集气体装置
(4).①充分反应后,熄灭D处酒精灯之前,需继续通入O2至硬质玻璃管冷却,原因为将装置中残留的的水蒸气和CO2全部吹入吸收剂被吸收。
1.将甘氨酸和丙氨酸混合后,在一定条件下发生成肽反应,能生成的二肽有(?? )
A.1种????????B.2种????????
C.3种????????D.4种
2.据美国《农业研究》杂志报道,美国的科学家发现半胱氨酸能增强艾滋病毒感染者的免疫力,对控制艾滋病毒的蔓延有奇效。已知半胱氨酸的结构简式为,则下列说法错误的是( )
A.两分子半胱氨酸脱水形成的二肽结构简式为:
B.半胱氨酸是一种两性物质
C.可与过量NaOH溶液反应放出氨气
D.天然蛋白质水解产物均为α﹣氨基酸
3.欲将蛋白质从水中析出而又不改变它的性质, 应加入(?? )
A.(NH4)2SO4溶液 B.75%的酒精溶液 C.CuSO4溶液 D.NaOH浓溶液
4.在有机化合物中,若一个碳原子连有4个不同的原子或原子团,则这个碳原子称为"手性碳原子"。有手性碳原子的物质具有光学活性。下列物质中不具有光学活性的是(?? )
A.
B.氨基乙酸
C.α-氨基丙酸
D.
5.构成下列结构片段蛋白质的氨基酸的种类数目为(?? )
A.2种 B.3种 C.4种 D.5种
6.三国时代,诸葛亮领兵南征孟获,遇到了"哑泉",士兵饮后致哑,腹痛,甚至死亡。又有一"安乐泉"饮后可解"哑泉"之毒。1995年10月国内某报刊报道,经科研人员研究,“哑泉”水中溶有CuSO4,"安乐泉"水质偏碱性。下列有关说法符合题意的是(?? )
①"哑泉"之毒是由于水中的Cu2+使人体中的蛋白质变性引起
②"哑泉"之毒是由于水中的使人体中的蛋白质变性引起
③"哑泉"之毒是由于水中的Cu2+水解显酸性使人体中的蛋白质变性引起
④"安乐泉"能解“哑泉”之毒的离子方程式为Cu2++2OH-Cu(OH)2↓
①④???????B.②④???????
C.③?????????D.均不正确
7.有关核酸的叙述正确的是(?? )
A.核酸对生物体的生长繁殖、遗传变异等起着决定性作用,是生命活动的控制者,大量存在于细胞核中
B.核酸指挥控制着蛋白质的合成,细胞的分裂,主要存在于细胞质中
C.生物体遗传信息的载体DNA,大量存在于细胞核中,决定蛋白质的合成
D.生物体遗传信息的载体RNA,大量存在于细胞质?中,控制蛋白质的合成
8.在亚洲地区肆虐的禽流感又称为真性鸡瘟,亚洲的一些国家和地区发现了人类因感染禽流感死亡的病例。据专家分析,该病毒中有70%~75%的化学组成为蛋白质,因此要重视高温杀毒,在56℃时加热30分钟,60℃时加热10分钟,70℃时加热数分钟,阳光直射40到48小时均可杀死禽流感病毒。专家的上述建议是利用了蛋白质性质中的(?? )
A.盐析???????B.变性???????
C.水解???????D.颜色反应
9.三国时代,诸葛亮领兵南征孟获,遇到了“哑泉”,士兵饮后致哑,腹痛,甚至死亡。又有一“安乐泉”饮后可解“哑泉”之毒。1995年10月国内某报刊报道,经科研人员研究,“哑泉”水中溶有CuSO4,“安乐泉”水质偏碱性。下列有关说法中可能符合题意的是( )
A.“哑泉”之毒是由于水中的Cu2+使人体中的蛋白质变性
B.“哑泉”之毒是由于水中的使人体中的蛋白质变性
C.“哑泉”之毒是由于水中的Cu2+水解显酸性使人体中的蛋白质变性
D.“安乐泉”能解“哑泉”之毒的离子方程式为H++OH-=H2O
10."克隆羊"的关键技术之一是找到一些特殊的酶,这些酶能激活普通体细胞,使之能像生殖细胞一样发育成个体。下列说法不正确的是(?? )
A.酶具有催化作用
B.酶的催化作用具有选择性和专一性
C.高温或重金属盐能降低酶的活性
D.酶只有在强酸性或强碱性条件下才能发挥作用
11.下列对氨基酸和蛋白质的描述中正确的是(?? )
A.加热能杀死流感病毒是因为蛋白质受热变性
B.氨基酸和蛋白质遇重金属离子均会变性
C.α-氨基丙酸与α-氨基苯丙酸混合物脱水成肽,只生成2种二肽
D.氨基酸溶于过量氢氧化钠溶液中,生成的离子在电场作用下向负极移动
12.DNA复制是按半保留方式进行的。如果一个完全放射标记的双链DNA分子在不含有放射标记的溶液中,进行两轮复制。如此产生的4个DNA分子的放射活性将会出现(?? )
A.半数分子没有放射性
B.所有分子都有放射性
C.半数分子的两条链都有放射性
D.—个分子的两条链都有放射性
13.青霉素是重要的抗生素,其在体内经酸性水解后得到一种有机物R。R的结构如图所示,下列有关R的说法正确的是(?? )
A.R的分子式为C5H10NO2S B.R只能发生取代反应
C.R既可以与酸反应也可与碱反应 D.R属于烃的含氧衍生物
14.糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质。以下叙述正确的是(?? )
A.植物油不能使溴的四氯化碳溶液褪色
B.淀粉水解的最终产物是葡萄糖
C.葡萄糖能发生氧化反应和水解反应
D.蛋白质溶液遇硫酸铜后产生的沉淀能重新溶于水
15.有一分子式为的二肽,经水解得丙氨酸和另一种氨基酸X,则X的化学式可能是(?? )
A.C3H7NO3?????B.C5H9NO4?????C.C5H11NO5?????D.C5H7NO4
16.A是某天然蛋白质在一定条件下发生水解得到的产物之一。经测定:A的相对分子质量不超过200,其中氧元素所占质量分数约为26.5%;等物质的量的A分别与NaOH、Na充分反应,消耗两者的物质的量之比为1:2;经仪器分析A分子中含有苯环,不含-CH2-和-CH3基团。
(1)测定A的相对分子质量的仪器是__________,A的摩尔质量为__________。
(2)一定条件下A分子间发生反应生成聚酯的化学方程式为__________。
(3)A的同分异构体有多种,写出符合下列条件的所有异构体的结构简式:__________。
① 与A具有相同的官能团,是二取代苯,且苯环上的一溴代物有两种
② 催化氧化产物能发生银镜反应
③ 分子中氨基与羧基的位置关系与A分子中的氨基与羧基的位置关系不同
17.某有机物含碳、氢、氧、氮四种元素。如图是该有机物的球棍模型(其中黑点表示原子,短线表示原子之间的共价键):
(1).则该有机物的化学式为__________,结构简式为__________。
(2).该有机物可能发生的化学反应有__________(填编号)。
①水解 ②加聚 ③取代 ④消去 ⑤酯化
(3).该有机物发生水解反应的化学方程式:__________
(4).写出该有机物的一种同分异构体,它的分子中含有两个,且是天然蛋白质水解的最终产物之一,则该同分异构体的结构简式为__________
18.下图中A、B、C、D、E、F、G均为有机化合物。根据如图所示转化关系回答下列问题:
(1).D的化学名称是__________.
(2).反应③的化学方程式是__________.
(3).B的分子式是__________,A的结构简式是__________.反应①的反应类型是__________.
(4). 符合下列两个条件的B的同分异构体(不包括B)有__________种。
①与B有相同官能团且苯环上只有两个取代基
②不与FeCl3溶液发生显色反应
写出其中任意一种同分异构体的结构简式:__________.
(5). 反应④的化学方程式是__________.G是重要的工业原料,用化学方程式表示G形成高聚物的反应:__________.
19.用作软质隐形眼镜材料的聚合物W的结构简式如图:
一种合成聚合物W的路线如下:
已知:①的质谱图表明其相对分子质量为58;
②常用作果实催熟剂;
③
根据以上信息,回答下列问题:
(1). 中含有的官能团名称是__________。
(2). 的结构简式为__________,的反应类型是__________反应。
(3).写出下列反应的化学方程式:①:__________,
②:__________。
(4). 有多种同分异构体。属于酯类且含有碳碳双键的同分异构体共有__________(不考虑顺反异构)种,写出其中核磁共振氢谱峰面积之比为1:1:1:3的同分异构体的结构简式:__________。
20.某课外小组设计的实验室制取乙酸乙酯的装置如图所示,其中A中盛有浓硫酸,B中盛有乙醇、无水醋酸,D中盛有饱和碳酸钠溶液。
已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH;②有关有机物的沸点如下:
试剂
乙醚
乙醇
乙酸
乙酸乙酯
沸点/℃
34.6
78.3
117.9
77
请回答下列问题:
(1).若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示18O位置的化学方程式:__________.
(2). 球形干燥管C的作用是__________。若反应前向D中加入几滴酚酞,溶液呈红色,产生此现象的原因是__________(用离子方程式表示),反应结束后D中的现象是__________.
(3).从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出__________,再加__________(填序号),然后进行蒸馏,收集77℃左右的馏分,以得到较纯净的乙酸乙酯。
A.五氧化二磷?
B.碱石灰?
C.无水硫酸钠?
D.生石灰
21.实验小组测定某蛋白质的组成(假定只含C、H、O、N元素),设计如下实验(夹持装置略去)。
I.样品中碳、氢含量的测定
(1).仪器a的名称为__________
(2).导管g的作用为__________
(3).选择上述装置,按气流从左到右的方向,合理的连接顺序为__________(填大写字母,仪器可重复使用)→排水法收集气体装置。
(4).称取4.65g蛋白质样品,用上述连接好的装置进行实验。
①充分反应后,熄灭D处酒精灯之前,需继续通入O2至硬质玻璃管冷却,原因为__________
②充分反应后,测得用于接收气体产物的碱石灰和P2O5分别增重7.7g、2.25g
(5).样品中氮元素含量的测定已知:在催化剂存在下,浓硫酸能将样品中的氮元素转化为铵盐。i.重新称取4.65g蛋白质样品,将其中的氮元素全部转化为铵盐;ii.所得铵盐与足量NaOH溶液反应,并用100mL 1mol·L-1 盐酸将生成的氨气全部吸收;iii.将吸收液稀释至500mL;iv.取25.00mL稀释后的溶液,用0.1000mol·L-1 的NaOH 溶液平行滴定,平均消耗标准液25.00mL。
蛋白质样品中C、H、N、O的原子数目之比为__________。若步骤iii 中定容时仰视容量瓶刻度线,则所测氮元素含量__________(填“偏高”“偏低”或“无影响”)。
有同学认为,通过3中收集到的气体体积即可得到氮元素的含量,你认为其观点__________(填“正确”或“不正确”),理由为__________
参考答案
1.答案:D
解析:甘氨酸与丙氨酸混合发生成肽反应,若是两者间的成肽反应,可生成2中二肽;若是自身间的成肽反应,也可得到2中二肽,故共生成4中二肽。
2.答案:A
解析:一个半胱氨酸分子中的羧基与另一个半胱氨酸分子中的氨基发生脱水缩合,生成二肽的结构简式应为,故A错误;半膀氨酸分子中含有羧基和氨基,羧基显酸性,氨基显碱性,因此半胱氨酸是一种两性物质,故B正确;中含有,加入过量NaOH溶液,能产生,故C正确;天然蛋白质水解的最终产物是α-氨基酸,故D正确。
3.答案:A
解析:(NH4)2SO4溶液能够降低蛋白质的溶解度,向蛋白质溶液中加入(NH4)2SO4溶液会使蛋白质从水中析出而又不改变它的性质,故A符合题意;酒精、CuSO4、NaOH均会使蛋白质失活,改变了它的性质,故B、C、D不符合题意。
4.答案:B
解析:氨基乙酸的α碳上有两个氢原子,不满足"手性碳原子"的结构条件。
5.答案:B
解析:两个氨基酸分子在酸或碱的存在下加热,通过一分子的氨基和另一分子的羧基间脱去一分子水缩合形成含有肽键的化合物,称为成肽反应,蛋白质水解断裂的是肽键,生成相应的氨基酸,故该片断蛋白质水解生成的氨基酸的结构简式依次为H2NCH(CH3)COOH、H2NCH2COOH、H2NCH(CH3)COOH、H2NCH(C2H5)COOH、H2NCH2COOH,可见共3种氨基酸,B正确。
6.答案:A
解析:Cu2+是重金属离子,可以使"生命的基石"----蛋白质变性而失去生理活性。OH-可以使Cu2+转变成不溶性的Cu(OH)2而失去作用
7.答案:C
解析:根据五碳糖不同可以将核酸分为DNA和RNA,核酸是遗传信息的携带者,对于生物的遗传变异及蛋白质的生物合成具有重要作用。RNA主要存在于细胞质中,DNA大量存在于细胞核中,A错误;RNA主要存在于细胞质中,根据DNA提供的信息控制体内蛋白质的合成,B错误;DNA大量存在于细胞核中,是生物体遗传信息的载体,决定蛋白质的合成,C正确;生物体遗传信息的载体是DNA,D错误。
8.答案:B
解析:题干中信息是使蛋白质失去活性,即变性。
9.答案:A
解析:“哑泉”有毒是因为其含有的CuSO4电离出的Cu2+为重金属离子,重金属离子能使蛋白质变性,不能使人体中的蛋白质变性,A符合题意,B、C不符合题意;要解“哑泉”之毒就要使可溶性的Cu2+转变成沉淀,离子方程式为Cu2++2OH-=Cu(OH)2↓,D不符合题意。
10.答案:D
解析:酶在强酸性或强碱性条件下才会发生变性。
11.答案:A
解析:A项,加热能使蛋白质发生变性,杀死流感病毒,正确;B项,蛋白质遇重金属离子会变性,氨基酸与重金属离子的作用不属于变性,错误;C项,α-氨基丙酸与α-氨基苯丙酸混合物脱水成肽可生成4种二肽,自身脱水可形成2种二肽,不同分子间脱水可形成2种二肽(α-氨基丙酸的羧基脱羟基与α-氨基苯丙酸的氨基脱氢或α-氨基丙酸的氨基脱氢与α-氨基苯丙酸的羧基脱羟基),错误;D项,氨基酸溶于过量NaOH溶液,其中羧基与NaOH反应生成酸根阴离子,在电场作用下向正极移动,错误。
12.答案:A
解析:第一轮复制时,旧DNA分子的双螺旋结构在某些蛋白质的作用下解旋,2条链中间的碱基对分开,成为2条具有放射标记的单链,然后每条链按照碱基互补配对原则从不含有放射标记的溶液中吸收核苷酸,生成均具有放射标记的两个新的DNA分子,但是都是一条链上有放射标记。第二轮复制时,两个新的DNA分子解旋得到4条单链,2条有放射标记,2条没有,然后各自吸收没有放射标记的核苷酸形成4个DNA分子。很显然,4个DNA分子只有2个有放射标记,且都是只有一条链上有放射标记。
13.答案:C
解析:由有机物R的键线式可知,其分子式为C5H11NO2S,故A错误;R除了能发生取代反应外,还可以发生氧化反应(如燃烧、氨基被氧化)、还原反应(羧基被LiAlH4还原)等,故B错误;R分子中既含有氨基也含有羧基,所以既可以与酸反应也可以与碱反应,故C正确;R的组成中除了C、H、O元素之外还含有N、S元素,不属于烃的含氧衍生物,故D错误。
14.答案:B
解析:植物油中含有碳碳不饱和键,可使溴的四氯化碳溶液褪色;葡萄糖为单糖,不能发生水解反应;蛋白质遇重金属盐溶液发生变性,是不可逆过程。
15.答案:B
解析:水解方程式为+X,根据质量守恒可得X的化学式。
16.答案:(1)质谱仪;181g·mol-1
(2)
(3)
解析:(1)测定有机物的相对分子质量的仪器是质谱仪。A的相对分子质量不超过200,其中氧元素所占质量分数约为26.5%,由可知,A中最多可有3个氧原子,A是天然蛋白质的水解产物,则A为α-氨基酸,分子中含有-NH2、-COOH,由等物质的量的A分别与NaOH、Na充分反应,消耗两者的物质的量之比为1:2,可知分子中还含有-OH,-COOH与-OH个数之比为1:1,即分子中含有1个-COOH和1个-OH,则A分子中含有3个氧原子,A的摩尔质量为。
(2)根据上述分析,A分子中含有苯环、-NH2、-COOH、-OH,不含-CH2-和-CH3,可推得A的结构简式为;A分子中含-OH和-COOH,一定条件下可发生缩聚反应生成聚酯。
(3)满足条件:①与A具有相同的官能团,是二取代苯,且苯环上的一溴代物有两种,说明含有-NH2、-OH、-COOH,两取代基在苯环上是对位位置关系;②催化氧化产物能发生银镜反应,说明分子中含有-CH2OH结构;③分子中氨基与羧基的位置关系与A分子中的氨基与羧基的位置关系不同,符合条件的有机物的结构简式为。
17.答案:(1).C5H11O2N;?? CH3CH2CONHCH2CH2OH
(2).①③④⑤; (3).CH3CH2CONHCH2CH2OH+H2O→CH3CH2COOH+H2NCH2CH2OH
(4).
解析:(1).形成一个共价键的为氢原子,形成两个共价键的为氧原子,形成三个共价键的为氮原子,形成四个共价键的为碳原子。
(4).所写物质为天然蛋白质水解产物即为α-氨基酸,故可表示为。由题意知, 中应含有一个,故只能为
18.答案:(1).乙醇; (2).CH3COOH+C2H5OHCH3COOC2H5+H2O
(3). ;;水解反应
(4).11;
(5).C2H5OHCH2=CH2↑+H2O;nCH2=CH2
解析:(1). B在浓硫酸、加热条件下反应生成E,则B中含有羧基和羟基,由此可知B的结构简式为。D在浓硫酸、170℃下反应生成乙烯,结合D的分子式,可知D是乙醇.C和乙醇在浓硫酸、加热条件下发生酯化反应生成F,结合F的分子式可知C的结构简式为CH3COOH,则A的结构简式为.
(4). 由①可知其结构中含有羟基和羧基,由②可知其苯环上无羟基,故其含有的取代基为-CH2COOH和-CH2OH、-COOH和-CHOHCH3、-COOH和-CH2CH2OH、-CH3和-CHOHCOOH,两个取代基在苯环上有三种位置关系,故符合条件的同分异构体(不包括B)共有11种.
19.答案:(1).碳碳双键、醛基; (2). ;加聚
(3).①
②
(4).5;
解析:(1).结合信息知, 生成是先醛、醛加成然后失水生成烯醛的反应,由于式量为58,所以为丙醛, 为2-甲基丙烯醛, 为2-甲基丙烯酸,根据的结构知, 为乙二醇,所以为乙烯, 为1,2-二溴乙烷。
由于为2-甲基丙烯醛,所以中含碳碳双键和醛基。
(2). 为丙醛, 生成是中双键发生加聚形成高分子。
(3). 生成为乙烯与溴单质加成的反应, 与生成为酯化反应。
(4). 为2-甲基丙烯酸,含双键含酯基的异构体中,甲酸酯3种,乙酸酯1种,丙烯酸酯1种,共5种,符合核磁共振氢谱要求的结构只有。
20.答案:(1).
(2).冷凝蒸气,防止倒吸; ;溶液分层,上层为无色油状液体,下层溶液颜色变浅
(3).乙醇; C
解析:(1).考查利用同位素示踪法表示酯化反应的机理.酯化反应中羧酸提供羟基,醇提供氢原子,据此可写出该反应的化学方程式。
(2).考查盐类的水解、酯化反应的可逆性及饱和Na2CO3溶液在制取乙酸乙酯时的作用.由于生成的乙酸乙酯中含有乙酸和乙醇,二者都与水互溶,所以球形干燥管C的作用除了起到冷凝蒸气的作用外,还起到防止倒吸的作用.碳酸钠水解,溶液显碱性,因此滴加酚酞溶液显红色。乙酸乙酯不溶于水,而乙酸能和碳酸钠反应,所以反应结束后D中的现象是溶液分层,上层为无色油状液体,下层溶液颜色变浅.
(3).根据题给信息“①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH",说明加入无水氯化钙可除去乙醇,之后加入的物质既要吸收水,又要与乙酸乙酯不反应,C项符合题意.
21.答案:(1).长颈漏斗; (2).平衡压强,使分液漏斗中的水容易滴下;(3).BEDECC; (4).将装置中残留的的水蒸气和CO2全部吹入吸收剂被吸收
(5).7:10:2:4; 偏高; 不正确; 收集的氮气中混有未参加反应的氧气
解析:(1).仪器a的名称为长颈漏斗
(2).导管g的作用为平衡压强,使分液漏斗中的水容易滴下
(3).选择上述装置,按气流从左到右的方向,合理的连接顺序为BEDECC(填大写字母,仪器可重复使用)→排水法收集气体装置
(4).①充分反应后,熄灭D处酒精灯之前,需继续通入O2至硬质玻璃管冷却,原因为将装置中残留的的水蒸气和CO2全部吹入吸收剂被吸收。
