5.1质量守恒定律课件(课件37页)
图片预览











文档简介
第五单元 化学方程式
课题1 质量守恒定律(课时1)
2020年秋人教版化学九年级上册精品课件
学习目标
1.理解质量守恒定律。
2.会用原子、分子的观点解释质量守恒的原因。
3.掌握质量守恒定律的应用。
返回
新课导入
为什么蜡烛在燃烧的过程中会逐渐变短?
新课导入
提出问题
物质在发生化学变化时,反应物的质量总和与生成物的质量总和之间存在什么关系呢?
新课导入
返回
(1)参加化学反应的各物质的质量之和大于生成的各物质的质量之和。
(2)参加化学反应的各物质的质量之和等于生成的各物质的质量之和。
(3)参加化学反应的各物质的质量之和小于生成的各物质的质量之和。
猜想和假设
一、质量守恒定律
新课讲解
1.白磷燃烧反应前后质量测定
【实验步骤】
(1)在锥形瓶中放一小块红磷,按图组装;
(2)称量锥形瓶内物质的总质量;
(3)点燃红磷,观察现象;
(4)冷却后称量锥形瓶内物质的总质量。
新课讲解
【实验现象】产生大量白烟,气球先膨胀后缩小,冷却后称量,天平仍然平衡。
磷+氧气 五氧化二磷
点燃
气球的作用:防止燃烧时产生的大量热导致装置中的气体膨胀,会使胶塞弹出,从而导致实验失败。
新课讲解
反应前物质(或物体)
反应后物质(或物体)
锥形瓶
锥形瓶
细砂
细砂
橡皮塞
橡皮塞
气球
气球
参加反应的红磷
五氧化二磷
参加反应的氧气
其它气体等
其它气体等
参加反应的红磷质量 + 参加反应的氧气质量 = 五氧化二磷质量
新课讲解
2.铁和硫酸铜溶液反应前后质量变化
铁+硫酸铜→铜 +硫酸亚铁
m1 = m2
【现象】铁钉表面变成红色,溶液颜色变浅。
称量烧杯中物质的总质量:
新课讲解
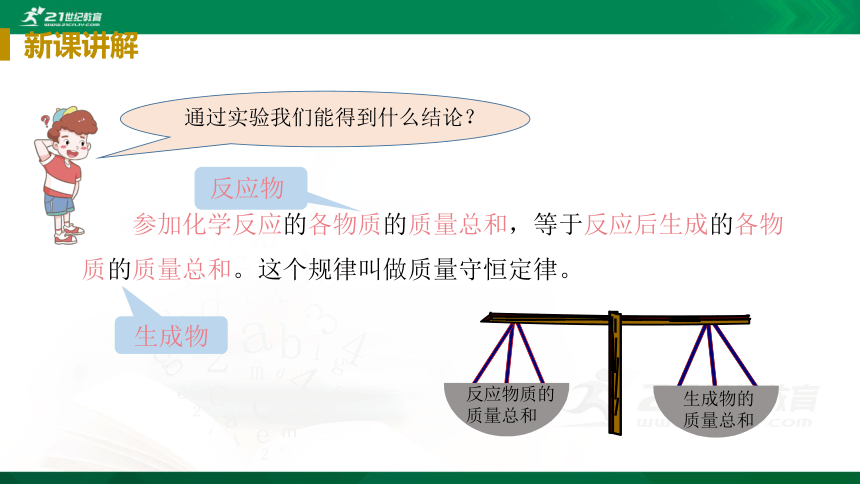
参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。这个规律叫做质量守恒定律。
生成物
反应物
反应物质的质量总和
生成物的质量总和
通过实验我们能得到什么结论?
新课讲解
3.盐酸和碳酸钠溶液反应前后质量的测定
【现象】产生大量气泡 ,最终砝码一端下降。
【结论】生成物的质量小于反应物的质量。
【文字表达式】
碳酸钠+盐酸→氯化钠+水+二氧化碳
原因:实验在敞口容器中进行,生成的气体逸散。
新课讲解
【现象】剧烈燃烧,发出耀眼白光,生成白色固体物质。
【结论】生成物的质量大于反应物的质量。
【文字表达式】
镁+氧气 → 氧化镁
4. 镁带燃烧前后质量的测定
点燃
原因:有气体参与或生成的反应,必须在密闭体系中进行。
新课讲解
(1)质量守恒定律是一切化学反应必须遵守的一个定律,但物理变化不属于此定律;
(2)质量守恒定律研究的仅是指“质量”,不能任意扩展到其他物理量;
(3)守恒的数量是“总质量”,不是部分反应物和生成物的质量。
新课讲解
典例分析
例1
将一定质量的a,b,c,d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得各物质的质量如表:下列有关说法正确的是( )
a和b是反应物 B. x=3.2
C. 该反应属于分解反应 D. d一定是催化剂
C
解析:求得x值为6.4,a,c反应后质量增加为生成物,b反应后质量减少为反应物,d质量不变,可能是催化剂。
新课讲解
二、质量守恒定律的微观解释
为什么化学反应前后的物质的质量总和相等?
怎样从分子、原子的观点解释质量守恒的原因?
思 考
新课讲解
分 子
通电
原 子
新分子
重新组合
O
H
H
O
H
H
通电
重新组合
O
O
H
H
H
H
H2O
2H2O 2H2+O2
原子的种类 ,
原子的数目 ,
原子的质量 。
不变
不变
不变
水的电解
新课讲解
原子数目
原子质量
原子种类
微观
元素质量
元素种类
不 变
物质的种类
分子的种类
改变
宏观
可能
改变
分子数目
物质的总质量
新课讲解
典例分析
例2
在化学变化中,下列说法正确的是( )
①原子的种类、元素的种类、分子的种类均不变
②原子的数目、分子的数目均不变
③原子的质量、元素的质量、物质的总质量均不变
④原子核的种类、数量、质量均不变
A.①② B.①③ C.③④ D.②④
C
解析:在化学变化中,分子的种类一定发生变化,分子的数目可能发生变化。
返回
课堂小结
返回
质量守恒定律
内容: 的各物质的 ,等于反应后生成的各物质的______________。
原因
宏观:反应前后 的种类、质量不变。
微观:反应前后 的种类、数目、质量不变。
应用
(1)根据反应前后物质总质量相等,确定反应中某物质的质量。
(2)根据反应前后元素的种类和质量不变,确定物质的元素组成。
(3)根据反应前后原子的种类和个数不变,确定物质的化学式。
(4)解决化学反应的微观图形题。
(5)解决图表数据分析题。
参加化学反应
质量总和
质量总和
原子
元素
D
当堂小练
1.下列说法正确的是( )
A.5g酒精溶解在55g水中形成60g溶液,这符合质量守恒定律
B.细铁丝在氧气中燃烧,生成物质量比细铁丝大,这个反应不遵守质量守恒定律
C.2L氢气和1L氧气点燃后,可生成3L水
D.完全电解10g水得到的氢气和氧气的质量之和仍是10g
D
D
当堂小练
2.生活中有时发生把亚硝酸钠误当食盐的中毒事件,确保食品安全的警钟再次敲响。亚硝酸钠(NaNO2)外观与食盐极相似,有咸味,区别它们的有效方法是隔绝空气加热,没有明显变化的是食盐,能分解放出刺激性气味气体的是亚硝酸钠,此气体可能是( )
A.S02 B.NH3 C.N2 D.N02
D
D
当堂小练
3.质量守恒定律是自然界最基本的规律之一。下列实验装置(天平省略)能用来验证质量守恒定律的是( )
A
D
当堂小练
返回
4.将20克甲、5克乙、8克丙三种纯净物混合,在密闭容器中加热发生化学反应,经分析可知:反应后混合物中含有5克甲、16克丙,还含有一种新物质丁。则丁物质的质量是( )
A.12 g B.9 g C.4 g D.17 g
A
第五单元 化学方程式
课题1 质量守恒定律(课时2)
2020年秋人教版化学九年级上册精品课件
学习目标
1能从具体的化学方程式中获取并说出有关反应信息,总结出化学方程式表示的意义,能说出化学方程式的读法。
2.培养思考、务实,勇于实践、不断创新的科学精神。
返回
新课导入
木炭在氧气中燃烧生成二氧化碳的反应可以用文字表示为:
碳 + 氧气 → 二氧化碳
点燃
反应物
生成物
“和”
“反应条件”
“生成”
写起来很麻烦,怎么办?
返回
一、化学方程式的意义
新课讲解
C
+
CO2
O2
点燃
12
:
16×2
:
12+16×2
12
:
32
:
44
量的含义1:每12份质量的碳跟32份
质量的氧气完全反应生成44份质量的
二氧化碳
质的含义:碳和氧气在
点燃条件下反应生成二
氧化碳
量的含义2:每一个碳原子和一个氧分子反应,生成一个二氧化碳分子
新课讲解
化学方程式:用化学式来表示化学反应的式子。
化学方程式的意义:
① 表示反应物、生成物
② 表示反应条件
③ 表示反应物和生成物间的质量比
④ 表示参加反应和生成的各微粒的数量关系
质的意义
量的意义
其他:a.该反应是什么反应;b.化学变化中分子可分,原子不可再分;c.化学变化中元素种类、原子种类、数量都不变。
新课讲解
在点燃的条件下,碳和氧气反应生成二氧化碳。
在点燃的条件下,每12份质量的碳和32份质量的氧气反应生成44份质量的二氧化碳。
C
+
CO2
O2
点燃
12 32 44
宏观上
质量上
微观上
在点燃的条件下,1个碳原子和1个氧原子反应生成1个二氧化碳分子。
二、化学方程式的读法
新课讲解
典例分析
例
判断下列说法:电灯通电发光发热是发生了什么变化?
关于化学方程式4P+5O2=2P2O5的理解,正确的是( )
A.反应前后分子总数保持不变
B.该反应的反应物是五氧化二磷
C.每四份质量的磷和五份质量的氧气完全反应
D.在点燃的条件下,磷和氧气反应生成五氧化二磷
解析:由化学方程式可知,该反应前后分子总数发生改变,反应物是磷和氧气,生成物是五氧化二磷;应为124份质量的磷与160份质量的氧气在点燃条件下生成284份质量的五氧化二磷。
D
返回
课堂小结
返回
化学方程式
2.意义: ①表示反应物、生成物和反应条件
②表示各物质之间的质量比
1.定义:用化学式来表示化学反应的式子
D
当堂小练
1.下图为某反应的微观示意图,其中不同的球代表不同元素的原子。下列说法错误的是( )
A.生成物可能都是氧化物
B.乙中元素的化合价在反应前后保持不变
C.生成物的分子个数比为1∶2
D.反应前后原子的种类和数目都不变
B
D
当堂小练
2.下列是初中化学中的一些重要实验,请回答:
(1)A中红磷必须足量的原因是
;?
(2)B中玻璃棒的作用是 ;?
(3)C中反应后天平不平衡,该反应是否遵守质量守恒定律? (填“是”或“否”)。?
为了耗尽装置内的氧气
引流
是
D
当堂小练
3.红磷在氧气中燃烧生成五氧化二磷,该反应中红磷、氧气、五氧化二磷的质量比为( )
A. 4∶5∶2 B. 31∶24∶47
C. 31∶32∶142 D. 124∶160∶284
B
谢 谢 观 看
谢谢
21世纪教育网(www.21cnjy.com) 中小学教育资源网站
有大把高质量资料?一线教师?一线教研员?
欢迎加入21世纪教育网教师合作团队!!月薪过万不是梦!!
详情请看:
https://www.21cnjy.com/help/help_extract.php
课题1 质量守恒定律(课时1)
2020年秋人教版化学九年级上册精品课件
学习目标
1.理解质量守恒定律。
2.会用原子、分子的观点解释质量守恒的原因。
3.掌握质量守恒定律的应用。
返回
新课导入
为什么蜡烛在燃烧的过程中会逐渐变短?
新课导入
提出问题
物质在发生化学变化时,反应物的质量总和与生成物的质量总和之间存在什么关系呢?
新课导入
返回
(1)参加化学反应的各物质的质量之和大于生成的各物质的质量之和。
(2)参加化学反应的各物质的质量之和等于生成的各物质的质量之和。
(3)参加化学反应的各物质的质量之和小于生成的各物质的质量之和。
猜想和假设
一、质量守恒定律
新课讲解
1.白磷燃烧反应前后质量测定
【实验步骤】
(1)在锥形瓶中放一小块红磷,按图组装;
(2)称量锥形瓶内物质的总质量;
(3)点燃红磷,观察现象;
(4)冷却后称量锥形瓶内物质的总质量。
新课讲解
【实验现象】产生大量白烟,气球先膨胀后缩小,冷却后称量,天平仍然平衡。
磷+氧气 五氧化二磷
点燃
气球的作用:防止燃烧时产生的大量热导致装置中的气体膨胀,会使胶塞弹出,从而导致实验失败。
新课讲解
反应前物质(或物体)
反应后物质(或物体)
锥形瓶
锥形瓶
细砂
细砂
橡皮塞
橡皮塞
气球
气球
参加反应的红磷
五氧化二磷
参加反应的氧气
其它气体等
其它气体等
参加反应的红磷质量 + 参加反应的氧气质量 = 五氧化二磷质量
新课讲解
2.铁和硫酸铜溶液反应前后质量变化
铁+硫酸铜→铜 +硫酸亚铁
m1 = m2
【现象】铁钉表面变成红色,溶液颜色变浅。
称量烧杯中物质的总质量:
新课讲解
参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。这个规律叫做质量守恒定律。
生成物
反应物
反应物质的质量总和
生成物的质量总和
通过实验我们能得到什么结论?
新课讲解
3.盐酸和碳酸钠溶液反应前后质量的测定
【现象】产生大量气泡 ,最终砝码一端下降。
【结论】生成物的质量小于反应物的质量。
【文字表达式】
碳酸钠+盐酸→氯化钠+水+二氧化碳
原因:实验在敞口容器中进行,生成的气体逸散。
新课讲解
【现象】剧烈燃烧,发出耀眼白光,生成白色固体物质。
【结论】生成物的质量大于反应物的质量。
【文字表达式】
镁+氧气 → 氧化镁
4. 镁带燃烧前后质量的测定
点燃
原因:有气体参与或生成的反应,必须在密闭体系中进行。
新课讲解
(1)质量守恒定律是一切化学反应必须遵守的一个定律,但物理变化不属于此定律;
(2)质量守恒定律研究的仅是指“质量”,不能任意扩展到其他物理量;
(3)守恒的数量是“总质量”,不是部分反应物和生成物的质量。
新课讲解
典例分析
例1
将一定质量的a,b,c,d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得各物质的质量如表:下列有关说法正确的是( )
a和b是反应物 B. x=3.2
C. 该反应属于分解反应 D. d一定是催化剂
C
解析:求得x值为6.4,a,c反应后质量增加为生成物,b反应后质量减少为反应物,d质量不变,可能是催化剂。
新课讲解
二、质量守恒定律的微观解释
为什么化学反应前后的物质的质量总和相等?
怎样从分子、原子的观点解释质量守恒的原因?
思 考
新课讲解
分 子
通电
原 子
新分子
重新组合
O
H
H
O
H
H
通电
重新组合
O
O
H
H
H
H
H2O
2H2O 2H2+O2
原子的种类 ,
原子的数目 ,
原子的质量 。
不变
不变
不变
水的电解
新课讲解
原子数目
原子质量
原子种类
微观
元素质量
元素种类
不 变
物质的种类
分子的种类
改变
宏观
可能
改变
分子数目
物质的总质量
新课讲解
典例分析
例2
在化学变化中,下列说法正确的是( )
①原子的种类、元素的种类、分子的种类均不变
②原子的数目、分子的数目均不变
③原子的质量、元素的质量、物质的总质量均不变
④原子核的种类、数量、质量均不变
A.①② B.①③ C.③④ D.②④
C
解析:在化学变化中,分子的种类一定发生变化,分子的数目可能发生变化。
返回
课堂小结
返回
质量守恒定律
内容: 的各物质的 ,等于反应后生成的各物质的______________。
原因
宏观:反应前后 的种类、质量不变。
微观:反应前后 的种类、数目、质量不变。
应用
(1)根据反应前后物质总质量相等,确定反应中某物质的质量。
(2)根据反应前后元素的种类和质量不变,确定物质的元素组成。
(3)根据反应前后原子的种类和个数不变,确定物质的化学式。
(4)解决化学反应的微观图形题。
(5)解决图表数据分析题。
参加化学反应
质量总和
质量总和
原子
元素
D
当堂小练
1.下列说法正确的是( )
A.5g酒精溶解在55g水中形成60g溶液,这符合质量守恒定律
B.细铁丝在氧气中燃烧,生成物质量比细铁丝大,这个反应不遵守质量守恒定律
C.2L氢气和1L氧气点燃后,可生成3L水
D.完全电解10g水得到的氢气和氧气的质量之和仍是10g
D
D
当堂小练
2.生活中有时发生把亚硝酸钠误当食盐的中毒事件,确保食品安全的警钟再次敲响。亚硝酸钠(NaNO2)外观与食盐极相似,有咸味,区别它们的有效方法是隔绝空气加热,没有明显变化的是食盐,能分解放出刺激性气味气体的是亚硝酸钠,此气体可能是( )
A.S02 B.NH3 C.N2 D.N02
D
D
当堂小练
3.质量守恒定律是自然界最基本的规律之一。下列实验装置(天平省略)能用来验证质量守恒定律的是( )
A
D
当堂小练
返回
4.将20克甲、5克乙、8克丙三种纯净物混合,在密闭容器中加热发生化学反应,经分析可知:反应后混合物中含有5克甲、16克丙,还含有一种新物质丁。则丁物质的质量是( )
A.12 g B.9 g C.4 g D.17 g
A
第五单元 化学方程式
课题1 质量守恒定律(课时2)
2020年秋人教版化学九年级上册精品课件
学习目标
1能从具体的化学方程式中获取并说出有关反应信息,总结出化学方程式表示的意义,能说出化学方程式的读法。
2.培养思考、务实,勇于实践、不断创新的科学精神。
返回
新课导入
木炭在氧气中燃烧生成二氧化碳的反应可以用文字表示为:
碳 + 氧气 → 二氧化碳
点燃
反应物
生成物
“和”
“反应条件”
“生成”
写起来很麻烦,怎么办?
返回
一、化学方程式的意义
新课讲解
C
+
CO2
O2
点燃
12
:
16×2
:
12+16×2
12
:
32
:
44
量的含义1:每12份质量的碳跟32份
质量的氧气完全反应生成44份质量的
二氧化碳
质的含义:碳和氧气在
点燃条件下反应生成二
氧化碳
量的含义2:每一个碳原子和一个氧分子反应,生成一个二氧化碳分子
新课讲解
化学方程式:用化学式来表示化学反应的式子。
化学方程式的意义:
① 表示反应物、生成物
② 表示反应条件
③ 表示反应物和生成物间的质量比
④ 表示参加反应和生成的各微粒的数量关系
质的意义
量的意义
其他:a.该反应是什么反应;b.化学变化中分子可分,原子不可再分;c.化学变化中元素种类、原子种类、数量都不变。
新课讲解
在点燃的条件下,碳和氧气反应生成二氧化碳。
在点燃的条件下,每12份质量的碳和32份质量的氧气反应生成44份质量的二氧化碳。
C
+
CO2
O2
点燃
12 32 44
宏观上
质量上
微观上
在点燃的条件下,1个碳原子和1个氧原子反应生成1个二氧化碳分子。
二、化学方程式的读法
新课讲解
典例分析
例
判断下列说法:电灯通电发光发热是发生了什么变化?
关于化学方程式4P+5O2=2P2O5的理解,正确的是( )
A.反应前后分子总数保持不变
B.该反应的反应物是五氧化二磷
C.每四份质量的磷和五份质量的氧气完全反应
D.在点燃的条件下,磷和氧气反应生成五氧化二磷
解析:由化学方程式可知,该反应前后分子总数发生改变,反应物是磷和氧气,生成物是五氧化二磷;应为124份质量的磷与160份质量的氧气在点燃条件下生成284份质量的五氧化二磷。
D
返回
课堂小结
返回
化学方程式
2.意义: ①表示反应物、生成物和反应条件
②表示各物质之间的质量比
1.定义:用化学式来表示化学反应的式子
D
当堂小练
1.下图为某反应的微观示意图,其中不同的球代表不同元素的原子。下列说法错误的是( )
A.生成物可能都是氧化物
B.乙中元素的化合价在反应前后保持不变
C.生成物的分子个数比为1∶2
D.反应前后原子的种类和数目都不变
B
D
当堂小练
2.下列是初中化学中的一些重要实验,请回答:
(1)A中红磷必须足量的原因是
;?
(2)B中玻璃棒的作用是 ;?
(3)C中反应后天平不平衡,该反应是否遵守质量守恒定律? (填“是”或“否”)。?
为了耗尽装置内的氧气
引流
是
D
当堂小练
3.红磷在氧气中燃烧生成五氧化二磷,该反应中红磷、氧气、五氧化二磷的质量比为( )
A. 4∶5∶2 B. 31∶24∶47
C. 31∶32∶142 D. 124∶160∶284
B
谢 谢 观 看
谢谢
21世纪教育网(www.21cnjy.com) 中小学教育资源网站
有大把高质量资料?一线教师?一线教研员?
欢迎加入21世纪教育网教师合作团队!!月薪过万不是梦!!
详情请看:
https://www.21cnjy.com/help/help_extract.php
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
