京改版九年级上册化学课件 7.1 质量守恒定律 课件 (共29张PPT)
文档属性
| 名称 | 京改版九年级上册化学课件 7.1 质量守恒定律 课件 (共29张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 434.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-08-23 00:00:00 | ||
图片预览







文档简介
1、磷燃烧的文字表达式.
2、镁带燃烧生成氧化镁的文字表达式。
3、铁和硫酸铜反应生成硫酸亚铁和铜的文字表达式。
4、盐酸和碳酸钠反应生成氯化钠、水和二氧化碳的文字表达式。
5、石蜡燃烧的文字表达式
6、水通电的文字表达式。
在生成新物质以后,物质的总质量,跟反应前相比,是否发生改变呢?请同学们大胆的猜想……
再次探究:
一、镁条燃烧
二、碳酸钠跟稀盐酸反应
讨论:
1、以上两个反应是否遵守质量守恒定律?
2、如何改进装置,才能把生成的气体也收集起来进行称量呢?
一天,福尔摩斯像往常一样滋滋有味地 抽着他的烟斗,房间里充满了刺鼻的烟味。华生问道:“敬爱的先生,别人都说你很聪明,那么你能告诉我你吐出的这些烟和气体有多重吗?”
福尔摩斯慢条斯理地说………………………………………。
4、判断下列说法是否正确:
(1)100克干冰升华变成100克二氧化碳气体符合质量守恒定律
(2)燃烧的镁带和生成的白色粉末质量相等。
(3)水在催化剂的作用下可变成燃油(主要含C、H元素)
(4)大麻是我国政府禁止的毒品,大麻在空气中燃烧能生成CO2和H2O,则大麻的组成中一定含 元素,可能含有 元素
质量守恒定律
磷+氧气 五氧化二磷
镁+氧气 氧化镁
铁+硫酸铜 硫酸亚铁+铜
盐酸+碳酸钠 氯化钠+水+二氧化碳
石蜡+氧气 水+二氧化碳
水 通电 氢气+氧气
点燃
点燃
反应物的质量总和 生成物的质量总和
等于
大于
小于
方案一、白磷燃烧前后质量变化
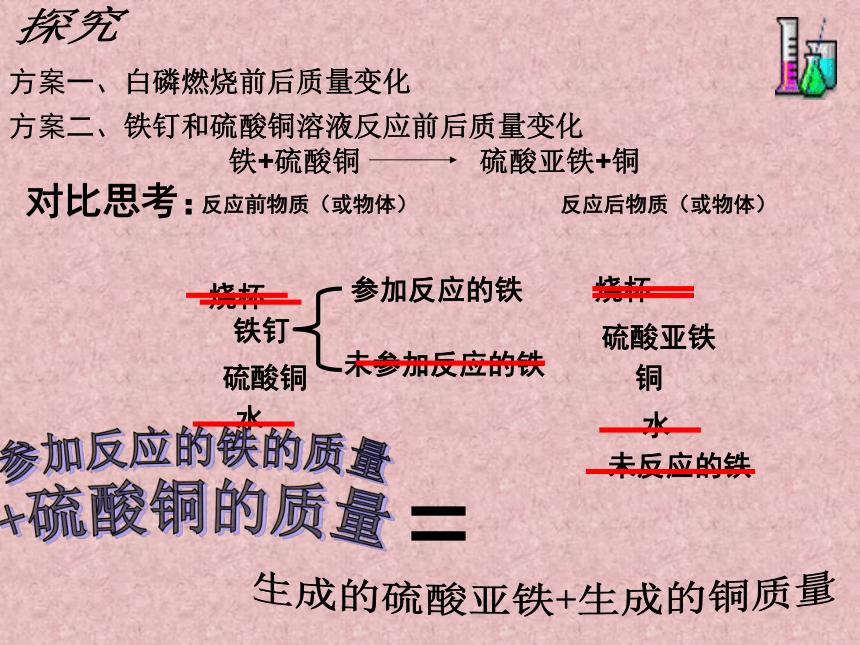
方案二、铁钉和硫酸铜溶液反应前后质量变化
对比思考:
反应前物质(或物体)
反应后物质(或物体)
烧杯
铁钉
硫酸铜
水
烧杯
铁+硫酸铜 硫酸亚铁+铜
硫酸亚铁
铜
水
未反应的铁
未参加反应的铁
参加反应的铁
=
参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。
问题:通过实验探究,同学们可以得出什么结论?
质量守恒定律
分析讨论:该定律内容有几处关键词?
1. 适用于 “一切化学反应”,不适用于物理变化。
2. 仅是指“质量”守恒,而不指其它物理量。
指反应或生成的“各种物质”,包括固体、 液体、气体都要考虑。
指“参加”反应的物质,未反应完的物质不计算在内。
温馨小提示
分析
结果
表达式
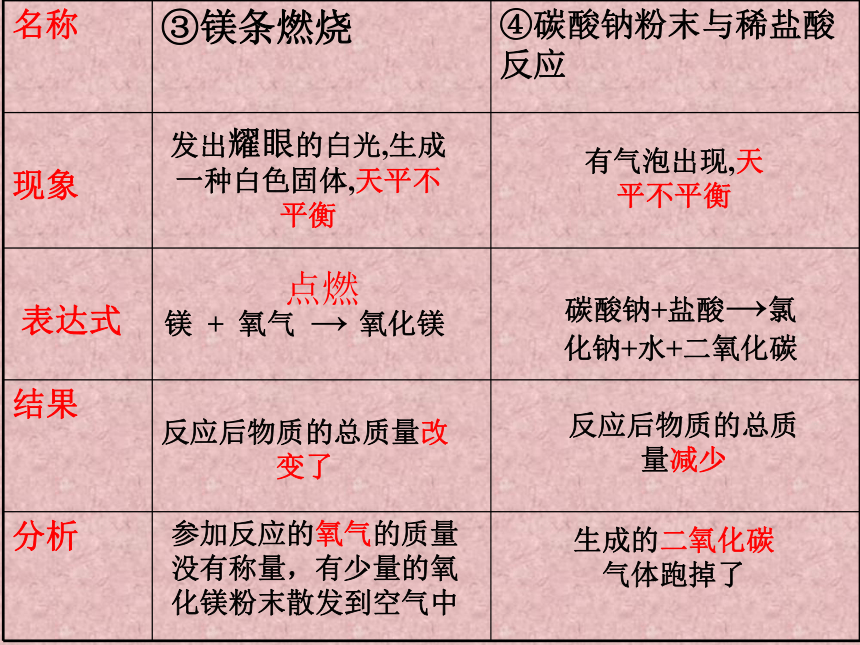
现象
④碳酸钠粉末与稀盐酸反应
③镁条燃烧
名称
发出耀眼的白光,生成一种白色固体,天平不平衡
有气泡出现,天平不平衡
镁 + 氧气 → 氧化镁
点燃
碳酸钠+盐酸→氯化钠+水+二氧化碳
反应后物质的总质量改变了
反应后物质的总质量减少
参加反应的氧气的质量没有称量,有少量的氧化镁粉末散发到空气中
生成的二氧化碳气体跑掉了
汇报交流、展示
改进后的装置
分 析
结 果
优化实验方案、再次探究
对有气体参与或有气体生成的反应,作定量研究时,需用密闭装置。
天平仍平衡,物质总质量不变
参加反应的镁和氧气的质量等于反应后生成的氧化镁的质量;
参加反应的碳酸钠和盐酸的质量等于反应后生成的氯化钠、水和二氧化碳的质量。
想一想
想一想
为什么化学反应前后的各物质的质量总和相等呢?
拆分
重新组合
电解水的微观过程
水 氢气 + 氧气
通电
分析讨论:
①化学反应前后,分子种类变了吗?
②化学反应前后,原子种类变了吗?
③化学反应过程的实质是什么?
H2O H2 + O2
通电
原子种类变了吗?
原子数目变了吗?
原子质量呢?
化学反应前后
元素种类呢?
元素的质量呢?
不变
不变
知识归纳:
反应前后元素种类不变。
原子种类没变。
原子个数没有增减。
原子质量没有变化。
(五不变)
质量守恒的原因:
反应前后元素质量不变。
微观:
宏观:
2.某大师说他能发功使铝(Al)发生化学变化变成黄金(Au)。他的说法是否有科学道理?
1.小明说蜡烛燃烧后质量变小,这一事实不符合质量守恒定律,你认为对吗?为什么?
不对。蜡烛燃烧后生成的CO2和H2O跑掉了,所以蜡烛燃烧后质量变小,仍符合质量守恒定律。
没有。化学反应前后,原子和元素种类不变。
形成性评价
福尔摩斯慢条斯理地说:“这个问题很简单,我只要称出抽烟前烟斗和烟丝的总重量,再减去抽完烟后烟斗和剩余烟灰的总重量,不就是我吐出烟和气体的重量了么!”
请分析福尔摩斯的做法正确吗?
小提示:烟丝和氧气反应
形成性评价
智能反馈:
1.在A+B=C+D反应中,4gA和5gB恰好完全反应
生成了3gC,则生成D的质量为________.
2. agKClO3和bgMnO2混合加热完全反应剩余
固体物质中含cgKCl,则生成O2的质量为________.
3. 在化学反应2XY2+Y2=2Z中Z的化学式为____.
A XY3 B XY2 C X3Y D X2Y
6 克
(a-c)克
则生成氧化镁
的质量为____克
24克镁与16克氧气恰好完全反应。
40
(2). 6克碳与一定量的氧气恰好完全反应,生成二氧化碳22克,有______克氧气参加了反应。
16
(1).
试试看:
1、用质量差确定某反应物或生成物的质量
二、反应前后元素种类、质量守恒
例题1:物质A在空气燃烧后生成CO2和H2O,则物质一定含有_________元素,可能含有_________元素。
A + O2 CO2 + H2O
点燃
∴ A中一定含C.H两种元素
C
H
O
O
C
H
A
O
可能含O元素
例题2:将2.3g无水酒精完全燃烧,则需消耗4.8g O2,生成4.4g CO2和2.7gH2O,根据上述事实,可以判断无水酒精中 ( )
A.只含有碳、氢、氧三种元素 B.只含碳氢、两种元素 C.2.3g酒精中含氧0.8g D.除去C、H、O外还含有其它元素
R + O2 CO2 + H2O
点燃
C
H
O
C
H
R
O
由此可知: R中一定含C.H元素
若R质量= C.H元素质量和
若R质量〉 C.H元素质量和
则R中不含氧元素
则R中一定含氧元素
R + O2 CO2 + H2O
点燃
2.3g
4.8g
2.7g
4.4g
C元素质量:
H元素质量:
C + H =
∴ R中一定含C H O三种元素
<R的质量(2.3g)
R中一定含C.H元素
CO2
~
C
44
12
4.4g
x
44
4.4g
12
x
=
x=1.2g
设C元素质量为x
H2O
~
2H
18
2
2.7g
y
18
2.7g
2
y
=
y=0.3g
设H元素质量为y
1.2g + 0.3g =
1.5g
O元素质量:
①
②
2.3g
-
1.5g
=
0.8g
总结:
所有的化学反应都遵守质量守恒定律,该定律具有普遍意义。因为有时考虑问题不全面或实验方案不完善,而导致表面上的不相等。
2、镁带燃烧生成氧化镁的文字表达式。
3、铁和硫酸铜反应生成硫酸亚铁和铜的文字表达式。
4、盐酸和碳酸钠反应生成氯化钠、水和二氧化碳的文字表达式。
5、石蜡燃烧的文字表达式
6、水通电的文字表达式。
在生成新物质以后,物质的总质量,跟反应前相比,是否发生改变呢?请同学们大胆的猜想……
再次探究:
一、镁条燃烧
二、碳酸钠跟稀盐酸反应
讨论:
1、以上两个反应是否遵守质量守恒定律?
2、如何改进装置,才能把生成的气体也收集起来进行称量呢?
一天,福尔摩斯像往常一样滋滋有味地 抽着他的烟斗,房间里充满了刺鼻的烟味。华生问道:“敬爱的先生,别人都说你很聪明,那么你能告诉我你吐出的这些烟和气体有多重吗?”
福尔摩斯慢条斯理地说………………………………………。
4、判断下列说法是否正确:
(1)100克干冰升华变成100克二氧化碳气体符合质量守恒定律
(2)燃烧的镁带和生成的白色粉末质量相等。
(3)水在催化剂的作用下可变成燃油(主要含C、H元素)
(4)大麻是我国政府禁止的毒品,大麻在空气中燃烧能生成CO2和H2O,则大麻的组成中一定含 元素,可能含有 元素
质量守恒定律
磷+氧气 五氧化二磷
镁+氧气 氧化镁
铁+硫酸铜 硫酸亚铁+铜
盐酸+碳酸钠 氯化钠+水+二氧化碳
石蜡+氧气 水+二氧化碳
水 通电 氢气+氧气
点燃
点燃
反应物的质量总和 生成物的质量总和
等于
大于
小于
方案一、白磷燃烧前后质量变化
方案二、铁钉和硫酸铜溶液反应前后质量变化
对比思考:
反应前物质(或物体)
反应后物质(或物体)
烧杯
铁钉
硫酸铜
水
烧杯
铁+硫酸铜 硫酸亚铁+铜
硫酸亚铁
铜
水
未反应的铁
未参加反应的铁
参加反应的铁
=
参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。
问题:通过实验探究,同学们可以得出什么结论?
质量守恒定律
分析讨论:该定律内容有几处关键词?
1. 适用于 “一切化学反应”,不适用于物理变化。
2. 仅是指“质量”守恒,而不指其它物理量。
指反应或生成的“各种物质”,包括固体、 液体、气体都要考虑。
指“参加”反应的物质,未反应完的物质不计算在内。
温馨小提示
分析
结果
表达式
现象
④碳酸钠粉末与稀盐酸反应
③镁条燃烧
名称
发出耀眼的白光,生成一种白色固体,天平不平衡
有气泡出现,天平不平衡
镁 + 氧气 → 氧化镁
点燃
碳酸钠+盐酸→氯化钠+水+二氧化碳
反应后物质的总质量改变了
反应后物质的总质量减少
参加反应的氧气的质量没有称量,有少量的氧化镁粉末散发到空气中
生成的二氧化碳气体跑掉了
汇报交流、展示
改进后的装置
分 析
结 果
优化实验方案、再次探究
对有气体参与或有气体生成的反应,作定量研究时,需用密闭装置。
天平仍平衡,物质总质量不变
参加反应的镁和氧气的质量等于反应后生成的氧化镁的质量;
参加反应的碳酸钠和盐酸的质量等于反应后生成的氯化钠、水和二氧化碳的质量。
想一想
想一想
为什么化学反应前后的各物质的质量总和相等呢?
拆分
重新组合
电解水的微观过程
水 氢气 + 氧气
通电
分析讨论:
①化学反应前后,分子种类变了吗?
②化学反应前后,原子种类变了吗?
③化学反应过程的实质是什么?
H2O H2 + O2
通电
原子种类变了吗?
原子数目变了吗?
原子质量呢?
化学反应前后
元素种类呢?
元素的质量呢?
不变
不变
知识归纳:
反应前后元素种类不变。
原子种类没变。
原子个数没有增减。
原子质量没有变化。
(五不变)
质量守恒的原因:
反应前后元素质量不变。
微观:
宏观:
2.某大师说他能发功使铝(Al)发生化学变化变成黄金(Au)。他的说法是否有科学道理?
1.小明说蜡烛燃烧后质量变小,这一事实不符合质量守恒定律,你认为对吗?为什么?
不对。蜡烛燃烧后生成的CO2和H2O跑掉了,所以蜡烛燃烧后质量变小,仍符合质量守恒定律。
没有。化学反应前后,原子和元素种类不变。
形成性评价
福尔摩斯慢条斯理地说:“这个问题很简单,我只要称出抽烟前烟斗和烟丝的总重量,再减去抽完烟后烟斗和剩余烟灰的总重量,不就是我吐出烟和气体的重量了么!”
请分析福尔摩斯的做法正确吗?
小提示:烟丝和氧气反应
形成性评价
智能反馈:
1.在A+B=C+D反应中,4gA和5gB恰好完全反应
生成了3gC,则生成D的质量为________.
2. agKClO3和bgMnO2混合加热完全反应剩余
固体物质中含cgKCl,则生成O2的质量为________.
3. 在化学反应2XY2+Y2=2Z中Z的化学式为____.
A XY3 B XY2 C X3Y D X2Y
6 克
(a-c)克
则生成氧化镁
的质量为____克
24克镁与16克氧气恰好完全反应。
40
(2). 6克碳与一定量的氧气恰好完全反应,生成二氧化碳22克,有______克氧气参加了反应。
16
(1).
试试看:
1、用质量差确定某反应物或生成物的质量
二、反应前后元素种类、质量守恒
例题1:物质A在空气燃烧后生成CO2和H2O,则物质一定含有_________元素,可能含有_________元素。
A + O2 CO2 + H2O
点燃
∴ A中一定含C.H两种元素
C
H
O
O
C
H
A
O
可能含O元素
例题2:将2.3g无水酒精完全燃烧,则需消耗4.8g O2,生成4.4g CO2和2.7gH2O,根据上述事实,可以判断无水酒精中 ( )
A.只含有碳、氢、氧三种元素 B.只含碳氢、两种元素 C.2.3g酒精中含氧0.8g D.除去C、H、O外还含有其它元素
R + O2 CO2 + H2O
点燃
C
H
O
C
H
R
O
由此可知: R中一定含C.H元素
若R质量= C.H元素质量和
若R质量〉 C.H元素质量和
则R中不含氧元素
则R中一定含氧元素
R + O2 CO2 + H2O
点燃
2.3g
4.8g
2.7g
4.4g
C元素质量:
H元素质量:
C + H =
∴ R中一定含C H O三种元素
<R的质量(2.3g)
R中一定含C.H元素
CO2
~
C
44
12
4.4g
x
44
4.4g
12
x
=
x=1.2g
设C元素质量为x
H2O
~
2H
18
2
2.7g
y
18
2.7g
2
y
=
y=0.3g
设H元素质量为y
1.2g + 0.3g =
1.5g
O元素质量:
①
②
2.3g
-
1.5g
=
0.8g
总结:
所有的化学反应都遵守质量守恒定律,该定律具有普遍意义。因为有时考虑问题不全面或实验方案不完善,而导致表面上的不相等。
同课章节目录
- 第1章 走进化学
- 第一节 化学让世界更美好
- 第二节 实验是化学的基础
- 第2章 空气之谜
- 第一节 空气
- 第二节 氧气的制法
- 第三节 氧气的性质
- 第3章 构成物质的微粒
- 第一节 原子
- 第二节 原子核外电子的排布 离子
- 第三节 分子
- 第4章 最常见的液体——水
- 第一节 水的净化
- 第二节 水的变化
- 第三节 水资源的开发、利用和保护
- 第5章 化学元素与物质组成的表示
- 第一节 初步认识化学元素
- 第二节 物质组成的表示——化学式
- 第三节 化合价
- 第6章 燃烧的学问
- 第一节 探索燃烧与灭火
- 第二节 化学反应中的能量变化
- 第三节 化石燃料
- 第7章 化学反应的定量研究
- 第一节 质量守恒定律
- 第二节 化学方程式
- 第三节 依据化学方程式的简单计算
- 第8章 碳的世界
- 第一节 碳的单质
- 第二节 二氧化碳的性质和用途
- 第三节 二氧化碳的实验室制法
