人教版(五四制)八年级全册化学 5.1 质量守恒定律 课件(33张PPT)
文档属性
| 名称 | 人教版(五四制)八年级全册化学 5.1 质量守恒定律 课件(33张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-08-23 00:00:00 | ||
图片预览











文档简介
什么是化学变化?
化学变化最主要的特征是有新物质生成,即物质种类一定发生变化,分子种类也发生变化。
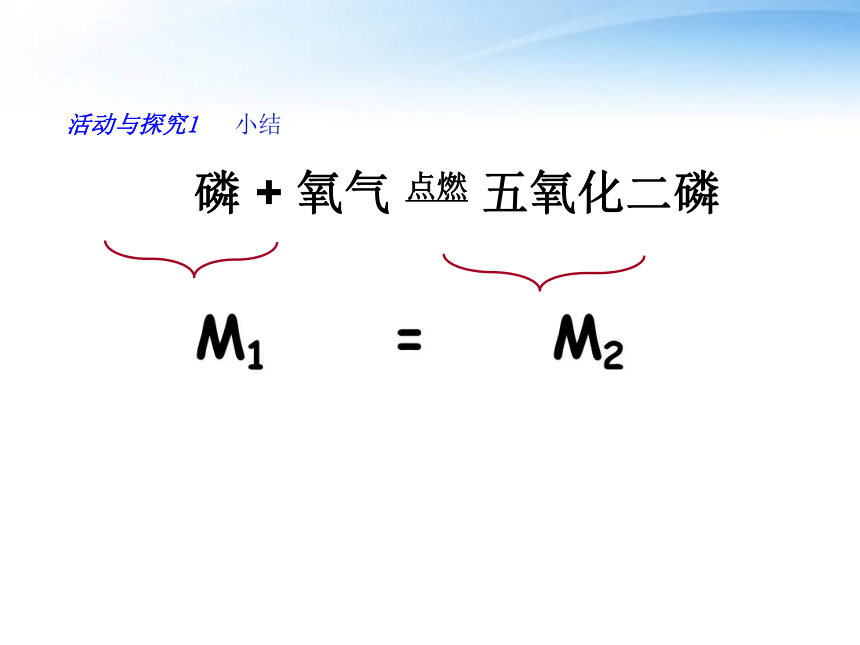
活动与探究1 小结
磷 + 氧气 点燃 五氧化二磷
注意事项
(1)质量守恒定律的适用范围是 变化,不包括 变化
(2)质量守恒定律强调的是 守恒,而不适合 守恒
(3)“参加”是“实际参加化学反应”的反应物的质量,反应物中 部分的质量不能计算在内
(4)“质量总和”是把各种 的反应物和生成物都算在内
讨论
这是 由于生成的二氧化碳气体逸散到空气中,造成左边质量减少,天平的指针偏右
如何证明稀盐酸和碳酸钠应前后物质的总质量相等呢?
实验2铜加热实验
实验过程
1调节天平使其平衡
2取一根用砂纸打磨干净的长铜丝和一个石棉网,将它们放到托盘天平上称量,记录所称的质量为m1
3在酒精灯上将铜丝全部变黑后,将铜丝放在托盘天平的石棉网上称量,记录所称质量为m2
生日宴会中我们发现生日蜡烛会越烧越短。
金属生锈后质量变大了。
1、结合生活中遇到的现象,提出问题: 化学反应前后物质的质量有没有变化呢?
2、你的猜想是 (变大、变小、或不变);
一、质量守恒定律
实验探究活动的一般步骤
提出假设
实验分析
得出结论
设计方案
进行实验
A大组按照课本92面完成磷燃烧前后质量的测定
B大组按照课本93面完成铁钉与硫酸铜溶液反应前后质量的测定
????????????????????????????????????????????????????????????????
探究实验1和2
1、锥形瓶底部为何要铺细沙?
2、玻璃管有何作用?
3、气球有何变化?为何有此现象?
4、能否将玻璃管换成玻璃棒,一端不系气球?
细砂
玻璃管
气球
白磷
(防止集气瓶底炸裂)
(引燃白磷)
(气球鼓起后瘪掉。气体热胀冷缩)
(不能,由于气压过大,瓶塞易被冲出)
1、锥形瓶底部为何要铺细沙?
2、玻璃管有何作用?
3、气球有何变化?为何有此现象?
4、能否将玻璃管换成玻璃棒,一端不系气球?
(1)实验原理:铁 + 硫酸铜 → 铜 + 硫酸亚铁
(2)实验目的:铁与硫酸铜反应前后的质量变化;
(3)实验的步骤:
①首先 ;
②然后,不动砝码和游码,取下烧杯,将铁丝的一端
放入到硫酸铜溶液中,过一会取出,观察现象;
③反应后 ;
④实验完毕,整理实验仪器 (砝码回盒,游码回零)
称量烧杯、硫酸铜、铁丝的质量
再次放到天平上称量,看天平是否平衡
【方案二】
活动与探究1 :
结论
反应前后天平是否平衡
实验现象
白磷在空气中燃烧
实验名称
化学反应前后的各物质质量总和,等于反应后生成的各物质质量总和
白磷燃烧产生大量白烟,放出热量气球先鼓后瘪
天平平衡
M1 = M2
活动与探究2 :铁钉与硫酸铜溶液反应
结论
反应前后天平是否平衡
实验现象
铁和硫酸铜溶液
实验名称
化学反应前后的各物质质量总和,等于反应后生成的各物质质量总和
天平平衡
铁钉表面有一层红色物质,溶液由蓝色变成浅绿色
活动与探究2 小结
硫酸铜 + 铁 → 硫酸亚铁 + 铜
??????????????????????????????????????????????????????????????
M1 = M2
一、质量守恒定律见书P94面
参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。这个规律叫做质量守恒定律。
为什么物质在发生化学变化前后,各物质的质量总和相等呢?
通电
4个
2个
6个
4个
2个
6个
原子重组
H2O H2+O2
通电
三不变
分子种类变化
原子种类不变
原子数目不变
原子质量不变
二变
物质种类变化
二、质量守恒的原因:
元 素
不 变。
(宏 观)
原 子
种 类
数 目
质 量
不 变;
(微 观)
种类
质量
物质总质量
3、在A+B→C+D的反应中,5克A和
一定的B恰好完全反应,生成3克C
和10克D,则B的质量是( )
(A)18克 (B)7克 (C)8克 (D)6克
C
1、现有一反应A+B→C+D,有10gA和5gB反应,反应结束后还剩余3gA,B无剩余,生成4g的C,则生成D的质量为 。
2、根据质量守恒定律,2L氢气和1L氧气反应能生成3L水,这句话对吗?
8g
不对
在实验5-1中,稀盐酸和碳酸钠反应前后物质的总质量为什么不相等呢?
在开放容器中:
盐酸 + 碳酸钠 → 氯化钠 + 水 +二氧化碳
????????????????????????????????????????????????????????????????
M1 > M2
实验5-1:
实验5-1小结
盐酸 + 碳酸钠 → 氯化钠 + 水 +二氧化碳
M1 = M2
在密闭容器中
资料链接:质量守恒定律的发现
波义耳的实验(1673年)
拉瓦锡的实验(1777年)
失败
成功
实验5-2:镁条燃烧前后质量的测定
实验5-2:
结论
反应前后天平是否平衡
实验现象
镁在空气中燃烧
实验名称
反应前的质量小于反应后的质量
天平不平衡
发出耀眼的白光,生成白色的固体
实验5-2 小结
在开放容器中:
镁 + 氧气 → 氧化镁
????????????????????????????????????????????????????????????????
M1 < M2
点燃
思考:
为什么蜡烛燃烧后质量减轻了?
这个反应符合质量守恒定律吗?
遵守质量守恒定律,石蜡燃烧生成的二氧化碳和水跑到空气中去了,所以质量减少,但石蜡和氧气的总质量等于二氧化碳和水的总质量。
碱石灰
想一想:如图所示,用碱石灰把二氧化碳和水都收集起来,你认为天平会平衡吗?
石蜡+氧气 二氧化碳+水
点燃
凡是有气体参加或有气体生成的化学反应,可以在密闭容器中进行,防止反应系统内物质与环境物质之间的物质交换,否则反应后剩余物质质量会增大或减小。
但这并不是违反质量守恒定律,反而是体现了质量守恒定律
化学变化最主要的特征是有新物质生成,即物质种类一定发生变化,分子种类也发生变化。
活动与探究1 小结
磷 + 氧气 点燃 五氧化二磷
注意事项
(1)质量守恒定律的适用范围是 变化,不包括 变化
(2)质量守恒定律强调的是 守恒,而不适合 守恒
(3)“参加”是“实际参加化学反应”的反应物的质量,反应物中 部分的质量不能计算在内
(4)“质量总和”是把各种 的反应物和生成物都算在内
讨论
这是 由于生成的二氧化碳气体逸散到空气中,造成左边质量减少,天平的指针偏右
如何证明稀盐酸和碳酸钠应前后物质的总质量相等呢?
实验2铜加热实验
实验过程
1调节天平使其平衡
2取一根用砂纸打磨干净的长铜丝和一个石棉网,将它们放到托盘天平上称量,记录所称的质量为m1
3在酒精灯上将铜丝全部变黑后,将铜丝放在托盘天平的石棉网上称量,记录所称质量为m2
生日宴会中我们发现生日蜡烛会越烧越短。
金属生锈后质量变大了。
1、结合生活中遇到的现象,提出问题: 化学反应前后物质的质量有没有变化呢?
2、你的猜想是 (变大、变小、或不变);
一、质量守恒定律
实验探究活动的一般步骤
提出假设
实验分析
得出结论
设计方案
进行实验
A大组按照课本92面完成磷燃烧前后质量的测定
B大组按照课本93面完成铁钉与硫酸铜溶液反应前后质量的测定
????????????????????????????????????????????????????????????????
探究实验1和2
1、锥形瓶底部为何要铺细沙?
2、玻璃管有何作用?
3、气球有何变化?为何有此现象?
4、能否将玻璃管换成玻璃棒,一端不系气球?
细砂
玻璃管
气球
白磷
(防止集气瓶底炸裂)
(引燃白磷)
(气球鼓起后瘪掉。气体热胀冷缩)
(不能,由于气压过大,瓶塞易被冲出)
1、锥形瓶底部为何要铺细沙?
2、玻璃管有何作用?
3、气球有何变化?为何有此现象?
4、能否将玻璃管换成玻璃棒,一端不系气球?
(1)实验原理:铁 + 硫酸铜 → 铜 + 硫酸亚铁
(2)实验目的:铁与硫酸铜反应前后的质量变化;
(3)实验的步骤:
①首先 ;
②然后,不动砝码和游码,取下烧杯,将铁丝的一端
放入到硫酸铜溶液中,过一会取出,观察现象;
③反应后 ;
④实验完毕,整理实验仪器 (砝码回盒,游码回零)
称量烧杯、硫酸铜、铁丝的质量
再次放到天平上称量,看天平是否平衡
【方案二】
活动与探究1 :
结论
反应前后天平是否平衡
实验现象
白磷在空气中燃烧
实验名称
化学反应前后的各物质质量总和,等于反应后生成的各物质质量总和
白磷燃烧产生大量白烟,放出热量气球先鼓后瘪
天平平衡
M1 = M2
活动与探究2 :铁钉与硫酸铜溶液反应
结论
反应前后天平是否平衡
实验现象
铁和硫酸铜溶液
实验名称
化学反应前后的各物质质量总和,等于反应后生成的各物质质量总和
天平平衡
铁钉表面有一层红色物质,溶液由蓝色变成浅绿色
活动与探究2 小结
硫酸铜 + 铁 → 硫酸亚铁 + 铜
??????????????????????????????????????????????????????????????
M1 = M2
一、质量守恒定律见书P94面
参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。这个规律叫做质量守恒定律。
为什么物质在发生化学变化前后,各物质的质量总和相等呢?
通电
4个
2个
6个
4个
2个
6个
原子重组
H2O H2+O2
通电
三不变
分子种类变化
原子种类不变
原子数目不变
原子质量不变
二变
物质种类变化
二、质量守恒的原因:
元 素
不 变。
(宏 观)
原 子
种 类
数 目
质 量
不 变;
(微 观)
种类
质量
物质总质量
3、在A+B→C+D的反应中,5克A和
一定的B恰好完全反应,生成3克C
和10克D,则B的质量是( )
(A)18克 (B)7克 (C)8克 (D)6克
C
1、现有一反应A+B→C+D,有10gA和5gB反应,反应结束后还剩余3gA,B无剩余,生成4g的C,则生成D的质量为 。
2、根据质量守恒定律,2L氢气和1L氧气反应能生成3L水,这句话对吗?
8g
不对
在实验5-1中,稀盐酸和碳酸钠反应前后物质的总质量为什么不相等呢?
在开放容器中:
盐酸 + 碳酸钠 → 氯化钠 + 水 +二氧化碳
????????????????????????????????????????????????????????????????
M1 > M2
实验5-1:
实验5-1小结
盐酸 + 碳酸钠 → 氯化钠 + 水 +二氧化碳
M1 = M2
在密闭容器中
资料链接:质量守恒定律的发现
波义耳的实验(1673年)
拉瓦锡的实验(1777年)
失败
成功
实验5-2:镁条燃烧前后质量的测定
实验5-2:
结论
反应前后天平是否平衡
实验现象
镁在空气中燃烧
实验名称
反应前的质量小于反应后的质量
天平不平衡
发出耀眼的白光,生成白色的固体
实验5-2 小结
在开放容器中:
镁 + 氧气 → 氧化镁
????????????????????????????????????????????????????????????????
M1 < M2
点燃
思考:
为什么蜡烛燃烧后质量减轻了?
这个反应符合质量守恒定律吗?
遵守质量守恒定律,石蜡燃烧生成的二氧化碳和水跑到空气中去了,所以质量减少,但石蜡和氧气的总质量等于二氧化碳和水的总质量。
碱石灰
想一想:如图所示,用碱石灰把二氧化碳和水都收集起来,你认为天平会平衡吗?
石蜡+氧气 二氧化碳+水
点燃
凡是有气体参加或有气体生成的化学反应,可以在密闭容器中进行,防止反应系统内物质与环境物质之间的物质交换,否则反应后剩余物质质量会增大或减小。
但这并不是违反质量守恒定律,反而是体现了质量守恒定律
同课章节目录
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的构成
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题1 质量守恒定律
- 课题2 如何正确书写化学方程式
- 课题3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动3 燃烧的条件
- 旧版目录
- 第五单元 物质组成的表示
- 课题2 燃料和热量
- 课题3 使用燃料对环境的影响
