人教版高中选修4化学4-2:化学电源(21张PPT)
文档属性
| 名称 | 人教版高中选修4化学4-2:化学电源(21张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-08-26 00:00:00 | ||
图片预览





文档简介
(共21张PPT)
第四章
电化学基础
第二节
化学电源
P74
学与问
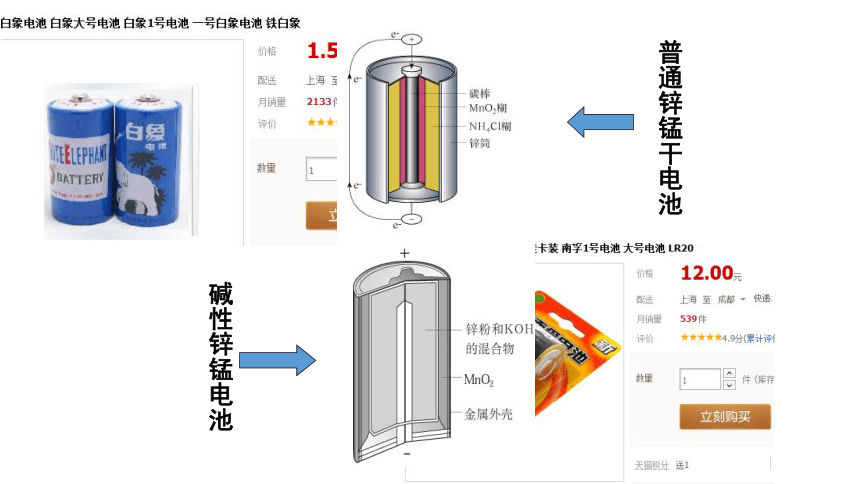
一.一次电池
普通锌锰干电池
碱性锌锰电池
2NH4+
+2e-
+
2MnO2
=
2NH3+2MnO(OH)
Zn+2NH4+
+2MnO2=
Zn2++2NH3+
2MnO(OH)
总反应式:
特点:
a:一次性电池,不可逆
b:NH4Cl显酸性,会腐蚀锌筒,用KOH代替NH4Cl能提高性能,延长寿命
Zn
—
2e
-
==
Zn2+
负极(Zn筒):
正极(石墨):
普通锌锰干电池
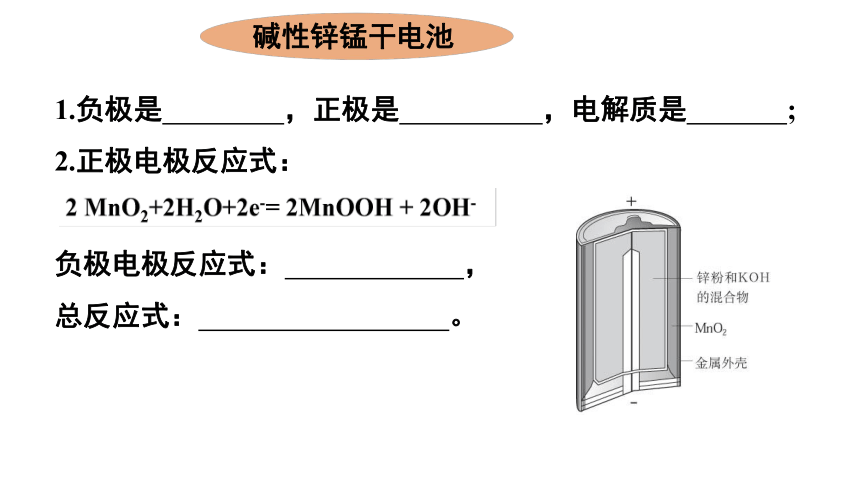
1.负极是
,正极是
,电解质是
;
2.正极电极反应式:
负极电极反应式:
,
总反应式:
。
碱性锌锰干电池
电子表和电子计算器中所用的是纽扣式微型银锌电池,其电极分别为O和Zn,电解质为KOH溶液,工作时电池总反应为O+Zn+O═2Ag+。
①工作时电流从极流向极(填“O”或“Zn”)。
②电极反应式:
正极:,
负极:.
③工作时电池正极区的pH(填“增大”“减小”或“不变”)。
银锌电池
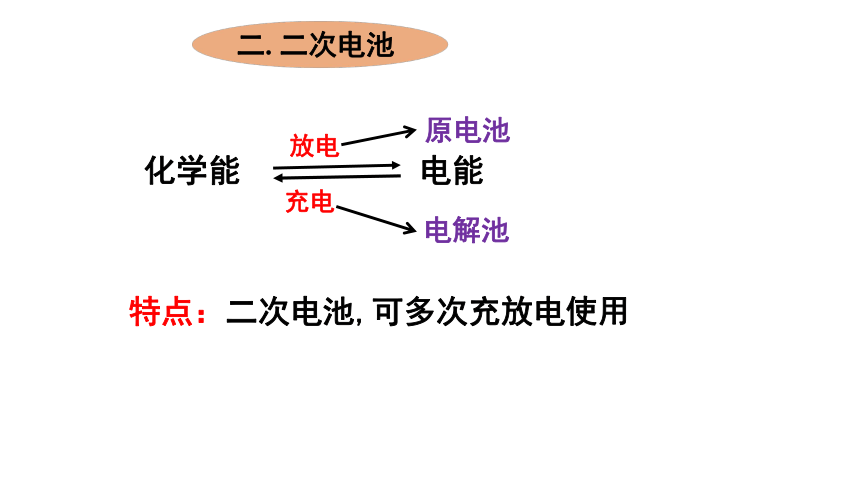
化学能
电能
放电
充电
原电池
电解池
特点:二次电池,可多次充放电使用
二.
二次电池
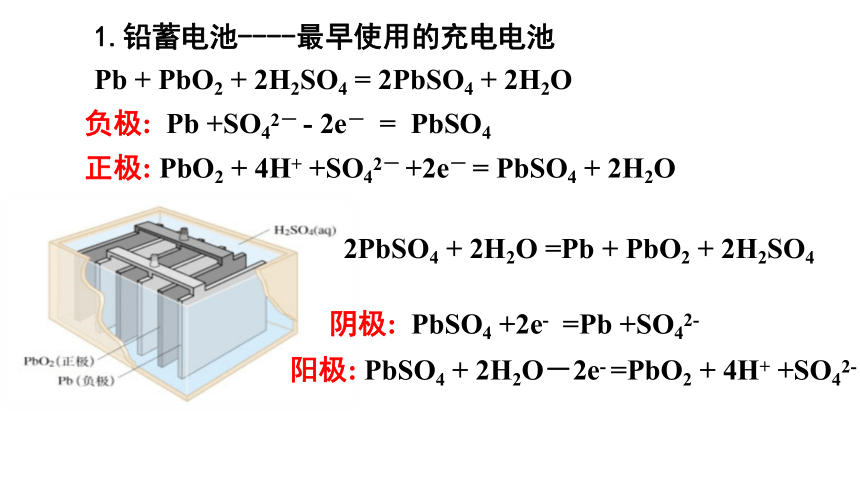
1.铅蓄电池----最早使用的充电电池
负极:
Pb
+SO42-
-
2e-
=
PbSO4
Pb
+
PbO2
+
2H2SO4
=
2PbSO4
+
2H2O
正极:
PbO2
+
4H+
+SO42-
+2e-
=
PbSO4
+
2H2O
2PbSO4
+
2H2O
=Pb
+
PbO2
+
2H2SO4
阴极:
PbSO4
+2e-
=Pb
+SO42-
阳极:
PbSO4
+
2H2O-2e-
=PbO2
+
4H+
+SO42-
例2:铅蓄电池是可充电型电池,电池总反应为:?
Pb+PbO2+2H2SO4
2PbSO4+2H2O
?下列说法正确的是
A.Pb为正极被氧化
B.充电Pb电极被氧化
C.该蓄电池放电工作时SO42-只向负极移动
D.铅蓄电池为电解电源,当蓄电池中有0.4mol
H+被消耗时,电路中通过的电子的物质的量为0.4mol
2.镍-镉碱性蓄电池
已知总反应为:Cd+2NiO(OH)+2H2O==Cd(OH)2+2Ni(OH)2
负极:Cd+2OH-—2e-=Cd(OH)2
正极:2NiO(OH)+2H2O=2Ni(OH)2+2
OH-
特点:体积小,便于携带
使用寿命长
Cd为致癌物质,对环境有污染
3.新一代可充电的绿色电池——锂离子电池
特点:质量轻,高能电池,贮存时间长等。
用途:电脑、电话、数码照相机等。
Li的金属性强,不能直接与电解质水溶液接触
Li1-xMn2O4+xLi
LiMn2O4
LixC6+Li1-xCoO2
C6+LiCoO2。
常见的锂离子电极材料
正极材料:LiMO2(M:Co、Ni、Mn等)
LiM2O4(M:Co、Ni、Mn等)
LiMPO4(M:Fe等)
负极材料:石墨(能吸附锂原子)
负极反应:LixCn-xe-===xLi++nC
正极反应:Li1-xMO2+xLi++xe-===LiMO2
锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+
通过电解质迁移入MnO2晶格中,生成LiMnO2。回答下列问题:
(1)外电路的电流方向是由________极流向________极。(填字母)
(2)电池正极反应式为_____________________。
(3)是否可用水代替电池中的混合有机溶剂?______(填“是”或“否”),原因是______________________
课堂练习
特点:(1)环境友好;
(2
)高效(理论利用率达85-90%,实际40-60%)
(3)燃料和氧化剂由外设备提供
2H2
+
O2
==
2H2O
点燃
三.燃料电池
2H2
+4OH-
-
4e-=4H2O
O2+2H2O+
4e-=
4OH-
2H2
+
O2
=
2H2O
(1)当电解质溶液为KOH溶液时
负极:
正极:
放电总反应式:
负极:
正极:
放电总反应式:
(2)当电解质溶液为稀H2SO4
2H2
-
4e-=4H+
O2+
4H+
+
4e-=
2H2O
2H2
+
O2
=
2H2O
【变式1】若该电池以固体氧化锆-氧化钇为电解质,已知这种固体电解质在高温下允许氧离子(O2-)在其间通过,各电极反应又如何?
负极:
.
正极:
.
总反应:
.
2H2
-
4e-+2O2-=2H2O
O2+
4e-=
2O2-
2H2
+
O2
=
2H2O
【变式2】若以甲烷为燃料电池电解质为熔融态的K2CO3,工作温度为600~800℃,正极辅助通入CO2。写出该燃料电池中各电极反应及总反应。
负极:
。
正极:
。
总反应
:
。
引入CO2的作用:
。
CH4
-8e-+4
CO32
-
=5CO2+2H2O
2O2+8e-+4CO2==
4
CO32
-
CH4+
2O2
=2H2O+
CO2
维持溶液中离子浓度不变
【变式3】写出甲烷燃料电池(CH4O-O2-KOH溶液)的电极反应式
负极
正极
总反应式
CH4
+10OH-
-8e-==CO32-+7H2O
CH4
+
2O2
+2OH-
=3H2O+
CO32-
2O2+8e-+4H2O==
8OH-
【变式4】若上述燃料电池以甲烷为燃料,在H2SO4溶液中发生反应构成原电池,试写出各极电极反应。
负极:
,
正极:
,
总反应:
。
CH4
+2H2O-8e-=CO2+8H+
CH4
+
2O2
=2H2O+
CO2
2O2+8e-+8H+=
4H2O
CO-O2熔融盐燃料电池的装置如图所示,电池工作时,C口产生的气体一部分通入B口被利用,另一部分被分离出来。若导线中流过2
mo1
e-,理论上C口被分离出的气体的物质的量最多为
。
课堂练习
电池的一个电极由有机光敏染料(s)涂覆在TiO2纳米晶体表面制成,另一电极南导电玻璃镀铂构成,电池中发生的反应为:
TiO2/S
???????
TiO2/S
(激发态)
TiO2/S
→TiO2/S++e-
I3-+2e-
→3I-
TiO2/S++3I
-
→2TiO2/S+I3-
下列关于该电池叙述错误的是
A电池工作时,I-离子在镀铂导电玻璃电极上放电
B电池工作时,是将太阳能转化为电能
C电池的电解质溶液中I-和I3-的浓度不会减少
D电池中镀铂导电玻璃为正极
四.太阳能电池
第四章
电化学基础
第二节
化学电源
P74
学与问
一.一次电池
普通锌锰干电池
碱性锌锰电池
2NH4+
+2e-
+
2MnO2
=
2NH3+2MnO(OH)
Zn+2NH4+
+2MnO2=
Zn2++2NH3+
2MnO(OH)
总反应式:
特点:
a:一次性电池,不可逆
b:NH4Cl显酸性,会腐蚀锌筒,用KOH代替NH4Cl能提高性能,延长寿命
Zn
—
2e
-
==
Zn2+
负极(Zn筒):
正极(石墨):
普通锌锰干电池
1.负极是
,正极是
,电解质是
;
2.正极电极反应式:
负极电极反应式:
,
总反应式:
。
碱性锌锰干电池
电子表和电子计算器中所用的是纽扣式微型银锌电池,其电极分别为O和Zn,电解质为KOH溶液,工作时电池总反应为O+Zn+O═2Ag+。
①工作时电流从极流向极(填“O”或“Zn”)。
②电极反应式:
正极:,
负极:.
③工作时电池正极区的pH(填“增大”“减小”或“不变”)。
银锌电池
化学能
电能
放电
充电
原电池
电解池
特点:二次电池,可多次充放电使用
二.
二次电池
1.铅蓄电池----最早使用的充电电池
负极:
Pb
+SO42-
-
2e-
=
PbSO4
Pb
+
PbO2
+
2H2SO4
=
2PbSO4
+
2H2O
正极:
PbO2
+
4H+
+SO42-
+2e-
=
PbSO4
+
2H2O
2PbSO4
+
2H2O
=Pb
+
PbO2
+
2H2SO4
阴极:
PbSO4
+2e-
=Pb
+SO42-
阳极:
PbSO4
+
2H2O-2e-
=PbO2
+
4H+
+SO42-
例2:铅蓄电池是可充电型电池,电池总反应为:?
Pb+PbO2+2H2SO4
2PbSO4+2H2O
?下列说法正确的是
A.Pb为正极被氧化
B.充电Pb电极被氧化
C.该蓄电池放电工作时SO42-只向负极移动
D.铅蓄电池为电解电源,当蓄电池中有0.4mol
H+被消耗时,电路中通过的电子的物质的量为0.4mol
2.镍-镉碱性蓄电池
已知总反应为:Cd+2NiO(OH)+2H2O==Cd(OH)2+2Ni(OH)2
负极:Cd+2OH-—2e-=Cd(OH)2
正极:2NiO(OH)+2H2O=2Ni(OH)2+2
OH-
特点:体积小,便于携带
使用寿命长
Cd为致癌物质,对环境有污染
3.新一代可充电的绿色电池——锂离子电池
特点:质量轻,高能电池,贮存时间长等。
用途:电脑、电话、数码照相机等。
Li的金属性强,不能直接与电解质水溶液接触
Li1-xMn2O4+xLi
LiMn2O4
LixC6+Li1-xCoO2
C6+LiCoO2。
常见的锂离子电极材料
正极材料:LiMO2(M:Co、Ni、Mn等)
LiM2O4(M:Co、Ni、Mn等)
LiMPO4(M:Fe等)
负极材料:石墨(能吸附锂原子)
负极反应:LixCn-xe-===xLi++nC
正极反应:Li1-xMO2+xLi++xe-===LiMO2
锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+
通过电解质迁移入MnO2晶格中,生成LiMnO2。回答下列问题:
(1)外电路的电流方向是由________极流向________极。(填字母)
(2)电池正极反应式为_____________________。
(3)是否可用水代替电池中的混合有机溶剂?______(填“是”或“否”),原因是______________________
课堂练习
特点:(1)环境友好;
(2
)高效(理论利用率达85-90%,实际40-60%)
(3)燃料和氧化剂由外设备提供
2H2
+
O2
==
2H2O
点燃
三.燃料电池
2H2
+4OH-
-
4e-=4H2O
O2+2H2O+
4e-=
4OH-
2H2
+
O2
=
2H2O
(1)当电解质溶液为KOH溶液时
负极:
正极:
放电总反应式:
负极:
正极:
放电总反应式:
(2)当电解质溶液为稀H2SO4
2H2
-
4e-=4H+
O2+
4H+
+
4e-=
2H2O
2H2
+
O2
=
2H2O
【变式1】若该电池以固体氧化锆-氧化钇为电解质,已知这种固体电解质在高温下允许氧离子(O2-)在其间通过,各电极反应又如何?
负极:
.
正极:
.
总反应:
.
2H2
-
4e-+2O2-=2H2O
O2+
4e-=
2O2-
2H2
+
O2
=
2H2O
【变式2】若以甲烷为燃料电池电解质为熔融态的K2CO3,工作温度为600~800℃,正极辅助通入CO2。写出该燃料电池中各电极反应及总反应。
负极:
。
正极:
。
总反应
:
。
引入CO2的作用:
。
CH4
-8e-+4
CO32
-
=5CO2+2H2O
2O2+8e-+4CO2==
4
CO32
-
CH4+
2O2
=2H2O+
CO2
维持溶液中离子浓度不变
【变式3】写出甲烷燃料电池(CH4O-O2-KOH溶液)的电极反应式
负极
正极
总反应式
CH4
+10OH-
-8e-==CO32-+7H2O
CH4
+
2O2
+2OH-
=3H2O+
CO32-
2O2+8e-+4H2O==
8OH-
【变式4】若上述燃料电池以甲烷为燃料,在H2SO4溶液中发生反应构成原电池,试写出各极电极反应。
负极:
,
正极:
,
总反应:
。
CH4
+2H2O-8e-=CO2+8H+
CH4
+
2O2
=2H2O+
CO2
2O2+8e-+8H+=
4H2O
CO-O2熔融盐燃料电池的装置如图所示,电池工作时,C口产生的气体一部分通入B口被利用,另一部分被分离出来。若导线中流过2
mo1
e-,理论上C口被分离出的气体的物质的量最多为
。
课堂练习
电池的一个电极由有机光敏染料(s)涂覆在TiO2纳米晶体表面制成,另一电极南导电玻璃镀铂构成,电池中发生的反应为:
TiO2/S
???????
TiO2/S
(激发态)
TiO2/S
→TiO2/S++e-
I3-+2e-
→3I-
TiO2/S++3I
-
→2TiO2/S+I3-
下列关于该电池叙述错误的是
A电池工作时,I-离子在镀铂导电玻璃电极上放电
B电池工作时,是将太阳能转化为电能
C电池的电解质溶液中I-和I3-的浓度不会减少
D电池中镀铂导电玻璃为正极
四.太阳能电池
