高中化学人教版选修4第四章第三节-电解池(56张PPT)
文档属性
| 名称 | 高中化学人教版选修4第四章第三节-电解池(56张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-08-26 00:00:00 | ||
图片预览






文档简介
(共56张PPT)
第三节
电解池
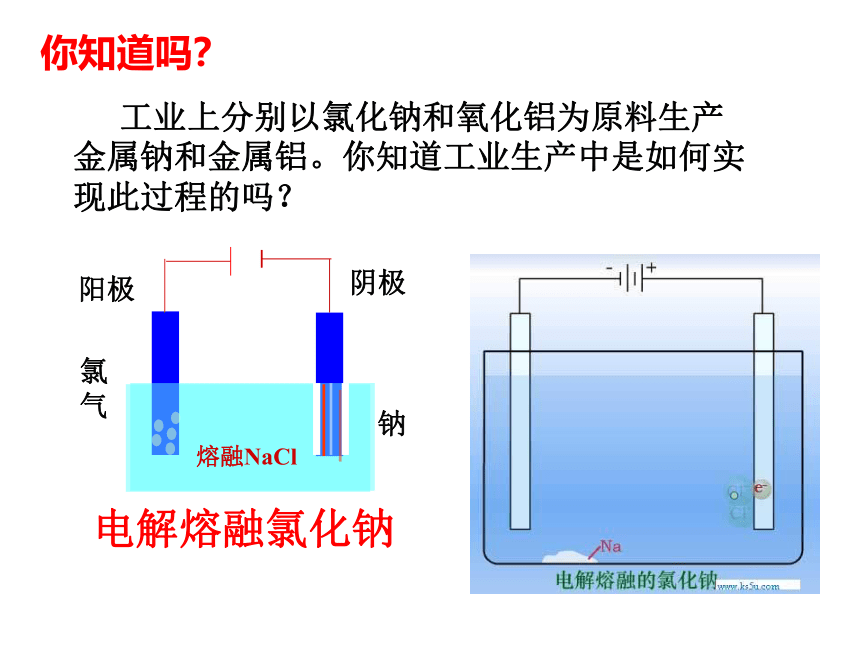
你知道吗?
工业上分别以氯化钠和氧化铝为原料生产金属钠和金属铝。你知道工业生产中是如何实现此过程的吗?
电解熔融氯化钠
阴极
阳极
氯
气
钠
熔融NaCl
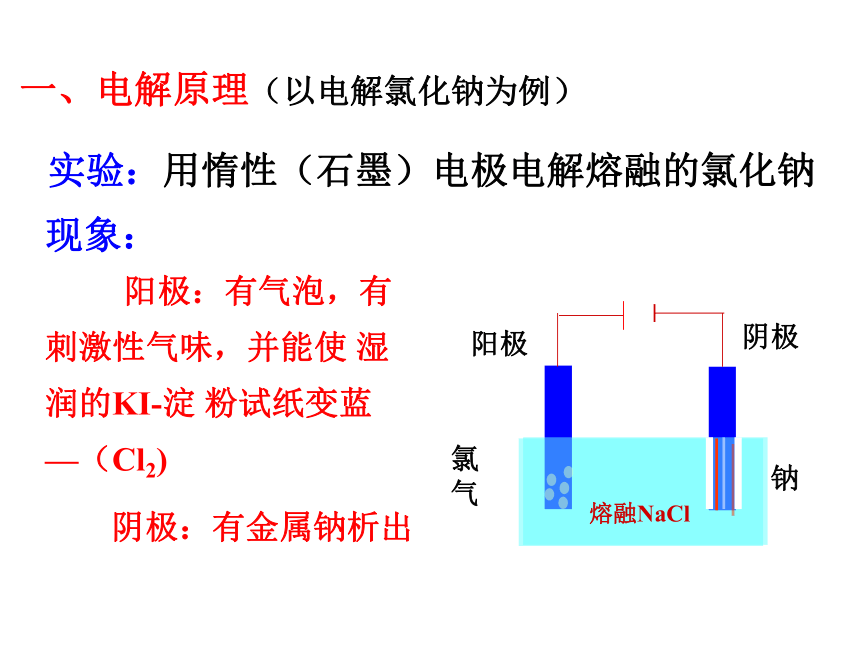
一、电解原理(以电解氯化钠为例)
实验:用惰性(石墨)电极电解熔融的氯化钠
现象:
阳极:有气泡,有刺激性气味,并能使
湿润的KI-淀
粉试纸变蓝
—(Cl2)
阴极:有金属钠析出
阴极
阳极
氯
气
钠
熔融NaCl
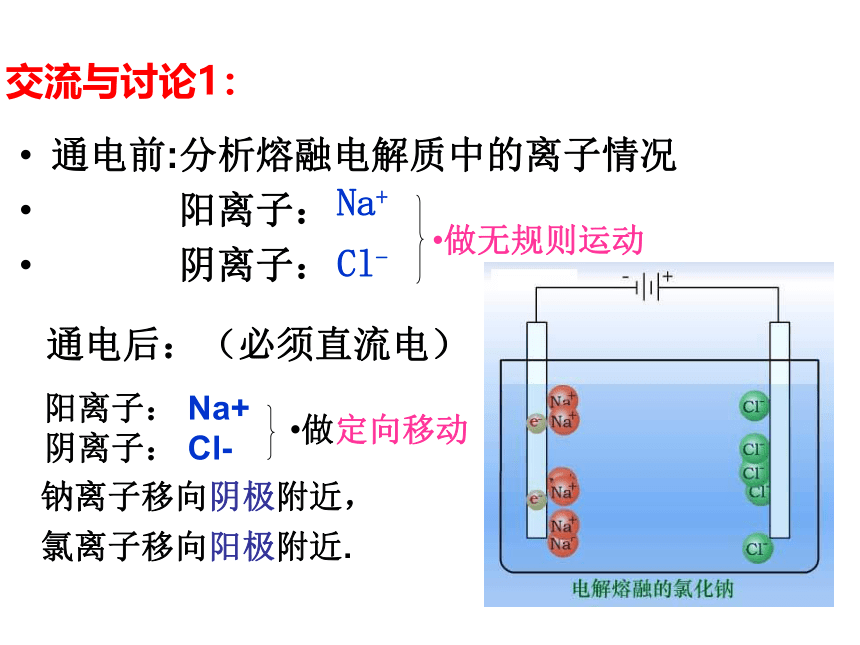
通电前:分析熔融电解质中的离子情况
阳离子:
阴离子:
通电后:(必须直流电)
Na+
Cl-
交流与讨论1:
做无规则运动
阳离子:
Na+
阴离子:
Cl-
钠离子移向阴极附近,
氯离子移向阳极附近.
做定向移动
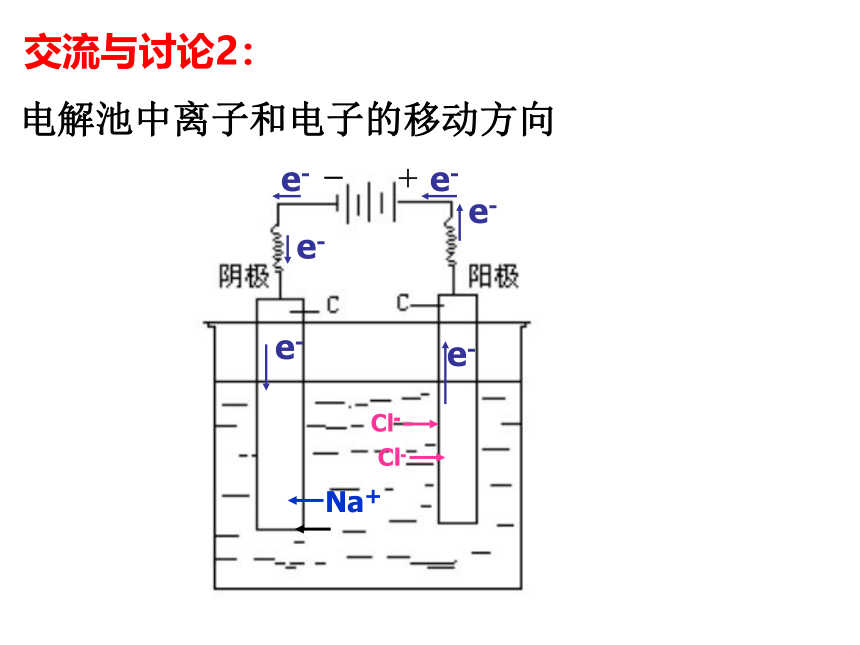
交流与讨论2:
e-
e-
e-
e-
e-
e-
电解池中离子和电子的移动方向
+
-
Cl-
Na+
Cl-
(1)确定电极名称:
阳极(接电源正极)
阴极(接电源负极)与电极材料无关
(2)判断电极产物并书写电极反应:
阳离子移向阴极放电,阴离子移向阳极放电
阳极:2Cl-
=
Cl2↑
+
2e-
氧化反应
阴极:2Na+
+2e-
=
2Na
还原反应
总式:
2NaCl
2Na+Cl2
↑
通电
使电流通过电解质溶液而在阴阳两极引起氧化还原反应的过程。
2.电解池:
把电能转化为化学能的装置.
或
借助于电流引起氧化还原反应的装置.
(1)外加直流电源
(2)与电源相连的两个电极
(3)电解质溶液或熔化的电解质
(4)形成闭合回路
1.电解:
3.构成条件:
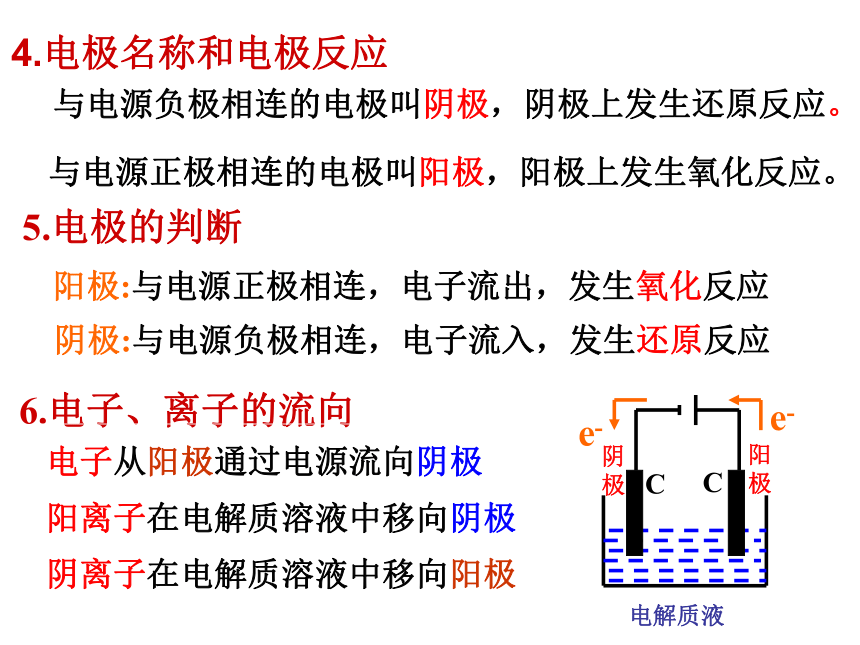
4.电极名称和电极反应
与电源负极相连的电极叫阴极,阴极上发生还原反应。
与电源正极相连的电极叫阳极,阳极上发生氧化反应。
阴极:与电源负极相连,电子流入,发生还原反应
阳极:与电源正极相连,电子流出,发生氧化反应
5.电极的判断
6.电子、离子的流向
电子从阳极通过电源流向阴极
阳离子在电解质溶液中移向阴极
阴离子在电解质溶液中移向阳极
e-
e-
C
C
阴极
阳极
电解质液
注:电子只在外电路定向移动,不能从溶液中
移动
7.惰性电极与活性电极:
惰性电极(铂、金、石墨):
仅仅导电,不参与反应
活性电极(除铂、金外的金属):
既可以导电、又可以参与电极反应
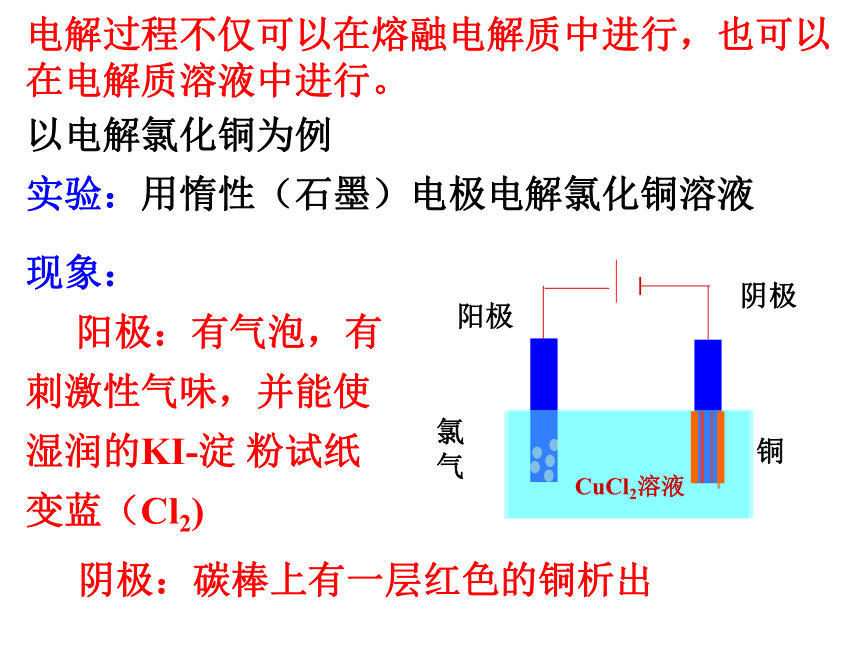
电解过程不仅可以在熔融电解质中进行,也可以在电解质溶液中进行。
以电解氯化铜为例
实验:用惰性(石墨)电极电解氯化铜溶液
现象:
阳极:有气泡,有刺激性气味,并能使
湿润的KI-淀
粉试纸变蓝(Cl2)
阴极:碳棒上有一层红色的铜析出
阴极
阳极
氯
气
铜
CuCl2溶液
实验分析:
通电前:分析电解质溶液中的离子情况
阳离子:H+、Cu2+
阴离子:OH-、Cl-
通电后:
(必须直流电)
(1)确定电极名称:
阳极(接电源正极)
阴极(接电源负极)与电极材料无关
做无规则运动
(2)判断离子的放电顺序:
阳离子:Cu2+>H+
(得电子顺序)
阴离子:Cl->OH-(失电子顺序)
(3)判断电极产物并书写电极反应:
阳离子移向阴极放电,阴离子移向阳极放电
阳极:2Cl-
-
2e-
=
Cl2
↑
氧化反应
阴极:Cu2+
+
2e-
=
Cu
还原反应
总式:
(4)分析电解质溶液的变化情况:氯化铜溶液浓度降低
CuCl2
Cu+Cl2
↑
电解
1.放电:
阴离子失去电子而阳离子得到电子的过程叫放电。
①活性材料作电极时:
金属在阳极失电子被氧化成阳离子进人溶液,阴
离子不容易在电极上放电。
②用惰性电极(Pt、Au、石墨、钛等)时:溶液中阴
离子的放电顺序(由易到难)是:
S
2->SO32->I
->Br
->Cl
->OH
->NO3
->SO42-(等含氧酸根离子)>F-
阳极:
小结:
2.放电顺序:
Ag+>Fe3+>Cu2+>H+>Pb2+>Sn2+>Fe2+>Zn2+>(H+)>
Al3+>Mg2+>Na+>Ca+>K+
注:①当离子浓度相差较大时,放电顺序要发生变
化.
②Al3+、Mg2+、Na+、Ca2+、K+在水溶液中均不
可能得到电子.
无论是惰性电极还是活性电极都不参与电极反
应,发生反应的是溶液中的阳离子。
阳离子在阴极上放电顺序是:
阴极:
练习:
分析以惰性电极电解下列溶液的电极反应。
(1)硝酸银溶液
(2)氯化钠溶液
(3)稀硫酸
(4)氢氧化钠溶液
把电能转化为化学能的装置
C
Fe
NaCl溶液
(1)两电极接直流电源;(2)电极插入电解质溶液;
(3)形成闭合电路。
阴极:与电源负极相连的电极
阳极:与电源正极相连的电极
2NaCl+2H2O==2NaOH+H2↑+
Cl2↑
通电
电解池知识小结
定义
装置
形成条件
电极
电极反应
电解反应
阴极:还原反应
2H++2e
-
=
H2↑
阳极:氧化反应
2Cl-
-
2e-
=
Cl2↑
第二课时
问题解决
分析下图,哪些是原电池——
哪些是电解池——
1、3、5
6、7
【原电池与电解池的比较】
整理与归纳:
负极
:氧化反应
正极
:还原反应
阳极
:氧化反应
阴极
:还原反应
电极反应
形成条件
举例说明
能量转换
电子流向
化学能转化为电能
电能转化为化学能
⑴铜锌原电池;
⑵氢氧燃料电池
⑴氯碱工业;
⑵电镀
负极 正极
阳极流出;阴极流入
装置举例
两个电极;电解质;闭合回路;一般能自发进行氧化还原反应
电源;两个电极;电解质
记
笔
记
分析电解反应的一般思路
溶液中存在的离子
两极上的电极反应
离子的移动方向及放电顺序
判断电解池的阴、阳极
电解Na2SO4溶液的分析
阴极
阳极
氧气
氢
气
实例
电极反应
浓度
PH值
复原
Na2SO4
?
?
?
?
?
阳极:
4OH--
4e-
=
2H2O+O2
阴极:
4H
++
4e-
=
2H2
2H2O
===
2H2
↑+O2
↑
通电
变大
不
变
加水
Na2SO4溶液
如电解H2SO4、HNO3、NaOH、Na2SO4等溶液时其电极反应式为:
阳极
:
4OH--4e-=2H2O
+O2↑
阴极:
4H+
+4e-=2H2
↑
总反应:2H2O==
O2↑
+2H2↑
电解
电解后溶液中溶质的质量分数增大,若要恢
复原来的浓度,只需加入一定量的水即可。
二.用惰性电极电解电解质溶液规律
1.电解水型:
阴极
阳极
氯
气
铜
实例
电极反应
浓度
PH值
复原
CuCl2
?
?
?
?
?
阳极:2Cl--2
e-
=Cl2↑
阴极:Cu2++
2e-=2Cu↓
减小
减小
CuCl2
CuCl2溶液
CuCl2
Cu+Cl2
↑
电解
电解CuCl2溶液的分析
如电解盐酸、CuCl2溶液等
电解后溶液中溶质的质量分数减小,若要恢复原来的组成和浓度,需加入一定量的溶质(通入一定量的HCl气体)
阳极:
2Cl
--
2e-=Cl2↑
阴极:
2H+
+2e-=
H2
↑
总反应:2HCl==
Cl2↑
+
H2↑
电解
电解盐酸
2.电解电解质本身:
阳极
阴极
氯气
氢
气
实例
电极反应
浓度
PH值
复原
NaCl
?
?
?
?
?
阳极:
2Cl-
→
2e-
+
Cl
2↑
阴极:
2H
++
2e-
→
H2
↑
2NaCl+2H2O
2NaOH+H2
↑
+
Cl2
↑
电解
减小
增
大
加
HCl
NaCl溶液
电解NaCl溶液的分析
如电解NaCl、KCl、MgCl2溶液等。
电解后原溶液中溶质的质量分数减小,若要恢复原来的组成和浓度,需通入一定量的HCl气体。
阳极
(C):
2Cl
--
2e-=Cl2↑
阴极
(C):
2H+
+2e-=
H2
↑
总反应:
2NaCl+2H2O==2NaOH+
Cl2↑
+
H2↑
电解
3.放出氢气生成碱型:
阳极
阴极
氧
气
铜
阳极:
4OH-
→
4e-
+
2H2O+O2
↑
阴极:Cu2++
2e-
→
Cu
减小
减小
加
CuO
CuSO4溶液
2CuSO4+
2H2O
2Cu
+O2
↑+
2H2SO4
电解
电解CuSO4溶液的分析
如电解CuSO4溶液、AgNO3溶液等。
阳极
:
4OH--4e-=2H2O
+O2↑
阴极:
2Cu2+
+4e-=2Cu
总反应:
2CuSO4
+2H2O
=
2Cu+O2↑
+2H2SO4
电解
电解后原溶液中溶质的质量分数减小,若要恢复原来的组成和浓度,需加入一定量金属氧化物。
电解CuSO4溶液
4.放出氧气生成酸型:
电解规律(惰性电极)小结
阳极:S2-
>
I-
>
Br-
>
Cl-
>
OH-
>
含氧酸根
>
F-
Ⅰ
Ⅱ
Ⅲ
Ⅳ
Ⅰ与Ⅲ区:电解本身型
如CuCl2
、HCl
Ⅰ与Ⅳ区:放氢生碱型
如NaCl
Ⅱ与Ⅲ区:放氧生酸型
如CuSO4、AgNO3
Ⅱ与Ⅳ区:电解水型
如Na2SO4、H2SO4
、NaOH
阴极:Ag+>Fe3+>Cu2+>H+>Fe2+>Zn2+>(H+)>Al3+>Mg2+>Na+
电解质溶液用惰性电极电解的示例:
含氧酸
H2SO4
强碱
NaOH
活泼金属的含氧酸盐
Na2SO4
无氧酸
HCl
阳极:4OH-→4e-+O2+2H2O
阴极:4H+
+
4e-
→
2H2↑
减小
增大
不变
H2O
阳极:2Cl-
→
2e-+Cl2↑
阴极:2H++2e-
→
H2↑
增大
HCl
不活泼金属的无氧酸盐
CuCl2
阳极:2Cl-
→
2e-
+Cl2↑
阴极:Cu2++2e-
→
Cu↓
减少
CuCl2
活泼金属的无氧酸盐
NaCl
阳极:2Cl-
→
2e-
+Cl2↑
阴极:2H++2e-
→
H2↑
增大
HCl
不活泼金属的含氧酸盐
CuSO4
阳极:4OH-
→
4e-
+O2↑+2H2O
阴极:2Cu2++4e-
→
2Cu↓
减小
CuO
(
A
)
(B)
(C)
(D)
CuSO4
AgNO3
AgNO3
NaHSO4
Ag
Cu
Cu
C
Pt
Pt
Ag
Fe
1.写出下列装置的电极反应式,并判断A、B、C溶液PH值的变化。
巩固练习
2.如上图所示,通电后A极上析出Ag,对该装置的有关叙述正确的是?
A.P是电源的正极
B.F极上发生的反应为:4OH-
-
4e-=2H2O+O2↑
C.电解时,甲、乙、丙三池中,除E、F两极外,其余电极均参加了反应
D.通电后,甲池的PH减小,而乙、丙两池溶液的PH不变
B
3.用铂电极电解下表中各组物质的水溶液,电解一段时间以后,甲、乙两池中溶液的pH值均减小,而在①和④两极,电极产物的物质的量之比为1︰2的是
甲
乙
A
B
C
D
甲
KOH
H2SO4
Na2SO4
CuSO4
乙
CuSO4
AgNO3
HCl
HNO3
4.为下图所示装置中,a、b都是惰性电极,通电一段
时间后,b极附近溶液呈红色。下列说法正确的是
A.X是正极,Y是负极
B.X是负极,Y是正极
C.CuSO4溶液的PH值逐渐减小
D.CuSO4溶液的PH值不变
a
?X
Y
?
b
Pt
Cu
CuSO4溶液
NaCl和酚酞溶液
AC
第三课时
三.电解原理的应用
电解饱和食盐水反应原理
思考:
(1)电解池的两极各产生什么现象?
若在两极附近均滴加酚酞试
液,会有什么现象?
(2)怎样初步检验两极产物的生成?
(3)结合教材,分析产生这种现象
的原因。
在U型管里装入饱和食盐
水,用一根碳棒作阳极,
一根铁棒作阴极。接通直
流电源
实验装置
1.电解食盐水
现象:
阳极:有气泡产生,使
湿润的淀粉-KI
溶液变蓝
阴极:有气泡产生,滴
加酚酞溶液变红
阳极:2Cl-
-
2e-
=
Cl2↑
阴极:2H+
+
2e-
=
H2↑
总式:
2NaCl+2H2O=2NaOH+H2↑+Cl2↑
(条件:通电)
实验装置
(1)生产设备名称:离子交换膜电解槽
阴极:碳钢
阳极:钛
阳离子交换膜:
只允许阳离子通过(Cl-、OH-离子和气体
不能通过),把电解槽隔成阴极室和阳极室。
(2)离子交换膜的作用:
a、防止氢气和氯气混合而引起爆炸;
b、避免氯气和氢氧化钠反应生成
,而影响氢氧化
钠的产量。
氯碱工业:离子交换膜法制烧碱
-
+
Cl2
Cl2
Cl—
H2
Na+
H+
OH—
淡盐水
NaOH溶液
精制饱和NaCl溶液
H2O(含少量NaOH)
离子交换膜
阳
极
金属钛网
阴
极
碳钢网
阳极室
阴极室
粗盐的成份:泥沙、Ca2+、Mg2+、Fe3+、SO42-杂质,会与碱性物质反应产生沉淀,损坏离子交换膜
精制食盐水
杂质的除去过程:
粗盐水
含少量Ca2+.Mg2+
精制盐水
2.
电镀
电镀是利用电解原理在某些金属表面镀上一薄层其他金属或合金的过程,它是电解原理的又一重要应用。电镀可以使金属更加美观耐用,增强防锈抗腐能力。例如,钢铁是人们最常用的金属,但钢铁有个致命的缺点,就是它们易被腐蚀。防止钢铁发生腐蚀的一种最常用方法就是在其表面镀上其他金属,如锌、铜、铬、镍等。
(1)电镀:电镀是利用电解原理在某些金属表面镀上一薄层其他金属或合金的过程。
阴极:待镀金属制品
阳极:镀层金属
电镀液:含有镀层金属阳离子的可溶性盐溶液
(2)
电镀池的形成条件
(3)电镀的结果,电镀液的浓度保持不变
镀件
铜
氯化铜溶液
实验现象
阳极:
阴极:
铜变小
有红色固体产生
电极反应
Cu-2e-=
Cu2+
Cu2++2e-=Cu
电镀液的组成及酸碱性不会变化
例:电镀铜原理
3.铜的电解精炼
一般火法冶炼得到的粗铜中含有多种杂质(如锌、铁、镍、银、金等),这种粗铜的导电性远不能满足电气工业的要求,如果用以制电线,就会大大降低电线的导电能力。因此必须利用电解的方法精炼粗铜。
粗铜
含杂质(Zn
Fe
Ni
Ag
Au
等)
粗铜
纯铜
电解精炼铜的原理示意图:
e-
?
-
+
纯铜作阴极,粗铜作阳极;
e-
e-
Ag
Au
硫酸铜溶液作电解液
阳极:
Zn
-
2e-
=
Zn2+
Fe
-
2e-
=
Fe2+
Ni
-
2e-
=
Ni2+
Cu
-
2e-
=
Cu2+
Zn
Fe
Ni
Cu
Ag
Au
阴极:
Cu2+
+
2e-
=
Cu
阳极泥
问:电解完后,CuSO4溶液的浓度有何变化?
CuSO4溶液
粗铜
纯铜
特征
纯铜作阴极,粗铜作阳极
阳极主要金属与电解质中的阳离子相同
电解液CuSO4的浓度基本不变
4.
电冶金
(1)制取金属钠
电解熔融状态的氯化钠
阳极:
2Cl
-
-2e-
=
Cl2↑
阴极:
2Na+
+
2e-
=
2Na
总反应:
2NaCl(熔融)
2Na
+
Cl2
↑
电解熔融氯化钠制钠
阳极:6O2--12
e-
=3O2↑
阴极:4Al3+
+
12e-
=4Al
(2)冶炼铝
通电
总式:2Al2O3
4Al+3O2
↑
原理:
助熔剂:冰晶石(Na3AlF6
六氟合铝酸钠)
阳极材料(碳)和熔融氧化铝需要定期补充
思考:
工业上为什么用电解熔融氧化铝的方法冶炼铝而不用AlCl3?
阳极
阴极
电解质Al2O3
Na3AlF3
碳块
铝的冶炼
铝
冶炼铝设备图
阳极C
电解质
烟罩
熔融态铝
钢壳
钢导电棒
阴极C
耐火材料
1.
a
、b哪一极为正极?
2.
若要给铁叉镀锌,a极选
用什么材料?选择何种
溶液?
3.
若要给铁叉镀金,a极选
用什么材料?选择何种
溶液?
思考:
e-
1.右图中x、y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色无臭气体放出,符合这一情况的
A
练习
Fe
Cu
氯化铜溶液
氯化铜溶液
Cu
C
氯化铜溶液
Cu
C
2.写出下列装置的电极反应,并标明氧化反应还原反应
A
B
D
C
Fe
Cu
氯化钠溶液
(
A
)
(B)
(C)
(D)
CuSO4
AgNO3
AgNO3
NaHSO4
Ag
Cu
Cu
C
Pt
Pt
Ag
Fe
3.写出下列装置的电极反应,并判断A、B、C溶液PH值的变化。
很多人都说,不要轻易的开玩笑,因为有的人真的会把玩笑当成真心话来对待,我们的青春无不都是以错过结束的,最好结婚的那个既不是旧爱阿明也不是刻骨铭心的阿强,努力了那么久最后的最后,依然没有在一起,那么多的错过,其实都是我们的青春。 张震说:这部电影是一个男人和三个女人的爱情故事,田季安对隐娘是逝去的爱,深刻的回味。 舒淇开玩笑反击:“你还不是娶了别人。” 都说“世界上没有所谓的玩笑,所有的玩笑都有认真的成分。”这个玩笑不仅认真,也最让人心碎。 前两天看了前任攻略2后,又挑了一个夜深人静的晚上,一个人在办公室看前任攻略1,当看到孟云和夏露结婚,罗茜知道再也等不到,一个人在家里看着他们那些年的美好时光,翻着那些照片,想着以前还能呆在孟云身边的点点滴滴,她的撕心裂肺可能在那个时刻达到了瓶颈,她端着酒杯,她瘫倒在沙发,她的痛心疾首,她的自责,或许更是一种超凡的解脱,因为再也不用去赌去等去猜了。 后来她去他们的大学呆了三天三夜,那一段真的很骗人眼泪。 他比我大几岁,遇见他的那时候却跟我一样还在上大学,在我们云南当兵后来考上的军校。我们隔着很远的距离,我在北方,他在南方,我甚至都不知道我俩算不算在一起过,他舍友都以为他谈恋爱了,而且那时候我们特别低调,但我还是被他那帮战友给揪出来。 我不知道是不是职业病的原因,他就是那种什么都会跟你坦白,什么都会跟你报告的那种人,要是在今天我一定会跟他发那种“好人卡”。2013年,他的前女友五一结婚,给他发了请帖,那天晚上他还跑来问我要不要去,我还记得那天晚上我特别支持地说:去啊,她都邀请了,你干嘛不去。 后来我们俩再没提过这个事,五一过了我也没问他,因为我知道他根本就没有假期,人肯定是不可能亲自到的,其实我也是一直把这事装心里的,我就是等着他自己跟我坦白。#p#副标题#e# 大概是暑假了,不知道是谁说起这个事,跟我预想的一样,人肯定是没去的,至于红包送不送到现在我都忘记了。 难不成领导还会批你请假理由为“参加前女友的婚礼”这样的假条,肯定不会的,特别对于这种党国的人,想都别想,过年让你踏踏实实回家就算不错了。当时类似我这点小九九现在想起来我就想给自己几个大耳光子,扇死。 但是别以为我让他去说的是反话,我有时也很奇怪我那到底是什么心理,吃饭的时候这么爱吃醋的一个姑娘那个时候怎么心里还会明晃晃地斩钉截铁地真真实实地让他去参加呢,要是我跟他在一起的话,没准还会跟他去呢。 都说二十多岁是一个特别迷茫的年纪,因为很多未知,不知道你会成为一个什么样的人,还有不知道未来陪伴你走下去的那个人又是谁。然而那时候的我们大概都比较会憧憬,会想跟他一起见家长的情形,会想以后应该在哪座城市生活,会想对于他这种职业,我以后应该要更坚强,什么都要学会,所以从大学时候,我就一直逼着自己独立,逼着自己一个人做很多事,逼着自己什么都要学会。 因为知道未来应该是跟这样的制服男一起生活。即使那时候一年还见不上几天,一年还见不上一次面,晚上要十一点之后才能联系上,有时候突然就会一个星期没有联系,但还是会两个人有很多很多约定与对未来的想象。甚至在很早以前他就说:无论大学这几年之间怎么样,毕业了就在一起吧! 接下来的日子里,还是发生了很多事,跟大多数学生时代的恋爱一样,我们还是分开了。#p#副标题#e# 毕业的时候,他肩上扛上了星星,我也穿起了我的学士服,我们还是没有在一起。那天我突然在我的公众号里面看到了他,其实这两年里,我们几乎删除了对方所有的联系方式,但是有些东西即使删除应该也记在心里面了。 我知道,他知道我的全部动态,而我也对他的生活有所了解。但是我们知道,再也回不去了,我们都趟过了那条河,曾经的美好就让它留在那里吧,错过的人终究不属于你。曾经能在一起促膝而谈去参加他前女友婚礼的我,到今天也变成了他的“前任”。 就像舒淇的那句“最后你还是娶了别人”一样,后来,我还是成为了他的前任。感情真的说不来它究竟是什么样的一种东西,或是一种怎么样的一种味道,但是曾经有过,就已经足够。 青春大概就是这样,不是当初的你们说谎或者承诺的时候不是真的,我依然相信那时候他说的那些话绝对出于真心,我也相信过他曾经许下的那些誓言,只是那份青春年少里的感情终究抵不过缘分的交错,我们都在慢慢地从对方生命里淡去,他身边有爱他的女孩,而我在未来的那么一天也会遇到那个陪伴在自己身边的人。 就在前一秒,我选择删除所有,包括慢慢遗忘,我曾经也以为可以做朋友,但后来发现不再联系才是这段故事最好的结局,要是很多年过去了,还能再某个街头遇见坐下来聊聊家常也未尝不可,我相信时间是个伟大的东西。但是现在,让我们都放下包袱轻轻松松大大方方地去寻找属于各自的幸福。 我想起想起罗茜很快答应了求婚,在自己的婚礼上说的那句话:有人说,你结婚的那个人一定不是你最爱的,我不信,我不信了十几年,可是我输了。#p#副标题#e# 我记得看第一遍的时候,是跟朋友一起看的,当时我们还讨论这个事情:你结婚的那个人是不是你最爱的。 那时候我的答案是:这辈子结婚对象不是你最爱的。 但是后来,我发现心里的很多观点在变,很多想法也在变,我想没有什么能比最后那个陪你走下去的那种爱更可贵吧,那种爱是互相忍耐,风风雨雨走过几十年,是长久,是家庭与温暖,是那种生命里持久的交汇与融入,那个人才是真正爱你的,也是你最爱的。 后来,我们还是没有在一起。但是,曾经陪伴的那一段时光大概也是青春里最美的记忆,有些人,来过就是你遇见他的所有意义。
第三节
电解池
你知道吗?
工业上分别以氯化钠和氧化铝为原料生产金属钠和金属铝。你知道工业生产中是如何实现此过程的吗?
电解熔融氯化钠
阴极
阳极
氯
气
钠
熔融NaCl
一、电解原理(以电解氯化钠为例)
实验:用惰性(石墨)电极电解熔融的氯化钠
现象:
阳极:有气泡,有刺激性气味,并能使
湿润的KI-淀
粉试纸变蓝
—(Cl2)
阴极:有金属钠析出
阴极
阳极
氯
气
钠
熔融NaCl
通电前:分析熔融电解质中的离子情况
阳离子:
阴离子:
通电后:(必须直流电)
Na+
Cl-
交流与讨论1:
做无规则运动
阳离子:
Na+
阴离子:
Cl-
钠离子移向阴极附近,
氯离子移向阳极附近.
做定向移动
交流与讨论2:
e-
e-
e-
e-
e-
e-
电解池中离子和电子的移动方向
+
-
Cl-
Na+
Cl-
(1)确定电极名称:
阳极(接电源正极)
阴极(接电源负极)与电极材料无关
(2)判断电极产物并书写电极反应:
阳离子移向阴极放电,阴离子移向阳极放电
阳极:2Cl-
=
Cl2↑
+
2e-
氧化反应
阴极:2Na+
+2e-
=
2Na
还原反应
总式:
2NaCl
2Na+Cl2
↑
通电
使电流通过电解质溶液而在阴阳两极引起氧化还原反应的过程。
2.电解池:
把电能转化为化学能的装置.
或
借助于电流引起氧化还原反应的装置.
(1)外加直流电源
(2)与电源相连的两个电极
(3)电解质溶液或熔化的电解质
(4)形成闭合回路
1.电解:
3.构成条件:
4.电极名称和电极反应
与电源负极相连的电极叫阴极,阴极上发生还原反应。
与电源正极相连的电极叫阳极,阳极上发生氧化反应。
阴极:与电源负极相连,电子流入,发生还原反应
阳极:与电源正极相连,电子流出,发生氧化反应
5.电极的判断
6.电子、离子的流向
电子从阳极通过电源流向阴极
阳离子在电解质溶液中移向阴极
阴离子在电解质溶液中移向阳极
e-
e-
C
C
阴极
阳极
电解质液
注:电子只在外电路定向移动,不能从溶液中
移动
7.惰性电极与活性电极:
惰性电极(铂、金、石墨):
仅仅导电,不参与反应
活性电极(除铂、金外的金属):
既可以导电、又可以参与电极反应
电解过程不仅可以在熔融电解质中进行,也可以在电解质溶液中进行。
以电解氯化铜为例
实验:用惰性(石墨)电极电解氯化铜溶液
现象:
阳极:有气泡,有刺激性气味,并能使
湿润的KI-淀
粉试纸变蓝(Cl2)
阴极:碳棒上有一层红色的铜析出
阴极
阳极
氯
气
铜
CuCl2溶液
实验分析:
通电前:分析电解质溶液中的离子情况
阳离子:H+、Cu2+
阴离子:OH-、Cl-
通电后:
(必须直流电)
(1)确定电极名称:
阳极(接电源正极)
阴极(接电源负极)与电极材料无关
做无规则运动
(2)判断离子的放电顺序:
阳离子:Cu2+>H+
(得电子顺序)
阴离子:Cl->OH-(失电子顺序)
(3)判断电极产物并书写电极反应:
阳离子移向阴极放电,阴离子移向阳极放电
阳极:2Cl-
-
2e-
=
Cl2
↑
氧化反应
阴极:Cu2+
+
2e-
=
Cu
还原反应
总式:
(4)分析电解质溶液的变化情况:氯化铜溶液浓度降低
CuCl2
Cu+Cl2
↑
电解
1.放电:
阴离子失去电子而阳离子得到电子的过程叫放电。
①活性材料作电极时:
金属在阳极失电子被氧化成阳离子进人溶液,阴
离子不容易在电极上放电。
②用惰性电极(Pt、Au、石墨、钛等)时:溶液中阴
离子的放电顺序(由易到难)是:
S
2->SO32->I
->Br
->Cl
->OH
->NO3
->SO42-(等含氧酸根离子)>F-
阳极:
小结:
2.放电顺序:
Ag+>Fe3+>Cu2+>H+>Pb2+>Sn2+>Fe2+>Zn2+>(H+)>
Al3+>Mg2+>Na+>Ca+>K+
注:①当离子浓度相差较大时,放电顺序要发生变
化.
②Al3+、Mg2+、Na+、Ca2+、K+在水溶液中均不
可能得到电子.
无论是惰性电极还是活性电极都不参与电极反
应,发生反应的是溶液中的阳离子。
阳离子在阴极上放电顺序是:
阴极:
练习:
分析以惰性电极电解下列溶液的电极反应。
(1)硝酸银溶液
(2)氯化钠溶液
(3)稀硫酸
(4)氢氧化钠溶液
把电能转化为化学能的装置
C
Fe
NaCl溶液
(1)两电极接直流电源;(2)电极插入电解质溶液;
(3)形成闭合电路。
阴极:与电源负极相连的电极
阳极:与电源正极相连的电极
2NaCl+2H2O==2NaOH+H2↑+
Cl2↑
通电
电解池知识小结
定义
装置
形成条件
电极
电极反应
电解反应
阴极:还原反应
2H++2e
-
=
H2↑
阳极:氧化反应
2Cl-
-
2e-
=
Cl2↑
第二课时
问题解决
分析下图,哪些是原电池——
哪些是电解池——
1、3、5
6、7
【原电池与电解池的比较】
整理与归纳:
负极
:氧化反应
正极
:还原反应
阳极
:氧化反应
阴极
:还原反应
电极反应
形成条件
举例说明
能量转换
电子流向
化学能转化为电能
电能转化为化学能
⑴铜锌原电池;
⑵氢氧燃料电池
⑴氯碱工业;
⑵电镀
负极 正极
阳极流出;阴极流入
装置举例
两个电极;电解质;闭合回路;一般能自发进行氧化还原反应
电源;两个电极;电解质
记
笔
记
分析电解反应的一般思路
溶液中存在的离子
两极上的电极反应
离子的移动方向及放电顺序
判断电解池的阴、阳极
电解Na2SO4溶液的分析
阴极
阳极
氧气
氢
气
实例
电极反应
浓度
PH值
复原
Na2SO4
?
?
?
?
?
阳极:
4OH--
4e-
=
2H2O+O2
阴极:
4H
++
4e-
=
2H2
2H2O
===
2H2
↑+O2
↑
通电
变大
不
变
加水
Na2SO4溶液
如电解H2SO4、HNO3、NaOH、Na2SO4等溶液时其电极反应式为:
阳极
:
4OH--4e-=2H2O
+O2↑
阴极:
4H+
+4e-=2H2
↑
总反应:2H2O==
O2↑
+2H2↑
电解
电解后溶液中溶质的质量分数增大,若要恢
复原来的浓度,只需加入一定量的水即可。
二.用惰性电极电解电解质溶液规律
1.电解水型:
阴极
阳极
氯
气
铜
实例
电极反应
浓度
PH值
复原
CuCl2
?
?
?
?
?
阳极:2Cl--2
e-
=Cl2↑
阴极:Cu2++
2e-=2Cu↓
减小
减小
CuCl2
CuCl2溶液
CuCl2
Cu+Cl2
↑
电解
电解CuCl2溶液的分析
如电解盐酸、CuCl2溶液等
电解后溶液中溶质的质量分数减小,若要恢复原来的组成和浓度,需加入一定量的溶质(通入一定量的HCl气体)
阳极:
2Cl
--
2e-=Cl2↑
阴极:
2H+
+2e-=
H2
↑
总反应:2HCl==
Cl2↑
+
H2↑
电解
电解盐酸
2.电解电解质本身:
阳极
阴极
氯气
氢
气
实例
电极反应
浓度
PH值
复原
NaCl
?
?
?
?
?
阳极:
2Cl-
→
2e-
+
Cl
2↑
阴极:
2H
++
2e-
→
H2
↑
2NaCl+2H2O
2NaOH+H2
↑
+
Cl2
↑
电解
减小
增
大
加
HCl
NaCl溶液
电解NaCl溶液的分析
如电解NaCl、KCl、MgCl2溶液等。
电解后原溶液中溶质的质量分数减小,若要恢复原来的组成和浓度,需通入一定量的HCl气体。
阳极
(C):
2Cl
--
2e-=Cl2↑
阴极
(C):
2H+
+2e-=
H2
↑
总反应:
2NaCl+2H2O==2NaOH+
Cl2↑
+
H2↑
电解
3.放出氢气生成碱型:
阳极
阴极
氧
气
铜
阳极:
4OH-
→
4e-
+
2H2O+O2
↑
阴极:Cu2++
2e-
→
Cu
减小
减小
加
CuO
CuSO4溶液
2CuSO4+
2H2O
2Cu
+O2
↑+
2H2SO4
电解
电解CuSO4溶液的分析
如电解CuSO4溶液、AgNO3溶液等。
阳极
:
4OH--4e-=2H2O
+O2↑
阴极:
2Cu2+
+4e-=2Cu
总反应:
2CuSO4
+2H2O
=
2Cu+O2↑
+2H2SO4
电解
电解后原溶液中溶质的质量分数减小,若要恢复原来的组成和浓度,需加入一定量金属氧化物。
电解CuSO4溶液
4.放出氧气生成酸型:
电解规律(惰性电极)小结
阳极:S2-
>
I-
>
Br-
>
Cl-
>
OH-
>
含氧酸根
>
F-
Ⅰ
Ⅱ
Ⅲ
Ⅳ
Ⅰ与Ⅲ区:电解本身型
如CuCl2
、HCl
Ⅰ与Ⅳ区:放氢生碱型
如NaCl
Ⅱ与Ⅲ区:放氧生酸型
如CuSO4、AgNO3
Ⅱ与Ⅳ区:电解水型
如Na2SO4、H2SO4
、NaOH
阴极:Ag+>Fe3+>Cu2+>H+>Fe2+>Zn2+>(H+)>Al3+>Mg2+>Na+
电解质溶液用惰性电极电解的示例:
含氧酸
H2SO4
强碱
NaOH
活泼金属的含氧酸盐
Na2SO4
无氧酸
HCl
阳极:4OH-→4e-+O2+2H2O
阴极:4H+
+
4e-
→
2H2↑
减小
增大
不变
H2O
阳极:2Cl-
→
2e-+Cl2↑
阴极:2H++2e-
→
H2↑
增大
HCl
不活泼金属的无氧酸盐
CuCl2
阳极:2Cl-
→
2e-
+Cl2↑
阴极:Cu2++2e-
→
Cu↓
减少
CuCl2
活泼金属的无氧酸盐
NaCl
阳极:2Cl-
→
2e-
+Cl2↑
阴极:2H++2e-
→
H2↑
增大
HCl
不活泼金属的含氧酸盐
CuSO4
阳极:4OH-
→
4e-
+O2↑+2H2O
阴极:2Cu2++4e-
→
2Cu↓
减小
CuO
(
A
)
(B)
(C)
(D)
CuSO4
AgNO3
AgNO3
NaHSO4
Ag
Cu
Cu
C
Pt
Pt
Ag
Fe
1.写出下列装置的电极反应式,并判断A、B、C溶液PH值的变化。
巩固练习
2.如上图所示,通电后A极上析出Ag,对该装置的有关叙述正确的是?
A.P是电源的正极
B.F极上发生的反应为:4OH-
-
4e-=2H2O+O2↑
C.电解时,甲、乙、丙三池中,除E、F两极外,其余电极均参加了反应
D.通电后,甲池的PH减小,而乙、丙两池溶液的PH不变
B
3.用铂电极电解下表中各组物质的水溶液,电解一段时间以后,甲、乙两池中溶液的pH值均减小,而在①和④两极,电极产物的物质的量之比为1︰2的是
甲
乙
A
B
C
D
甲
KOH
H2SO4
Na2SO4
CuSO4
乙
CuSO4
AgNO3
HCl
HNO3
4.为下图所示装置中,a、b都是惰性电极,通电一段
时间后,b极附近溶液呈红色。下列说法正确的是
A.X是正极,Y是负极
B.X是负极,Y是正极
C.CuSO4溶液的PH值逐渐减小
D.CuSO4溶液的PH值不变
a
?X
Y
?
b
Pt
Cu
CuSO4溶液
NaCl和酚酞溶液
AC
第三课时
三.电解原理的应用
电解饱和食盐水反应原理
思考:
(1)电解池的两极各产生什么现象?
若在两极附近均滴加酚酞试
液,会有什么现象?
(2)怎样初步检验两极产物的生成?
(3)结合教材,分析产生这种现象
的原因。
在U型管里装入饱和食盐
水,用一根碳棒作阳极,
一根铁棒作阴极。接通直
流电源
实验装置
1.电解食盐水
现象:
阳极:有气泡产生,使
湿润的淀粉-KI
溶液变蓝
阴极:有气泡产生,滴
加酚酞溶液变红
阳极:2Cl-
-
2e-
=
Cl2↑
阴极:2H+
+
2e-
=
H2↑
总式:
2NaCl+2H2O=2NaOH+H2↑+Cl2↑
(条件:通电)
实验装置
(1)生产设备名称:离子交换膜电解槽
阴极:碳钢
阳极:钛
阳离子交换膜:
只允许阳离子通过(Cl-、OH-离子和气体
不能通过),把电解槽隔成阴极室和阳极室。
(2)离子交换膜的作用:
a、防止氢气和氯气混合而引起爆炸;
b、避免氯气和氢氧化钠反应生成
,而影响氢氧化
钠的产量。
氯碱工业:离子交换膜法制烧碱
-
+
Cl2
Cl2
Cl—
H2
Na+
H+
OH—
淡盐水
NaOH溶液
精制饱和NaCl溶液
H2O(含少量NaOH)
离子交换膜
阳
极
金属钛网
阴
极
碳钢网
阳极室
阴极室
粗盐的成份:泥沙、Ca2+、Mg2+、Fe3+、SO42-杂质,会与碱性物质反应产生沉淀,损坏离子交换膜
精制食盐水
杂质的除去过程:
粗盐水
含少量Ca2+.Mg2+
精制盐水
2.
电镀
电镀是利用电解原理在某些金属表面镀上一薄层其他金属或合金的过程,它是电解原理的又一重要应用。电镀可以使金属更加美观耐用,增强防锈抗腐能力。例如,钢铁是人们最常用的金属,但钢铁有个致命的缺点,就是它们易被腐蚀。防止钢铁发生腐蚀的一种最常用方法就是在其表面镀上其他金属,如锌、铜、铬、镍等。
(1)电镀:电镀是利用电解原理在某些金属表面镀上一薄层其他金属或合金的过程。
阴极:待镀金属制品
阳极:镀层金属
电镀液:含有镀层金属阳离子的可溶性盐溶液
(2)
电镀池的形成条件
(3)电镀的结果,电镀液的浓度保持不变
镀件
铜
氯化铜溶液
实验现象
阳极:
阴极:
铜变小
有红色固体产生
电极反应
Cu-2e-=
Cu2+
Cu2++2e-=Cu
电镀液的组成及酸碱性不会变化
例:电镀铜原理
3.铜的电解精炼
一般火法冶炼得到的粗铜中含有多种杂质(如锌、铁、镍、银、金等),这种粗铜的导电性远不能满足电气工业的要求,如果用以制电线,就会大大降低电线的导电能力。因此必须利用电解的方法精炼粗铜。
粗铜
含杂质(Zn
Fe
Ni
Ag
Au
等)
粗铜
纯铜
电解精炼铜的原理示意图:
e-
?
-
+
纯铜作阴极,粗铜作阳极;
e-
e-
Ag
Au
硫酸铜溶液作电解液
阳极:
Zn
-
2e-
=
Zn2+
Fe
-
2e-
=
Fe2+
Ni
-
2e-
=
Ni2+
Cu
-
2e-
=
Cu2+
Zn
Fe
Ni
Cu
Ag
Au
阴极:
Cu2+
+
2e-
=
Cu
阳极泥
问:电解完后,CuSO4溶液的浓度有何变化?
CuSO4溶液
粗铜
纯铜
特征
纯铜作阴极,粗铜作阳极
阳极主要金属与电解质中的阳离子相同
电解液CuSO4的浓度基本不变
4.
电冶金
(1)制取金属钠
电解熔融状态的氯化钠
阳极:
2Cl
-
-2e-
=
Cl2↑
阴极:
2Na+
+
2e-
=
2Na
总反应:
2NaCl(熔融)
2Na
+
Cl2
↑
电解熔融氯化钠制钠
阳极:6O2--12
e-
=3O2↑
阴极:4Al3+
+
12e-
=4Al
(2)冶炼铝
通电
总式:2Al2O3
4Al+3O2
↑
原理:
助熔剂:冰晶石(Na3AlF6
六氟合铝酸钠)
阳极材料(碳)和熔融氧化铝需要定期补充
思考:
工业上为什么用电解熔融氧化铝的方法冶炼铝而不用AlCl3?
阳极
阴极
电解质Al2O3
Na3AlF3
碳块
铝的冶炼
铝
冶炼铝设备图
阳极C
电解质
烟罩
熔融态铝
钢壳
钢导电棒
阴极C
耐火材料
1.
a
、b哪一极为正极?
2.
若要给铁叉镀锌,a极选
用什么材料?选择何种
溶液?
3.
若要给铁叉镀金,a极选
用什么材料?选择何种
溶液?
思考:
e-
1.右图中x、y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色无臭气体放出,符合这一情况的
A
练习
Fe
Cu
氯化铜溶液
氯化铜溶液
Cu
C
氯化铜溶液
Cu
C
2.写出下列装置的电极反应,并标明氧化反应还原反应
A
B
D
C
Fe
Cu
氯化钠溶液
(
A
)
(B)
(C)
(D)
CuSO4
AgNO3
AgNO3
NaHSO4
Ag
Cu
Cu
C
Pt
Pt
Ag
Fe
3.写出下列装置的电极反应,并判断A、B、C溶液PH值的变化。
很多人都说,不要轻易的开玩笑,因为有的人真的会把玩笑当成真心话来对待,我们的青春无不都是以错过结束的,最好结婚的那个既不是旧爱阿明也不是刻骨铭心的阿强,努力了那么久最后的最后,依然没有在一起,那么多的错过,其实都是我们的青春。 张震说:这部电影是一个男人和三个女人的爱情故事,田季安对隐娘是逝去的爱,深刻的回味。 舒淇开玩笑反击:“你还不是娶了别人。” 都说“世界上没有所谓的玩笑,所有的玩笑都有认真的成分。”这个玩笑不仅认真,也最让人心碎。 前两天看了前任攻略2后,又挑了一个夜深人静的晚上,一个人在办公室看前任攻略1,当看到孟云和夏露结婚,罗茜知道再也等不到,一个人在家里看着他们那些年的美好时光,翻着那些照片,想着以前还能呆在孟云身边的点点滴滴,她的撕心裂肺可能在那个时刻达到了瓶颈,她端着酒杯,她瘫倒在沙发,她的痛心疾首,她的自责,或许更是一种超凡的解脱,因为再也不用去赌去等去猜了。 后来她去他们的大学呆了三天三夜,那一段真的很骗人眼泪。 他比我大几岁,遇见他的那时候却跟我一样还在上大学,在我们云南当兵后来考上的军校。我们隔着很远的距离,我在北方,他在南方,我甚至都不知道我俩算不算在一起过,他舍友都以为他谈恋爱了,而且那时候我们特别低调,但我还是被他那帮战友给揪出来。 我不知道是不是职业病的原因,他就是那种什么都会跟你坦白,什么都会跟你报告的那种人,要是在今天我一定会跟他发那种“好人卡”。2013年,他的前女友五一结婚,给他发了请帖,那天晚上他还跑来问我要不要去,我还记得那天晚上我特别支持地说:去啊,她都邀请了,你干嘛不去。 后来我们俩再没提过这个事,五一过了我也没问他,因为我知道他根本就没有假期,人肯定是不可能亲自到的,其实我也是一直把这事装心里的,我就是等着他自己跟我坦白。#p#副标题#e# 大概是暑假了,不知道是谁说起这个事,跟我预想的一样,人肯定是没去的,至于红包送不送到现在我都忘记了。 难不成领导还会批你请假理由为“参加前女友的婚礼”这样的假条,肯定不会的,特别对于这种党国的人,想都别想,过年让你踏踏实实回家就算不错了。当时类似我这点小九九现在想起来我就想给自己几个大耳光子,扇死。 但是别以为我让他去说的是反话,我有时也很奇怪我那到底是什么心理,吃饭的时候这么爱吃醋的一个姑娘那个时候怎么心里还会明晃晃地斩钉截铁地真真实实地让他去参加呢,要是我跟他在一起的话,没准还会跟他去呢。 都说二十多岁是一个特别迷茫的年纪,因为很多未知,不知道你会成为一个什么样的人,还有不知道未来陪伴你走下去的那个人又是谁。然而那时候的我们大概都比较会憧憬,会想跟他一起见家长的情形,会想以后应该在哪座城市生活,会想对于他这种职业,我以后应该要更坚强,什么都要学会,所以从大学时候,我就一直逼着自己独立,逼着自己一个人做很多事,逼着自己什么都要学会。 因为知道未来应该是跟这样的制服男一起生活。即使那时候一年还见不上几天,一年还见不上一次面,晚上要十一点之后才能联系上,有时候突然就会一个星期没有联系,但还是会两个人有很多很多约定与对未来的想象。甚至在很早以前他就说:无论大学这几年之间怎么样,毕业了就在一起吧! 接下来的日子里,还是发生了很多事,跟大多数学生时代的恋爱一样,我们还是分开了。#p#副标题#e# 毕业的时候,他肩上扛上了星星,我也穿起了我的学士服,我们还是没有在一起。那天我突然在我的公众号里面看到了他,其实这两年里,我们几乎删除了对方所有的联系方式,但是有些东西即使删除应该也记在心里面了。 我知道,他知道我的全部动态,而我也对他的生活有所了解。但是我们知道,再也回不去了,我们都趟过了那条河,曾经的美好就让它留在那里吧,错过的人终究不属于你。曾经能在一起促膝而谈去参加他前女友婚礼的我,到今天也变成了他的“前任”。 就像舒淇的那句“最后你还是娶了别人”一样,后来,我还是成为了他的前任。感情真的说不来它究竟是什么样的一种东西,或是一种怎么样的一种味道,但是曾经有过,就已经足够。 青春大概就是这样,不是当初的你们说谎或者承诺的时候不是真的,我依然相信那时候他说的那些话绝对出于真心,我也相信过他曾经许下的那些誓言,只是那份青春年少里的感情终究抵不过缘分的交错,我们都在慢慢地从对方生命里淡去,他身边有爱他的女孩,而我在未来的那么一天也会遇到那个陪伴在自己身边的人。 就在前一秒,我选择删除所有,包括慢慢遗忘,我曾经也以为可以做朋友,但后来发现不再联系才是这段故事最好的结局,要是很多年过去了,还能再某个街头遇见坐下来聊聊家常也未尝不可,我相信时间是个伟大的东西。但是现在,让我们都放下包袱轻轻松松大大方方地去寻找属于各自的幸福。 我想起想起罗茜很快答应了求婚,在自己的婚礼上说的那句话:有人说,你结婚的那个人一定不是你最爱的,我不信,我不信了十几年,可是我输了。#p#副标题#e# 我记得看第一遍的时候,是跟朋友一起看的,当时我们还讨论这个事情:你结婚的那个人是不是你最爱的。 那时候我的答案是:这辈子结婚对象不是你最爱的。 但是后来,我发现心里的很多观点在变,很多想法也在变,我想没有什么能比最后那个陪你走下去的那种爱更可贵吧,那种爱是互相忍耐,风风雨雨走过几十年,是长久,是家庭与温暖,是那种生命里持久的交汇与融入,那个人才是真正爱你的,也是你最爱的。 后来,我们还是没有在一起。但是,曾经陪伴的那一段时光大概也是青春里最美的记忆,有些人,来过就是你遇见他的所有意义。
