人教版物理选修3-3高中7.1:物体是由大量分子组成的(24张PPT)
文档属性
| 名称 | 人教版物理选修3-3高中7.1:物体是由大量分子组成的(24张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 物理 | ||
| 更新时间 | 2020-08-25 00:00:00 | ||
图片预览







文档简介
(共24张PPT)
7.1
物体是由大量分子组成的
第七章
分子动理论
1.物质是由大量分子组成。
2.分子永不停息的做无规则热运动。
3.分子间存在着相互作用的引力和斥力。
分子动理论的基本内容
物质各种各样
各种物质是由什么组成的?
物质是由大量分子组成的
两千多年前,古希腊的著名思想家德谟克利特说:万物都是由极小的微粒组成的。
科学技术发展到现在,这种猜想已被证实。构成物质的单元多种多样,如:原子、离子和分子等.在热学中由于原子、离子、或分子做热运动时遵从相同的规律,所以统称为分子。
物质是由大量分子组成的。
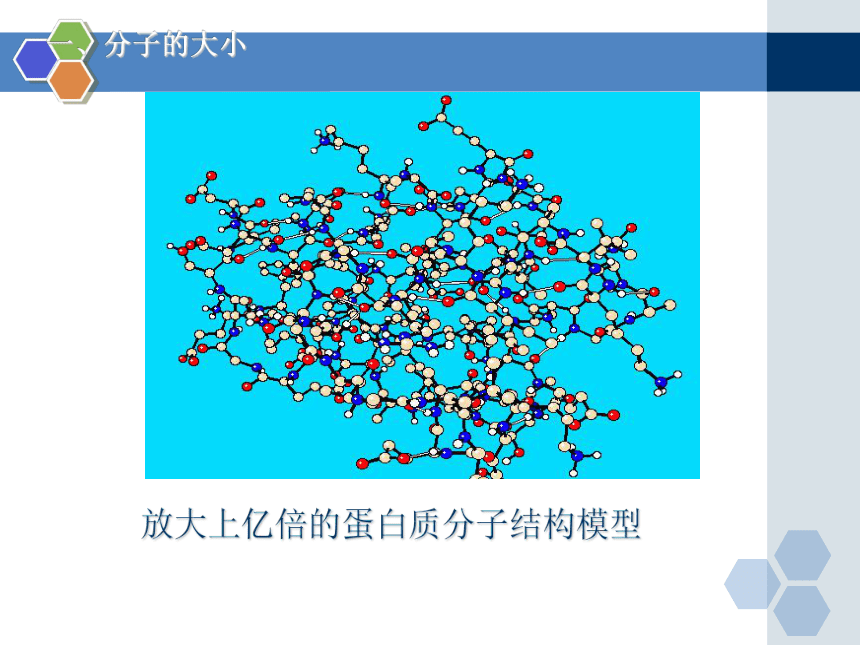
一、分子的大小
放大上亿倍的蛋白质分子结构模型
利用纳米技术把铁原子排成“师”字
1.分子的大小测定方法
(1)用离子显微镜观测
硅表面硅原子的排列
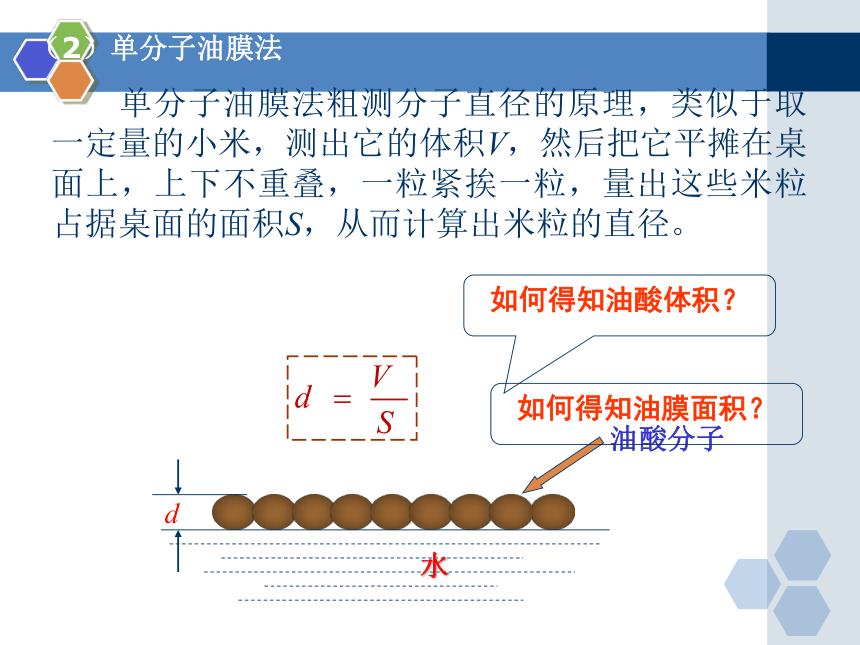
(2)单分子油膜法
单分子油膜法粗测分子直径的原理,类似于取一定量的小米,测出它的体积V,然后把它平摊在桌面上,上下不重叠,一粒紧挨一粒,量出这些米粒占据桌面的面积S,从而计算出米粒的直径。
水
油酸分子
d
如何得知油酸体积?
如何得知油膜面积?
用单分子油膜法测得分子直径的数量级为
利用现代技术,使用不同的方法测出的分子大小并不完全相同,但数量级是一样的,均为
注意:除一些有机物质的大分子外,一般分子的直径数量级为上面数值。以后无特别说明,我们就以上面数值作为分子直径的数量级.
二、阿伏加德罗常数
1.阿伏加德罗常数NA:1摩尔(mol)任何物质所含的微粒数叫做阿伏加德罗常数。
2.阿伏加德罗常数是联系微观世界和宏观世界的桥梁.
二、微观量的估算方法
1.固体或者液体分子的估算方法:
对固体或液体来说,分子间隙数量级远小于分子大小的数量级,所以可以近似认为分子紧密排列,据这一理想化模型,1mol任何固体或液体都含有NA个分子,其摩尔体积Nmol可以认为是NA个分子体积的总和。
如果把分子简化成球体,可进一步求出分子的直径d
二、微观量的估算方法
2、气体分子间平均距离的估算:
气体分子间的间隙不能忽略,设想气体分子平均分布,且每个气体分子平均占有的空间设想成一个小立方体,据这一微观模型,气体分子间的距离就等于小立方体的边长L,即:(d并非分子的直径)。
二、微观量的估算方法
3.物质分子所含分子数的估算:
关键为求出分子的摩尔数,便可以利用阿佛加德罗常数求出含有的分子数
例1:
已知空气的摩尔质量是
则空气中气体分子的平均质量多大?成年人做一次深呼吸,约吸入450
cm3的空气,则做一次深呼吸所吸入的空气质量是多少?所吸入的气体分子数量是多少?(按标准状况估算)
解析
:
1.空气分子的平均质量为:
2.成年人做一次深呼吸所吸入的空气质量为:
3.所吸入的分子数为:
例2:下列叙述中正确的是:
A.
1cm3的氧气中所含有的氧分子数为6.02×1023个
B.
1克氧气中所含有的氧分子数为6
.02
×1023个;
C.
1升氧气中含氧分子数是6
.02
×1023个;
D.
1摩氧气中所含有的氧分子数是6
.02
×1023
摩尔质量=分子量
摩尔体积=摩尔质量/密度
例题3
水的分子量18,水的密度为103kg/m3,阿伏加德罗常数为NA=6.02×1023个/
mol,则:
(1)水的摩尔质量MA=__________
18g/mol
(2)水的摩尔体积VA=__________
MA/ρ=18/1=18cm3/mol
(3)一个水分子的质量m0
=_____________
MA/
NA
=18
/
6.02×1023g
=2.99
×10-26
kg
(4)一个水分子的体积V0
=_____________
VA/
NA
=2.99
×10-23
cm3
(5)将水分子看作球体,分子直径(取1位有效数字)
d=_______________
(6v0/π)-3
=1×10-10m
(6)10g水中含有的分子数目N=___________________
mNA/M=3.344
×1021
※可见阿伏加德罗常数是联系宏观量和微观量的桥梁
例4:已知氢气的摩尔质量是2×10-3kg/mol,水的摩尔质量是1.8×10-2kg/mol,计算1个氢分子和水分子的质量。
解:
已知
MH=2×10-3kg·mol-1
NA=6.02×1023mol-1
同理:一个水分子质量
m水=M水/NA=1.8×10-2/
6.02×1023=3×10-26kg.
例5.若已知铁的原子量是56,铁的密度是7.8×103kg/m3,试
求质量是1g的铁块中铁原子的数目(取1位有效数字)及
一个铁原子的体积.
解:
1g铁的物质量是1/56mol,设其中铁原子的数目是n
:
n=1/56×
NA=1/56×6×1023≈1×1022个.
1g铁的体积v:
V
=m/ρ=1×10-3/7.8×103
≈1×10
–7m3
.
一个铁原子的体积Vo:
Vo=V/n=
(1×10
–7)/
(1×1022
)
≈
1×10
–29
m3.
解析
:
1.空气分子的平均质量为:
2.成年人做一次深呼吸所吸入的空气质量为:
3.所吸入的分子数为:
课堂小结
物质是由大量分子构成的:
1、分子很小,直径数量级10-10
m
(单分子油膜法测直径)
2、分子的质量很小,一般数量级为10-26
kg
3、分子间有间隙
4、阿伏加德罗常数:NA=
6
.02
×1023
mol-1
(1)已知物质的摩尔质量MA,可求出分子质量m0
(其中,VA为摩尔体积,?为物质的密度)
(2)已知物质的量(摩尔数)n,可求出物体所含分子的数目N.
(3)已知物质的摩尔体积VA
,可求出分子的体积
V0
7.1
物体是由大量分子组成的
第七章
分子动理论
1.物质是由大量分子组成。
2.分子永不停息的做无规则热运动。
3.分子间存在着相互作用的引力和斥力。
分子动理论的基本内容
物质各种各样
各种物质是由什么组成的?
物质是由大量分子组成的
两千多年前,古希腊的著名思想家德谟克利特说:万物都是由极小的微粒组成的。
科学技术发展到现在,这种猜想已被证实。构成物质的单元多种多样,如:原子、离子和分子等.在热学中由于原子、离子、或分子做热运动时遵从相同的规律,所以统称为分子。
物质是由大量分子组成的。
一、分子的大小
放大上亿倍的蛋白质分子结构模型
利用纳米技术把铁原子排成“师”字
1.分子的大小测定方法
(1)用离子显微镜观测
硅表面硅原子的排列
(2)单分子油膜法
单分子油膜法粗测分子直径的原理,类似于取一定量的小米,测出它的体积V,然后把它平摊在桌面上,上下不重叠,一粒紧挨一粒,量出这些米粒占据桌面的面积S,从而计算出米粒的直径。
水
油酸分子
d
如何得知油酸体积?
如何得知油膜面积?
用单分子油膜法测得分子直径的数量级为
利用现代技术,使用不同的方法测出的分子大小并不完全相同,但数量级是一样的,均为
注意:除一些有机物质的大分子外,一般分子的直径数量级为上面数值。以后无特别说明,我们就以上面数值作为分子直径的数量级.
二、阿伏加德罗常数
1.阿伏加德罗常数NA:1摩尔(mol)任何物质所含的微粒数叫做阿伏加德罗常数。
2.阿伏加德罗常数是联系微观世界和宏观世界的桥梁.
二、微观量的估算方法
1.固体或者液体分子的估算方法:
对固体或液体来说,分子间隙数量级远小于分子大小的数量级,所以可以近似认为分子紧密排列,据这一理想化模型,1mol任何固体或液体都含有NA个分子,其摩尔体积Nmol可以认为是NA个分子体积的总和。
如果把分子简化成球体,可进一步求出分子的直径d
二、微观量的估算方法
2、气体分子间平均距离的估算:
气体分子间的间隙不能忽略,设想气体分子平均分布,且每个气体分子平均占有的空间设想成一个小立方体,据这一微观模型,气体分子间的距离就等于小立方体的边长L,即:(d并非分子的直径)。
二、微观量的估算方法
3.物质分子所含分子数的估算:
关键为求出分子的摩尔数,便可以利用阿佛加德罗常数求出含有的分子数
例1:
已知空气的摩尔质量是
则空气中气体分子的平均质量多大?成年人做一次深呼吸,约吸入450
cm3的空气,则做一次深呼吸所吸入的空气质量是多少?所吸入的气体分子数量是多少?(按标准状况估算)
解析
:
1.空气分子的平均质量为:
2.成年人做一次深呼吸所吸入的空气质量为:
3.所吸入的分子数为:
例2:下列叙述中正确的是:
A.
1cm3的氧气中所含有的氧分子数为6.02×1023个
B.
1克氧气中所含有的氧分子数为6
.02
×1023个;
C.
1升氧气中含氧分子数是6
.02
×1023个;
D.
1摩氧气中所含有的氧分子数是6
.02
×1023
摩尔质量=分子量
摩尔体积=摩尔质量/密度
例题3
水的分子量18,水的密度为103kg/m3,阿伏加德罗常数为NA=6.02×1023个/
mol,则:
(1)水的摩尔质量MA=__________
18g/mol
(2)水的摩尔体积VA=__________
MA/ρ=18/1=18cm3/mol
(3)一个水分子的质量m0
=_____________
MA/
NA
=18
/
6.02×1023g
=2.99
×10-26
kg
(4)一个水分子的体积V0
=_____________
VA/
NA
=2.99
×10-23
cm3
(5)将水分子看作球体,分子直径(取1位有效数字)
d=_______________
(6v0/π)-3
=1×10-10m
(6)10g水中含有的分子数目N=___________________
mNA/M=3.344
×1021
※可见阿伏加德罗常数是联系宏观量和微观量的桥梁
例4:已知氢气的摩尔质量是2×10-3kg/mol,水的摩尔质量是1.8×10-2kg/mol,计算1个氢分子和水分子的质量。
解:
已知
MH=2×10-3kg·mol-1
NA=6.02×1023mol-1
同理:一个水分子质量
m水=M水/NA=1.8×10-2/
6.02×1023=3×10-26kg.
例5.若已知铁的原子量是56,铁的密度是7.8×103kg/m3,试
求质量是1g的铁块中铁原子的数目(取1位有效数字)及
一个铁原子的体积.
解:
1g铁的物质量是1/56mol,设其中铁原子的数目是n
:
n=1/56×
NA=1/56×6×1023≈1×1022个.
1g铁的体积v:
V
=m/ρ=1×10-3/7.8×103
≈1×10
–7m3
.
一个铁原子的体积Vo:
Vo=V/n=
(1×10
–7)/
(1×1022
)
≈
1×10
–29
m3.
解析
:
1.空气分子的平均质量为:
2.成年人做一次深呼吸所吸入的空气质量为:
3.所吸入的分子数为:
课堂小结
物质是由大量分子构成的:
1、分子很小,直径数量级10-10
m
(单分子油膜法测直径)
2、分子的质量很小,一般数量级为10-26
kg
3、分子间有间隙
4、阿伏加德罗常数:NA=
6
.02
×1023
mol-1
(1)已知物质的摩尔质量MA,可求出分子质量m0
(其中,VA为摩尔体积,?为物质的密度)
(2)已知物质的量(摩尔数)n,可求出物体所含分子的数目N.
(3)已知物质的摩尔体积VA
,可求出分子的体积
V0
