第三单元课题2 原子的结构 同步练习(含解析)
文档属性
| 名称 | 第三单元课题2 原子的结构 同步练习(含解析) |

|
|
| 格式 | doc | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-08-28 00:00:00 | ||
图片预览


文档简介
中小学教育资源及组卷应用平台
初中化学人教版九年级上册 第三单元课题2 原子的结构
一、单选题
1.法国科学家发现一种_?????±????????????_构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”,它与天体中的中子星构成类似,有关该粒子的说法错误的是(? ) 21世纪教育网版权所有
A.?不显电性????????????????????????????????????????????????????????????B.?相当于一个氦原子的质量
C.?失去一个中子后显+1价???????????????????????????????????D.?周期表中没有该“元素”的位置21cnjy.com
2.下面是四种粒子的结构示意图,下列分析错误的是(? )
A.?①③化学性质相似????????B.?②为阴离子????????C.?③④属于同一种元素????????D.?③为第三周期元素的原子
3.钛是一种广泛_?????¨???è???¤????_航海工业的金属。已知一种钛原子核内有22个质子和26个中子,该原子的核外电子数为( ?) 2·1·c·n·j·y
A.?4?????????????????????????????????????????B.?22?????????????????????????????????????????C.?26?????????????????????????????????????????D.?48
4.下列结构示意图表示阴离子的是(? )
A.??????????????????????B.??????????????????????C.??????????????????????D.?
5.元素X的核电荷数为a,它的阳离子 与元素Y的阴离子 的电子层结构相同,则元素Y的核电荷数是(? ) www-2-1-cnjy-com
A.??????????????????????????????B.??????????????????????????????C.??????????????????????????????D.?
6.根据下列结构示意图判断,属于原子且容易失去电子的是( ?)
A.??????????????????????B.??????????????????????C.??????????????????????D.?
7.某元素R的原子序数为m,可形成核外有x个电子的Rn+离子,下列关系式正确的是(? )
A.?m=n????????????????????????????????B.?m=n-x????????????????????????????????C.?m=x-n????????????????????????????????D.?m=n+x
8.一种铁原子的原子核内有26个质子和30个中子,该原子的原子序数为(?? )
A.?4?????????????????????????????????????????B.?26?????????????????????????????????????????C.?30?????????????????????????????????????????D.?56
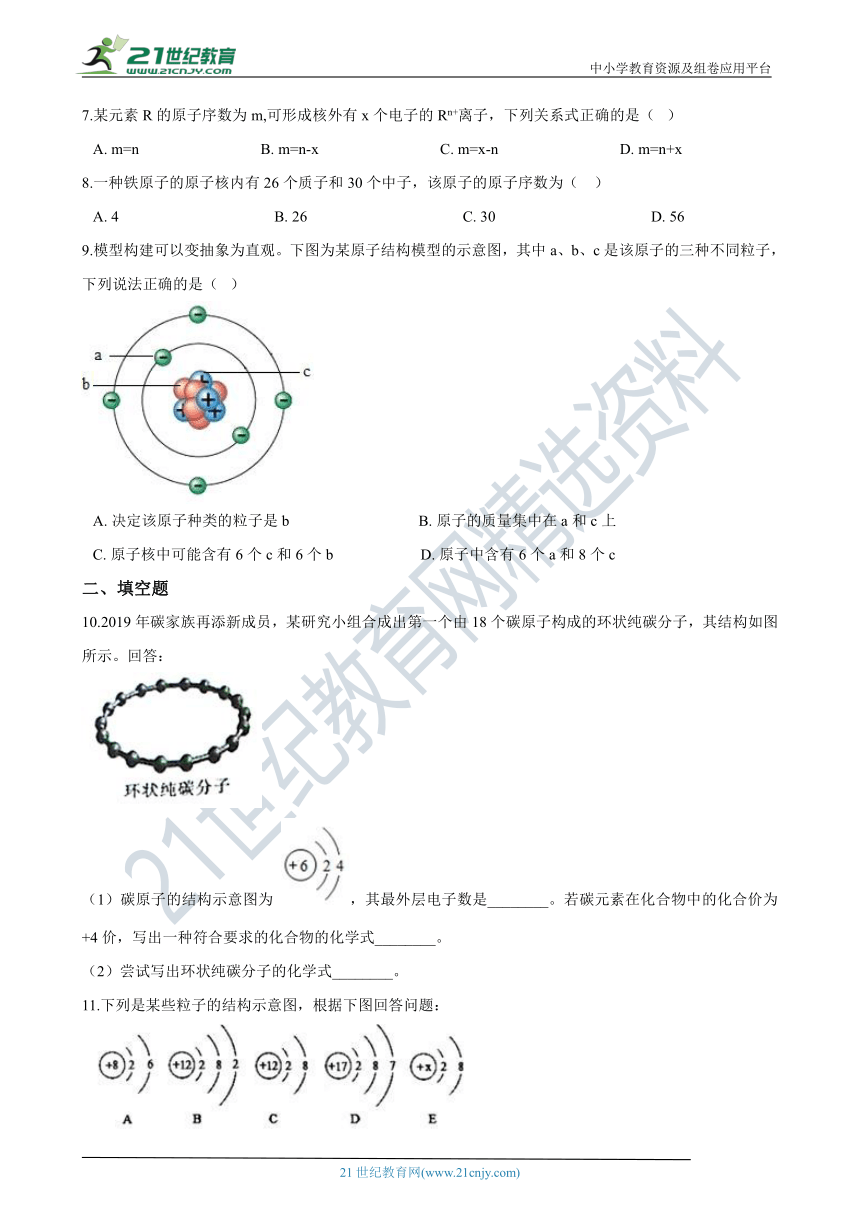
9.模型构建可以变抽象为直观。下图为某原子结构模型的示意图,其中a、b、c是该原子的三种不同粒子,下列说法正确的是( ?) www.21-cn-jy.com
A.?决定该原子种类的粒子是b??????????????????????????????????B.?原子的质量集中在a和c上
C.?原子核中可能含有6个c和6个b???????????????????????D.?原子中含有6个a和8个c
二、填空题
10.2019年碳家族再添新成员,某研究小组合成出第一个由18个碳原子构成的环状纯碳分子,其结构如图所示。回答: 【来源:21cnj*y.co*m】
(1)碳原子的结构示意图为 ,其最外层电子数是________。若碳元素在化合物中的化合价为+4价,写出一种符合要求的化合物的化学式________。
(2)尝试写出环状纯碳分子的化学式________。
11.下列是某些粒子的结构示意图,根据下图回答问题:
(1)A,B,C,D所示的粒子共表示________种元素(填数字)
(2)B所示粒子在化学反应中容易________电子(填“失去”或“得到”)
(3)若E中x=10时,则该粒子属于________(填“原子”或“离子”)
答案解析部分
一、单选题
1. C
解析:A、该微粒只由四个中子构成,中子不带电,因此不显电性,故A不符合题意;
B、因为中子的质量≈质子的质量,该粒子的质量≈一个氦原子的质量=4,故B不符合题意;
C、中子不带电,故“失去一个中子后显+1价”,说法不符合题意,故C符合题意;
D、因为它不是某种元素,而只有中子,故周期表中没有该“元素”的位置,故D不符合题意。
故答案为:C。
分析:只由四个中子构成的粒子,则该微粒无质子,根据“原子序数=核内质子数”,则知它不是某种元素,而只有中子,又知中子不带电。【出处:21教育名师】
2. B
解析:A、元素的化学性_è?¨???è?¨????????±_原子的最外层电子数决定的,①③均为原子,原子的最外层电子数相同,其化学性质也相似,故A选项不符合题意; 【版权所有:21教育】
B、②中原子核内质子数为11,核外电子数是10,核内质子带正电,核外电子带负电,因此②是阳离子,而不是阴离子,故B选项符合题意;
C、核内质子数相同的微粒是同一种元素,可以判断③④属于同一种元素,故C选项不符合题意;
D、元素周期表的周期数等于原子的电子层数,③是原子,且有三个电子层,因此③处在第三周期,故D选项不符合题意。
故答案为:B。
分析:原子的核内质子数等于核外电子数,因此①③是原子,而②④的核内质子数不等于核外电子数,因此是离子。21·世纪*教育网
3. B
解析:由题意一种Ti原子的原子核内有22个质子,根据核电荷数=质子数=电子数,故该钛原子核外的电子数为22。
故答案为:B。
分析:本题难度不是很大,掌握原子中核电荷数=质子数=电子数是解答本题的关键。
4. D
解析:A.该粒子中,质子数=核外电子数,属于原子,故不符合题意;
B.该粒子中,质子数>核外电子数,属于阳离子,故不符合题意;
C.该粒子中,质子数=核外电子数,属于原子,故不符合题意;
D.该粒子中,质子数<核外电子数,属于阴离子,故符合题意。
故答案为:D。
分析:根据微粒结构示意图分析,质子数=电子数,则为原子,质子数>电子数,为阳离子,质子数<电子数,为阴离子。21教育网
5. B
解析:设元素Y的核电荷数是b。a-m=b+n,b=a-m-n。
故答案为:B。
分析:原子失去电子变成阳离子,得到电子变成阴离子。
6. C
解析:A、为氦原子,是稀有气体,不易得电子也不易失电子,故A不符合题意;
B、为碳原子,为非金属元素,不易得电子也不易失电子,只会形成共价化合物,和另外一种元素共享电子,故B不符合题意;21·cn·jy·com
C、为镁原子,为金属元素,易失电子形成阳离子,故C符合题意;
D、为钾离子,最外层电子已达8个,达到稳定结构,不会再失去电子,故D不符合题意.
故答案为:C.
分析:在原子中,质子数=核外电子数,当最外层电子数小于4时,化学反应中失去电子,据此分析
7. D
解析:Rn+离子是表示失去n个电子后形成的阳离子,所以m=n +x。
故答案为:D。
分析:明确由原子变成离子,变化的是核外电子数,不变的是核内质子数。
8. B
解析:在原子中,质子数等于核电荷数等于电子数,铁原子的原子核内有26个质子,故该原子的核外电子数为26, 【来源:21·世纪·教育·网】
故答案为:B。
分析:在原子中,原子序数=原子的质子数
9. C
解析:A、质子数决定元素的种类,决定该原子种类的粒子是c,故A不符合题意;
B、原子的质量主要集中在原子核上,集中在b和c上,故B不符合题意;
C、c是质子,b是中子,质子数可能和中子数相同,则原子核中可能含有6个c和6个b,故C符合题意;
D、在原子中,质子数=核外电子数,a与c的数目一定相同,故D不符合题意。
故答案为:C。
分析:由原子结构模型的示意图可知,c是质子,b是中子,a是核外电子。原子的质量主要集中在原子核上,在原子中,质子数=核外电子数。2-1-c-n-j-y
二、填空题
10. (1)4;
(2)
解析:(1)碳原子的结构示意图为 ,可见其最外层电子数是4。若碳元素在化合物中的化合价为+4价,符合要求的化合物可以是二氧化碳,化学式为 (或碳酸 等)。
(2)环状纯碳分子由18个碳原子构成,化学式为 。
分析:(1)根据碳原子的结构示意图,进行分析。
在化合物中,元素的正负化合价代数和为零,推导出化学式。
(2)一个环状纯碳分子由18个碳原子构成的。21*cnjy*com
11. (1)3
(2)失去
(3)原子
解析:(1)原子核內_???è?¨?????°??????_,就表示不同种的元素,所以A,B,C,D所示的粒子共表示3种元素。
故答案为:1、3;
(2)B所示粒子,最外层电子数又2个电子,在化学反应中容易失去电子,达到8电子的稳定结构。
故答案为:1、失去;
(3)若E中x=10时,则:10=2+8,所以该粒子属于原子。
故答案为:1、原子。 21教育名师原创作品
分析:(1)元素是具有相同质子_??°???????±???????_的总称。
元素不同的本质区别是原子核內的质子数不同。
(2)根据原子的结构示意图可知,当最外层电子数小于4时,反应中易失去电子;当最外层电子数大于4时,反应中易得到电子,达到稳定结构。
(3)在原子中,核电荷数=核内质子数=核外电子数。21*cnjy*com
_21?????????è?????(www.21cnjy.com)_
初中化学人教版九年级上册 第三单元课题2 原子的结构
一、单选题
1.法国科学家发现一种_?????±????????????_构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”,它与天体中的中子星构成类似,有关该粒子的说法错误的是(? ) 21世纪教育网版权所有
A.?不显电性????????????????????????????????????????????????????????????B.?相当于一个氦原子的质量
C.?失去一个中子后显+1价???????????????????????????????????D.?周期表中没有该“元素”的位置21cnjy.com
2.下面是四种粒子的结构示意图,下列分析错误的是(? )
A.?①③化学性质相似????????B.?②为阴离子????????C.?③④属于同一种元素????????D.?③为第三周期元素的原子
3.钛是一种广泛_?????¨???è???¤????_航海工业的金属。已知一种钛原子核内有22个质子和26个中子,该原子的核外电子数为( ?) 2·1·c·n·j·y
A.?4?????????????????????????????????????????B.?22?????????????????????????????????????????C.?26?????????????????????????????????????????D.?48
4.下列结构示意图表示阴离子的是(? )
A.??????????????????????B.??????????????????????C.??????????????????????D.?
5.元素X的核电荷数为a,它的阳离子 与元素Y的阴离子 的电子层结构相同,则元素Y的核电荷数是(? ) www-2-1-cnjy-com
A.??????????????????????????????B.??????????????????????????????C.??????????????????????????????D.?
6.根据下列结构示意图判断,属于原子且容易失去电子的是( ?)
A.??????????????????????B.??????????????????????C.??????????????????????D.?
7.某元素R的原子序数为m,可形成核外有x个电子的Rn+离子,下列关系式正确的是(? )
A.?m=n????????????????????????????????B.?m=n-x????????????????????????????????C.?m=x-n????????????????????????????????D.?m=n+x
8.一种铁原子的原子核内有26个质子和30个中子,该原子的原子序数为(?? )
A.?4?????????????????????????????????????????B.?26?????????????????????????????????????????C.?30?????????????????????????????????????????D.?56
9.模型构建可以变抽象为直观。下图为某原子结构模型的示意图,其中a、b、c是该原子的三种不同粒子,下列说法正确的是( ?) www.21-cn-jy.com
A.?决定该原子种类的粒子是b??????????????????????????????????B.?原子的质量集中在a和c上
C.?原子核中可能含有6个c和6个b???????????????????????D.?原子中含有6个a和8个c
二、填空题
10.2019年碳家族再添新成员,某研究小组合成出第一个由18个碳原子构成的环状纯碳分子,其结构如图所示。回答: 【来源:21cnj*y.co*m】
(1)碳原子的结构示意图为 ,其最外层电子数是________。若碳元素在化合物中的化合价为+4价,写出一种符合要求的化合物的化学式________。
(2)尝试写出环状纯碳分子的化学式________。
11.下列是某些粒子的结构示意图,根据下图回答问题:
(1)A,B,C,D所示的粒子共表示________种元素(填数字)
(2)B所示粒子在化学反应中容易________电子(填“失去”或“得到”)
(3)若E中x=10时,则该粒子属于________(填“原子”或“离子”)
答案解析部分
一、单选题
1. C
解析:A、该微粒只由四个中子构成,中子不带电,因此不显电性,故A不符合题意;
B、因为中子的质量≈质子的质量,该粒子的质量≈一个氦原子的质量=4,故B不符合题意;
C、中子不带电,故“失去一个中子后显+1价”,说法不符合题意,故C符合题意;
D、因为它不是某种元素,而只有中子,故周期表中没有该“元素”的位置,故D不符合题意。
故答案为:C。
分析:只由四个中子构成的粒子,则该微粒无质子,根据“原子序数=核内质子数”,则知它不是某种元素,而只有中子,又知中子不带电。【出处:21教育名师】
2. B
解析:A、元素的化学性_è?¨???è?¨????????±_原子的最外层电子数决定的,①③均为原子,原子的最外层电子数相同,其化学性质也相似,故A选项不符合题意; 【版权所有:21教育】
B、②中原子核内质子数为11,核外电子数是10,核内质子带正电,核外电子带负电,因此②是阳离子,而不是阴离子,故B选项符合题意;
C、核内质子数相同的微粒是同一种元素,可以判断③④属于同一种元素,故C选项不符合题意;
D、元素周期表的周期数等于原子的电子层数,③是原子,且有三个电子层,因此③处在第三周期,故D选项不符合题意。
故答案为:B。
分析:原子的核内质子数等于核外电子数,因此①③是原子,而②④的核内质子数不等于核外电子数,因此是离子。21·世纪*教育网
3. B
解析:由题意一种Ti原子的原子核内有22个质子,根据核电荷数=质子数=电子数,故该钛原子核外的电子数为22。
故答案为:B。
分析:本题难度不是很大,掌握原子中核电荷数=质子数=电子数是解答本题的关键。
4. D
解析:A.该粒子中,质子数=核外电子数,属于原子,故不符合题意;
B.该粒子中,质子数>核外电子数,属于阳离子,故不符合题意;
C.该粒子中,质子数=核外电子数,属于原子,故不符合题意;
D.该粒子中,质子数<核外电子数,属于阴离子,故符合题意。
故答案为:D。
分析:根据微粒结构示意图分析,质子数=电子数,则为原子,质子数>电子数,为阳离子,质子数<电子数,为阴离子。21教育网
5. B
解析:设元素Y的核电荷数是b。a-m=b+n,b=a-m-n。
故答案为:B。
分析:原子失去电子变成阳离子,得到电子变成阴离子。
6. C
解析:A、为氦原子,是稀有气体,不易得电子也不易失电子,故A不符合题意;
B、为碳原子,为非金属元素,不易得电子也不易失电子,只会形成共价化合物,和另外一种元素共享电子,故B不符合题意;21·cn·jy·com
C、为镁原子,为金属元素,易失电子形成阳离子,故C符合题意;
D、为钾离子,最外层电子已达8个,达到稳定结构,不会再失去电子,故D不符合题意.
故答案为:C.
分析:在原子中,质子数=核外电子数,当最外层电子数小于4时,化学反应中失去电子,据此分析
7. D
解析:Rn+离子是表示失去n个电子后形成的阳离子,所以m=n +x。
故答案为:D。
分析:明确由原子变成离子,变化的是核外电子数,不变的是核内质子数。
8. B
解析:在原子中,质子数等于核电荷数等于电子数,铁原子的原子核内有26个质子,故该原子的核外电子数为26, 【来源:21·世纪·教育·网】
故答案为:B。
分析:在原子中,原子序数=原子的质子数
9. C
解析:A、质子数决定元素的种类,决定该原子种类的粒子是c,故A不符合题意;
B、原子的质量主要集中在原子核上,集中在b和c上,故B不符合题意;
C、c是质子,b是中子,质子数可能和中子数相同,则原子核中可能含有6个c和6个b,故C符合题意;
D、在原子中,质子数=核外电子数,a与c的数目一定相同,故D不符合题意。
故答案为:C。
分析:由原子结构模型的示意图可知,c是质子,b是中子,a是核外电子。原子的质量主要集中在原子核上,在原子中,质子数=核外电子数。2-1-c-n-j-y
二、填空题
10. (1)4;
(2)
解析:(1)碳原子的结构示意图为 ,可见其最外层电子数是4。若碳元素在化合物中的化合价为+4价,符合要求的化合物可以是二氧化碳,化学式为 (或碳酸 等)。
(2)环状纯碳分子由18个碳原子构成,化学式为 。
分析:(1)根据碳原子的结构示意图,进行分析。
在化合物中,元素的正负化合价代数和为零,推导出化学式。
(2)一个环状纯碳分子由18个碳原子构成的。21*cnjy*com
11. (1)3
(2)失去
(3)原子
解析:(1)原子核內_???è?¨?????°??????_,就表示不同种的元素,所以A,B,C,D所示的粒子共表示3种元素。
故答案为:1、3;
(2)B所示粒子,最外层电子数又2个电子,在化学反应中容易失去电子,达到8电子的稳定结构。
故答案为:1、失去;
(3)若E中x=10时,则:10=2+8,所以该粒子属于原子。
故答案为:1、原子。 21教育名师原创作品
分析:(1)元素是具有相同质子_??°???????±???????_的总称。
元素不同的本质区别是原子核內的质子数不同。
(2)根据原子的结构示意图可知,当最外层电子数小于4时,反应中易失去电子;当最外层电子数大于4时,反应中易得到电子,达到稳定结构。
(3)在原子中,核电荷数=核内质子数=核外电子数。21*cnjy*com
_21?????????è?????(www.21cnjy.com)_
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
