粤教版九上化学4.3质量守恒定律(共17张PPT)
文档属性
| 名称 | 粤教版九上化学4.3质量守恒定律(共17张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 609.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-08-29 00:00:00 | ||
图片预览






文档简介
(共17张PPT)
已知:原子是化学变化中的最小粒子,大家先猜想一下:
①化学反应的前后,原子的种类有无变化?
②化学反应的前后,原子的个数有无变化?
③化学反应的前后,各种物质的总质量有无变化?
4.3质量守恒定律
学习目标:
1、理解质量守恒定律
并能用它
解释生活中一些现象。
探究活动
方案1.石灰石与稀盐酸的反应
实验现象:产生气泡,天平不平衡
实验现象:产生气泡,天平保持平衡
实验4-8:
实验4-7:
方案2.CuSO4溶液与NaOH溶液反应
实验4-9:
实验现象:产生蓝色沉淀,天平保持平衡
实验结论
天平平衡,
反应前各物质的质量总和m1
反应后各物质的质量总和m2
质量守恒定律
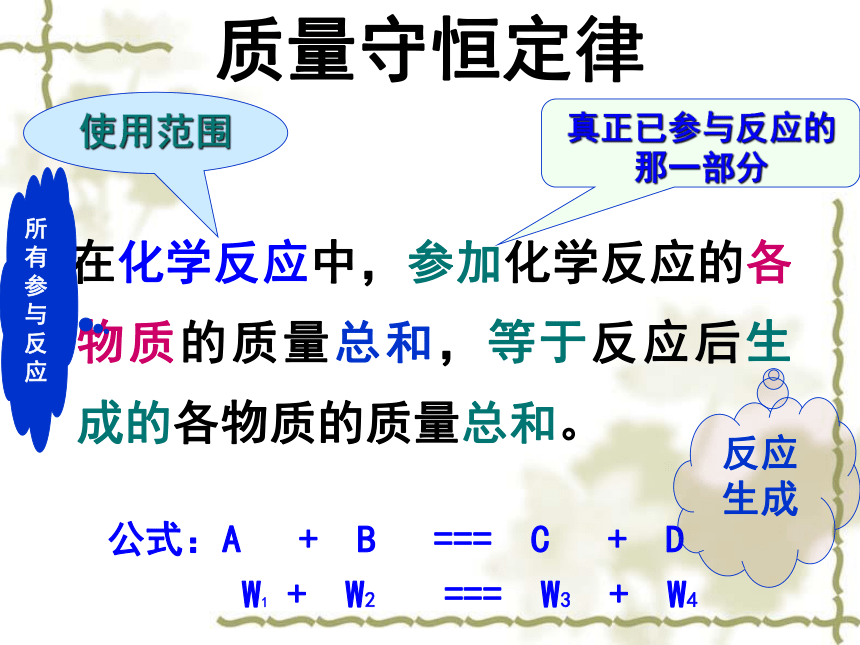
在化学反应中,参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。
公式:A
+
B
===
C
+
D
W1
+
W2
===
W3
+
W4
使用范围
真正已参与反应的那一部分
所有参与反应
反应生成
想一想
为什么参加化学反应的各物质的质量总和等于反应生成的各物质的质量总和?
水分子分解(图解)
O
H
H
O
H
H
水分子
水分子分解(图解)
O
H
H
O
H
H
O
H
H
O
H
H
水分子
氢分子
氧分子
重播
水分子
氧原子
氢原子
氧分子
氢分子
质量守恒的原因:
化学反应前后:
原子的种类、
原子的数目、
原子的质量
均不变。
水分解示意图
水分解示意图
水分子
氧原子
氢原子
氧分子
氢分子
在化学反应中,肯定会发生改变是什么?
分子的种类
【讨论与交流】
某同学在实验中发现:铁器生锈后,质量增加;木材燃烧后,质量减少;镁条燃烧后质量也减少。据此他推断:质量守恒定律有例外。你认为这位同学的推断对吗?
要正确理解、牢固掌握和灵活运用质量守恒定律,必须抓住以下三个守恒。
1.化学反应前后各元素的原子数目守恒
2.化学反应前后各元素的质量守恒
3.化学反应前后各物质质量总和守恒
【总结】
1、确定某物质组成元素种类。
1、某物质加热分解产生氧化铜和水。则该物质含有的全部元素是
(
)
A.Cu、O??
B.Cu、O、H?
?C.O、H??
D.Cu、H
2
、根据蜡烛燃烧后生成水蒸气和二氧化碳的实验事实,可以推断石蜡(蜡烛的主要成分)的组成里一定含有
(
)
A.碳一种元素??
B.氢一种元素
C.碳和氢两种元素??D.碳、氢、氧三种元素
B
C
2、推断反应物或生成物的化学式
1、根据质量守恒定律可知:反应2XY+Y2
=
2Z中,Z的化学式为
(
)
A.XY2??
B.X2Y2??
C.X2Y4??
D.X2Y
2、根据反应3AB
+
C2B3
=
2C
+
3X,判断X的化学式(
)
A、A2B3
B、A3B2
C、AB2
D、A2B
A
C
3.
确定反应物或生成物的质量。
根据质量守恒定律,4g氢气完全燃烧生成了36g水,则参加反应的氧气的质量为
(
)
32g
已知:原子是化学变化中的最小粒子,大家先猜想一下:
①化学反应的前后,原子的种类有无变化?
②化学反应的前后,原子的个数有无变化?
③化学反应的前后,各种物质的总质量有无变化?
4.3质量守恒定律
学习目标:
1、理解质量守恒定律
并能用它
解释生活中一些现象。
探究活动
方案1.石灰石与稀盐酸的反应
实验现象:产生气泡,天平不平衡
实验现象:产生气泡,天平保持平衡
实验4-8:
实验4-7:
方案2.CuSO4溶液与NaOH溶液反应
实验4-9:
实验现象:产生蓝色沉淀,天平保持平衡
实验结论
天平平衡,
反应前各物质的质量总和m1
反应后各物质的质量总和m2
质量守恒定律
在化学反应中,参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。
公式:A
+
B
===
C
+
D
W1
+
W2
===
W3
+
W4
使用范围
真正已参与反应的那一部分
所有参与反应
反应生成
想一想
为什么参加化学反应的各物质的质量总和等于反应生成的各物质的质量总和?
水分子分解(图解)
O
H
H
O
H
H
水分子
水分子分解(图解)
O
H
H
O
H
H
O
H
H
O
H
H
水分子
氢分子
氧分子
重播
水分子
氧原子
氢原子
氧分子
氢分子
质量守恒的原因:
化学反应前后:
原子的种类、
原子的数目、
原子的质量
均不变。
水分解示意图
水分解示意图
水分子
氧原子
氢原子
氧分子
氢分子
在化学反应中,肯定会发生改变是什么?
分子的种类
【讨论与交流】
某同学在实验中发现:铁器生锈后,质量增加;木材燃烧后,质量减少;镁条燃烧后质量也减少。据此他推断:质量守恒定律有例外。你认为这位同学的推断对吗?
要正确理解、牢固掌握和灵活运用质量守恒定律,必须抓住以下三个守恒。
1.化学反应前后各元素的原子数目守恒
2.化学反应前后各元素的质量守恒
3.化学反应前后各物质质量总和守恒
【总结】
1、确定某物质组成元素种类。
1、某物质加热分解产生氧化铜和水。则该物质含有的全部元素是
(
)
A.Cu、O??
B.Cu、O、H?
?C.O、H??
D.Cu、H
2
、根据蜡烛燃烧后生成水蒸气和二氧化碳的实验事实,可以推断石蜡(蜡烛的主要成分)的组成里一定含有
(
)
A.碳一种元素??
B.氢一种元素
C.碳和氢两种元素??D.碳、氢、氧三种元素
B
C
2、推断反应物或生成物的化学式
1、根据质量守恒定律可知:反应2XY+Y2
=
2Z中,Z的化学式为
(
)
A.XY2??
B.X2Y2??
C.X2Y4??
D.X2Y
2、根据反应3AB
+
C2B3
=
2C
+
3X,判断X的化学式(
)
A、A2B3
B、A3B2
C、AB2
D、A2B
A
C
3.
确定反应物或生成物的质量。
根据质量守恒定律,4g氢气完全燃烧生成了36g水,则参加反应的氧气的质量为
(
)
32g
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
