鲁教版九年级上册化学 2.3 原子的构成 课件(21张PPT)
文档属性
| 名称 | 鲁教版九年级上册化学 2.3 原子的构成 课件(21张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-09-01 00:00:00 | ||
图片预览





文档简介
你知道原子核
到底有多大吗?
现代原子结构
现代原子结构
+
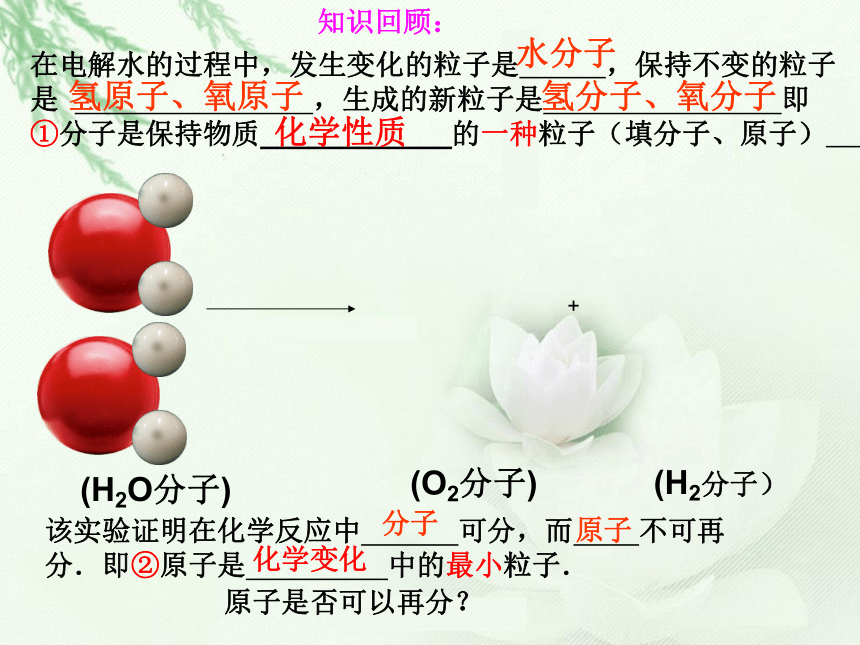
(H2O分子)
(O2分子)
(H2分子)
知识回顾:
在电解水的过程中,发生变化的粒子是 ,保持不变的粒子是 ,生成的新粒子是 即
①分子是保持物质____________的一种粒子(填分子、原子)
该实验证明在化学反应中 可分,而 不可再
分.即②原子是 中的最小粒子.
水分子
氢原子、氧原子
氢分子、氧分子
化学性质
分子
原子
化学变化
原子是否可以再分?
乒乓球
乒乓球
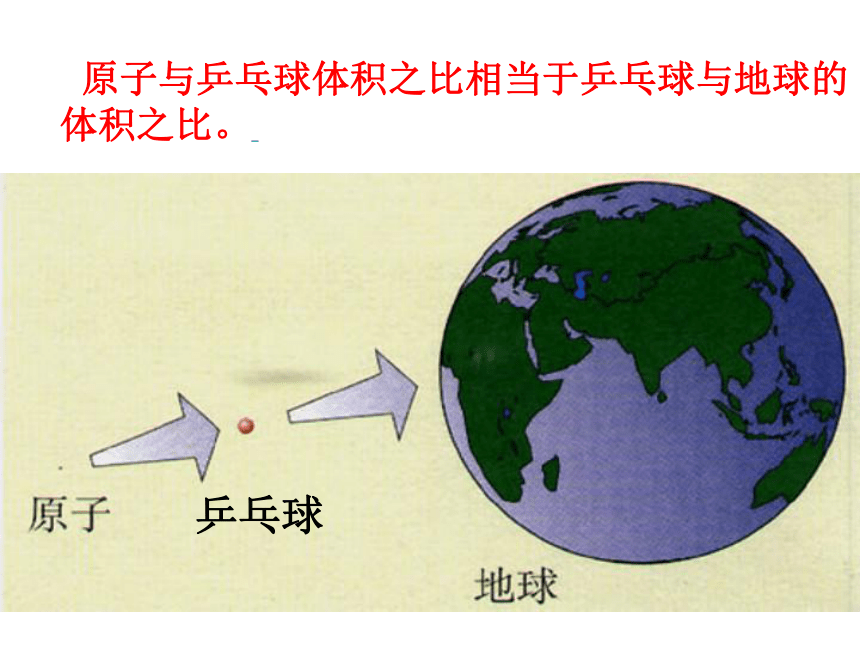
原子与乒乓球体积之比相当于乒乓球与地球的
体积之比。
原子
α粒子束
带正电的粒子质量比电子大的多
原子
α粒子束
α粒子是带正电、质量比电子大的多的微粒
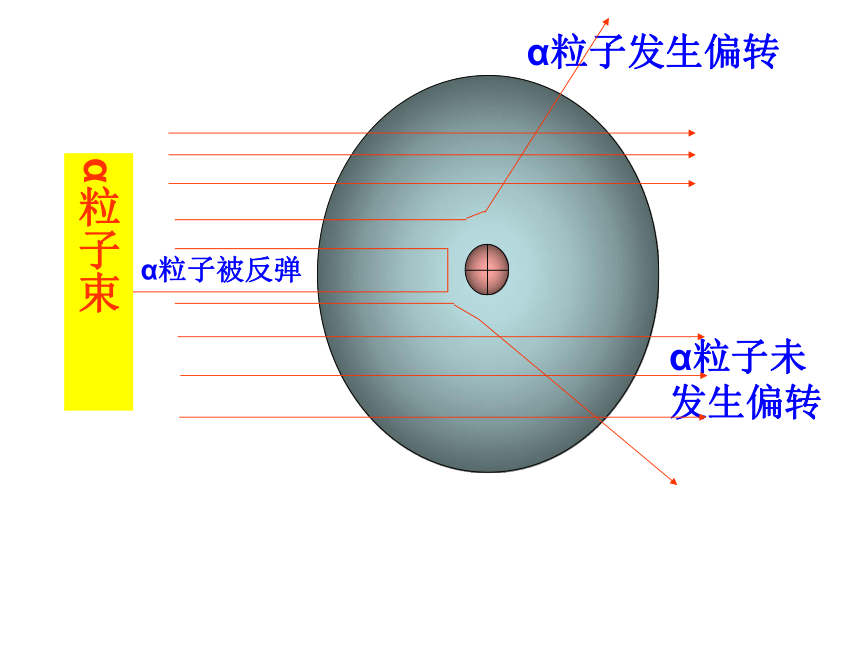
α粒子未发生偏转
α粒子发生偏转
α粒子束
α粒子被反弹
卢瑟福α粒子散射实验
α粒子是带正电的质量比电子大的多
1、大多数α粒子顺利穿透金箔
2、一小部分α粒子改变原来的方向
原子核体积很小,原子内部空间很大
原子核带正电,当带正电的α粒子经过原子核附近时受到排斥而改变方向
3、极少数α粒子被反弹回来
原子核的质量比α粒子大得多,当α粒子正面撞击原子核时, α粒子被反弹回来
假如当时你在现场,你能试着对上述现象加以解释吗?
(提示:考虑原子核的体积、所带正、负电荷、质量)
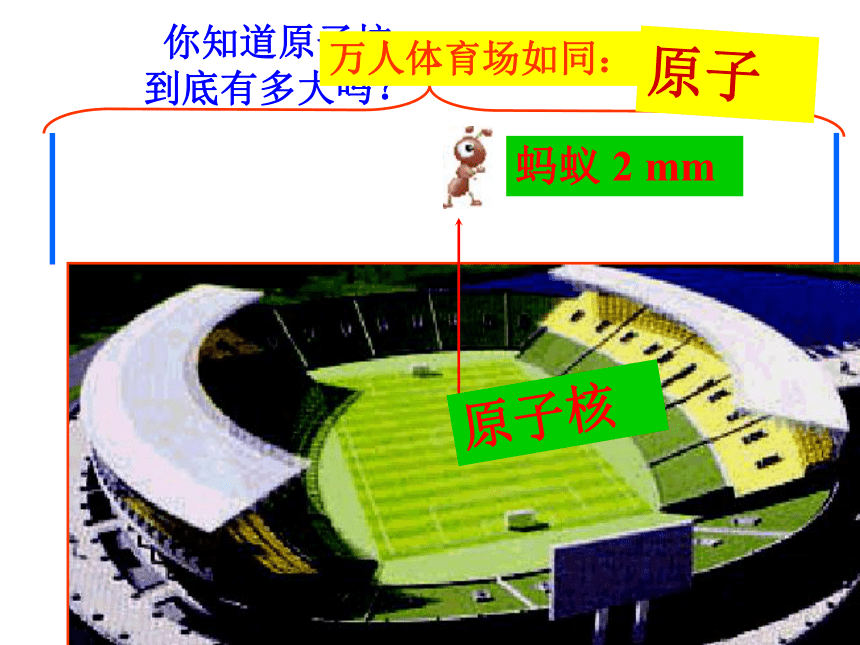
万人体育场如同:
原子
蚂蚁 2 mm
原子核
原子内部有一个很大的空间,电子在原子内绕原子核作高速运动
太阳系
原子内部有一个很大的空间
一、原子的结构
原子
原子核(带正电)
核外电子(带负电)
原子核带的正电荷数=核外电子带的负电荷数
(核电荷数) = 核外电子数
原子不显电性
自从发现原子核和电子后,卢瑟福一直在考虑一个问题:能否打开原子核?原子核内究竟有什么?
1919年,卢瑟福和他的助手用α粒子“轰击”了氮原子核等,发现原子核里面有质子,1个质子带1个单位正电荷。1920年,卢瑟福又预言:原子核中有不带电荷的中性粒子。1932年,经过不少科学家的反复实验后确实发现,α粒子打在铍原子核上,产生了一种高速的不显电性的中性粒子,他们将其命名为中子。中子的质量与质子的质量几乎相等。卢瑟福的预言再一次被证实了。实验证明,原子核确实可以再分为质子和中子。
原子弹的爆炸是由原子核的裂变,释放出巨大的能量引起的.
原子核内有什么?
原子核的构成:
质子
中子
原子
原子核
核外电子
1个质子带一个单位正电荷
1个电子带一个单位负电荷
不带电
在原子中:核电荷数=核内质子数=核外电子数
=质子质量的1/1836
电子
=1.6749×10-27
中子
=1.6726×10-27
质子
质量(kg)
粒子种类
原子的质量几乎全部集中在原子核上
根据表格你得到什么启示?
原子
原 子 核
质子:
一个质子带一个单位的正电荷
中子:
中子不带电
核外电子:
一个电子带一个单位的负电荷
原子核所带的电荷数简称为核电荷数
(不显电性)
质量
原子的质量几乎全部集中在原子核上
核电荷数=质子数
=核外电子数
(带正电)
(带负电)
6
8
6
6
碳—14
6
7
6
6
碳—13
6
6
6
6
碳—12
26
30
26
26
铁
11
12
11
11
钠
8
8
8
8
氧
1
0
1
1
氢
中子数
质子数
核电荷数
核外电子数
原子核
原子种类
分析下表,总结出一些规律
交流共享
2、不同种原子之间有哪些区别?
不同种原子:质子数或核电荷数不同,中子数可能相同
3、所有原子都是由质子、中子、电子构成的吗
氢原子的中子数为0,因此,不是所有的原子都有中子。
1、质子、中子、电子在数量上有什么关系?
核电荷数=质子数=核外电子数,但不一定等于中子数。
课堂练习
质子数
H
O
C
中子数
电子数
Na
原子种类
Cl
N
Al
1
0
6
6
7
7
8
8
12
11
14
13
18
17
质子数
中子数
电子数
分子种类
H2
CO2
O2
H2O
CH4
H2O2
Al2O3
1
6
7
8
11
13
17
2
2
16
16
0
16
核电荷数
=质子数
= 核外电子数
10
8
10
原子构成的物质:
金属
固态非金属
稀有气体
到底有多大吗?
现代原子结构
现代原子结构
+
(H2O分子)
(O2分子)
(H2分子)
知识回顾:
在电解水的过程中,发生变化的粒子是 ,保持不变的粒子是 ,生成的新粒子是 即
①分子是保持物质____________的一种粒子(填分子、原子)
该实验证明在化学反应中 可分,而 不可再
分.即②原子是 中的最小粒子.
水分子
氢原子、氧原子
氢分子、氧分子
化学性质
分子
原子
化学变化
原子是否可以再分?
乒乓球
乒乓球
原子与乒乓球体积之比相当于乒乓球与地球的
体积之比。
原子
α粒子束
带正电的粒子质量比电子大的多
原子
α粒子束
α粒子是带正电、质量比电子大的多的微粒
α粒子未发生偏转
α粒子发生偏转
α粒子束
α粒子被反弹
卢瑟福α粒子散射实验
α粒子是带正电的质量比电子大的多
1、大多数α粒子顺利穿透金箔
2、一小部分α粒子改变原来的方向
原子核体积很小,原子内部空间很大
原子核带正电,当带正电的α粒子经过原子核附近时受到排斥而改变方向
3、极少数α粒子被反弹回来
原子核的质量比α粒子大得多,当α粒子正面撞击原子核时, α粒子被反弹回来
假如当时你在现场,你能试着对上述现象加以解释吗?
(提示:考虑原子核的体积、所带正、负电荷、质量)
万人体育场如同:
原子
蚂蚁 2 mm
原子核
原子内部有一个很大的空间,电子在原子内绕原子核作高速运动
太阳系
原子内部有一个很大的空间
一、原子的结构
原子
原子核(带正电)
核外电子(带负电)
原子核带的正电荷数=核外电子带的负电荷数
(核电荷数) = 核外电子数
原子不显电性
自从发现原子核和电子后,卢瑟福一直在考虑一个问题:能否打开原子核?原子核内究竟有什么?
1919年,卢瑟福和他的助手用α粒子“轰击”了氮原子核等,发现原子核里面有质子,1个质子带1个单位正电荷。1920年,卢瑟福又预言:原子核中有不带电荷的中性粒子。1932年,经过不少科学家的反复实验后确实发现,α粒子打在铍原子核上,产生了一种高速的不显电性的中性粒子,他们将其命名为中子。中子的质量与质子的质量几乎相等。卢瑟福的预言再一次被证实了。实验证明,原子核确实可以再分为质子和中子。
原子弹的爆炸是由原子核的裂变,释放出巨大的能量引起的.
原子核内有什么?
原子核的构成:
质子
中子
原子
原子核
核外电子
1个质子带一个单位正电荷
1个电子带一个单位负电荷
不带电
在原子中:核电荷数=核内质子数=核外电子数
=质子质量的1/1836
电子
=1.6749×10-27
中子
=1.6726×10-27
质子
质量(kg)
粒子种类
原子的质量几乎全部集中在原子核上
根据表格你得到什么启示?
原子
原 子 核
质子:
一个质子带一个单位的正电荷
中子:
中子不带电
核外电子:
一个电子带一个单位的负电荷
原子核所带的电荷数简称为核电荷数
(不显电性)
质量
原子的质量几乎全部集中在原子核上
核电荷数=质子数
=核外电子数
(带正电)
(带负电)
6
8
6
6
碳—14
6
7
6
6
碳—13
6
6
6
6
碳—12
26
30
26
26
铁
11
12
11
11
钠
8
8
8
8
氧
1
0
1
1
氢
中子数
质子数
核电荷数
核外电子数
原子核
原子种类
分析下表,总结出一些规律
交流共享
2、不同种原子之间有哪些区别?
不同种原子:质子数或核电荷数不同,中子数可能相同
3、所有原子都是由质子、中子、电子构成的吗
氢原子的中子数为0,因此,不是所有的原子都有中子。
1、质子、中子、电子在数量上有什么关系?
核电荷数=质子数=核外电子数,但不一定等于中子数。
课堂练习
质子数
H
O
C
中子数
电子数
Na
原子种类
Cl
N
Al
1
0
6
6
7
7
8
8
12
11
14
13
18
17
质子数
中子数
电子数
分子种类
H2
CO2
O2
H2O
CH4
H2O2
Al2O3
1
6
7
8
11
13
17
2
2
16
16
0
16
核电荷数
=质子数
= 核外电子数
10
8
10
原子构成的物质:
金属
固态非金属
稀有气体
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
