山西省运城市景胜中学2020-2021学年高一上学期入学摸底考试化学试题
文档属性
| 名称 | 山西省运城市景胜中学2020-2021学年高一上学期入学摸底考试化学试题 |

|
|
| 格式 | doc | ||
| 文件大小 | 2.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-09-03 00:00:00 | ||
图片预览



文档简介
____________________________________________________________________________________________
景胜中学2020—2021学年高一摸底考试(9月)
化学试题?????时间90分钟??总分100分
本试卷分为选择题和非选择题两部分,共8页,满分100分。考试时间60分钟。
可能用到的相对原子质量:H-l? C-l2? O-16 ? Na-23?? Mg- 24 ? Cu-64
?
第一部分? 选择题(共40分)
?
一、选择题(本题包括20小,题,每小题2分,共40分)
注意:每道选择题有四个选项,其中只有一项符合题意。请用铅笔在答题卡上作答。选错、不选、多选或涂改不清的,均不给分。
1.下列标识,适合贴在液化石油气瓶上的是
?
2.下列变化属于化学变化的是
A.冰升华,形成白雾? ??????????? ?? B.浓盐酸挥发,形成白雾
C.水加热到沸腾,产生白汽??????? ?? D.镁条在空气中燃烧,产生白烟
3.下列有关水的说法,正确的是
A.过滤可将硬水转化为软水
B.天然水经过煮沸会变成纯净水
C.水通电会分解,说明水是纯净物
D.明矾能使天然水中悬浮的杂质沉降下来
4. 下列关于空气成分的说法,正确的是
A.空气中的N2可作为生产氮肥的原料
B.空气中的CO2是导致酸雨的主要原因
??? C.空气中的稀有气体没有任何使用价值
??? D.空气中的O2只有点燃时才能发生化学反应
5.淀粉【(C6H12O6)n】和葡萄糖(C6H12O6)的不同之处是
A.组成元素??????????????? ?? ? ?? B.各元素的质量比??
C.相对分子质量???????????? ??? ? ? D.充分燃烧后的生成物
6.铁是一种应用广泛的金属。下列有关铁的叙述正确的是
A.铁是地壳中含量最多的金属???? ?? B.铁丝在氧气中燃烧生成氧化铁
C.用铁可以回收硝酸银废液中的银?? ? D.炼铁就是把铁矿石变成纯净的氧化铁?
7.下列有关现象的解释,正确的是
??? A.铝锭难被压缩,因为铝原子间没有间隙
??? B.在花园里可嗅到花香,因为分子在不断运动
??? C.石油气加压后贮存在钢瓶中,因为气体分子体积很小
??? D.温度计里的汞柱下降,因为原子随温度的降低而变小
8. 下列操作能达到实验目的的是
A.用过量的稀盐酸除去氧化铜中的铜粉
B.用适量的稀盐酸除去热水瓶胆壁上的水垢
C.用过滤的方法分离NaCl和NaNO3的混合物
D.通过盛氢氧化钠溶液的洗气瓶除去CO2中的HCl气体
9.下列关于化肥的说法正确的是
?A.(NH4)2SO4属于复合肥料
?B.凡施用过化肥的蔬菜都会危害健康
?C.农作物生长,只需要氮肥、磷肥和钾肥
?D.铵态氮肥与熟石灰混合、研磨,能闻到刺激性的气味
10.右图是元素X的原子结构示意图。下列说法正确的是
A.X属于金属元素
B.该原子的核外电子数为17
C.X与氢元素形成的化台物为H2X
D.该原子形成的离子,核外有两个电子层
11.莽草酸是抗H1N1流感病毒药品的主要原料。它的下列性质中,属于化学性质的是
A.易溶于水????????????????? B.熔点为185℃-191℃
C.通常是白色粉末状????????? D.能被酸性高锰酸钾溶液氧化
12.向饱和氯化钠溶液中通入NH3和CO2后,溶液变浑浊(析出碳酸氢钠固体);过滤,滤液中含有氯化铵。下列化学方程式能表示上述反应的是
A.? NH3+CO2+H2O == NH4HCO3↓
B.? 2NH3+CO2+H2O == (NH4)2CO3
C. NaCl+NH3+CO2+H2O == NaHCO3+NH4Cl
D.? NaCl+NH3+CO2+H2O == NaHCO3↓+NH4Cl
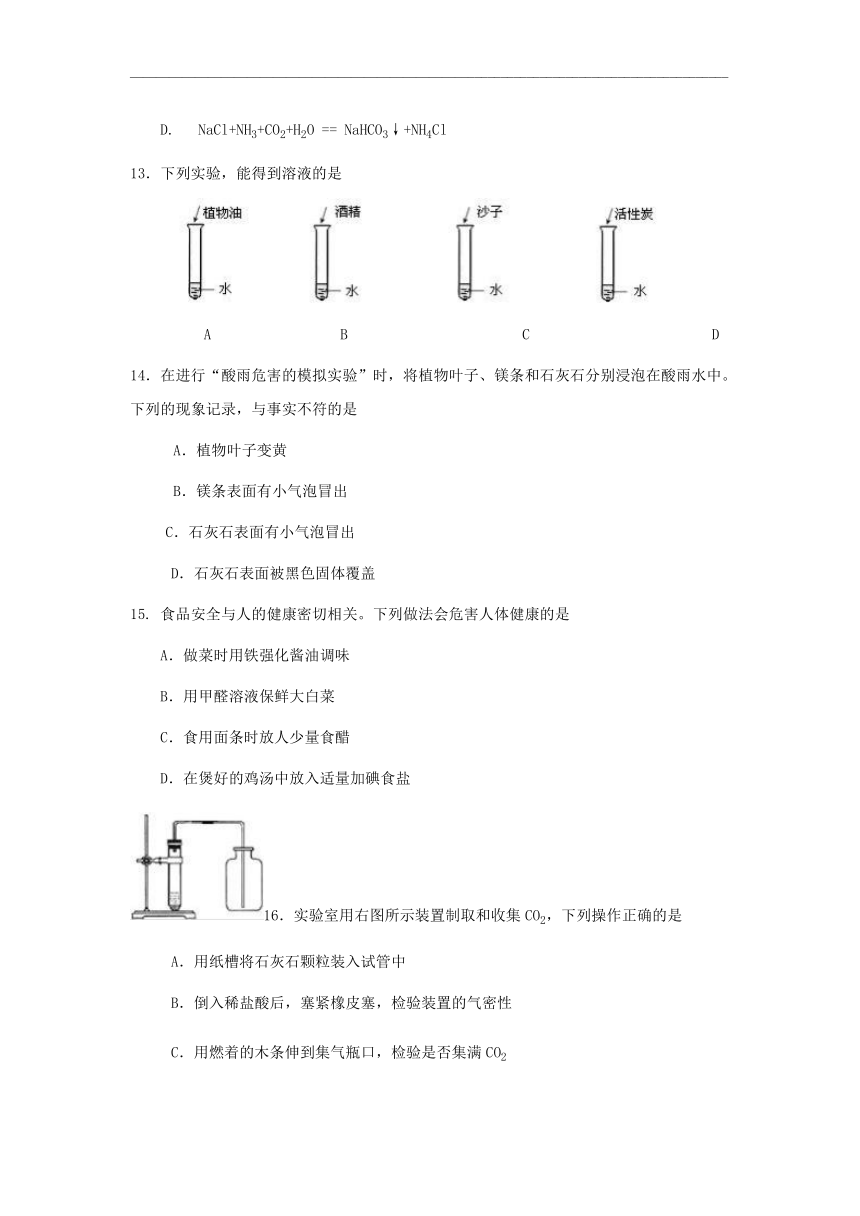
13.下列实验,能得到溶液的是
?
A???????? B??????????? C????????? ?? D
14.在进行“酸雨危害的模拟实验”时,将植物叶子、镁条和石灰石分别浸泡在酸雨水中。下列的现象记录,与事实不符的是
?A.植物叶子变黄
?B.镁条表面有小气泡冒出
C.石灰石表面有小气泡冒出
D.石灰石表面被黑色固体覆盖
15. 食品安全与人的健康密切相关。下列做法会危害人体健康的是
A.做菜时用铁强化酱油调味
B.用甲醛溶液保鲜大白菜
C.食用面条时放人少量食醋
D.在煲好的鸡汤中放入适量加碘食盐
16.实验室用右图所示装置制取和收集CO2,下列操作正确的是
?A.用纸槽将石灰石颗粒装入试管中
?B.倒入稀盐酸后,塞紧橡皮塞,检验装置的气密性
?C.用燃着的木条伸到集气瓶口,检验是否集满CO2
?D.收集满了CO2后,取来干燥的玻璃片,盖住瓶口
17.下列事实与液态二氧化碳的灭火原理无关的是
A.二氧化碳气体是无色无味
B.二氧化碳的密度比空气大
C.二氧化碳不能燃烧,也不支持燃烧
D.液态二氧化碳气化时吸热,能降低可燃物周围的温度
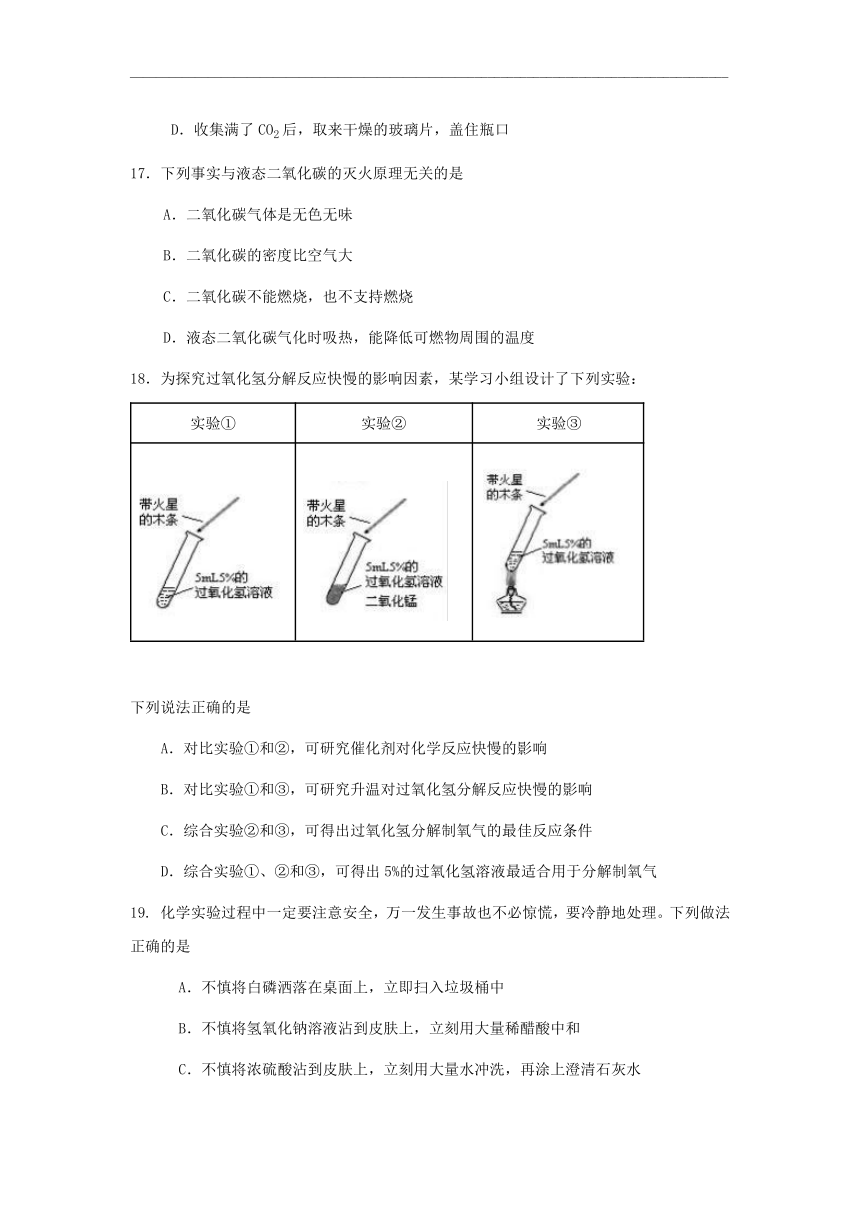
18.为探究过氧化氢分解反应快慢的影响因素,某学习小组设计了下列实验:
实验① 实验② 实验③
? ? ?
?
下列说法正确的是
A.对比实验①和②,可研究催化剂对化学反应快慢的影响
B.对比实验①和③,可研究升温对过氧化氢分解反应快慢的影响
C.综合实验②和③,可得出过氧化氢分解制氧气的最佳反应条件
D.综合实验①、②和③,可得出5%的过氧化氢溶液最适合用于分解制氧气
19. 化学实验过程中一定要注意安全,万一发生事故也不必惊慌,要冷静地处理。下列做法正确的是
? A.不慎将白磷洒落在桌面上,立即扫入垃圾桶中
? B.不慎将氢氧化钠溶液沾到皮肤上,立刻用大量稀醋酸中和
? C.不慎将浓硫酸沾到皮肤上,立刻用大量水冲洗,再涂上澄清石灰水
? D.不慎将酒精灯碰倒,洒出的酒精在桌上燃烧起来,立刻用湿布扑灭
20.下列实验现象预测正确的是
???
实验I??????????????? 实验II???????????? 实验III????? ? ?????? 实验IV
?
A. 实验I:加热后,试管中的粉末逐渐变成黑色
B. 实验II:放置一段时间后,②号烧杯中的液体呈红色
C. 实验III:红磷熄灭后打开止水夹,水面上升,浸没燃烧匙
D. 实验IV:放置一段时间后,饱和CuSO4溶液中出现蓝色晶体
第二部分? 非选择题(共60分)
二、本题包括5小题,共30分。
21.(5分)明胶在生产、生活中应用广泛。
(1)食用明胶由动物骨头、皮肤和筋腱制成的,常用于制作果冻和其它甜点。食用明胶能补充的营养素是?________。如果点燃它,能闻到类似于_________的气味。
(2)工业明胶含较多的重金属离子。这类离子(如Cu2+、Ba2+、Ag+)会使蛋白质丧失生理功能,危害健康。请用化学用语回答下列问题:
①硫酸铜、氯化钡和氯化钠这三种物质中,不含重金属离子的是?_________? ;
②医疗上,制作“钡餐”不能用碳酸钡;因碳酸钡遇人体胃液中的盐酸会反应,生成可溶的钡盐使人中毒。此反应的化学方程式是_________。
22. (7分)下表是NaCl和KNO3的部分溶解度数据。
温度(℃) 溶解度(g) 0 10 20 30 40 50
NaCl 35.7 35.8 36.0 36.3 36.6 37.0
KNO3 13.3 20.9 31.6 45.8 63.9 85.5
(1)根据上表绘制KNO3和NaCl的溶解度曲线。
?
(2)在 _________℃时,KNO3和NaCl的溶解度相等。
(3)现有95℃的248g溶液,内含110gKNO3和38gNaCl,则此溶液中水的质量为______ g。将此溶液降温到20℃,过滤,可得到约 _________ g固体。
23.(6分)某氢氧化钠固体样品中混有少量氯化钠。有一兴趣小组,称取该固体样品10.0g,进行了如下实验:
请回答下列问题:
(1)加入过量氯化镁溶液后,发生反应的化学方程式是_________
。
(2)滤液Ⅰ中含有的阳离子是??_________?(用离子符号表示)。
(3)混合物中氢氧化钠的质量分数为?_________ 。
24.(7分)硫元素有-2、+4和+6价。
(1)请用化学式表示硫元素的氧化物:_________。
(2)观察以下反应微观示意图,并根据此图填空。
?
用化学用语表示反应后的生成物(包括粒子个数):_________? 。
?
(3)有一实验装置如图所示,瓶内气体均为无色。实验时,抽开两个集气瓶中间的玻璃片,保持瓶口紧对,一段时间后,可观察到两集气瓶内壁均附有淡黄色固体颗粒。请回答下列问题:
①请写出此反应的化学方程式:_________
。
②已知,反应前两瓶气体的分子数相等。则反应后瓶内剩余的气体是_________(填化学式)。
25.(5分)硫酸铜晶体常用于农业、渔业的杀虫、杀菌剂。以下是由废铜料(含铁)生产硫酸铜晶体的流程。
?
?
(1)?物质B的化学式为_________,试剂X的名称是_________ 。
(2)反应③的化学方程式为_________?????????????????????????? ;
(3)已知:Cu+2H2SO4(浓)???? ? CuSO4+ SO2↑+2H2O。从环保和经济的角度比较途径I和途径Ⅱ,可以得出途径I的优点是:不产生有害气体和?_________??。?
三、本题包括4小题,共30分。
26.(5分)某小组做过滤粗盐水和配制溶液的实验。
(1)请指出右图所示过滤操作中的两处错误:_________.
;_____ 。
(2)下图是配制50g质量分数为10%氢氧化钠溶液的实验操作。
?
?
①a操作中的错误是_________________________________________________________。
②下列操作,会使所配溶液的溶质质量分数偏低的是__________。
A.a操作中砝码和氢氧化钠放错盘,砝码质量为5g
B.b操作中读数为50 mL
C.进行c操作时有少量水溅出
?27.(8分)SO2易溶于水,密度比空气大。
(1)用反应Na2SO3(固)+ H2SO4?=== Na2SO4+SO2↑+H2O制取SO2,备选仪器装置如下。
?
?
①装置A的名称为??_________ ;仪器F的名称为_________?。
②要组装SO2的发生装置,需选择上图中的??_________??(填相应的编号)。
③若用D、H组合收集SO2,则进气口是?_________ (填“a”或“b”)。
(2)某同学想通过以下3个实验,验证二氧化硫会与水反应生成酸。请分析回答问题。
实验l:取一片干燥的紫色石蕊试纸,往试纸上滴上几滴水。
实验2:······
实验3:将二氧化硫通入盛有水的试管中,之后用胶头滴管取试管中液体,滴到干燥的紫色石蕊试纸上。
②?实验1的目的是:?_________;
②实验2的目的是:________;?
实验2的操作与现象是:?_________ 。
?
28.(9分)资料表明,CH4有还原性。甲、乙两位同学设计以下装置,探究CH4还原CuO的生成物。请按要求填空。
(1)生成物假设
假设1:Cu、CO、H2O
假设2:Cu、H2O、???????
假设3:Cu、CO、CO2、H2O
(2)操作设计
甲同学设计了4项实验操作:
①通入CH4?? ②停止通CH4? ③点燃酒精灯加热? ④停止加热。乙同学认为还应补充操作⑤??_________?。这5项操作的正确顺序是_________ (填编号)。
(3)实验记录与数据处理
①实验时,A装置中能观察到的现象是_________? 。
②实验过程中记录的实验数据如下:
? 装置A 装置B 装置C
实验前的质量(g) 150.0 256.6 156.8
实验后的质量(g) 147.2 258.4 157.9
请根据上表数据计算出:此反应各生成物的质量比?? ?????????????????????????
(
4)实验结论与讨论
①根据实验现象及数据判断,原假设_________是正确的。
②实验时,若先加热A中试管,再通入CH4,可能会引起?_________ 。
29.(8分)实验台上摆放了六瓶液体试剂(如下图所示)。
?
(1)上图的第4瓶的标签破损了。从物质类别上判断,这瓶试剂可能是??_________?? 。
A.酸????? B.碱?????C.盐?? ? D. 氧化物
(2)小明用pH试纸测试此试剂的酸碱度。正确的操作应该是:在白瓷板或玻璃片上放一小片pH试纸,将被测液滴到试纸上,?_________?,即可得出被测液的pH。实验结果:此试剂的pH值为10。
?(3)小俊利用上图试剂鉴别出,这瓶试剂是K2CO3溶液。请按小俊的做法,填写实验报告。
操作步骤 实验现象 结论及化学方程式
? ? ?
? 结论:
?
化学方程式:
?
?
?
?
?
?
?
?
?
?
?
?
高一化学参考答案
一、选择题(本题包括20小题,每小题2分,共40分)
题号 1 2 3 4 5 6 7 8 9 10
答案 A D D A C C B B D B
题号 11 12 13 14 15 16 17 18 19 20
答案 D D B D B C A B D D
二、本题包括5小题,共30分。
21.(5分)
(1)蛋白质?? 烧焦羽毛 (各1分)
(2)NaCl(1分)??? BaCO3?+2HCl= BaCl2?+ H2O +CO2↑(2分,配平和条件合扣1分)
22.(7分)
(1)(图示如右,2分)?
(2)23℃(1分,22~24℃均可)
(3)?100 (2分),?
?80.4 (2分)
23. (共6分)
(1)MgCl2 + 2NaOH == Mg(OH)2↓+ 2NaCl (2分,配平和条件合扣1分)
(2)Na+?、? Mg2+?(2分,有错得0分)
(3)80% (2分)
24.(7分)
(1)?SO2?? SO3?(各1分)
(2)?3S?? 2 H2O (各1分)
(3) ①SO2+2H2S === 2H2O + 3S↓(2分,配平和条件合扣1分)?
?②SO2? (1分)
25.(5分)
??? (1)?CuO (1分)??? 稀硫酸(1分)
??? (2)?CuO+ H2SO4=== CuSO4+H2O (2分,配平和条件合扣1分)
??? (3) 硫酸的利用率高?(1分)???? (合理答案均给分)
三、本题包括4小题,共30分。
26.(5分)
(1)未用玻璃棒引流;滤纸高出漏斗边缘。(各1分)(或“滤纸未紧贴漏斗内壁“、 “漏斗下端尖嘴未紧靠烧杯B的内壁”;无顺序要求,合理均可)
(2)①氢氧化钠直接放在纸上称量(1分)? ②?B(2分)
27.(8分)
(1)①铁架台?? 水槽(各1分)? ②ABC(1分)? ③?b(1分)
(2)①证明水不能使紫色石蕊变红(1分)
②证明二氧化硫不能使紫色石蕊变红(1分);将干燥的紫色石蕊试纸放入SO2中(1分),试纸不变色(1分)。
28.(9分)
(1)CO2(1分)
(2)检查装置气密性(1分) ⑤①③④②(2分)
(3)①?黑色粉末逐渐变成红色(1分)?
②?m(Cu) : m(CO) : m(CO2) : m(H2O) = 112 : 7 : 11 : 18? (2分)
(4)①?3(1分) ??? ②?CH4在装置A中剧烈燃烧,引起爆炸(1分)
29.(共8分)
(1)A? (1分)
(2)把试纸显示的颜色与标准比色卡比较 (1分)
(3)步骤2分,现象1分,结论1分,化学方程式?2分。
操作步骤 实验现象 结论及化学方程式
取少量标签破损的溶液于试管中(1分),滴入盐酸(1分),振荡。 有气泡产生(1分) 结论:标签破损的溶液是碳酸钾溶液。(1分)
化学方程式:
K2CO3?+2HCl ==2KCl +CO2↑+ H2O (2分,配平和条件合扣1分)
或:
操作步骤 实验现象 结论及化学方程式
取少量标签破损的溶液于试管中(1分),滴入氢氧化钙溶液(或氯化钡溶液)(1分),振荡。 有白色沉淀(溶液浑浊)。(1分) 结论:标签破损的溶液是碳酸钾溶液。(1分)
化学方程式:
K2CO3?+Ca(OH)2?== CaCO3↓ +2KOH(2分,配平和条件合扣1分)
景胜中学2020—2021学年高一摸底考试(9月)
化学试题?????时间90分钟??总分100分
本试卷分为选择题和非选择题两部分,共8页,满分100分。考试时间60分钟。
可能用到的相对原子质量:H-l? C-l2? O-16 ? Na-23?? Mg- 24 ? Cu-64
?
第一部分? 选择题(共40分)
?
一、选择题(本题包括20小,题,每小题2分,共40分)
注意:每道选择题有四个选项,其中只有一项符合题意。请用铅笔在答题卡上作答。选错、不选、多选或涂改不清的,均不给分。
1.下列标识,适合贴在液化石油气瓶上的是
?
2.下列变化属于化学变化的是
A.冰升华,形成白雾? ??????????? ?? B.浓盐酸挥发,形成白雾
C.水加热到沸腾,产生白汽??????? ?? D.镁条在空气中燃烧,产生白烟
3.下列有关水的说法,正确的是
A.过滤可将硬水转化为软水
B.天然水经过煮沸会变成纯净水
C.水通电会分解,说明水是纯净物
D.明矾能使天然水中悬浮的杂质沉降下来
4. 下列关于空气成分的说法,正确的是
A.空气中的N2可作为生产氮肥的原料
B.空气中的CO2是导致酸雨的主要原因
??? C.空气中的稀有气体没有任何使用价值
??? D.空气中的O2只有点燃时才能发生化学反应
5.淀粉【(C6H12O6)n】和葡萄糖(C6H12O6)的不同之处是
A.组成元素??????????????? ?? ? ?? B.各元素的质量比??
C.相对分子质量???????????? ??? ? ? D.充分燃烧后的生成物
6.铁是一种应用广泛的金属。下列有关铁的叙述正确的是
A.铁是地壳中含量最多的金属???? ?? B.铁丝在氧气中燃烧生成氧化铁
C.用铁可以回收硝酸银废液中的银?? ? D.炼铁就是把铁矿石变成纯净的氧化铁?
7.下列有关现象的解释,正确的是
??? A.铝锭难被压缩,因为铝原子间没有间隙
??? B.在花园里可嗅到花香,因为分子在不断运动
??? C.石油气加压后贮存在钢瓶中,因为气体分子体积很小
??? D.温度计里的汞柱下降,因为原子随温度的降低而变小
8. 下列操作能达到实验目的的是
A.用过量的稀盐酸除去氧化铜中的铜粉
B.用适量的稀盐酸除去热水瓶胆壁上的水垢
C.用过滤的方法分离NaCl和NaNO3的混合物
D.通过盛氢氧化钠溶液的洗气瓶除去CO2中的HCl气体
9.下列关于化肥的说法正确的是
?A.(NH4)2SO4属于复合肥料
?B.凡施用过化肥的蔬菜都会危害健康
?C.农作物生长,只需要氮肥、磷肥和钾肥
?D.铵态氮肥与熟石灰混合、研磨,能闻到刺激性的气味
10.右图是元素X的原子结构示意图。下列说法正确的是
A.X属于金属元素
B.该原子的核外电子数为17
C.X与氢元素形成的化台物为H2X
D.该原子形成的离子,核外有两个电子层
11.莽草酸是抗H1N1流感病毒药品的主要原料。它的下列性质中,属于化学性质的是
A.易溶于水????????????????? B.熔点为185℃-191℃
C.通常是白色粉末状????????? D.能被酸性高锰酸钾溶液氧化
12.向饱和氯化钠溶液中通入NH3和CO2后,溶液变浑浊(析出碳酸氢钠固体);过滤,滤液中含有氯化铵。下列化学方程式能表示上述反应的是
A.? NH3+CO2+H2O == NH4HCO3↓
B.? 2NH3+CO2+H2O == (NH4)2CO3
C. NaCl+NH3+CO2+H2O == NaHCO3+NH4Cl
D.? NaCl+NH3+CO2+H2O == NaHCO3↓+NH4Cl
13.下列实验,能得到溶液的是
?
A???????? B??????????? C????????? ?? D
14.在进行“酸雨危害的模拟实验”时,将植物叶子、镁条和石灰石分别浸泡在酸雨水中。下列的现象记录,与事实不符的是
?A.植物叶子变黄
?B.镁条表面有小气泡冒出
C.石灰石表面有小气泡冒出
D.石灰石表面被黑色固体覆盖
15. 食品安全与人的健康密切相关。下列做法会危害人体健康的是
A.做菜时用铁强化酱油调味
B.用甲醛溶液保鲜大白菜
C.食用面条时放人少量食醋
D.在煲好的鸡汤中放入适量加碘食盐
16.实验室用右图所示装置制取和收集CO2,下列操作正确的是
?A.用纸槽将石灰石颗粒装入试管中
?B.倒入稀盐酸后,塞紧橡皮塞,检验装置的气密性
?C.用燃着的木条伸到集气瓶口,检验是否集满CO2
?D.收集满了CO2后,取来干燥的玻璃片,盖住瓶口
17.下列事实与液态二氧化碳的灭火原理无关的是
A.二氧化碳气体是无色无味
B.二氧化碳的密度比空气大
C.二氧化碳不能燃烧,也不支持燃烧
D.液态二氧化碳气化时吸热,能降低可燃物周围的温度
18.为探究过氧化氢分解反应快慢的影响因素,某学习小组设计了下列实验:
实验① 实验② 实验③
? ? ?
?
下列说法正确的是
A.对比实验①和②,可研究催化剂对化学反应快慢的影响
B.对比实验①和③,可研究升温对过氧化氢分解反应快慢的影响
C.综合实验②和③,可得出过氧化氢分解制氧气的最佳反应条件
D.综合实验①、②和③,可得出5%的过氧化氢溶液最适合用于分解制氧气
19. 化学实验过程中一定要注意安全,万一发生事故也不必惊慌,要冷静地处理。下列做法正确的是
? A.不慎将白磷洒落在桌面上,立即扫入垃圾桶中
? B.不慎将氢氧化钠溶液沾到皮肤上,立刻用大量稀醋酸中和
? C.不慎将浓硫酸沾到皮肤上,立刻用大量水冲洗,再涂上澄清石灰水
? D.不慎将酒精灯碰倒,洒出的酒精在桌上燃烧起来,立刻用湿布扑灭
20.下列实验现象预测正确的是
???
实验I??????????????? 实验II???????????? 实验III????? ? ?????? 实验IV
?
A. 实验I:加热后,试管中的粉末逐渐变成黑色
B. 实验II:放置一段时间后,②号烧杯中的液体呈红色
C. 实验III:红磷熄灭后打开止水夹,水面上升,浸没燃烧匙
D. 实验IV:放置一段时间后,饱和CuSO4溶液中出现蓝色晶体
第二部分? 非选择题(共60分)
二、本题包括5小题,共30分。
21.(5分)明胶在生产、生活中应用广泛。
(1)食用明胶由动物骨头、皮肤和筋腱制成的,常用于制作果冻和其它甜点。食用明胶能补充的营养素是?________。如果点燃它,能闻到类似于_________的气味。
(2)工业明胶含较多的重金属离子。这类离子(如Cu2+、Ba2+、Ag+)会使蛋白质丧失生理功能,危害健康。请用化学用语回答下列问题:
①硫酸铜、氯化钡和氯化钠这三种物质中,不含重金属离子的是?_________? ;
②医疗上,制作“钡餐”不能用碳酸钡;因碳酸钡遇人体胃液中的盐酸会反应,生成可溶的钡盐使人中毒。此反应的化学方程式是_________。
22. (7分)下表是NaCl和KNO3的部分溶解度数据。
温度(℃) 溶解度(g) 0 10 20 30 40 50
NaCl 35.7 35.8 36.0 36.3 36.6 37.0
KNO3 13.3 20.9 31.6 45.8 63.9 85.5
(1)根据上表绘制KNO3和NaCl的溶解度曲线。
?
(2)在 _________℃时,KNO3和NaCl的溶解度相等。
(3)现有95℃的248g溶液,内含110gKNO3和38gNaCl,则此溶液中水的质量为______ g。将此溶液降温到20℃,过滤,可得到约 _________ g固体。
23.(6分)某氢氧化钠固体样品中混有少量氯化钠。有一兴趣小组,称取该固体样品10.0g,进行了如下实验:
请回答下列问题:
(1)加入过量氯化镁溶液后,发生反应的化学方程式是_________
。
(2)滤液Ⅰ中含有的阳离子是??_________?(用离子符号表示)。
(3)混合物中氢氧化钠的质量分数为?_________ 。
24.(7分)硫元素有-2、+4和+6价。
(1)请用化学式表示硫元素的氧化物:_________。
(2)观察以下反应微观示意图,并根据此图填空。
?
用化学用语表示反应后的生成物(包括粒子个数):_________? 。
?
(3)有一实验装置如图所示,瓶内气体均为无色。实验时,抽开两个集气瓶中间的玻璃片,保持瓶口紧对,一段时间后,可观察到两集气瓶内壁均附有淡黄色固体颗粒。请回答下列问题:
①请写出此反应的化学方程式:_________
。
②已知,反应前两瓶气体的分子数相等。则反应后瓶内剩余的气体是_________(填化学式)。
25.(5分)硫酸铜晶体常用于农业、渔业的杀虫、杀菌剂。以下是由废铜料(含铁)生产硫酸铜晶体的流程。
?
?
(1)?物质B的化学式为_________,试剂X的名称是_________ 。
(2)反应③的化学方程式为_________?????????????????????????? ;
(3)已知:Cu+2H2SO4(浓)???? ? CuSO4+ SO2↑+2H2O。从环保和经济的角度比较途径I和途径Ⅱ,可以得出途径I的优点是:不产生有害气体和?_________??。?
三、本题包括4小题,共30分。
26.(5分)某小组做过滤粗盐水和配制溶液的实验。
(1)请指出右图所示过滤操作中的两处错误:_________.
;_____ 。
(2)下图是配制50g质量分数为10%氢氧化钠溶液的实验操作。
?
?
①a操作中的错误是_________________________________________________________。
②下列操作,会使所配溶液的溶质质量分数偏低的是__________。
A.a操作中砝码和氢氧化钠放错盘,砝码质量为5g
B.b操作中读数为50 mL
C.进行c操作时有少量水溅出
?27.(8分)SO2易溶于水,密度比空气大。
(1)用反应Na2SO3(固)+ H2SO4?=== Na2SO4+SO2↑+H2O制取SO2,备选仪器装置如下。
?
?
①装置A的名称为??_________ ;仪器F的名称为_________?。
②要组装SO2的发生装置,需选择上图中的??_________??(填相应的编号)。
③若用D、H组合收集SO2,则进气口是?_________ (填“a”或“b”)。
(2)某同学想通过以下3个实验,验证二氧化硫会与水反应生成酸。请分析回答问题。
实验l:取一片干燥的紫色石蕊试纸,往试纸上滴上几滴水。
实验2:······
实验3:将二氧化硫通入盛有水的试管中,之后用胶头滴管取试管中液体,滴到干燥的紫色石蕊试纸上。
②?实验1的目的是:?_________;
②实验2的目的是:________;?
实验2的操作与现象是:?_________ 。
?
28.(9分)资料表明,CH4有还原性。甲、乙两位同学设计以下装置,探究CH4还原CuO的生成物。请按要求填空。
(1)生成物假设
假设1:Cu、CO、H2O
假设2:Cu、H2O、???????
假设3:Cu、CO、CO2、H2O
(2)操作设计
甲同学设计了4项实验操作:
①通入CH4?? ②停止通CH4? ③点燃酒精灯加热? ④停止加热。乙同学认为还应补充操作⑤??_________?。这5项操作的正确顺序是_________ (填编号)。
(3)实验记录与数据处理
①实验时,A装置中能观察到的现象是_________? 。
②实验过程中记录的实验数据如下:
? 装置A 装置B 装置C
实验前的质量(g) 150.0 256.6 156.8
实验后的质量(g) 147.2 258.4 157.9
请根据上表数据计算出:此反应各生成物的质量比?? ?????????????????????????
(
4)实验结论与讨论
①根据实验现象及数据判断,原假设_________是正确的。
②实验时,若先加热A中试管,再通入CH4,可能会引起?_________ 。
29.(8分)实验台上摆放了六瓶液体试剂(如下图所示)。
?
(1)上图的第4瓶的标签破损了。从物质类别上判断,这瓶试剂可能是??_________?? 。
A.酸????? B.碱?????C.盐?? ? D. 氧化物
(2)小明用pH试纸测试此试剂的酸碱度。正确的操作应该是:在白瓷板或玻璃片上放一小片pH试纸,将被测液滴到试纸上,?_________?,即可得出被测液的pH。实验结果:此试剂的pH值为10。
?(3)小俊利用上图试剂鉴别出,这瓶试剂是K2CO3溶液。请按小俊的做法,填写实验报告。
操作步骤 实验现象 结论及化学方程式
? ? ?
? 结论:
?
化学方程式:
?
?
?
?
?
?
?
?
?
?
?
?
高一化学参考答案
一、选择题(本题包括20小题,每小题2分,共40分)
题号 1 2 3 4 5 6 7 8 9 10
答案 A D D A C C B B D B
题号 11 12 13 14 15 16 17 18 19 20
答案 D D B D B C A B D D
二、本题包括5小题,共30分。
21.(5分)
(1)蛋白质?? 烧焦羽毛 (各1分)
(2)NaCl(1分)??? BaCO3?+2HCl= BaCl2?+ H2O +CO2↑(2分,配平和条件合扣1分)
22.(7分)
(1)(图示如右,2分)?
(2)23℃(1分,22~24℃均可)
(3)?100 (2分),?
?80.4 (2分)
23. (共6分)
(1)MgCl2 + 2NaOH == Mg(OH)2↓+ 2NaCl (2分,配平和条件合扣1分)
(2)Na+?、? Mg2+?(2分,有错得0分)
(3)80% (2分)
24.(7分)
(1)?SO2?? SO3?(各1分)
(2)?3S?? 2 H2O (各1分)
(3) ①SO2+2H2S === 2H2O + 3S↓(2分,配平和条件合扣1分)?
?②SO2? (1分)
25.(5分)
??? (1)?CuO (1分)??? 稀硫酸(1分)
??? (2)?CuO+ H2SO4=== CuSO4+H2O (2分,配平和条件合扣1分)
??? (3) 硫酸的利用率高?(1分)???? (合理答案均给分)
三、本题包括4小题,共30分。
26.(5分)
(1)未用玻璃棒引流;滤纸高出漏斗边缘。(各1分)(或“滤纸未紧贴漏斗内壁“、 “漏斗下端尖嘴未紧靠烧杯B的内壁”;无顺序要求,合理均可)
(2)①氢氧化钠直接放在纸上称量(1分)? ②?B(2分)
27.(8分)
(1)①铁架台?? 水槽(各1分)? ②ABC(1分)? ③?b(1分)
(2)①证明水不能使紫色石蕊变红(1分)
②证明二氧化硫不能使紫色石蕊变红(1分);将干燥的紫色石蕊试纸放入SO2中(1分),试纸不变色(1分)。
28.(9分)
(1)CO2(1分)
(2)检查装置气密性(1分) ⑤①③④②(2分)
(3)①?黑色粉末逐渐变成红色(1分)?
②?m(Cu) : m(CO) : m(CO2) : m(H2O) = 112 : 7 : 11 : 18? (2分)
(4)①?3(1分) ??? ②?CH4在装置A中剧烈燃烧,引起爆炸(1分)
29.(共8分)
(1)A? (1分)
(2)把试纸显示的颜色与标准比色卡比较 (1分)
(3)步骤2分,现象1分,结论1分,化学方程式?2分。
操作步骤 实验现象 结论及化学方程式
取少量标签破损的溶液于试管中(1分),滴入盐酸(1分),振荡。 有气泡产生(1分) 结论:标签破损的溶液是碳酸钾溶液。(1分)
化学方程式:
K2CO3?+2HCl ==2KCl +CO2↑+ H2O (2分,配平和条件合扣1分)
或:
操作步骤 实验现象 结论及化学方程式
取少量标签破损的溶液于试管中(1分),滴入氢氧化钙溶液(或氯化钡溶液)(1分),振荡。 有白色沉淀(溶液浑浊)。(1分) 结论:标签破损的溶液是碳酸钾溶液。(1分)
化学方程式:
K2CO3?+Ca(OH)2?== CaCO3↓ +2KOH(2分,配平和条件合扣1分)
同课章节目录
