人教版九年级上册化学 7.2 燃l料的合理利用与开发 课件(35张PPT)
文档属性
| 名称 | 人教版九年级上册化学 7.2 燃l料的合理利用与开发 课件(35张PPT) |  | |
| 格式 | ppt | ||
| 文件大小 | 2.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-09-02 21:50:27 | ||
图片预览






文档简介
课题2 燃料的合理利用与开发
一.化学反应中的能量变化
实验7-3 .在一支试管中加入一小匙干燥的生石灰,再加入2 mL水,观察现象,并用手触摸试管外壁。
现 象
手的感觉
分 析
生石灰和水剧烈反应,产生大量水蒸气,放热。
热或烫手。
生石灰和水剧烈反应,产生大量水蒸气,并放出热量,说明这是一个 放热反应。
结论:化学反应在生成新物质的同时,还伴随着能量的变化。而能量的变化通常表现为热量的变化。其中,放出热量的为放热反应,吸收热量的为吸热反应。
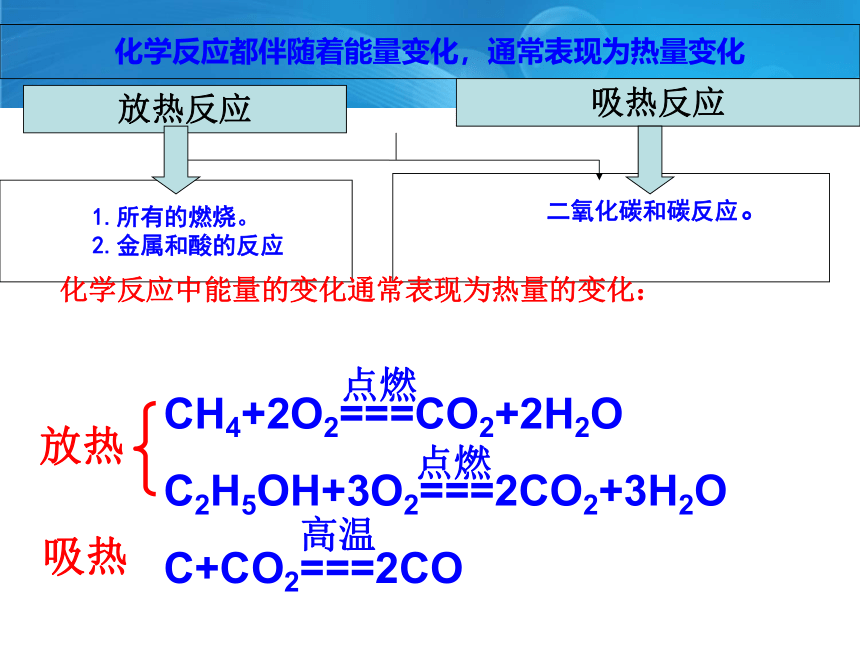
化学反应都伴随着能量变化,通常表现为热量变化
1.所有的燃烧。
2.金属和酸的反应
二氧化碳和碳反应。
放热反应
吸热反应
CH4+2O2===CO2+2H2O
C2H5OH+3O2===2CO2+3H2O
C+CO2===2CO
放热
吸热
点燃
点燃
高温
化学反应中能量的变化通常表现为热量的变化:
利用化学反应放出热量的实例
生活燃料的使用:做饭、取暖等;
还有发电、烧制陶瓷、冶炼金属和发射火箭;
开山炸石和拆除危旧建筑;等等
对于我们自身来说,维持体温和日常活动所需的能量,都与食物在体内发生的化学反应有关。
讨论:举出一些利用化学反应放出热量的实例。
切割或焊接金属、驱动汽车、加热物质等。
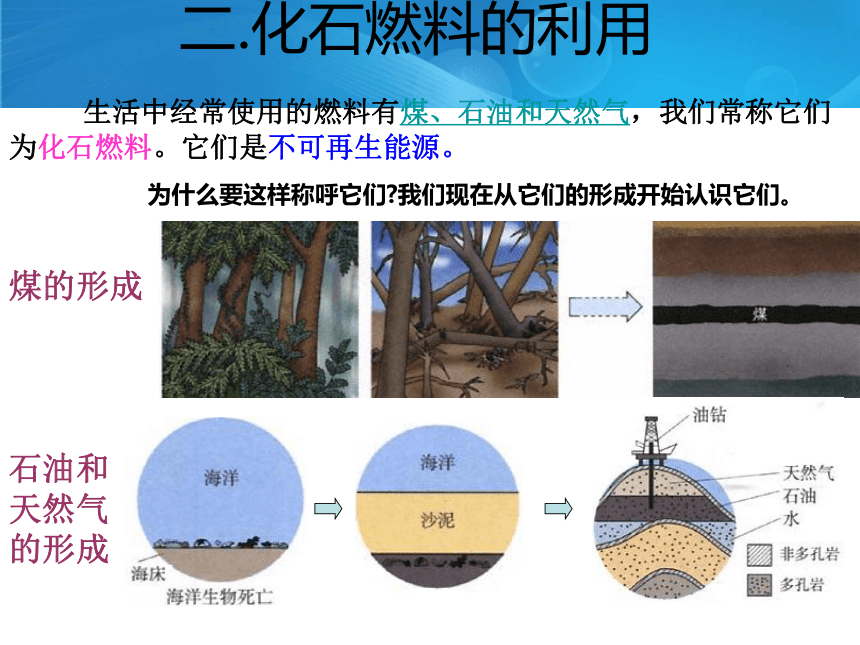
生活中经常使用的燃料有煤、石油和天然气,我们常称它们为化石燃料。它们是不可再生能源。
为什么要这样称呼它们?我们现在从它们的形成开始认识它们。
煤的形成
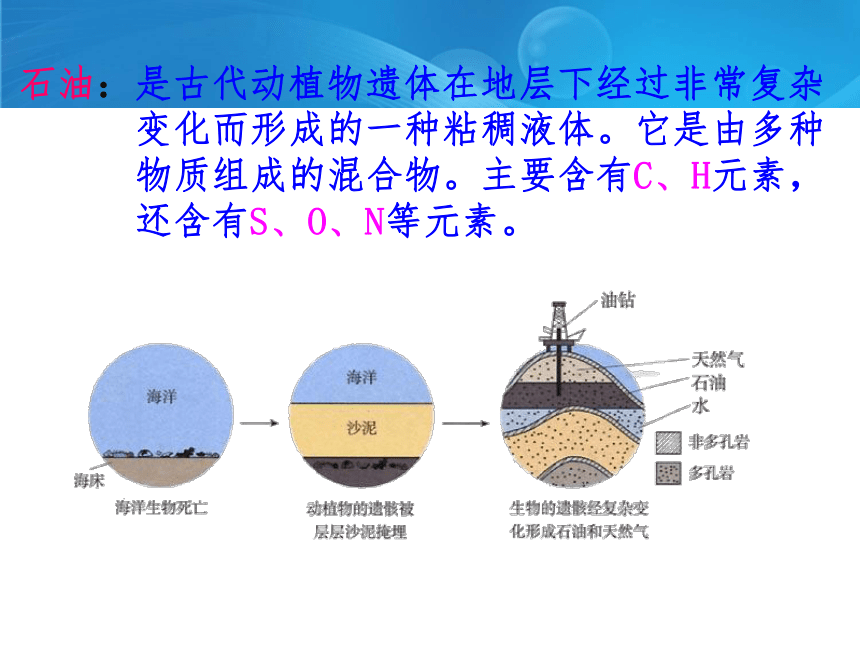
石油和天然气的形成
二.化石燃料的利用
1.煤和石油 (阅读课本138~139页,思考下列问题)
1、煤是纯净物还是混合物? 主要组成元素是什么?还含 有哪些少量元素?
2、煤完全燃烧的产物有哪些?
4、煤气的主要成分有哪些?
3、如何将煤综合利用?
混合物
碳元素
氢 氮 硫 氧元素
CO2
H2O
NO2
SO2
将煤隔绝空气加热,生成焦炭、煤焦油、煤气等。(煤干馏[化学变化]后的综合利用,既可以充分利用煤的资源,还可以极大的减少污染。)
氢气H2 甲烷CH4 一氧化碳CO 其他气体
煤燃烧
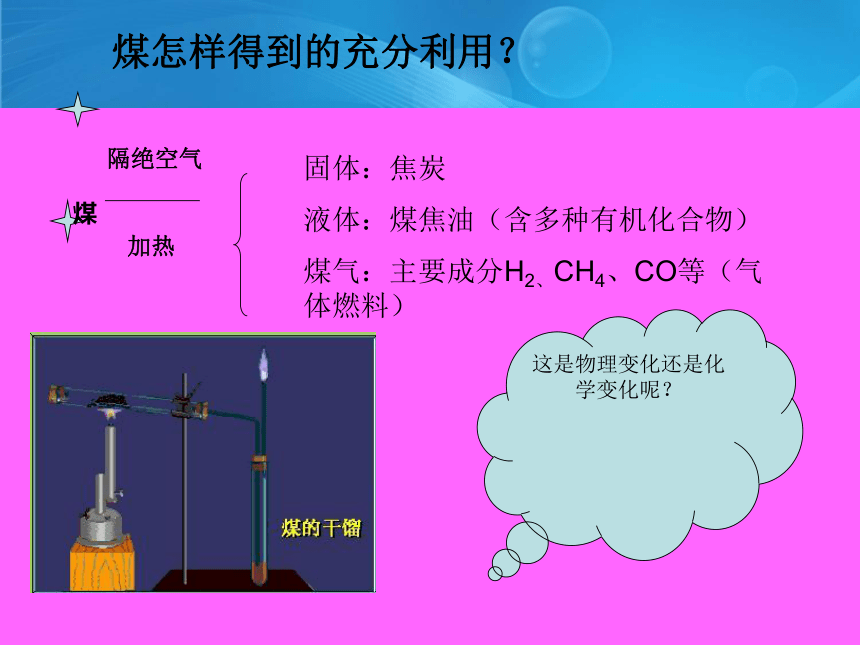
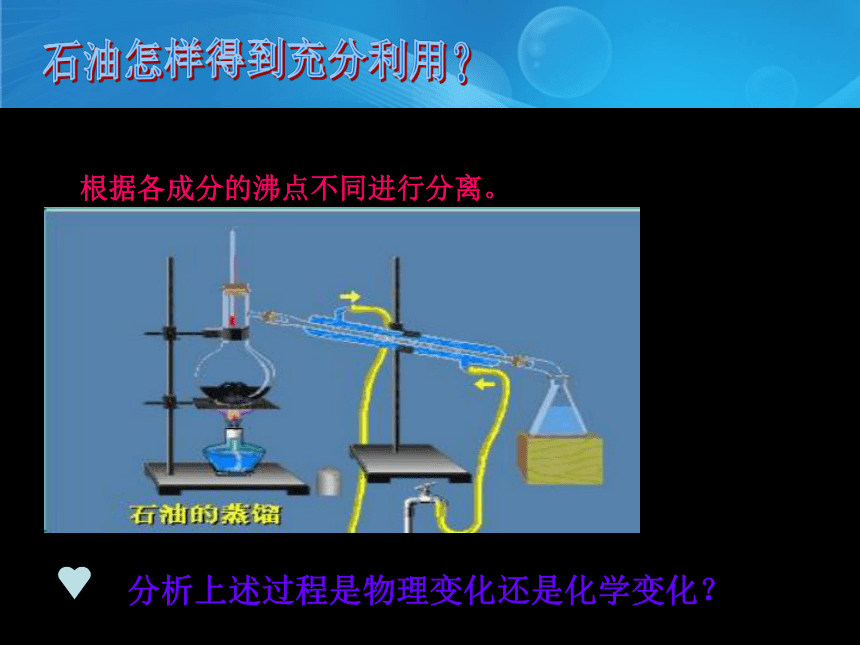
煤怎样得到的充分利用?
煤
隔绝空气
加热
固体:焦炭
液体:煤焦油(含多种有机化合物)
煤气:主要成分H2、CH4、CO等(气体燃料)
这是物理变化还是化学变化呢?
煤的用途
工业的粮食
石油:是古代动植物遗体在地层下经过非常复杂
变化而形成的一种粘稠液体。它是由多种
物质组成的混合物。主要含有C、H元素,
还含有S、O、N等元素。
讨论:
石油可直接用做燃料吗?石油产品中有哪些是常用的燃料?
石油燃烧
不可以,因为石油是混合物,
里面有很多的杂质,
导致石油的易燃度减低
而且直接燃烧石油会
产生很多的废气,污染环境
如果把石油的原油
提炼后会分解出
多种产物如:汽油,煤油
沥青,柴油等,可以充分利用。
根据各成分的沸点不同进行分离。
分析上述过程是物理变化还是化学变化?
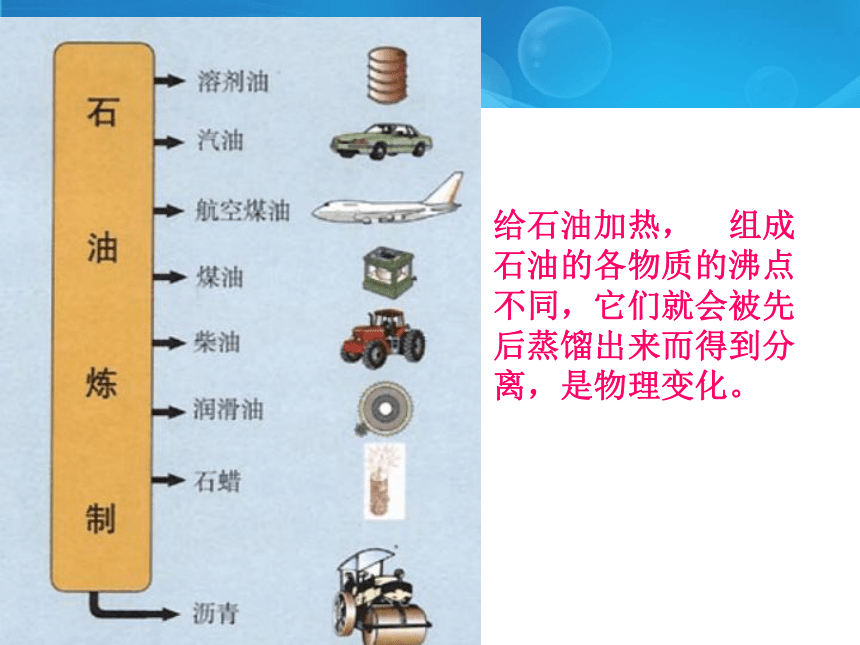
给石油加热, 组成石油的各物质的沸点不同,它们就会被先后蒸馏出来而得到分离,是物理变化。
城镇的许多家庭做饭使用一种罐装“煤气”作为燃料,罐中所装的是液化石油气,这是石油化工的一种产品。液化石油气是经加压后压缩到钢瓶中的,瓶内压强是大气压强的7~8倍。
2、煤气泄漏会造成什么危害?使用罐装液化石油气在安全上应注意什么?
煤气的主要成分是一氧化碳,它是可燃性气体并且是有剧毒的气体, 一旦泄漏,一方面可能引起火灾甚至爆炸事故,另一方面可使人中毒死亡,所以要谨防泄漏事故发生;灌装液化石油气(主要成分为丙烷、丁烷、丙烯和丁烯等)是经加压后压缩在钢瓶中,由于这些气体都属于易燃易爆物,使用时一定要注意安全、轻拿轻放、放置在远离火源处、用毕要关紧阀门、防止泄漏、定期检查等,一旦泄漏要立即关闭阀门、打开门窗,切记产生火花,如开灯、碰撞电子打火装置等。
工业的血液
石油的用途
2.天然气
甲烷是一种无色密度比空气小的气体。
天然气的成分?
为混合物,主要成分为甲烷气体。
极难溶于水。
这是用排水法收集到的甲烷气体,根据图片,思考甲烷的物理性质有哪些?
实验验证
设计实验:验证甲烷燃烧的产物是水和二氧化碳?
实验现象:
①明亮的蓝色火焰;
②烧杯内壁有水雾(干冷的烧杯);
③杯壁上澄清石灰水变浑浊
(内壁涂有澄清石灰水的烧杯);
④放出热量。
在有石油的地方,一般都有天然气的存在。天然气的主要成分是甲烷(CH4)(俗称沼气)。
[实验7-4]观察甲烷的颜色、状态。点燃从导管放出的甲烷(点燃前,要先检验甲烷的纯度),在火焰的上方罩一个冷而干燥的烧杯。过一会儿,观察烧杯上的现象。
现象
火焰明亮且呈蓝色,放热;烧杯内壁上有水珠
迅速把烧杯倒过来,向烧杯内注入少量澄清的石灰水,振荡,观察现象。
现象
澄清的石灰水变浑浊
CH4 + 2O2
点燃
2H2O
+ CO2
这个实验说明甲烷中肯定含有氢元素、碳元素
CO2=
CO2+Ca(OH)2=H2O+CaCO3↓
甲烷的存在
(1)甲烷还存在于池沼的底部(常称为沼气)
(2)甲烷还存在于煤矿的坑道中。甲烷混在空气中达到一定程度时,遇火会发生爆炸。
人工能制取沼气吗?
把秸秆、杂草、人畜粪便等废弃物放在密闭的沼气池中发酵,就可产生甲烷。
在我国农村利用沼气,不仅可以解决生活用燃料问题;还能综合治理环境卫生问题。
化石燃料的用途
化石燃料形成的时间非常长,储量有限。化石燃料属于不可再生能源。人类目前消耗的能量主要来自化石燃料。
在不久的将来,我们将面临严重的能源危机!
探 明 储 量
年 产 量
开采年限
石 油
23亿吨
1.74亿吨
约13年
天然气
2.23x104亿立方米
408亿立方米
约55年
煤
1145亿吨
9.9亿吨
约116年
我国2004年化石能源探明储量、年产量及开采年限
燃料不充分燃烧的危害:
燃料燃烧不充分时,产生黑烟,并生成CO等物质,使燃料的利用率降低,浪费资源,且污染空气。
如何做到使燃料充分燃烧呢?
使燃料充分燃烧通常需要考虑两点:
1.燃烧时要有足够多的空气
2.燃料要与空气要有足够大的接触面
讨论:工业上有时使用煤等固体燃料,为了使燃料与空气有足够的接触面,你认为应将固体燃料进行怎样的处理?
加工成小块、打成粉末、做成蜂窝多孔形状
可燃冰燃烧图
可燃冰的学名为“天然气水合物”,化学式为CH4.xH2O是天然气在0℃和30个大气压的作用下结晶而成的“冰块”。“冰块”里甲烷占80%—99.9%,可直接点燃,燃烧后几乎不产生任何残渣,污染比煤、石
油、天然气都要小得多。西方学者称其为
“21世纪能源”或“未来能源”。但是可燃冰埋藏于海底的岩石中,如果在开采中甲烷气体大量泄漏于大气中造成的温室效应将比二氧化碳更加严重。所以还需要解决技术上的问题。
石油没了
汽车不动了
我又该如何面对?
一切可能乱了
CO 有毒气体
CO2 温室效应
SO2
NO2
酸雨
讨论:据上述实验,试说明酸雨可能对环境造成什么样的破坏?
碳元素
氮元素
硫元素
思考2:这些元素燃
烧后生成哪些物质?
思考1:煤中主要含哪种元素?还含哪些元素?
煤的燃烧
三.使用燃料对环境的影响
1.燃料燃烧对空气的影响
三
文物雕像腐蚀
水体污染、土壤酸化
森林受到破坏
桥梁等建筑物受到腐蚀
损害人体健康
2、汽车用燃料的燃烧
汽车尾气中的主要污染物有哪些?
减少汽车尾气对空气污染的措施有哪些?
汽车用燃料的燃烧
尾气中的主要污染物有CO,末燃烧的碳氢化合物、氮的氧化物、含铅化合物和烟尘
减少汽车气对空气的污染可采取DE措施:
(1)使用催化净化装置
(2)使用无铅汽油禁止含铅物质的排放
(3)改进发动机的燃烧方式,使汽油能充分燃料
(4)改用压缩天然气(CNG)或液化石油气(LPG)
(5)在汽油中加入乙醇(混合物)既节省汽油,又减少污染。
四、能源的利用和开发
1.乙醇(化学式C2H5OH)俗称酒精。
物理性质: 有特殊气味,密度比水小 ,能与水互溶,易挥发
化学性质: 可燃性,燃烧时放出大量的热.
C2H5OH+3O2 === 2CO2+3H2O
点燃
优点:无污染 、热效率高、节省汽油、减少汽车尾气污染
制取:高梁、玉米、薯类经过发酵,蒸馏可得酒精(可再生能源)
2.氢气(H2)
燃烧产物是水,不污染空气,被认为是理想的清洁、高能(液氢完全燃烧放出的热量约为等质量甲烷的2倍多,同质量汽油的3倍多)燃料
氢气的实验室制法:常用锌和稀硫酸反应制取氢气
方程式是: Zn + H2SO4 = ZnSO4 + H2↑
3.人们正在开发利用的能源:
太阳能、风能、地热能、潮汐能、生物质能和核能等
氢气的制取成本高,不安全,暂时未能广泛应用
开发和利用新能源
核能
太阳能
风能
水能
潮汐能
一.化学反应中的能量变化
实验7-3 .在一支试管中加入一小匙干燥的生石灰,再加入2 mL水,观察现象,并用手触摸试管外壁。
现 象
手的感觉
分 析
生石灰和水剧烈反应,产生大量水蒸气,放热。
热或烫手。
生石灰和水剧烈反应,产生大量水蒸气,并放出热量,说明这是一个 放热反应。
结论:化学反应在生成新物质的同时,还伴随着能量的变化。而能量的变化通常表现为热量的变化。其中,放出热量的为放热反应,吸收热量的为吸热反应。
化学反应都伴随着能量变化,通常表现为热量变化
1.所有的燃烧。
2.金属和酸的反应
二氧化碳和碳反应。
放热反应
吸热反应
CH4+2O2===CO2+2H2O
C2H5OH+3O2===2CO2+3H2O
C+CO2===2CO
放热
吸热
点燃
点燃
高温
化学反应中能量的变化通常表现为热量的变化:
利用化学反应放出热量的实例
生活燃料的使用:做饭、取暖等;
还有发电、烧制陶瓷、冶炼金属和发射火箭;
开山炸石和拆除危旧建筑;等等
对于我们自身来说,维持体温和日常活动所需的能量,都与食物在体内发生的化学反应有关。
讨论:举出一些利用化学反应放出热量的实例。
切割或焊接金属、驱动汽车、加热物质等。
生活中经常使用的燃料有煤、石油和天然气,我们常称它们为化石燃料。它们是不可再生能源。
为什么要这样称呼它们?我们现在从它们的形成开始认识它们。
煤的形成
石油和天然气的形成
二.化石燃料的利用
1.煤和石油 (阅读课本138~139页,思考下列问题)
1、煤是纯净物还是混合物? 主要组成元素是什么?还含 有哪些少量元素?
2、煤完全燃烧的产物有哪些?
4、煤气的主要成分有哪些?
3、如何将煤综合利用?
混合物
碳元素
氢 氮 硫 氧元素
CO2
H2O
NO2
SO2
将煤隔绝空气加热,生成焦炭、煤焦油、煤气等。(煤干馏[化学变化]后的综合利用,既可以充分利用煤的资源,还可以极大的减少污染。)
氢气H2 甲烷CH4 一氧化碳CO 其他气体
煤燃烧
煤怎样得到的充分利用?
煤
隔绝空气
加热
固体:焦炭
液体:煤焦油(含多种有机化合物)
煤气:主要成分H2、CH4、CO等(气体燃料)
这是物理变化还是化学变化呢?
煤的用途
工业的粮食
石油:是古代动植物遗体在地层下经过非常复杂
变化而形成的一种粘稠液体。它是由多种
物质组成的混合物。主要含有C、H元素,
还含有S、O、N等元素。
讨论:
石油可直接用做燃料吗?石油产品中有哪些是常用的燃料?
石油燃烧
不可以,因为石油是混合物,
里面有很多的杂质,
导致石油的易燃度减低
而且直接燃烧石油会
产生很多的废气,污染环境
如果把石油的原油
提炼后会分解出
多种产物如:汽油,煤油
沥青,柴油等,可以充分利用。
根据各成分的沸点不同进行分离。
分析上述过程是物理变化还是化学变化?
给石油加热, 组成石油的各物质的沸点不同,它们就会被先后蒸馏出来而得到分离,是物理变化。
城镇的许多家庭做饭使用一种罐装“煤气”作为燃料,罐中所装的是液化石油气,这是石油化工的一种产品。液化石油气是经加压后压缩到钢瓶中的,瓶内压强是大气压强的7~8倍。
2、煤气泄漏会造成什么危害?使用罐装液化石油气在安全上应注意什么?
煤气的主要成分是一氧化碳,它是可燃性气体并且是有剧毒的气体, 一旦泄漏,一方面可能引起火灾甚至爆炸事故,另一方面可使人中毒死亡,所以要谨防泄漏事故发生;灌装液化石油气(主要成分为丙烷、丁烷、丙烯和丁烯等)是经加压后压缩在钢瓶中,由于这些气体都属于易燃易爆物,使用时一定要注意安全、轻拿轻放、放置在远离火源处、用毕要关紧阀门、防止泄漏、定期检查等,一旦泄漏要立即关闭阀门、打开门窗,切记产生火花,如开灯、碰撞电子打火装置等。
工业的血液
石油的用途
2.天然气
甲烷是一种无色密度比空气小的气体。
天然气的成分?
为混合物,主要成分为甲烷气体。
极难溶于水。
这是用排水法收集到的甲烷气体,根据图片,思考甲烷的物理性质有哪些?
实验验证
设计实验:验证甲烷燃烧的产物是水和二氧化碳?
实验现象:
①明亮的蓝色火焰;
②烧杯内壁有水雾(干冷的烧杯);
③杯壁上澄清石灰水变浑浊
(内壁涂有澄清石灰水的烧杯);
④放出热量。
在有石油的地方,一般都有天然气的存在。天然气的主要成分是甲烷(CH4)(俗称沼气)。
[实验7-4]观察甲烷的颜色、状态。点燃从导管放出的甲烷(点燃前,要先检验甲烷的纯度),在火焰的上方罩一个冷而干燥的烧杯。过一会儿,观察烧杯上的现象。
现象
火焰明亮且呈蓝色,放热;烧杯内壁上有水珠
迅速把烧杯倒过来,向烧杯内注入少量澄清的石灰水,振荡,观察现象。
现象
澄清的石灰水变浑浊
CH4 + 2O2
点燃
2H2O
+ CO2
这个实验说明甲烷中肯定含有氢元素、碳元素
CO2=
CO2+Ca(OH)2=H2O+CaCO3↓
甲烷的存在
(1)甲烷还存在于池沼的底部(常称为沼气)
(2)甲烷还存在于煤矿的坑道中。甲烷混在空气中达到一定程度时,遇火会发生爆炸。
人工能制取沼气吗?
把秸秆、杂草、人畜粪便等废弃物放在密闭的沼气池中发酵,就可产生甲烷。
在我国农村利用沼气,不仅可以解决生活用燃料问题;还能综合治理环境卫生问题。
化石燃料的用途
化石燃料形成的时间非常长,储量有限。化石燃料属于不可再生能源。人类目前消耗的能量主要来自化石燃料。
在不久的将来,我们将面临严重的能源危机!
探 明 储 量
年 产 量
开采年限
石 油
23亿吨
1.74亿吨
约13年
天然气
2.23x104亿立方米
408亿立方米
约55年
煤
1145亿吨
9.9亿吨
约116年
我国2004年化石能源探明储量、年产量及开采年限
燃料不充分燃烧的危害:
燃料燃烧不充分时,产生黑烟,并生成CO等物质,使燃料的利用率降低,浪费资源,且污染空气。
如何做到使燃料充分燃烧呢?
使燃料充分燃烧通常需要考虑两点:
1.燃烧时要有足够多的空气
2.燃料要与空气要有足够大的接触面
讨论:工业上有时使用煤等固体燃料,为了使燃料与空气有足够的接触面,你认为应将固体燃料进行怎样的处理?
加工成小块、打成粉末、做成蜂窝多孔形状
可燃冰燃烧图
可燃冰的学名为“天然气水合物”,化学式为CH4.xH2O是天然气在0℃和30个大气压的作用下结晶而成的“冰块”。“冰块”里甲烷占80%—99.9%,可直接点燃,燃烧后几乎不产生任何残渣,污染比煤、石
油、天然气都要小得多。西方学者称其为
“21世纪能源”或“未来能源”。但是可燃冰埋藏于海底的岩石中,如果在开采中甲烷气体大量泄漏于大气中造成的温室效应将比二氧化碳更加严重。所以还需要解决技术上的问题。
石油没了
汽车不动了
我又该如何面对?
一切可能乱了
CO 有毒气体
CO2 温室效应
SO2
NO2
酸雨
讨论:据上述实验,试说明酸雨可能对环境造成什么样的破坏?
碳元素
氮元素
硫元素
思考2:这些元素燃
烧后生成哪些物质?
思考1:煤中主要含哪种元素?还含哪些元素?
煤的燃烧
三.使用燃料对环境的影响
1.燃料燃烧对空气的影响
三
文物雕像腐蚀
水体污染、土壤酸化
森林受到破坏
桥梁等建筑物受到腐蚀
损害人体健康
2、汽车用燃料的燃烧
汽车尾气中的主要污染物有哪些?
减少汽车尾气对空气污染的措施有哪些?
汽车用燃料的燃烧
尾气中的主要污染物有CO,末燃烧的碳氢化合物、氮的氧化物、含铅化合物和烟尘
减少汽车气对空气的污染可采取DE措施:
(1)使用催化净化装置
(2)使用无铅汽油禁止含铅物质的排放
(3)改进发动机的燃烧方式,使汽油能充分燃料
(4)改用压缩天然气(CNG)或液化石油气(LPG)
(5)在汽油中加入乙醇(混合物)既节省汽油,又减少污染。
四、能源的利用和开发
1.乙醇(化学式C2H5OH)俗称酒精。
物理性质: 有特殊气味,密度比水小 ,能与水互溶,易挥发
化学性质: 可燃性,燃烧时放出大量的热.
C2H5OH+3O2 === 2CO2+3H2O
点燃
优点:无污染 、热效率高、节省汽油、减少汽车尾气污染
制取:高梁、玉米、薯类经过发酵,蒸馏可得酒精(可再生能源)
2.氢气(H2)
燃烧产物是水,不污染空气,被认为是理想的清洁、高能(液氢完全燃烧放出的热量约为等质量甲烷的2倍多,同质量汽油的3倍多)燃料
氢气的实验室制法:常用锌和稀硫酸反应制取氢气
方程式是: Zn + H2SO4 = ZnSO4 + H2↑
3.人们正在开发利用的能源:
太阳能、风能、地热能、潮汐能、生物质能和核能等
氢气的制取成本高,不安全,暂时未能广泛应用
开发和利用新能源
核能
太阳能
风能
水能
潮汐能
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
