仁爱版初中化学九年级上册专题2《空气和水》检测题(含答案)
文档属性
| 名称 | 仁爱版初中化学九年级上册专题2《空气和水》检测题(含答案) |
|
|
| 格式 | zip | ||
| 文件大小 | 120.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 仁爱科普版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-09-06 00:00:00 | ||
图片预览


文档简介
本卷由系统自动生成,请仔细校对后使用,答案仅供参考。
《空气和水》检测题
一、单选题
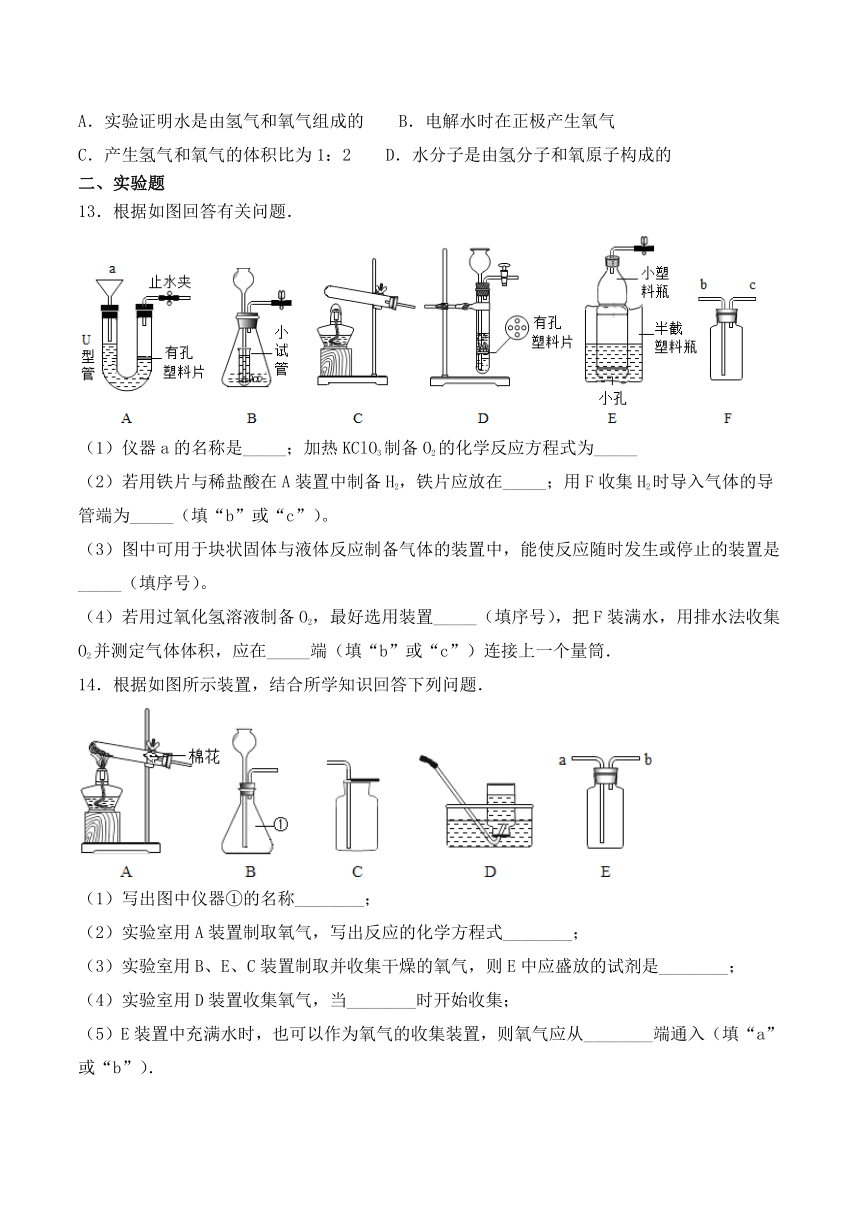
1.以下是初中化学中的一些基本经验,不能达到实验目的是( )
2.下列各组物质中,都属于纯净物的是(
)
A.低钠盐;奶粉
B.大理石;鸡蛋壳
C.矿泉水;生理盐水
D.氧气;二氧化碳
3.下列有关水的说法中正确的是(
)
A.水(H2O)和过氧化氢(H2O2)分子中都含有氢气分子(H2)
B.电解水实验证明水是由氢原子和氧原子构成的
C.用肥皂水可以软化硬水
D.常用吸附、沉淀、过滤和蒸馏等方法净化水
4.通过实验测定了空气的组成科学家是(
)
A.门捷列夫
B.阿伏伽德罗
C.拉瓦锡
D.道尔顿
5.下列关于空气的说法中,不正确的是( )
A.工业上采用分离液态空气法获得氧气
B.二氧化硫是空气污染物之一
C.空气中氧气质量占空气质量的21%
D.稀有气体可用于制作霓虹灯
6.分子模型可以直观的表示分子的微观结构(分子模型中,不同颜色、大小的小球代表不同的原子)。如图所示的分子模型表示的分子是
A.HCHO
B.CO2
C.NH3
D.CH4
7.水是生命之源,下列有关水的说法错误的是
A.软水和硬水可用肥皂水来区分
B.电解水时产生氧气与氢气的体积比约为1:2
C.吸附能除去天然水中所有的杂质
D.水体污染主要来源于工业污染、农业污染、生活污染
8.家庭日常生活经常用到的下列物质中,属于纯净物的是
A.降温用的冰水共存物
B.餐饮用的可口可乐
C.调味用的加碘食盐
D.炒菜用的铁锅
9.下列四个反应属于化合反应的是
①.氧化汞汞+氧气
②.石灰石+盐酸
氯化钙+二氧化碳+水
③.酒精+氧气水+二氧化碳
④.木炭+氧气二氧化碳
A.①
B.③④
C.③
D.④
10.北京大学生命科学学院蒋争凡教授研究组发现,锰离子是细胞内天然免疫激活剂和警报素。锰元素的相关信息如图所示,下列有关锰的说法不正确的是( )
A.原子序数为25
B.属于金属元素
C.原子核外电子数为25
D.原子的质量为54.94
11.下列物质属于氧化物的是( )
A.O3
B.SiO2
C.Cu2(OH)2CO3
D.Fe(OH)3
12.关于电解水实验的说法中正确的是(
)
A.实验证明水是由氢气和氧气组成的
B.电解水时在正极产生氧气
C.产生氢气和氧气的体积比为1:2
D.水分子是由氢分子和氧原子构成的
二、实验题
13.根据如图回答有关问题.
(1)仪器a的名称是_____;加热KClO3制备O2的化学反应方程式为_____
(2)若用铁片与稀盐酸在A装置中制备H2,铁片应放在_____;用F收集H2时导入气体的导管端为_____(填“b”或“c”)。
(3)图中可用于块状固体与液体反应制备气体的装置中,能使反应随时发生或停止的装置是_____(填序号)。
(4)若用过氧化氢溶液制备O2,最好选用装置_____(填序号),把F装满水,用排水法收集O2并测定气体体积,应在_____端(填“b”或“c”)连接上一个量筒.
14.根据如图所示装置,结合所学知识回答下列问题.
(1)写出图中仪器①的名称________;
(2)实验室用A装置制取氧气,写出反应的化学方程式________;
(3)实验室用B、E、C装置制取并收集干燥的氧气,则E中应盛放的试剂是________;
(4)实验室用D装置收集氧气,当________时开始收集;
(5)E装置中充满水时,也可以作为氧气的收集装置,则氧气应从________端通入(填“a”或“b”).
三、推断题
15.甲、乙、丙三种物质均含地壳中含量最多的元素。甲、乙是组成元素完全相同的化合物,丙是单质;乙通常为液体,在一定条件下可分解生成丙;它们之间有如图所示的转化关系(部分物质和反应条件已经略去)。则:
(1)甲为______(填化学式,下同),乙为______,丙为______;
(2)乙分解生成丙的化学方程式为______。
(3)从微观的角度解释甲、乙性质有差异的原因是______。
16.将某紫黑色固体粉末A加热,可产生无色气体B,同时生成一种黑色固体C
和另一种固
体物质D.黑色固体C通常可用于加热氯酸钾制氧气时的催化剂.另一黑色固体E
在无色气体B
中燃烧,产生使澄清石灰水变浑浊的气体F.绿色植物可将气体F通过光合作用吸收,并转化为无色气体B.回答:
(1)写出名称
A__________,C__________;写出化学符号:B__________,F__________.
(2)写出黑色固体E在无色气体B中燃烧的反应的文字表达式:___________________,该反应的基本类型是____________________。
17.已知A~G都是初中化学常见的物质,通常状况下,A、C为无色液体,且组成元素相同,D、E为气体,它们之间的转化关系如图所示。回答下列问题:
(1)物质B在反应①中的作用是________________。
(2)检验气体D的方法是______________。
(3)若F为黑色固体,写出反应③的符号表达式________________。若G为黑色固体,写出反应③的符号表达式_____________。
四、计算题
18.高铁酸钠(Na2FeO4)是一种高效多功能水处理剂,工业上常采用次氯酸钠(NaClO)氧化法生产,反应原理用化学方程式表示为:3NaClO
+
2Fe(NO3)3+
10NaOH
=
2Na2FeO4↓+3NaCl
+6NaNO3+
5H2O
(1)在Fe(NO3)3中,铁元素和氮元素的质量比为
(填最简比)。
(2)县称取44.7g次氯酸钠,最多能制得高铁酸钠的质量是多少?(列式计算)
温馨提示:NaClO的相对分子质量为74.5;Na2FeO4的相对分子质量为166。
19.食品添加剂的使用,改善了食品的品质和特色。苯甲酸(C7H6O2)是一种应用广泛的食品添加剂,其具有防腐的作用。试回答下列问题:
(1)苯甲酸中,碳、氢元素的质量比__________(填最简整数比)。
(2)苯甲酸中,元素质量分数最小的元素是___________。
20.测定空气的组成后,同学们知道了氧气的体积约占空气总体积的,某初中化学兴趣小组的同学查阅资料得知:氧气的密度约为1.43g/L,空气的密度约为1.29g/L.小芳想知道100g空气中氧气的质量,请你帮她计算,并写出计算过程。(计算结果精确到0.01)
参考答案
1.A
2.D
3.D
4.C
5.C
6.A
7.C
8.A
9.D
10.D
11.B
12.B
13.漏斗
有孔塑料片上
c
B
B
b
14.锥形瓶;2KMnO4K2MnO4+MnO2+O2↑;浓硫酸;气泡连续均匀冒出;b
15.H2O2
H2O
O2
2H2O22H2O+O2↑
构成物质的分子不同
16.高锰酸钾
二氧化锰
O2
CO2
碳+氧气
二氧化碳
化合反应
17.催化作用
用带火星的木条伸入集气瓶中,木条复燃则为氧气
C+O2CO2
Fe+O2Fe3O4
18.(1)4:3;⑵最多可得到高铁酸钾的质量为66.4g。
19.
14:1
氢
20.22.17g
答案第1页,总2页
《空气和水》检测题
一、单选题
1.以下是初中化学中的一些基本经验,不能达到实验目的是( )
2.下列各组物质中,都属于纯净物的是(
)
A.低钠盐;奶粉
B.大理石;鸡蛋壳
C.矿泉水;生理盐水
D.氧气;二氧化碳
3.下列有关水的说法中正确的是(
)
A.水(H2O)和过氧化氢(H2O2)分子中都含有氢气分子(H2)
B.电解水实验证明水是由氢原子和氧原子构成的
C.用肥皂水可以软化硬水
D.常用吸附、沉淀、过滤和蒸馏等方法净化水
4.通过实验测定了空气的组成科学家是(
)
A.门捷列夫
B.阿伏伽德罗
C.拉瓦锡
D.道尔顿
5.下列关于空气的说法中,不正确的是( )
A.工业上采用分离液态空气法获得氧气
B.二氧化硫是空气污染物之一
C.空气中氧气质量占空气质量的21%
D.稀有气体可用于制作霓虹灯
6.分子模型可以直观的表示分子的微观结构(分子模型中,不同颜色、大小的小球代表不同的原子)。如图所示的分子模型表示的分子是
A.HCHO
B.CO2
C.NH3
D.CH4
7.水是生命之源,下列有关水的说法错误的是
A.软水和硬水可用肥皂水来区分
B.电解水时产生氧气与氢气的体积比约为1:2
C.吸附能除去天然水中所有的杂质
D.水体污染主要来源于工业污染、农业污染、生活污染
8.家庭日常生活经常用到的下列物质中,属于纯净物的是
A.降温用的冰水共存物
B.餐饮用的可口可乐
C.调味用的加碘食盐
D.炒菜用的铁锅
9.下列四个反应属于化合反应的是
①.氧化汞汞+氧气
②.石灰石+盐酸
氯化钙+二氧化碳+水
③.酒精+氧气水+二氧化碳
④.木炭+氧气二氧化碳
A.①
B.③④
C.③
D.④
10.北京大学生命科学学院蒋争凡教授研究组发现,锰离子是细胞内天然免疫激活剂和警报素。锰元素的相关信息如图所示,下列有关锰的说法不正确的是( )
A.原子序数为25
B.属于金属元素
C.原子核外电子数为25
D.原子的质量为54.94
11.下列物质属于氧化物的是( )
A.O3
B.SiO2
C.Cu2(OH)2CO3
D.Fe(OH)3
12.关于电解水实验的说法中正确的是(
)
A.实验证明水是由氢气和氧气组成的
B.电解水时在正极产生氧气
C.产生氢气和氧气的体积比为1:2
D.水分子是由氢分子和氧原子构成的
二、实验题
13.根据如图回答有关问题.
(1)仪器a的名称是_____;加热KClO3制备O2的化学反应方程式为_____
(2)若用铁片与稀盐酸在A装置中制备H2,铁片应放在_____;用F收集H2时导入气体的导管端为_____(填“b”或“c”)。
(3)图中可用于块状固体与液体反应制备气体的装置中,能使反应随时发生或停止的装置是_____(填序号)。
(4)若用过氧化氢溶液制备O2,最好选用装置_____(填序号),把F装满水,用排水法收集O2并测定气体体积,应在_____端(填“b”或“c”)连接上一个量筒.
14.根据如图所示装置,结合所学知识回答下列问题.
(1)写出图中仪器①的名称________;
(2)实验室用A装置制取氧气,写出反应的化学方程式________;
(3)实验室用B、E、C装置制取并收集干燥的氧气,则E中应盛放的试剂是________;
(4)实验室用D装置收集氧气,当________时开始收集;
(5)E装置中充满水时,也可以作为氧气的收集装置,则氧气应从________端通入(填“a”或“b”).
三、推断题
15.甲、乙、丙三种物质均含地壳中含量最多的元素。甲、乙是组成元素完全相同的化合物,丙是单质;乙通常为液体,在一定条件下可分解生成丙;它们之间有如图所示的转化关系(部分物质和反应条件已经略去)。则:
(1)甲为______(填化学式,下同),乙为______,丙为______;
(2)乙分解生成丙的化学方程式为______。
(3)从微观的角度解释甲、乙性质有差异的原因是______。
16.将某紫黑色固体粉末A加热,可产生无色气体B,同时生成一种黑色固体C
和另一种固
体物质D.黑色固体C通常可用于加热氯酸钾制氧气时的催化剂.另一黑色固体E
在无色气体B
中燃烧,产生使澄清石灰水变浑浊的气体F.绿色植物可将气体F通过光合作用吸收,并转化为无色气体B.回答:
(1)写出名称
A__________,C__________;写出化学符号:B__________,F__________.
(2)写出黑色固体E在无色气体B中燃烧的反应的文字表达式:___________________,该反应的基本类型是____________________。
17.已知A~G都是初中化学常见的物质,通常状况下,A、C为无色液体,且组成元素相同,D、E为气体,它们之间的转化关系如图所示。回答下列问题:
(1)物质B在反应①中的作用是________________。
(2)检验气体D的方法是______________。
(3)若F为黑色固体,写出反应③的符号表达式________________。若G为黑色固体,写出反应③的符号表达式_____________。
四、计算题
18.高铁酸钠(Na2FeO4)是一种高效多功能水处理剂,工业上常采用次氯酸钠(NaClO)氧化法生产,反应原理用化学方程式表示为:3NaClO
+
2Fe(NO3)3+
10NaOH
=
2Na2FeO4↓+3NaCl
+6NaNO3+
5H2O
(1)在Fe(NO3)3中,铁元素和氮元素的质量比为
(填最简比)。
(2)县称取44.7g次氯酸钠,最多能制得高铁酸钠的质量是多少?(列式计算)
温馨提示:NaClO的相对分子质量为74.5;Na2FeO4的相对分子质量为166。
19.食品添加剂的使用,改善了食品的品质和特色。苯甲酸(C7H6O2)是一种应用广泛的食品添加剂,其具有防腐的作用。试回答下列问题:
(1)苯甲酸中,碳、氢元素的质量比__________(填最简整数比)。
(2)苯甲酸中,元素质量分数最小的元素是___________。
20.测定空气的组成后,同学们知道了氧气的体积约占空气总体积的,某初中化学兴趣小组的同学查阅资料得知:氧气的密度约为1.43g/L,空气的密度约为1.29g/L.小芳想知道100g空气中氧气的质量,请你帮她计算,并写出计算过程。(计算结果精确到0.01)
参考答案
1.A
2.D
3.D
4.C
5.C
6.A
7.C
8.A
9.D
10.D
11.B
12.B
13.漏斗
有孔塑料片上
c
B
B
b
14.锥形瓶;2KMnO4K2MnO4+MnO2+O2↑;浓硫酸;气泡连续均匀冒出;b
15.H2O2
H2O
O2
2H2O22H2O+O2↑
构成物质的分子不同
16.高锰酸钾
二氧化锰
O2
CO2
碳+氧气
二氧化碳
化合反应
17.催化作用
用带火星的木条伸入集气瓶中,木条复燃则为氧气
C+O2CO2
Fe+O2Fe3O4
18.(1)4:3;⑵最多可得到高铁酸钾的质量为66.4g。
19.
14:1
氢
20.22.17g
答案第1页,总2页
同课章节目录
- 专题一 走进化学殿堂
- 单元1 化学使生活更美好
- 单元2 如何学习化学
- 专题二 空气和水
- 单元1 多组分的空气
- 单元2 氧气
- 单元3 自然界的水
- 专题三 物质的构成
- 单元1 构成物质的微粒
- 单元2 组成物质的元素
- 单元3 纯净物组成的表示方法
- 专题四 燃料与燃烧
- 单元1 燃烧与灭火
- 单元2 碳及其化合物
- 单元3 化石燃料的利用
- 专题五 化学变化及其表示
- 单元1 化学变化是有条件的
- 单元2 质量守恒定律
- 单元3 化学方程式
- 专题六 物质的溶解
- 单元1 物质的溶解过程
- 单元2 物质的溶解性
- 单元3 物质的溶解性的改变
- 学生实验
- 实验1 实验基本操作
- 实验2 氧气的实验室制取与性质
- 实验3 燃烧的条件
- 实验4 二氧化碳的实验室制取与性质
- 实验5 一定浓度溶液的配置
