第一节 酸及其性质第2课时 酸的化学性质教案
文档属性
| 名称 | 第一节 酸及其性质第2课时 酸的化学性质教案 |

|
|
| 格式 | doc | ||
| 文件大小 | 697.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-09-07 00:00:00 | ||
图片预览


文档简介
第2课时 酸的化学性质
【教学目标】
1.知识与技能
(1)初步了解什么是盐和复分解反应。
(2)初步掌握盐酸、稀硫酸的主要化学性质及用途
2.过程与方法
(1)学习研究酸的性质的大致顺序、通过实验探究酸的性质,根据酸的性质思考其用途的科学方法。
(2)通过酸的化学性质探究活动,培养学生回忆、类推、归纳和小结的能力。
3.情感、态度与价值观
通过认真观察、分析探究酸的性质的有关实验,培养实事求是的科学态度和探究精神。
【教学重点】
酸的化学性质。
【教学难点】
根据实验归纳酸的化学性质。
【教学准备】
投影仪,计算机药品:稀盐酸、稀硫酸、硝酸银溶液、BaCl2溶液、AgNO3溶液、石蕊溶液、酚酞溶液、镁、生锈严重的铁钉、粗铜丝。
仪器:试管、烧杯、量筒、玻璃棒、滴管、镊子、药匙、试管夹、酒精灯(附火柴)。
一、导入新课
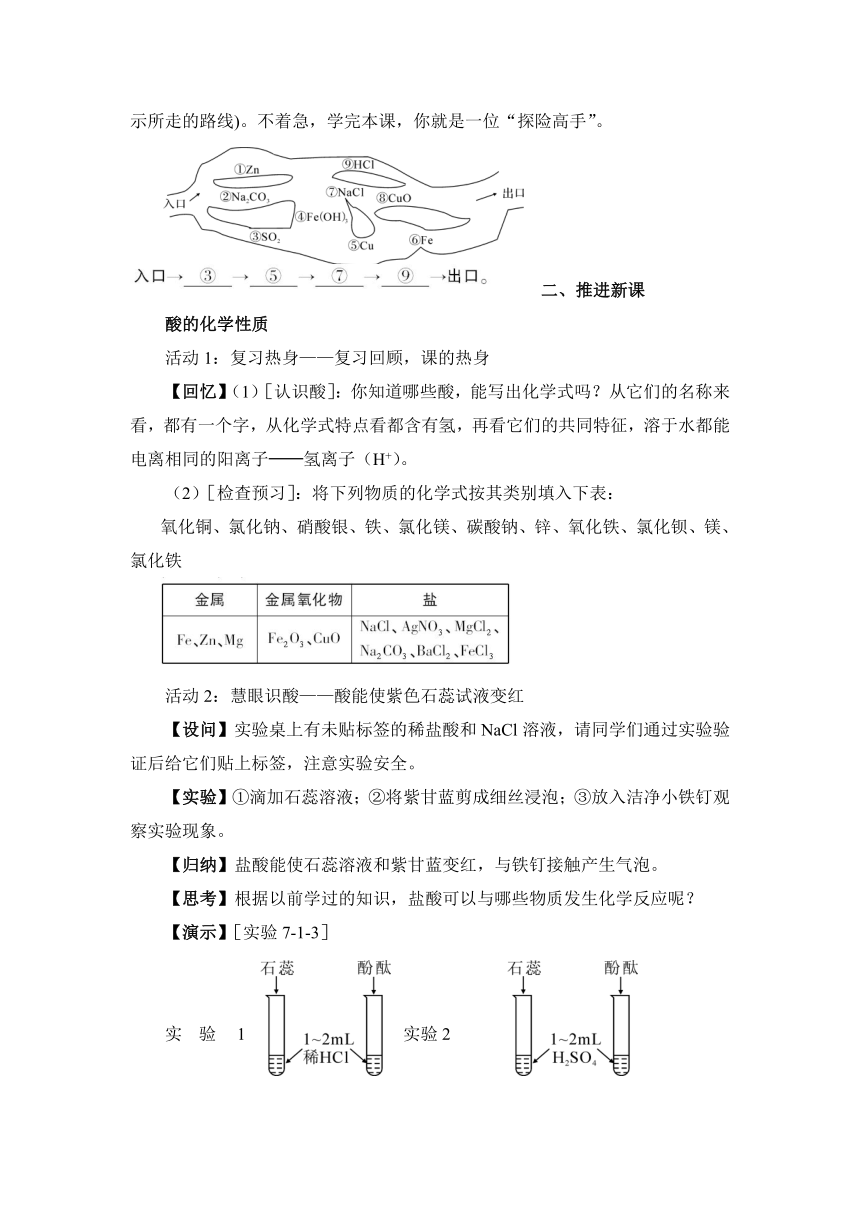
“探险队员”—硫酸,不小心走进了化学迷宫(下图所示),不知怎样走出来,因为迷宫中有许多“吃人的野兽”(即能与硫酸发生反应的物质),硫酸必须避开它,否则就无法通过。你能帮助它走出迷宫(请用图中物质前的序号连接起来表示所走的路线)。不着急,学完本课,你就是一位“探险高手”。
二、推进新课
酸的化学性质
活动1:复习热身——复习回顾,课的热身
【回忆】(1)[认识酸]:你知道哪些酸,能写出化学式吗?从它们的名称来看,都有一个字,从化学式特点看都含有氢,再看它们的共同特征,溶于水都能电离相同的阳离子──氢离子(H+)。
(2)[检查预习]:将下列物质的化学式按其类别填入下表:
氧化铜、氯化钠、硝酸银、铁、氯化镁、碳酸钠、锌、氧化铁、氯化钡、镁、氯化铁
活动2:慧眼识酸——酸能使紫色石蕊试液变红
【设问】实验桌上有未贴标签的稀盐酸和NaCl溶液,请同学们通过实验验证后给它们贴上标签,注意实验安全。
【实验】①滴加石蕊溶液;②将紫甘蓝剪成细丝浸泡;③放入洁净小铁钉观察实验现象。
【归纳】盐酸能使石蕊溶液和紫甘蓝变红,与铁钉接触产生气泡。
【思考】根据以前学过的知识,盐酸可以与哪些物质发生化学反应呢?
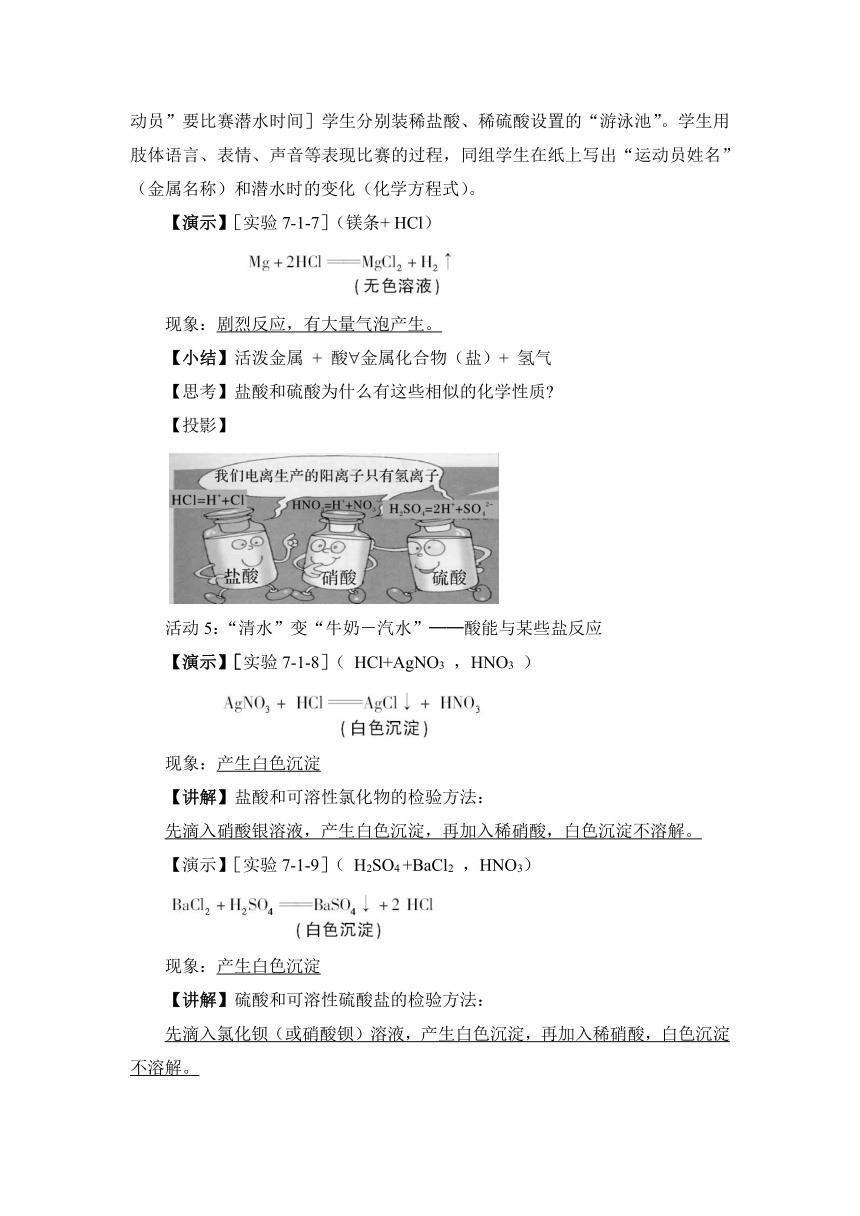
【演示】[实验7-1-3]
实验1 实验2
【观察】石蕊和酚酞试液的颜色以及它们遇盐酸、稀硫酸后颜色的变化。
【归纳】盐酸、稀硫酸能使石蕊试液变红。遇无色的酚酞试液不变色。
活动3:除锈专家——酸能与某些金属氧化物反应
【设问】同学们在生活中见到过哪些除铁锈的方法,用到过哪些除锈的方法?(小瓦片磨铁锅;砂纸打磨生锈的部位等。)
【过渡】这些都是物理方法除锈。在化工生产中人们用什么化学原理除锈?
【演示】[实验7-1-4]
(锈铁钉+ HCl(适量)
现象:铁锈逐渐消失,溶液由无色慢慢变成黄色。
【演示】[实验7-1-5](锈铁钉 + HCl(过量)
铁锈逐渐消失,一会儿产生气泡。
【讲解】盐酸能使生锈的铁钉上的铁锈都逐渐溶解,溶液变成黄色,说明酸能与金属氧化物发生反应。但使用的盐酸必须适量,否则过量盐酸与铁反应。工人师傅用盐酸除去铁锈时,特别注意除锈时间不宜过长。
【演示】[实验7-1-6]
现象:黑色固体溶解,溶液由无色变为蓝色。
【归纳】金属氧化物 + 酸=金属化合物(盐) + 水
活动4:猜它是谁——酸能与某些金属反应
【引入】请同学们回忆一下,在上学期第六单元做“氢气的燃烧和爆炸”的实验里,我们是用什么原料来制取氢气的?由此说明了盐酸具有什么性质?
现象:剧烈反应,有大量气泡产生。
【游戏】[设置游戏场景,有四种金属(镁、锌、铁、铜)王国的“潜水运动员”要比赛潜水时间]学生分别装稀盐酸、稀硫酸设置的“游泳池”。学生用肢体语言、表情、声音等表现比赛的过程,同组学生在纸上写出“运动员姓名”(金属名称)和潜水时的变化(化学方程式)。
【演示】[实验7-1-7](镁条+ HCl)
现象:剧烈反应,有大量气泡产生。
【小结】活泼金属 + 酸金属化合物(盐)+ 氢气
【思考】盐酸和硫酸为什么有这些相似的化学性质?
【投影】
活动5:“清水”变“牛奶-汽水”──酸能与某些盐反应
【演示】[实验7-1-8]( HCl+AgNO3 ,HNO3 )
现象:产生白色沉淀
【讲解】盐酸和可溶性氯化物的检验方法:
先滴入硝酸银溶液,产生白色沉淀,再加入稀硝酸,白色沉淀不溶解。
【演示】[实验7-1-9]( H2SO4 +BaCl2 ,HNO3)
现象:产生白色沉淀
【讲解】硫酸和可溶性硫酸盐的检验方法:
先滴入氯化钡(或硝酸钡)溶液,产生白色沉淀,再加入稀硝酸,白色沉淀不溶解。
【演示】[实验7-1-10]( HCl+ Na2CO3)
现象:固体溶解,产生大量气泡
【演示】[实验7-1-11]( HCl+BaCl2)
现象:无现象发生。
【归纳】盐+酸金属化合物(盐)+酸
【小结】“探险队员”──硫酸,走进了化学迷宫。你知道是怎样走出的?掌握了酸的五大通性,有人要给你们送挑战书了!这个“人”就是盐酸!盐酸要穿过一个极其险恶的迷宫,把挑战书送给你们。迷宫里面有一些吃人的野兽。能与盐酸发生反应的野兽会把他吃掉,哪些野兽会吃掉盐酸呢?现在我们进行小组比赛。
比赛规则:前后四个同学为一小组,寻找出所有吃人的野兽,然后每人轮流写出1个野兽吃掉盐酸时发生反应的化学方程式,写好后立刻交给老师,写得既快又准确的小组胜出。
(设计意图:落实盐酸与四类物质反应的化学方程式。用实物投影仪将前三名的小组写的方程式投出来,引导学生逐一分析每个反应中“野兽”所属的物质类别。)
活动6:概念上架──盐、复分解反应
【提问】NaCl、AgNO3、MgCl2、Na2CO3、BaCl2、FeCl3属于盐一类的化合物,盐的组成有什么特点?
【分析】
【归纳】由金属离子和酸根离子构成的化合物叫做盐。
【强调】此外,由铵根离子(NH4+)和酸根离子构成的化合物也属于盐类,称为铵盐,例如NH4NO3、(NH4)2SO4等。
【讨论】以下化学反应有什么特点?
【归纳】两种化合物互相交换成分生成另外两种化合物。这类化学反应叫做复分解反应。
【强调】形式:AB + CDAD + CB
特点:双交换,价不变
活动7:轻松阅读──了解酸的用途
【阅读】教材P5“常见酸的主要用途和我国年产量”
【强调】盐酸的用途:①制CO2
②除锈
③制药物和试剂
三、典例剖析
例 为验证“酸的化学通性”,某班同学在实验室进行如下实验。请分析并回答相关问题:
(1)写出A中发生的现象 。
(2)写出上述实验中酸与金属氧化物反应的化学方程式
。
(3)要全面验证酸的化学通性,D试管中能与酸反应的固体单质是
(写一种即可)。
(4)实验完成后,将全部废液倒入废液缸内,测得溶液仍为红色,则废液中所含溶质最多有 种(溶质不计指示剂与气体)。
【解析】(1)盐酸能紫色的石蕊试液变红。(2)氧化铜属于金属氧化物,该物质与盐酸反应的方程式为CuO+2HCl=CuCl2+H2O。(3)与酸反应的固体单质是金属单质且该金属较活泼,所以该固体可以是Mg或Al或Zn或Fe(镁或铝或锌或铁)等。(4)实验完成后,将全部废液倒入废液缸内。溶液呈红色,则溶液呈酸性,所以溶液中不可能存在碳酸钠,则溶液存在的溶质主要有碳酸钠与盐酸反应生成生物氯化钠,氧化铜和盐酸反应生成的氯化铜,金属单质与盐酸反应生成的盐,还有剩余的盐酸共四种。
【答案】(1)溶液变红 (2)CuO+2HCl=CuCl2+H2O
(3)Mg(或Al或Zn或Fe,任选其中一种) (4)四
四、课堂小结
【教师】今天我们学到了什么知识?掌握了哪些学习方法?明确了哪些道理?
【学生】知识类:酸的五条化学性质,酸的化学性质是由它的H+体现出来的。方法类:类比迁移方法──盐酸、硫酸使石蕊溶液变红,则硝酸、醋酸、苹果汁、桔子汁都能使石蕊溶液变红;酸能除铁锈,也能除掉铜表面的氧化铜等。
归纳推理方法──已知:
则可归纳推理出:含有CO32-的化合物能与酸反应生成H2O、CO2与另一种化合物。
实验对比鉴定方法──运用酸的化学性质鉴别稀盐酸和NaCl溶液等。
道理类:在学习中只有科学的态度,才能保证形成科学的方法,有了科学的方法才能使我们的大脑真正聪明起来。
五、布置作业
1.完成本课时对应练习。
2.完成课本P6习题1、2 题。
挑战自我(P6)
1.a.(×)【解析】浓硫酸没有挥发性,只有浓盐酸和浓硝酸有挥发性,挥发出的物质与空气中的水蒸气接触形成白雾。
b.(√)【解析】酸溶液中含有氢离子,氢离子能使紫色石蕊溶液变红。
c.(√)【解析】酸溶液中含有共同的氢离子(H+)。
2.
3.浓盐酸易挥发(具有强挥发性),浓硫酸具有强吸水性,都应密封保存。
第2课时 酸的化学性质
1.教师做完一个“较理想”的演示实验后,在小结基础知识后,让学生自己来重复刚才的实验,但未给学生点明“酸的用量”的要求,这样就挑起学生的一个新的“思维矛盾”。在这个矛盾中学生通过争论、再探究等主动活动,理解了新知识,明确了实验一定要有一个实事求是的科学价值观。最后又拓展学生思维,更全面、深刻地认识了酸是“除锈专家”的内涵。
2.用游戏的方式巧妙探究新知,对金属拟人化的处理并及时联系生活,在学生理解知识的层面促进知识向运用层面转化。
3.在除锈这一块补充“用物理方法也可以除锈”,这样使学生认识在不同的场合或要求下可使用不同的除锈方法。
4.学生亲身感受酸有相似的化学性质,在大脑中生成了酸的印象。通过实验验证,体验科学探究的步骤,将思维活动由认识知识提升到认识方法。
【教学目标】
1.知识与技能
(1)初步了解什么是盐和复分解反应。
(2)初步掌握盐酸、稀硫酸的主要化学性质及用途
2.过程与方法
(1)学习研究酸的性质的大致顺序、通过实验探究酸的性质,根据酸的性质思考其用途的科学方法。
(2)通过酸的化学性质探究活动,培养学生回忆、类推、归纳和小结的能力。
3.情感、态度与价值观
通过认真观察、分析探究酸的性质的有关实验,培养实事求是的科学态度和探究精神。
【教学重点】
酸的化学性质。
【教学难点】
根据实验归纳酸的化学性质。
【教学准备】
投影仪,计算机药品:稀盐酸、稀硫酸、硝酸银溶液、BaCl2溶液、AgNO3溶液、石蕊溶液、酚酞溶液、镁、生锈严重的铁钉、粗铜丝。
仪器:试管、烧杯、量筒、玻璃棒、滴管、镊子、药匙、试管夹、酒精灯(附火柴)。
一、导入新课
“探险队员”—硫酸,不小心走进了化学迷宫(下图所示),不知怎样走出来,因为迷宫中有许多“吃人的野兽”(即能与硫酸发生反应的物质),硫酸必须避开它,否则就无法通过。你能帮助它走出迷宫(请用图中物质前的序号连接起来表示所走的路线)。不着急,学完本课,你就是一位“探险高手”。
二、推进新课
酸的化学性质
活动1:复习热身——复习回顾,课的热身
【回忆】(1)[认识酸]:你知道哪些酸,能写出化学式吗?从它们的名称来看,都有一个字,从化学式特点看都含有氢,再看它们的共同特征,溶于水都能电离相同的阳离子──氢离子(H+)。
(2)[检查预习]:将下列物质的化学式按其类别填入下表:
氧化铜、氯化钠、硝酸银、铁、氯化镁、碳酸钠、锌、氧化铁、氯化钡、镁、氯化铁
活动2:慧眼识酸——酸能使紫色石蕊试液变红
【设问】实验桌上有未贴标签的稀盐酸和NaCl溶液,请同学们通过实验验证后给它们贴上标签,注意实验安全。
【实验】①滴加石蕊溶液;②将紫甘蓝剪成细丝浸泡;③放入洁净小铁钉观察实验现象。
【归纳】盐酸能使石蕊溶液和紫甘蓝变红,与铁钉接触产生气泡。
【思考】根据以前学过的知识,盐酸可以与哪些物质发生化学反应呢?
【演示】[实验7-1-3]
实验1 实验2
【观察】石蕊和酚酞试液的颜色以及它们遇盐酸、稀硫酸后颜色的变化。
【归纳】盐酸、稀硫酸能使石蕊试液变红。遇无色的酚酞试液不变色。
活动3:除锈专家——酸能与某些金属氧化物反应
【设问】同学们在生活中见到过哪些除铁锈的方法,用到过哪些除锈的方法?(小瓦片磨铁锅;砂纸打磨生锈的部位等。)
【过渡】这些都是物理方法除锈。在化工生产中人们用什么化学原理除锈?
【演示】[实验7-1-4]
(锈铁钉+ HCl(适量)
现象:铁锈逐渐消失,溶液由无色慢慢变成黄色。
【演示】[实验7-1-5](锈铁钉 + HCl(过量)
铁锈逐渐消失,一会儿产生气泡。
【讲解】盐酸能使生锈的铁钉上的铁锈都逐渐溶解,溶液变成黄色,说明酸能与金属氧化物发生反应。但使用的盐酸必须适量,否则过量盐酸与铁反应。工人师傅用盐酸除去铁锈时,特别注意除锈时间不宜过长。
【演示】[实验7-1-6]
现象:黑色固体溶解,溶液由无色变为蓝色。
【归纳】金属氧化物 + 酸=金属化合物(盐) + 水
活动4:猜它是谁——酸能与某些金属反应
【引入】请同学们回忆一下,在上学期第六单元做“氢气的燃烧和爆炸”的实验里,我们是用什么原料来制取氢气的?由此说明了盐酸具有什么性质?
现象:剧烈反应,有大量气泡产生。
【游戏】[设置游戏场景,有四种金属(镁、锌、铁、铜)王国的“潜水运动员”要比赛潜水时间]学生分别装稀盐酸、稀硫酸设置的“游泳池”。学生用肢体语言、表情、声音等表现比赛的过程,同组学生在纸上写出“运动员姓名”(金属名称)和潜水时的变化(化学方程式)。
【演示】[实验7-1-7](镁条+ HCl)
现象:剧烈反应,有大量气泡产生。
【小结】活泼金属 + 酸金属化合物(盐)+ 氢气
【思考】盐酸和硫酸为什么有这些相似的化学性质?
【投影】
活动5:“清水”变“牛奶-汽水”──酸能与某些盐反应
【演示】[实验7-1-8]( HCl+AgNO3 ,HNO3 )
现象:产生白色沉淀
【讲解】盐酸和可溶性氯化物的检验方法:
先滴入硝酸银溶液,产生白色沉淀,再加入稀硝酸,白色沉淀不溶解。
【演示】[实验7-1-9]( H2SO4 +BaCl2 ,HNO3)
现象:产生白色沉淀
【讲解】硫酸和可溶性硫酸盐的检验方法:
先滴入氯化钡(或硝酸钡)溶液,产生白色沉淀,再加入稀硝酸,白色沉淀不溶解。
【演示】[实验7-1-10]( HCl+ Na2CO3)
现象:固体溶解,产生大量气泡
【演示】[实验7-1-11]( HCl+BaCl2)
现象:无现象发生。
【归纳】盐+酸金属化合物(盐)+酸
【小结】“探险队员”──硫酸,走进了化学迷宫。你知道是怎样走出的?掌握了酸的五大通性,有人要给你们送挑战书了!这个“人”就是盐酸!盐酸要穿过一个极其险恶的迷宫,把挑战书送给你们。迷宫里面有一些吃人的野兽。能与盐酸发生反应的野兽会把他吃掉,哪些野兽会吃掉盐酸呢?现在我们进行小组比赛。
比赛规则:前后四个同学为一小组,寻找出所有吃人的野兽,然后每人轮流写出1个野兽吃掉盐酸时发生反应的化学方程式,写好后立刻交给老师,写得既快又准确的小组胜出。
(设计意图:落实盐酸与四类物质反应的化学方程式。用实物投影仪将前三名的小组写的方程式投出来,引导学生逐一分析每个反应中“野兽”所属的物质类别。)
活动6:概念上架──盐、复分解反应
【提问】NaCl、AgNO3、MgCl2、Na2CO3、BaCl2、FeCl3属于盐一类的化合物,盐的组成有什么特点?
【分析】
【归纳】由金属离子和酸根离子构成的化合物叫做盐。
【强调】此外,由铵根离子(NH4+)和酸根离子构成的化合物也属于盐类,称为铵盐,例如NH4NO3、(NH4)2SO4等。
【讨论】以下化学反应有什么特点?
【归纳】两种化合物互相交换成分生成另外两种化合物。这类化学反应叫做复分解反应。
【强调】形式:AB + CDAD + CB
特点:双交换,价不变
活动7:轻松阅读──了解酸的用途
【阅读】教材P5“常见酸的主要用途和我国年产量”
【强调】盐酸的用途:①制CO2
②除锈
③制药物和试剂
三、典例剖析
例 为验证“酸的化学通性”,某班同学在实验室进行如下实验。请分析并回答相关问题:
(1)写出A中发生的现象 。
(2)写出上述实验中酸与金属氧化物反应的化学方程式
。
(3)要全面验证酸的化学通性,D试管中能与酸反应的固体单质是
(写一种即可)。
(4)实验完成后,将全部废液倒入废液缸内,测得溶液仍为红色,则废液中所含溶质最多有 种(溶质不计指示剂与气体)。
【解析】(1)盐酸能紫色的石蕊试液变红。(2)氧化铜属于金属氧化物,该物质与盐酸反应的方程式为CuO+2HCl=CuCl2+H2O。(3)与酸反应的固体单质是金属单质且该金属较活泼,所以该固体可以是Mg或Al或Zn或Fe(镁或铝或锌或铁)等。(4)实验完成后,将全部废液倒入废液缸内。溶液呈红色,则溶液呈酸性,所以溶液中不可能存在碳酸钠,则溶液存在的溶质主要有碳酸钠与盐酸反应生成生物氯化钠,氧化铜和盐酸反应生成的氯化铜,金属单质与盐酸反应生成的盐,还有剩余的盐酸共四种。
【答案】(1)溶液变红 (2)CuO+2HCl=CuCl2+H2O
(3)Mg(或Al或Zn或Fe,任选其中一种) (4)四
四、课堂小结
【教师】今天我们学到了什么知识?掌握了哪些学习方法?明确了哪些道理?
【学生】知识类:酸的五条化学性质,酸的化学性质是由它的H+体现出来的。方法类:类比迁移方法──盐酸、硫酸使石蕊溶液变红,则硝酸、醋酸、苹果汁、桔子汁都能使石蕊溶液变红;酸能除铁锈,也能除掉铜表面的氧化铜等。
归纳推理方法──已知:
则可归纳推理出:含有CO32-的化合物能与酸反应生成H2O、CO2与另一种化合物。
实验对比鉴定方法──运用酸的化学性质鉴别稀盐酸和NaCl溶液等。
道理类:在学习中只有科学的态度,才能保证形成科学的方法,有了科学的方法才能使我们的大脑真正聪明起来。
五、布置作业
1.完成本课时对应练习。
2.完成课本P6习题1、2 题。
挑战自我(P6)
1.a.(×)【解析】浓硫酸没有挥发性,只有浓盐酸和浓硝酸有挥发性,挥发出的物质与空气中的水蒸气接触形成白雾。
b.(√)【解析】酸溶液中含有氢离子,氢离子能使紫色石蕊溶液变红。
c.(√)【解析】酸溶液中含有共同的氢离子(H+)。
2.
3.浓盐酸易挥发(具有强挥发性),浓硫酸具有强吸水性,都应密封保存。
第2课时 酸的化学性质
1.教师做完一个“较理想”的演示实验后,在小结基础知识后,让学生自己来重复刚才的实验,但未给学生点明“酸的用量”的要求,这样就挑起学生的一个新的“思维矛盾”。在这个矛盾中学生通过争论、再探究等主动活动,理解了新知识,明确了实验一定要有一个实事求是的科学价值观。最后又拓展学生思维,更全面、深刻地认识了酸是“除锈专家”的内涵。
2.用游戏的方式巧妙探究新知,对金属拟人化的处理并及时联系生活,在学生理解知识的层面促进知识向运用层面转化。
3.在除锈这一块补充“用物理方法也可以除锈”,这样使学生认识在不同的场合或要求下可使用不同的除锈方法。
4.学生亲身感受酸有相似的化学性质,在大脑中生成了酸的印象。通过实验验证,体验科学探究的步骤,将思维活动由认识知识提升到认识方法。
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
